文档内容
CH (g)+2O (g)═CO (g)+2H O(l)△H=﹣890kJ•mol﹣1.
2009年全国统一高考化学试卷(全国卷Ⅱ) 4 2 2 2
现有H 与CH 的混合气体112L(标准状况),使其完全燃烧生成 CO 和H O(l),若实验测得
2 4 2 2
一、选择题
反应放热3695kJ,则原混合气体中H 与CH 的物质的量之比是( )
2 4
1.(3分)物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N O,反应结束后锌
2 A.1:1 B.1:3 C.1:4 D.2:3
没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
A.1:4 B.1:5 C.2:3 D.2:5
7.(3分)1mol 与足量的NaOH溶液充分反应,消耗的 NaOH的物
2.(3分)下列关于溶液和胶体的叙述,正确的是( )
质的量为( )
A.溶液是电中性的,胶体是带电的
A.5 mol B.4 mol C.3 mol D.2 mol
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
8.(3分)根据已知回答24﹣25题
C.溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
已知:2Fe2++Cl =2Cl﹣+2Fe3+,2Br﹣+Cl =Br +2Cl﹣,2Fe2++Br =2Br﹣+2Fe3+.
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 2 2 2 2
含有amol FeBr 的溶液中,通入xmol Cl .下列各项为通Cl 过程中,溶液内发生反应的离子方程
3.(3分)下列叙述中正确的是( ) 2 2 2
式,其中不正确的是( )
A.向含有CaCO 沉淀的水中通入CO 至沉淀恰好溶解,再向溶液中加入NaHCO 饱和溶液,
3 2 3
A.x=0.4a,2Fe2++Cl =2Fe3++2Cl﹣
又有CaCO 沉淀生成 2
3
B.x=0.6a,2Br﹣+Cl =Br +2Cl﹣
B.向Na CO 溶液中逐滴加入等物质的量的稀盐酸,生成的CO 与原Na CO 的物质的量之比 2 2
2 3 2 2 3
C.x=a,2Fe2++2Br﹣+2Cl =Br +2Fe3++4Cl﹣
为1:2 2 2
D.x=1.5a,2Fe2++4Br﹣+3Cl =2Br +2Fe3++6Cl﹣
C.等质量的NaHCO 和Na CO 分别与足量盐酸反应,在同温同压下,生成的CO 体积相同 2 2
3 2 3 2
D.向Na CO 饱和溶液中通入CO ,有NaHCO 结晶析出
2 3 2 3
二、非选题
4.(3 分)某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为
9.(15分)某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量
152.0,原子核外的电子数为63.下列叙述中错误的是( )
随时间的变化如表所示.
A.它是副族元素
t/min X/mol Y/mol Z/mol
B.它是第六周期元素
C.它的原子核内有63个质子 0 1.00 1.00 0.00
D.它的一种同位素的核内有89个中子 1 0.90 0.80 0.20
5.(3分)现有等浓度的下列溶液:①醋酸,②苯酚,③苯酚钠,④碳酸,⑤碳酸钠,⑥碳酸氢
3 0.75 0.50 0.50
钠.按溶液pH由小到大排列正确的是( )
5 0.65 0.30 0.70
A.①④②③⑥⑤ B.④①②⑥⑤③ C.①④②⑥③⑤ D.④①②③⑥⑤
9 0.55 0.10 0.90
6.(3分)已知:
10 0.55 0.10 0.90
2H (g)+O (g)═2H O(l)△H=﹣571.6kJ•mol﹣1;
2 2 2
14 0.55 0.10 0.9011.(15分)现有A、B、C、D、E、F六种化合物,已知它们的阳离子有K+,Ag+,Ca2+,Ba2+,
Fe2+,Al3+,阴离子有 Cl﹣,OH﹣,CH COO﹣,NO ﹣,SO 2﹣,CO 2﹣,现将它们分别配成
3 3 4 3
0.1mol•L﹣1的溶液,进行如下实验:
①测得溶液A、C、E呈碱性,且碱性为A>E>C;
②向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③向D溶液中滴加Ba(NO ) 溶液,无明显现象;
3 2
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色.
根据上述实验现象,回答下列问题:
(1)实验②中反应的化学方程式是
(2)E溶液是 ,判断依据是 ;
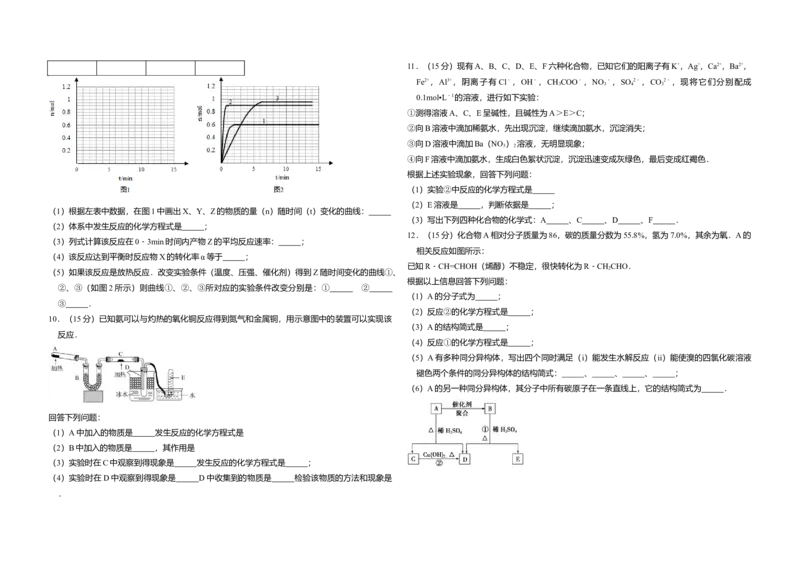
(1)根据左表中数据,在图1中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
(3)写出下列四种化合物的化学式:A 、C 、D 、F .
(2)体系中发生反应的化学方程式是 ;
12.(15分)化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的
(3)列式计算该反应在0﹣3min时间内产物Z的平均反应速率: ;
相关反应如图所示:
(4)该反应达到平衡时反应物X的转化率α等于 ;
已知R﹣CH=CHOH(烯醇)不稳定,很快转化为R﹣CH CHO.
2
(5)如果该反应是放热反应.改变实验条件(温度、压强、催化剂)得到 Z随时间变化的曲线①、
根据以上信息回答下列问题:
②、③(如图2所示)则曲线①、②、③所对应的实验条件改变分别是:① ②
(1)A的分子式为 ;
③ .
(2)反应②的化学方程式是 ;
10.(15分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该
(3)A的结构简式是 ;
反应.
(4)反应①的化学方程式是 ;
(5)A有多种同分异构体,写出四个同时满足(i)能发生水解反应(ii)能使溴的四氯化碳溶液
褪色两个条件的同分异构体的结构简式: 、 、 、 ;
(6)A的另一种同分异构体,其分子中所有碳原子在一条直线上,它的结构简式为 .
回答下列问题:
(1)A中加入的物质是 发生反应的化学方程式是
(2)B中加入的物质是 ,其作用是
(3)实验时在C中观察到得现象是 发生反应的化学方程式是 ;
(4)实验时在D中观察到得现象是 D中收集到的物质是 检验该物质的方法和现象是
.