文档内容
2013年普通高等学校招生全国统一考试
浙江理科综合能力测试
一、选择题(本题17小题。在每小题给出的四个选项中,只有一项是符合题目
要求的。)
7.下列说法不正确的是
A.多孔碳可用氢氧燃料电池的电极材料
B.pH计不能用于酸碱中和滴定终点的判断ks5u
C.科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代了普通
DNA链中的P元素
D.CHCH—CH 和CO 反应生成可降解聚合物[ O—CHCH —O—C ] ,该反应符合绿
3 2 2 2 n
O CH O
3
化学的原则
8.下列说法正确的是ks5u
A.实验室从海带提取单质碘的方法是:取样 灼烧 溶解 过滤 萃取
B.用乙醇和浓HSO 制备乙烯时,可用水浴加热控制反应的温度
2 4
C.氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器
中
D.将(NH )SO 、CuSO 溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白
4 2 4 4
质变性
9.短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层
电子数是最外层电子数的一半,则下列说法正确的是
A.钠与W可能形成NaW 化合物
2 2 X Y
B.由Z与Y组成的物质在熔融时能导电
Z W Q
C.W得电子能力比Q强
D.X有多种同素异形体,而Y不存在同素异形体
10.下列说法正确的是
A.按系统命名法,化合物 的名称是2,3,5,5-四甲基-4,4-二乙基己烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.苯与甲苯互为同系物,均能使KMnO 酸性溶液褪色
4
OH OH OH
……
D.结构片段为 的高聚物,…其…单体是甲醛和苯酚
11.电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定
的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐
变浅。
已知:3I +6OH—==IO —+5I—+3H O
2 3 2
下列说法不正确的是
A.右侧发生的电极方程式:2HO+2e—==H ↑+2OH—
2 2
B.电解结束时,右侧溶液中含有IO —
3C.电解槽内发生反应的总化学方程式KI+3HO======KIO +3H ↑
2 3 2
D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变
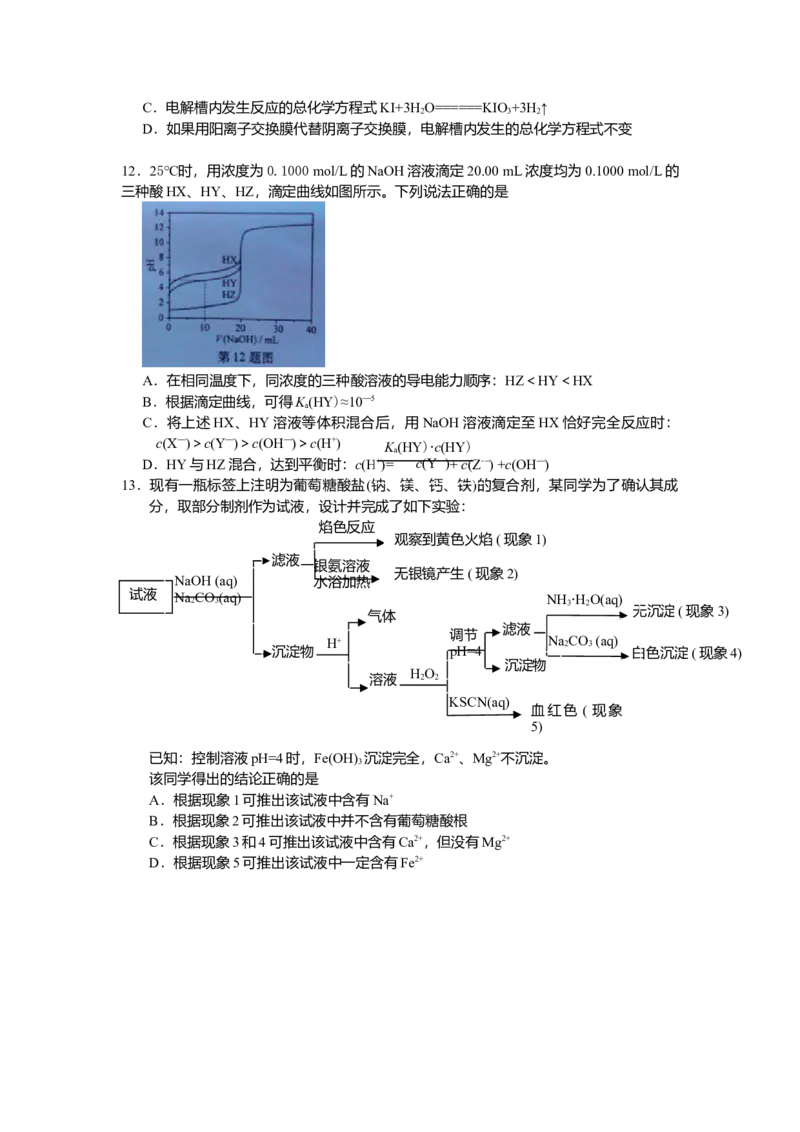
12.25℃时,用浓度为0.1000 mol/L的NaOH溶液滴定20.00 mL浓度均为0.1000 mol/L的
三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得K(HY)≈10—5
a
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:
c(X—)>c(Y—)>c(OH—)>c(H+) K(HY)·c(HY)
a
D.HY与HZ混合,达到平衡时:c(H+)= c ( Y — ) + c(Z—) +c(OH—)
13.现有一瓶标签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合剂,某同学为了确认其成
分,取部分制剂作为试液,设计并完成了如下实验:
焰色反应
观察到黄色火焰(现象1)
滤液
银氨溶液
无银镜产生(现象2)
NaOH (aq) 水浴加热
试液 Na 2 CO 3 (aq) NH 3 ·H 2 O(aq)
无沉淀(现象3)
气体
调节
滤液
H+ Na 2 CO 3 (aq)
沉淀物 pH=4 白色沉淀(现象4)
沉淀物
H O
溶液 2 2
KSCN(aq)
血红色 ( 现象
5)
已知:控制溶液pH=4时,Fe(OH) 沉淀完全,Ca2+、Mg2+不沉淀。
3
该同学得出的结论正确的是
A.根据现象1可推出该试液中含有Na+
B.根据现象2可推出该试液中并不含有葡萄糖酸根
C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D.根据现象5可推出该试液中一定含有Fe2+非选择题部分(共 180 分)
非选择题部分共12题,共180分。
26、氢能源是一种重要的清洁能源。现有两种可产生 H 的化合物甲和乙。将6.00 g甲加热
2
至完全分解,只得到一种短周期元素的金属单质和6.72 LH (已折算成标准状况)。甲与
2
水反应也能产生H ,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物
2
乙在催化剂存在下可分解得到 H 和另一种单质气体丙,丙在标准状态下的密度为 1.25
2
g/L。请回答下列问题:
(1)甲的化学式是_________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________________________________-。
(3)气体丙与金属镁反应的产物是_______(用化学式表示)。
(4)乙在加热条件下与 CuO 反应可生成 Cu 和气体丙,写出该反应的化学方程式
_________。
有人提出产物Cu中可能还含有Cu O,请设计实验方案验证之_________________________。
2
(已知Cu O+2H+==Cu+Cu2++H O)
2 2
(5)甲与乙之间_______(填“可能”或“不可能)发生反应产生H,判断理由是________。
2
27、捕碳技术(主要指捕获 CO)在降低温室气体排放中具有重要的作用。目前 NH 和
2 3
(NH )CO 已经被用作工业捕碳剂,它们与CO 可发生如下可逆反应:
4 2 3 2
反应Ⅰ:2NH (l)+ HO (l)+ CO (g) (NH )CO (aq) △H
3 2 2 4 2 3 1
反应Ⅱ:NH (l)+ HO (l)+ CO (g) NH HCO (aq) △H
3 2 2 4 3 2
反应Ⅲ:(NH )CO (aq) + HO (l)+ CO (g) 2NH HCO (aq) △H
4 2 3 2 2 4 3 3
请回答下列问题:
(1)△H 与△H、△H 之间的关系是:△H=____ _ _ _____。
1 2 3 3
(2)为研究温度对(NH )CO 捕获CO 气体效率的影响,在某温度T 下,将一定量的
4 2 3 2 1
(NH )CO 溶液置于密闭容器中,并充入一定量的CO 气体(用氮气作为稀释剂),在t时刻,
4 2 3 2
测得容器中CO 气体的浓度。然后分别在温度为T 、T 、T 、T 下,保持其它初始实验条
2 2 3 4 5
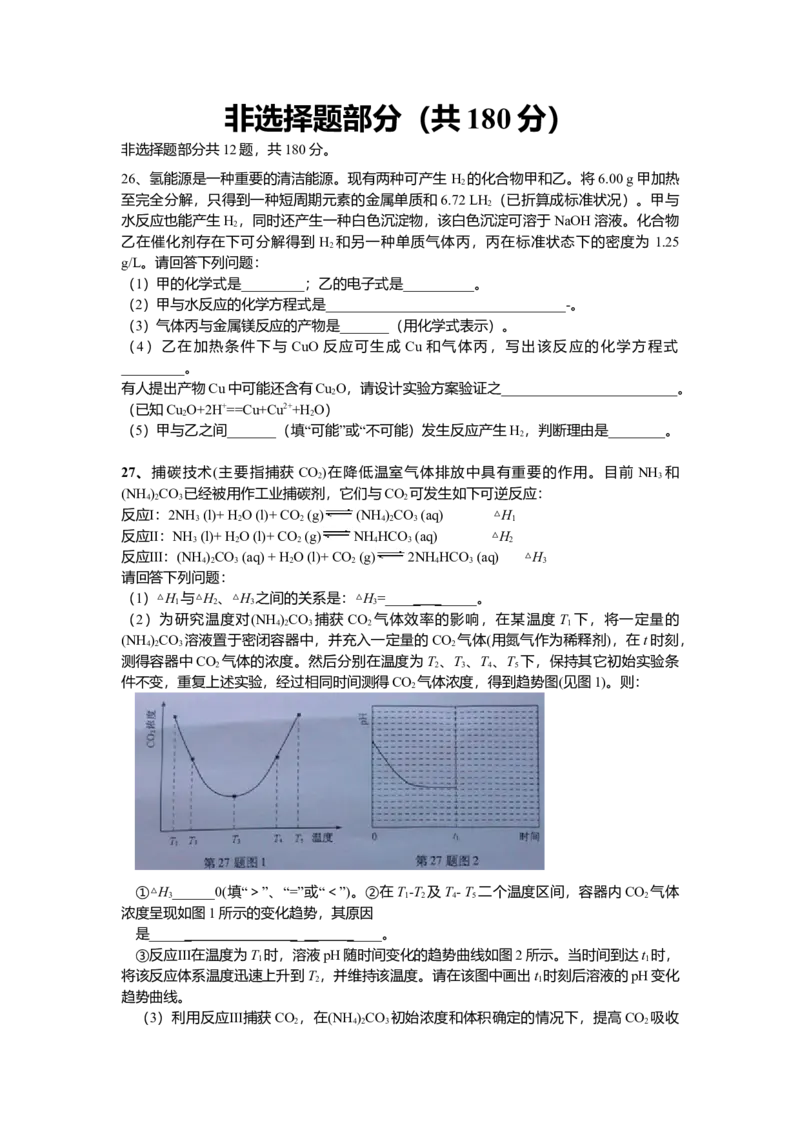
件不变,重复上述实验,经过相同时间测得CO 气体浓度,得到趋势图(见图1)。则:
2
①△H______0(填“>”、“=”或“<”)。②在T-T 及T- T 二个温度区间,容器内CO 气体
3 1 2 4 5 2
浓度呈现如图1所示的变化趋势,其原因
是_____ _ _ _ __ _ ____。
③反应Ⅲ在温度为T 时,溶液pH随时间变化的趋势曲线如图2所示。当时间到达t 时,
1 1
将该反应体系温度迅速上升到T,并维持该温度。请在该图中画出t 时刻后溶液的pH变化
2 1
趋势曲线。
(3)利用反应Ⅲ捕获CO ,在(NH )CO 初始浓度和体积确定的情况下,提高CO 吸收
2 4 2 3 2量的措施有_____(写出2个)。
(4)下列物质中也可能作为CO 捕获剂的是
2
A.NH Cl B.NaCO C.HOCH CHOH D.HOCH CHNH
4 2 3 2 2 2 2 2
28、利用废旧镀锌铁皮可制备磁性Fe O 胶体粒子及副产物ZnO。制备流程图如下:
3 4
调节pH
废旧 溶液A Zn(OH) 2 沉淀 …… ZnO
NaOH (aq)
镀锌
△
铁皮
稀H SO 调节pH=1~2 溶液B NaOH (aq) Fe 3 O 4
不溶物 2 4 适量H O (Fe2+ 、 △ 胶体粒子
2 2
Fe2+)
已知:Zn及其化合物的性质与Al及其化合物的性质相似。请回答下列问题:
(1)用NaOH溶液处理废旧镀锌铁皮的作用有_ _ _。
A.去除油污B.溶解镀锌层C.去除铁锈D.钝化
(2)调节溶液A的pH可产生Zn(OH) 沉淀,为制得ZnO,后续操作步骤是___________。
2
(3)由溶液B制得Fe O 胶体粒子的过程中,须持续通N,其原因是_______________。
3 4 2
(4)Fe O 胶体粒子能否用减压过滤法实现固液分离?_____(填“能”或“不能”),理由是
3 4
___________________________。
(5)用重铬酸钾法(一种氧化还原滴定法)可测得产物Fe O 中二价铁含量。若需配制浓
3 4
度为0.01000 mol/L的KCr O 的标准溶液250 mL,应准确称取______g KCr O (保留4位
2 2 7 2 2 7
有效数字,已知M ==294.0 g/mol)。配制该标准溶液时,下列仪器不必要用到的有
K2Cr2O7
_____(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6)滴定操作中,如果滴定前装有KCr O 标准溶液的滴定管尖嘴部分有气泡,而滴定
2 2 7
结束后气泡消失,则测定结果将_______(填“偏大”、“偏小”或“不变”)。
29、某课题组以苯为主要原料,采取以下路线合成利胆药——柳胺酚。
回答下列问题:
Cl
2 试剂 NaOH/H O HCl Fe
FeCl A B 2 C D E
3 HCl
F
C H O
7 6 3
C — NH OH
—
NO OH O
2 NH 2 柳胺酚
Fe
已知: H C l
(1)对于柳胺酚,下列说法正确的是ks5u
A.1 mol柳胺酚最多可以和2 mol NaOH反应 B.不发生硝化反应
C.可发生水解反应 D.可与溴发生取代反应
(2)写出A B反应所需的试剂______________。
(3)写出B C的化学方程式__________________________________。
(4)写出化合物F的结构简式_____________________________。
(5)写出同时符合下列条件的F的同分异构体的结构简式____________(写出3种)。
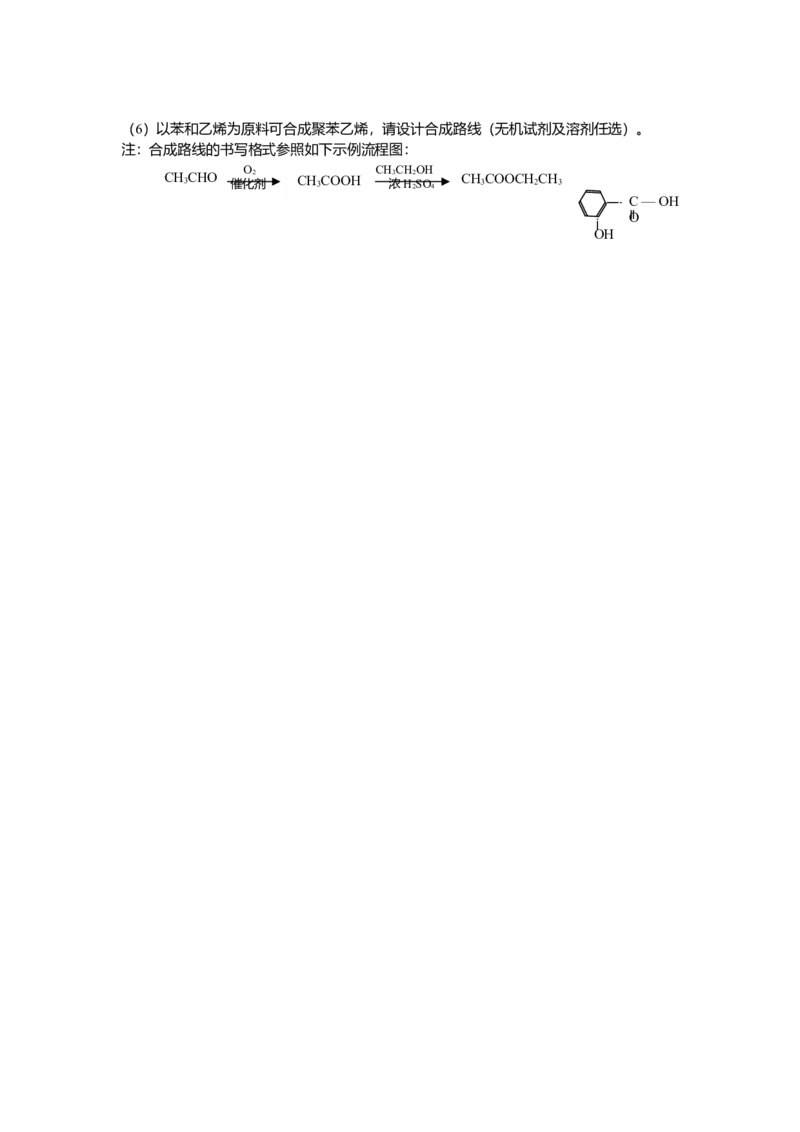
①属酚类化合物,且苯环上有三种不同化学环境的氢原子; ②能发生银镜反应(6)以苯和乙烯为原料可合成聚苯乙烯,请设计合成路线(无机试剂及溶剂任选)。
注:合成路线的书写格式参照如下示例流程图:
O CHCHOH
CH 3 CHO 催化 2 剂 CH 3 COOH 浓 3 H 2 2 SO 4 CH 3 COOCH 2 CH 3
C—OH
O
OH