文档内容
2014 年四川省高考化学试题及答案解析
1.(2014四川高考)化学与生活密切相关,下列说法不正确的是:
A.乙烯可作水果的催熟剂
B.硅胶可作袋装食品的干燥剂
C.褔尔马林可作食品的保鲜剂
D.氢氧化铝可作胃酸的中和剂
2.(2014四川高考)下列关于物质的分类说法正确的是:
A.金刚石、白磷都属于单质
B.漂白粉、石英都属于纯净物
C.氯化铵、次氯酸都属于强电解质
D.葡萄糖、蛋白质都属于高分子化合物
3.(2014四川高考)能正确表示下列反应的离子方程式是:
A.Cl 通往NaOH溶液中:Cl +OH-=Cl-+ClO-+H O
2 2 2
B.NaHCO 溶液中加入HC:CO 2-+2H+=CO ↑+H O
3 3 2 2
C.AlCl 溶液中加入过量稀氨水:Al3++4NH ·H O=AlO -+4NH ++2H O
3 3 2 2 4 2
D.Cu溶液于稀HNO :3Cu+8H++2NO -=3Cu2++2NO↑+4H O
3 3 2
4.(2014四川高考)下列实验方案中,不能达到实验目的的是:
选 实验目的 实验方案
项
A 检验CH CH Br在NaOH溶 将CH CH Br与NaOH溶液共热。冷却后,取出上层水溶液,用
3 2 3 2
液中是否发生水解 稀HNO 酸化,辊入AgNO 溶液,观察是否产生淡黄色沉淀
3 3
B 检验Fe(NO ) 晶体是否已 将Fe(NO ) 样品溶于稀硫酸后,滴加KSCN溶液,观察溶液是
3 2 3 2
氧化变质 否变红
C 验证Br 的氧化性强于I 将少量溴水加入KI溶液中,再加入CCl ,振荡,静置,可观察
2 2 4
到下层液体呈紫色
D 验证Fe(OH) 的溶解度小于将FeCl 溶液加入Mg(OH) 悬浊液中,振荡,可观察到沉淀由
3 3 2
Mg(OH) 白色变为红褐色
2
5.(2014四川高考)设N 为阿伏加德罗常数的值,下列说法正确的是:
A
A.高温下,0.2molFe与足量水蒸气反应,生成的H 分子数目为0.3N
2 A
B.室温下,1LpH=13的NOH溶液中,由水电离的OH-离子数目为0.1N
A
C.氢氧化燃料电池正极消耗 22.4L(标准状况)气体时,电路中通过和电子数目为2N
A
D.5NH NO 2HNO +4N ↑+9H2O反应中,生成28gN 时,转移的电子数目为3.75N
4 3 3 2 2 A
6.(2014四川高考)下列溶液中粒子的物质的量浓度关系正确的是:
A.0.1mol/L NH CO 溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:
4 3
C(Na+)>c(CO 2-)>c(HCO -)>c(OH-)
3 3
B.20ml0.1mol/L CH COONa溶液与10mlHCl溶液混合后溶液呈酸性,所得溶液中:
3
C(CH COO-)>c(Cl-)>c(CH COOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH +)>c(OH-)
4
D.0.1mo;/L CH COOH溶液与0.1mol/L NOH溶液等体积混合,所得溶液中:
3
c(OH-)>c(H+)+c(CH COOH)
3
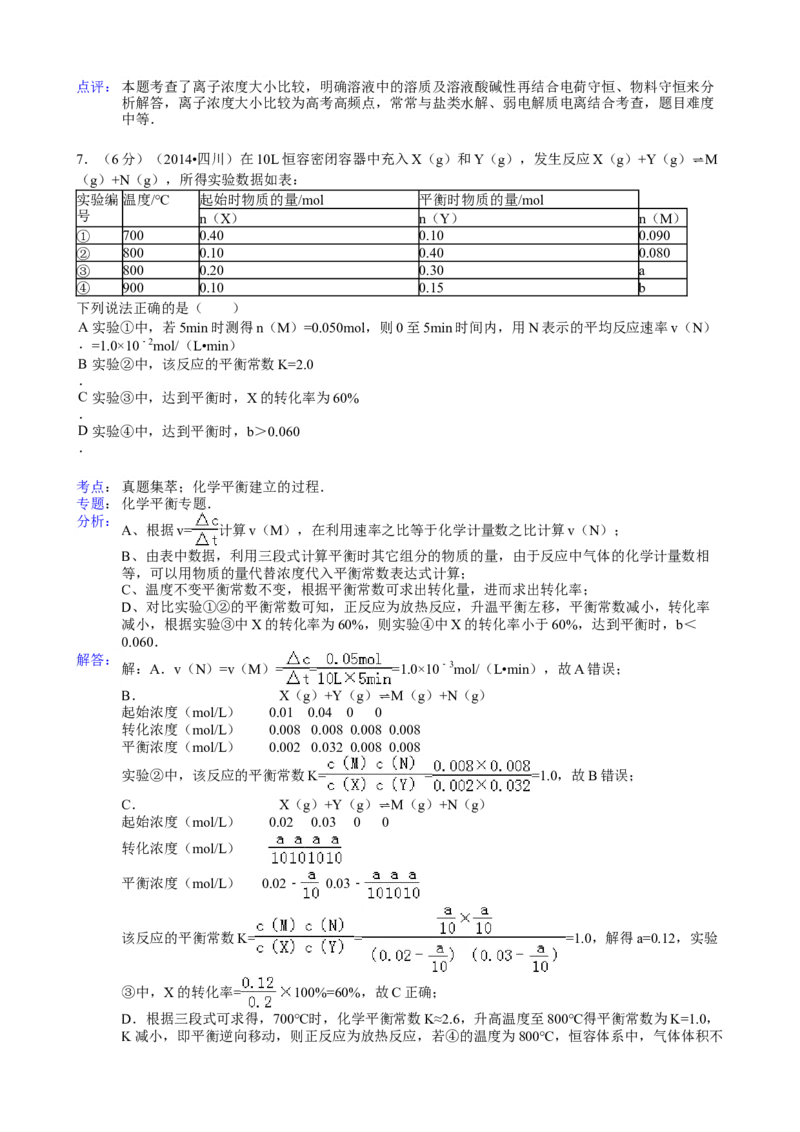
7.(2014四川高考)在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(g),
所得实验数据如下表:
实验 起始时物质的量/mol平衡时物质的量/mol
温度/℃
编号 n(X) n(Y) n(M)
① 700 0.40 0.10 0.090
② 800 0.10 0.40 0.080
③ 800 0.20 0.30 a
④ 900 0.10 0.15 b
下列说法正确的是:
A.实验①中,若5min时测得n(M)=0.50mol,则0至5min时间内,用N表示的平均反应速率v(N)
=1.0×10-2mol/(L·min)
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
8.(2014四川高考)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY 是红棕色气体;X与氢元
2
素可形成XH ;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:
3
(1)Y基态原子的电子排布式是 ;Z所在周期中第一电离能最大的元素是 。
(2)XY -离子的立体构型是 ;R2+的水合离子中, 提供孤电子对的原子是
2
。
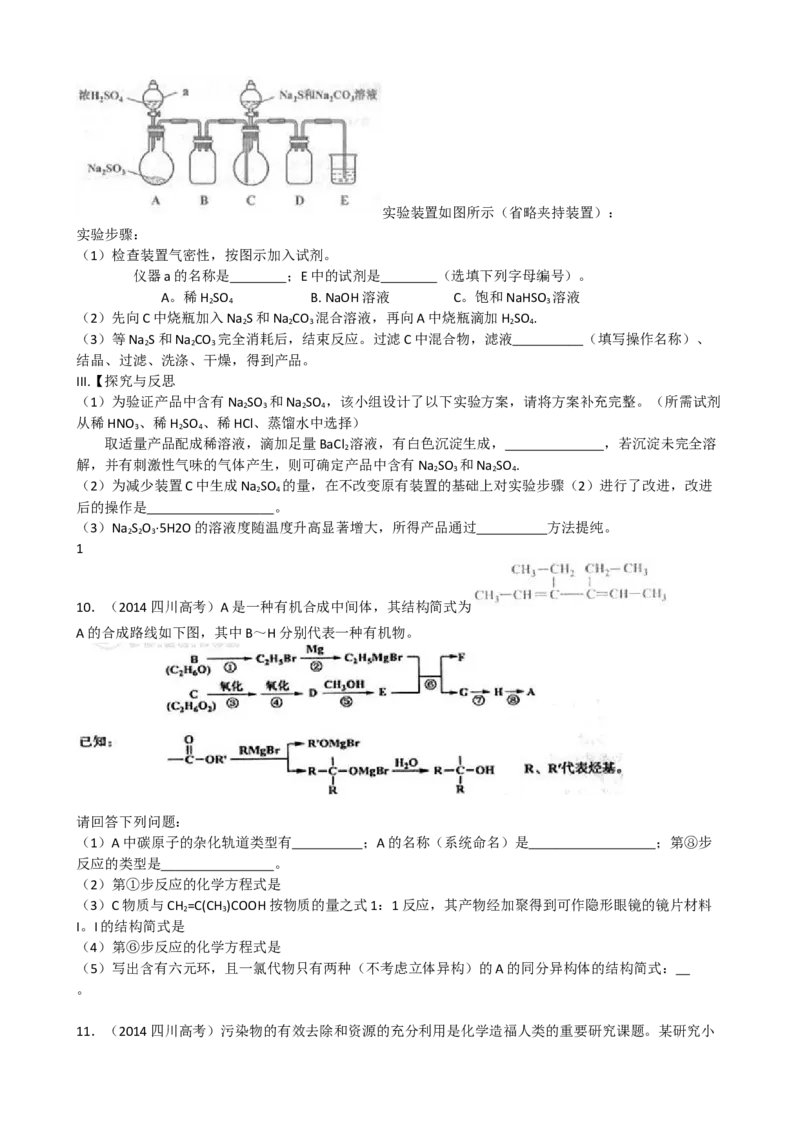
(3)Z与某元素形成的化合物的晶胞如图所示,晶胞中阴离子与阳离子的个数比是 。
(4)将R单质的粉末加入XH 的浓溶液中,通入Y ,充分反应后溶液呈深蓝色,该反应的离子方程式是
3 2
。
9.(2014四川高考)硫代硫酸钠一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体
(Na S O ·5H O).
2 2 3 2
I.【查阅资料】
(1)Na S O ·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl 溶液混合无沉淀生成。
2 2 3 2
(2)向Na CO 和Na S混合溶液中能入SO 可制得Na S O ;所得产品常含有少量Na SO 和Na SO .
2 3 2 2 2 2 3 2 3 2 4
(3)Na SO 易被氧化;BaSO 难溶于水,可溶于稀HCl。
2 3 3
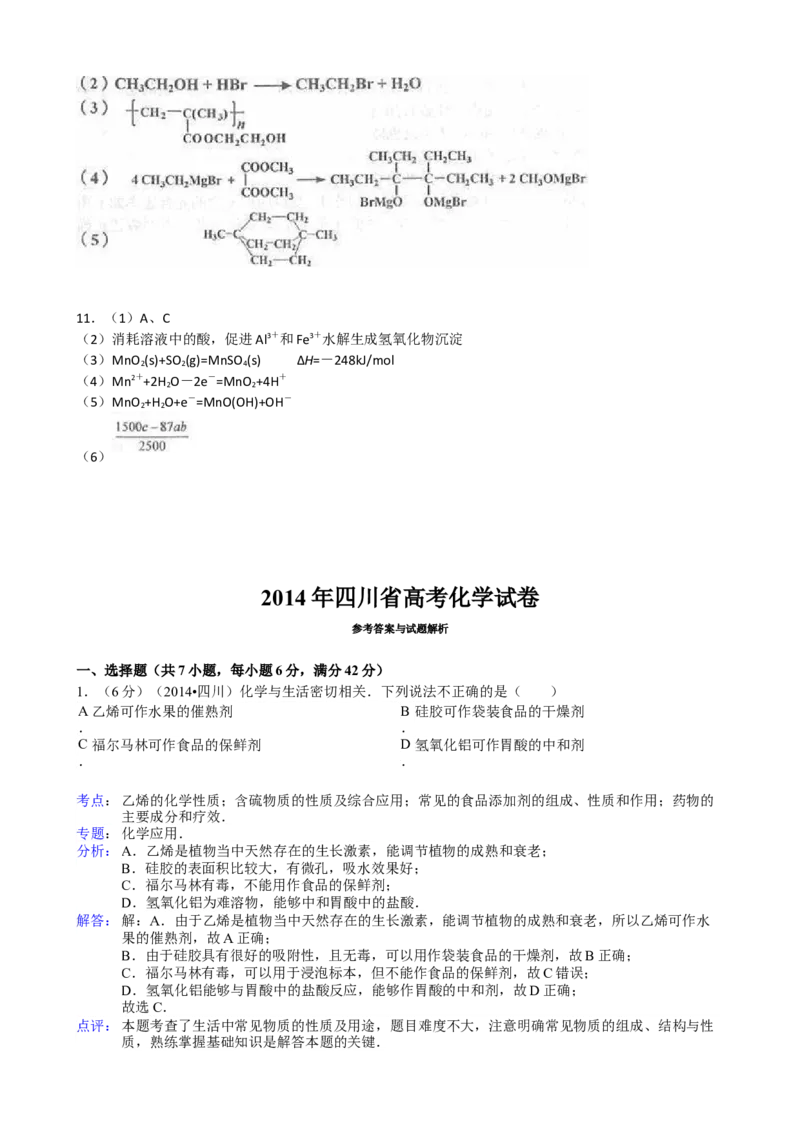
II.【制备产品】实验装置如图所示(省略夹持装置):
实验步骤:
(1)检查装置气密性,按图示加入试剂。
仪器a的名称是 ;E中的试剂是 (选填下列字母编号)。
A。稀H SO B. NaOH溶液 C。饱和NaHSO 溶液
2 4 3
(2)先向C中烧瓶加入Na S和Na CO 混合溶液,再向A中烧瓶滴加H SO .
2 2 3 2 4
(3)等Na S和Na CO 完全消耗后,结束反应。过滤C中混合物,滤液 (填写操作名称)、
2 2 3
结晶、过滤、洗涤、干燥,得到产品。
III.【探究与反思
(1)为验证产品中含有Na SO 和Na SO ,该小组设计了以下实验方案,请将方案补充完整。(所需试剂
2 3 2 4
从稀HNO 、稀H SO 、稀HCl、蒸馏水中选择)
3 2 4
取适量产品配成稀溶液,滴加足量BaCl 溶液,有白色沉淀生成, ,若沉淀未完全溶
2
解,并有刺激性气味的气体产生,则可确定产品中含有Na SO 和Na SO .
2 3 2 4
(2)为减少装置C中生成Na SO 的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进
2 4
后的操作是 。
(3)Na S O ·5H2O的溶液度随温度升高显著增大,所得产品通过 方法提纯。
2 2 3
1
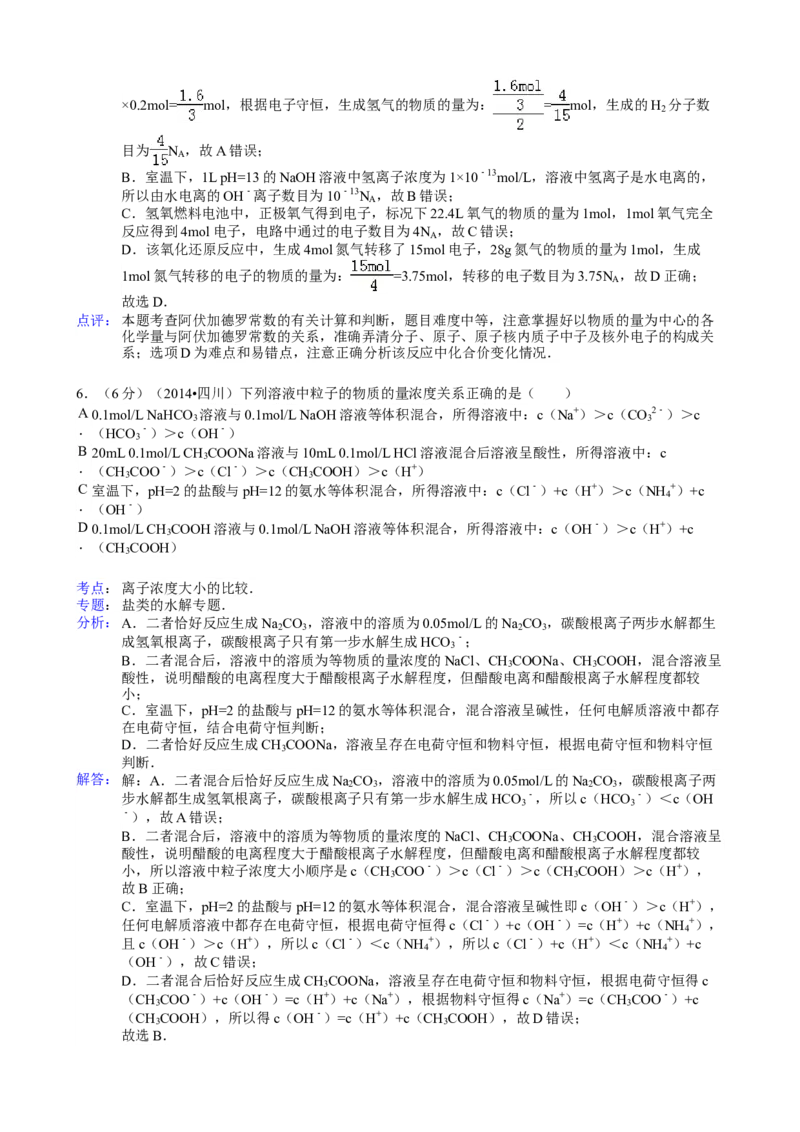
10.(2014四川高考)A是一种有机合成中间体,其结构简式为
A的合成路线如下图,其中B~H分别代表一种有机物。
请回答下列问题:
(1)A中碳原子的杂化轨道类型有 ;A的名称(系统命名)是 ;第⑧步
反应的类型是 。
(2)第①步反应的化学方程式是
(3)C物质与CH =C(CH )COOH按物质的量之式1:1反应,其产物经加聚得到可作隐形眼镜的镜片材料
2 3
I。I的结构简式是
(4)第⑥步反应的化学方程式是
(5)写出含有六元环,且一氯代物只有两种(不考虑立体异构)的A的同分异构体的结构简式:
。
11.(2014四川高考)污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO ,另含少量铁,铝,铜,镍等金属化合物)作脱硫剂,通过如下简化流
2
程,既脱除燃煤尾气中的SO ,又制得电池材料MnO (反应条件已省略)。
2 2
请回答下列问题:
(1)上述流程脱硫实现了 (选填下列字母编号)。
A。废弃物的综合利用 B。白色污染的减少 C。酸雨的减少
(2)用MnCO3能除去溶液中Al3+和Fe3+,其原因是 。
(3)已知:25℃、101kPa时,Mn(s)+O2(g)=MnO (s) ΔH=-520kJ/mol
2
S(s)+O2(g)=SO (g) ΔH=-297kJ/mol
2
Mn(s)+S(s)+2O2(g)=MnSO (s) ΔH=-1065kJ/mol
4
SO 与MnO 反应生成无水MnSO 的热化学方程式是
2 2 4
(4)MnO 可作超级电容材料。用惰性电极电解MnSO 溶液可制得MnO ,其阳极的电极反应式是
2 4 2
(5)MnO 是碱性锌锰电池的正极材料。碱性锌锰电池放电时,正极的电极反应式是
2
(6)假设脱除的SO 只与软锰矿浆中MnO 反应。按照图示流程,将a m3(标准状况)含SO 的体积分数为
2 2 2
b%的尾气通入矿浆,若SO 的脱除率为89.6%,最终得到MnO 的质量ckg,则除去铁、铝、铜、镍等杂质
2 2
时,所引入的锰元素相当于MnO kg。
2
《2014年普通高等学校招生考试四川卷化学试题》参考答案
1.C 2.A 3.D 4.B 5.D 6.B 7.C
8.(1)①1s22s22p4 ②Cl
(2)①V形 ②O
(3)2:1
(4)2Cu+8NH ·H O+O =2[Cu(NH ) ]2++4OH-+6H O
3 2 2 3 4 2
9.II(1)①分液漏斗 ②B ③蒸发
III(1)过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀HCl
(2)先向A中烧瓶滴加浓H SO ,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na S和
2 4 2
Na CO 混合溶液。
2 3
(3)重结晶
10.(1)①sp2、sp3 ②3,4-二乙基-2,4-已二烯 ③消去反应11.(1)A、C
(2)消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀
(3)MnO (s)+SO (g)=MnSO (s) ΔH=-248kJ/mol
2 2 4
(4)Mn2++2H O-2e-=MnO +4H+
2 2
(5)MnO +H O+e-=MnO(OH)+OH-
2 2
(6)
2014 年四川省高考化学试卷
参考答案与试题解析
一、选择题(共7小题,每小题6分,满分42分)
1.(6分)(2014•四川)化学与生活密切相关.下列说法不正确的是( )
A乙烯可作水果的催熟剂 B 硅胶可作袋装食品的干燥剂
. .
C 福尔马林可作食品的保鲜剂 D 氢氧化铝可作胃酸的中和剂
. .
考点:乙烯的化学性质;含硫物质的性质及综合应用;常见的食品添加剂的组成、性质和作用;药物的
主要成分和疗效.
菁优网版权所有
专题:化学应用.
分析:A.乙烯是植物当中天然存在的生长激素,能调节植物的成熟和衰老;
B.硅胶的表面积比较大,有微孔,吸水效果好;
C.福尔马林有毒,不能用作食品的保鲜剂;
D.氢氧化铝为难溶物,能够中和胃酸中的盐酸.
解答:解:A.由于乙烯是植物当中天然存在的生长激素,能调节植物的成熟和衰老,所以乙烯可作水
果的催熟剂,故A正确;
B.由于硅胶具有很好的吸附性,且无毒,可以用作袋装食品的干燥剂,故B正确;
C.福尔马林有毒,可以用于浸泡标本,但不能作食品的保鲜剂,故C错误;
D.氢氧化铝能够与胃酸中的盐酸反应,能够作胃酸的中和剂,故D正确;
故选C.
点评:本题考查了生活中常见物质的性质及用途,题目难度不大,注意明确常见物质的组成、结构与性
质,熟练掌握基础知识是解答本题的关键.2.(6分)(2014•四川)下列关于物质分类的说法正确的是( )
A金刚石、白磷都属于单质
.
B 漂白粉、石英都属于纯净物
.
C 氯化铵、次氯酸都属于强电解质
.
D葡萄糖、蛋白质都属于高分子化合物
.
考点:单质和化合物;混合物和纯净物;电解质与非电解质;有机高分子化合物的结构和性质.
菁优网版权所有
专题:物质的分类专题.
分析:A.由一种元素组成的纯净物是单质;
B.由一种物质组成的为纯净物;
C.完全电离的电解质是强电解质;
D.相对分子质量很大的化合物是高分子化合物,常见的天然有机高分子化合物有蛋白质、纤维
素和淀粉.
解答:解:A.由一种元素组成的纯净物是单质,金刚石、白磷都是由一种元素组成的纯净物,所以属
于单质,故A正确;
B.由一种物质组成的为纯净物,漂白粉的主要成分是氯化钙、次氯酸钙,所以为混合物,故B
错误;
C.完全电离的电解质是强电解质,次氯酸在水溶液里部分电离,为弱电解质,故C错误;
D.相对分子质量很大的化合物是高分子化合物,常见的天然有机高分子化合物有蛋白质、纤维
素和淀粉,葡萄糖是小分子有机物,故D错误;
故选A.
点评:本题考查了基本概念,明确单质、纯净物、强电解质、高分子化合物的概念是解本题关键,知道
常见物质的成分结合基本概念即可解答,题目难度不大.
3.(6分)(2014•四川)能正确表示下列反应的离子方程式的是( )
ACl 通入NaOH溶液:Cl +OH﹣═Cl﹣+ClO﹣+H O
2 2 2
.
B NaHCO 溶液中加入稀HCl:CO 2﹣+2H+═CO ↑+H O
3 3 2 2
.
C AlCl 溶液中加入过量稀氨水:Al3++4NH •H O═AlO ﹣+4NH ++2H O
3 3 2 2 4 2
.
DCu溶于稀HNO :3Cu+8H++2NO ﹣═3Cu2++2NO↑+4H O
3 3 2
.
考点:离子方程式的书写.
菁优网版权所有
专题:离子反应专题.
分析:A.原子不守恒;
B.碳酸氢根离子不能拆开;
C.氢氧化铝不溶于弱碱;
D.铜和稀硝酸反应生成硝酸铜、NO和水.
解答:解:A.原子不守恒,离子方程式为Cl +2OH﹣═Cl﹣+ClO﹣+H O,故A错误;
2 2
B.碳酸氢根离子不能拆开,离子方程式为HCO ﹣+H+═CO ↑+H O,故B错误;
3 2 2
C.氢氧化铝不溶于弱碱,离子方程式为Al3++3NH •H O=Al(OH) ↓+3NH +,故C错误;
3 2 3 4
D.铜和稀硝酸反应生成硝酸铜、NO和水,离子方程式为3Cu+8H++2NO ﹣═3Cu2+
3
+2NO↑+4H O,故D正确;
2
故选D.
点评:本题考查了离子方程式的书写,明确物质之间发生的反应是解本题关键,再结合离子方程式的书
写规则来分析解答,注意:有的化学反应与反应物的量有关,离子方程式书写是学习难点,也是
高考高频点,应熟练掌握.4.(6分)(2014•四川)下列实验方案中,不能达到实验目的是( )
选项实验目的 实验方案
A 检验CH CH Br在NaOH溶 将CH CH Br与NaOH溶液共热.冷却后,取出上层水溶液,用稀
3 2 3 2
液中是否发生水解 HNO 酸化,加入AgNO 溶液,观察是否产生淡黄色沉淀
3 3
B 检验Fe(NO ) 晶体是否已 将Fe(NO ) 样品溶于稀H SO 后,滴加KSCN溶液,观察溶液是否
3 2 3 2 2 4
氧化变质 变红
C 验证Br 的氧化性强于I 将少量溴水加入KI溶液中,再加入CCl ,振荡,静置.可观察到下层
2 2 4
液体呈紫色
D 验证Fe(OH) 的溶解度小 将FeCl 溶液加入Mg(OH) 悬浊液中,振荡,可观察到沉淀由白色
3 3 2
于Mg(OH) 变为红褐色
2
AA B B C C D D
. . . .
考点:化学实验方案的评价.
菁优网版权所有
专题:实验评价题.
分析:A.检验有机物中的溴元素时,先将溴元素转化为溴离子,再用硝酸酸化溶液,最后用硝酸银溶
液检验溴离子即可;
B.硝酸能将亚铁离子氧化为铁离子而干扰实验;
C.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.溶解度大的物质能向溶解度小的物质转化.
解答:解:A.检验有机物中的溴元素时,先将溴元素转化为溴离子,再用硝酸酸化溶液,最后用硝酸
银溶液检验溴离子,如果有淡黄色沉淀生成就说明含有溴元素,否则没有溴元素,故A正确;
B.加入稀硫酸后,酸性条件下,硝酸根离子具有强氧化性,能将亚铁离子氧化为铁离子而干扰实
验,所以不能实现实验目的,故B错误;
C.将少量溴水加入KI溶液中,再加入CCl ,振荡,静置.可观察到下层液体呈紫色,说明二者
4
发生氧化还原反应2I﹣+Br =2Br﹣+I ,溴是氧化剂、碘是氧化产物,所以溴的氧化性大于碘,所以
2 2
能实现实验目的,故C正确;
D.溶解度大的物质能向溶解度小的物质转化,将FeCl 溶液加入Mg(OH) 悬浊液中,振荡,
3 2
可观察到沉淀由白色变为红褐色,说明Fe(OH) 的溶解度小于Mg(OH) ,所以能实现实验目
3 2
的,故D正确;
故选B.
点评:本题考查了实验方案评价,明确实验原理是解本题关键,根据物质的性质来分析解答,易错选项
是AB,注意:用硝酸银检验溴离子时要先中和过量的碱,为易错点.
5.(6分)(2014•四川)设N 为阿伏伽德罗常数的值.下列说法正确的是( )
A
A高温下,0.2mol Fe与足量水蒸气反应,生成的H 分子数目为0.3N
2 A
.
B 室温下,1L pH=13的NaOH溶液中,由水电离的OH﹣离子数目为0.1N
A
.
C 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2N
A
.
D
5NH NO 2HNO +4N ↑+9H O反应中,生成28g N 时,转移的电子数目为3.75N
. 4 3 3 2 2 2 A
考点:阿伏加德罗常数.
菁优网版权所有
专题:阿伏加德罗常数和阿伏加德罗定律.
分析:A.铁与水蒸气反应生成的是四氧化三铁,根据电子守恒计算出生成氢气的物质的量及分子数;
B.氢氧化钠溶液的氢离子是水电离的,水电离的氢离子浓度为1×10﹣13mol/L;
C.氢氧燃料电池中,正极氧气得到电子,1mol氧气得到4mol电子;
D.该反应中,铵根离子中的氮原子被氧化成氮气,硝酸根离子中部分氮原子被氧化成氮气,生
成4mol氮气转移了15mol电子.
解答:
解:A.0.2mol铁与水蒸气完全反应生成四氧化三铁,失去电子的物质的量为:( ﹣0)×0.2mol= mol,根据电子守恒,生成氢气的物质的量为: = mol,生成的H 分子数
2
目为 N ,故A错误;
A
B.室温下,1L pH=13的NaOH溶液中氢离子浓度为1×10﹣13mol/L,溶液中氢离子是水电离的,
所以由水电离的OH﹣离子数目为10﹣13N ,故B错误;
A
C.氢氧燃料电池中,正极氧气得到电子,标况下22.4L氧气的物质的量为1mol,1mol氧气完全
反应得到4mol电子,电路中通过的电子数目为4N ,故C错误;
A
D.该氧化还原反应中,生成4mol氮气转移了15mol电子,28g氮气的物质的量为1mol,生成
1mol氮气转移的电子的物质的量为: =3.75mol,转移的电子数目为3.75N ,故D正确;
A
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各
化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关
系;选项D为难点和易错点,注意正确分析该反应中化合价变化情况.
6.(6分)(2014•四川)下列溶液中粒子的物质的量浓度关系正确的是( )
A0.1mol/L NaHCO 溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO 2﹣)>c
3 3
.(HCO ﹣)>c(OH﹣)
3
B 20mL 0.1mol/L CH COONa溶液与10mL 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c
3
.(CH COO﹣)>c(Cl﹣)>c(CH COOH)>c(H+)
3 3
C 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl﹣)+c(H+)>c(NH +)+c
4
.(OH﹣)
D0.1mol/L CH COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH﹣)>c(H+)+c
3
.(CH COOH)
3
考点:离子浓度大小的比较.
菁优网版权所有
专题:盐类的水解专题.
分析:A.二者恰好反应生成Na CO ,溶液中的溶质为0.05mol/L的Na CO ,碳酸根离子两步水解都生
2 3 2 3
成氢氧根离子,碳酸根离子只有第一步水解生成HCO ﹣;
3
B.二者混合后,溶液中的溶质为等物质的量浓度的NaCl、CH COONa、CH COOH,混合溶液呈
3 3
酸性,说明醋酸的电离程度大于醋酸根离子水解程度,但醋酸电离和醋酸根离子水解程度都较
小;
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,混合溶液呈碱性,任何电解质溶液中都存
在电荷守恒,结合电荷守恒判断;
D.二者恰好反应生成CH COONa,溶液呈存在电荷守恒和物料守恒,根据电荷守恒和物料守恒
3
判断.
解答:解:A.二者混合后恰好反应生成Na CO ,溶液中的溶质为0.05mol/L的Na CO ,碳酸根离子两
2 3 2 3
步水解都生成氢氧根离子,碳酸根离子只有第一步水解生成HCO ﹣,所以c(HCO ﹣)<c(OH
3 3
﹣),故A错误;
B.二者混合后,溶液中的溶质为等物质的量浓度的NaCl、CH COONa、CH COOH,混合溶液呈
3 3
酸性,说明醋酸的电离程度大于醋酸根离子水解程度,但醋酸电离和醋酸根离子水解程度都较
小,所以溶液中粒子浓度大小顺序是c(CH COO﹣)>c(Cl﹣)>c(CH COOH)>c(H+),
3 3
故B正确;
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,混合溶液呈碱性即c(OH﹣)>c(H+),
任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Cl﹣)+c(OH﹣)=c(H+)+c(NH +),
4
且c(OH﹣)>c(H+),所以c(Cl﹣)<c(NH +),所以c(Cl﹣)+c(H+)<c(NH +)+c
4 4
(OH﹣),故C错误;
D.二者混合后恰好反应生成CH COONa,溶液呈存在电荷守恒和物料守恒,根据电荷守恒得c
3
(CH COO﹣)+c(OH﹣)=c(H+)+c(Na+),根据物料守恒得c(Na+)=c(CH COO﹣)+c
3 3
(CH COOH),所以得c(OH﹣)=c(H+)+c(CH COOH),故D错误;
3 3
故选B.点评:本题考查了离子浓度大小比较,明确溶液中的溶质及溶液酸碱性再结合电荷守恒、物料守恒来分
析解答,离子浓度大小比较为高考高频点,常常与盐类水解、弱电解质电离结合考查,题目难度
中等.
7.(6分)(2014•四川)在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) ⇌M
(g)+N(g),所得实验数据如表:
实验编温度/℃ 起始时物质的量/mol 平衡时物质的量/mol
号 n(X) n(Y) n(M)
① 700 0.40 0.10 0.090
② 800 0.10 0.40 0.080
③ 800 0.20 0.30 a
④ 900 0.10 0.15 b
下列说法正确的是( )
A实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率v(N)
.=1.0×10﹣2mol/(L•min)
B 实验②中,该反应的平衡常数K=2.0
.
C 实验③中,达到平衡时,X的转化率为60%
.
D实验④中,达到平衡时,b>0.060
.
考点:真题集萃;化学平衡建立的过程.
菁优网版权所有
专题:化学平衡专题.
分析:
A、根据v= 计算v(M),在利用速率之比等于化学计量数之比计算v(N);
B、由表中数据,利用三段式计算平衡时其它组分的物质的量,由于反应中气体的化学计量数相
等,可以用物质的量代替浓度代入平衡常数表达式计算;
C、温度不变平衡常数不变,根据平衡常数可求出转化量,进而求出转化率;
D、对比实验①②的平衡常数可知,正反应为放热反应,升温平衡左移,平衡常数减小,转化率
减小,根据实验③中X的转化率为60%,则实验④中X的转化率小于60%,达到平衡时,b<
0.060.
解答:
解:A.v(N)=v(M)= = =1.0×10﹣3mol/(L•min),故A错误;
B. X(g)+Y(g) ⇌M(g)+N(g)
起始浓度(mol/L) 0.01 0.04 0 0
转化浓度(mol/L) 0.008 0.008 0.008 0.008
平衡浓度(mol/L) 0.002 0.032 0.008 0.008
实验②中,该反应的平衡常数K= = =1.0,故B错误;
C. X(g)+Y(g) ⇌M(g)+N(g)
起始浓度(mol/L) 0.02 0.03 0 0
转化浓度(mol/L)
平衡浓度(mol/L) 0.02﹣ 0.03﹣
该反应的平衡常数K= = =1.0,解得a=0.12,实验
③中,X的转化率= 100%=60%,故C正确;
D.根据三段式可求得,700℃时,化学平衡常数K≈2.6,升高温度至800℃得平衡常数为K=1.0,
K减小,即平衡逆向移动,则正反应为放热反应,若④的温度为800℃,恒容体系中,气体体积不变的反应,④与③为等效平衡,b= a=0.06mol,但④的实际温度为900℃,相比较800℃,平衡逆
向移动,b<0.06,故D错误;
故选C.
点评:本题考查化学反应速率、化学平衡常数、化学平衡的影响因素等,难度中等.
二、解答题(共4小题,满分58分)
8.(13分)(2014•四川)X、Y、Z、R为前四周期元素,且原子序数依次增大.XY 是红棕色气体;X
2
与氢元素可形成XH ;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子.
3
(1)Y基态原子的电子排布式是 1 s 2 2 s 2 2 p 4 ;Z所在周期中第一电离能最大的主族元素是 C l .
(2)XY ﹣离子的立体构型是 V 形 ;R2+的水合离子中,提供孤电子对的原子
2
是 O .
(3)Z与某元素形成的化合物的晶胞如图所示,晶胞中阴离子与阳离子的个数比是 2 : 1 .
(4)将R单质的粉末加入XH 的浓溶液中,通入Y ,充分反应后溶液呈深蓝色,该反应的离子方程式
3 2
是 2Cu+8NH •H O+O =2[Cu ( NH ) 2++4OH﹣+6H O .
3 2 2 3 4 2
]
考点:位置结构性质的相互关系应用.
菁优网版权所有
专题:元素周期律与元素周期表专题;化学键与晶体结构.
分析:X、Y、Z、R为前四周期元素,且原子序数依次增大,XY 是红棕色气体,应是NO ,则X为N
2 2
元素、Y为O元素;X与氢元素可形成NH ;Z基态原子的M层与K层电子数相等,则M层电子
3
数为2,故Z为Mg;R2+离子的3d轨道中有9个电子,R原子核外电子数=2+8+8+9+2=29,则R
为Cu元素,据此解答.
解答:解:X、Y、Z、R为前四周期元素,且原子序数依次增大,XY 是红棕色气体,应是NO ,则X
2 2
为N元素、Y为O元素;X与氢元素可形成NH ;Z基态原子的M层与K层电子数相等,则M层
3
电子数为2,故Z为Mg;R2+离子的3d轨道中有9个电子,R原子核外电子数=2+8+8+9+2=29,
则R为Cu元素,
(1)Y为O元素,基态原子的电子排布式是1s22s22p4,Z为Mg元素,所在周期中第一电离能最
大的主族元素是Cl元素,故答案为:1s22s22p4;Cl;
(2)NO ﹣离子中心N原子孤电子对= =1,价层电子对数=2+1=3,故NO ﹣离子的立
2 2
体构型是V形;Cu2+的水合离子中,提供孤电子对的原子是H O中O原子,
2
故答案为:V形;O;
(3)晶胞中阳离子处于体心与顶点,晶胞中阳离子数目=1+8× =2,阴离子处于处于体内及面
上,晶胞中阴离子数目=2+4× =4,故晶胞中阴离子与阳离子的个数比是4:2=2:1,故答案为:
2:1;
(4)将Cu单质的粉末加入NH 的浓溶液中,通入O ,充分反应后溶液呈深蓝色,说明得到四氨
3 2
合铜络离子,还应生成氢氧根离子与水,该反应的离子方程式是2Cu+8NH •H O+O =2[Cu
3 2 2
(NH ) 2++4OH﹣+6H O,
3 4 2
故答案为:2Cu+8NH •H O+O =2[Cu(NH ) 2++4OH﹣+6H O.
3 2 2 3 4 2
]
点评:本题是对物质结构的考查,涉及核外电子排布、电离能、分子结构、配合物、晶胞计算等,推断
元素是解题关键,注意掌握中学常见配合物,]难度中等.9.(13分)(2014•四川)硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体
(Na S O •5H O).
2 2 3 2
Ⅰ.【查阅资料】
(1)Na S O •5H O是无色透明晶体,易溶于水,其稀溶液与BaCl 溶液混合无沉淀生成.
2 2 3 2 2
(2)向Na CO 和Na S混合溶液中通入SO 可制得Na S O ,所得产品常含有少量Na SO 和Na SO .
2 3 2 2 2 2 3 2 3 2 4
(3)Na SO 易被氧化;BaSO 难溶于水,可溶于稀HCl.
2 3 3
Ⅱ.【产品制备】
实验装置如图所示(省略夹持装置):
实验步骤:
(1)检查装置气密性,按图示加入试剂.
仪器a的名称是 分液漏斗 ;E中的试剂是 B (选填下列字母编号).
A.稀H SO B.NaOH溶液 C.饱和NaHSO 溶液
2 4 3
(2)先向C中烧瓶加入Na S和Na CO 混合溶液,再向A中烧瓶滴加浓H SO .
2 2 3 2 4
(3)待Na S和Na CO 完全消耗后,结束反应.过滤C中混合物,滤液经 蒸发 (填操作名称)、结
2 2 3
晶、过滤、洗涤、干燥,得到产品.
Ⅲ.【探究与反思】
(1)为验证产品中含有Na SO 和Na SO ,该小组设计了以下实验方案,请将方案补充完整.
2 3 2 4
(所需试剂从稀HNO 、稀H SO 、稀HCl、蒸馏水中选择)
3 2 4
取适量产品配成稀溶液,滴加足量BaCl 溶液,有白色沉淀生成, 过滤,用蒸馏水洗涤沉淀,向沉淀中
2
加入足量稀盐酸 ,若沉淀未完全溶解,并有刺激性气味的气体产生,则可以确定产品中含有Na SO 和
2 3
Na SO .
2 4
(2)为减少装置C中生成Na SO 的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进
2 4
后的操作是 先向 A 中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向 C 中烧瓶加入硫化钠
和碳酸钠的混合溶液 .
(3)Na S O •5H O的溶解度随温度升高显著增大,所得产品通过 重结晶 方法提纯.
2 2 3 2
考点:真题集萃;制备实验方案的设计.
菁优网版权所有
专题:实验设计题.
分析:(1)仪器a的名称是 分液漏斗;E装置目的是吸收剩余的二氧化硫,因为二氧化硫能与氢氧化钠
溶液反应,与稀H SO 和饱和NaHSO 溶液不反应;
2 4 3
(3)根据将Na S O 结晶析出的操作分析;
2 2 3
Ⅲ.【探究与反思】
(1)根据:Na S O •5H O是无色透明晶体,易溶于水,其稀溶液与BaCl 溶液混合无沉淀生成;
2 2 3 2 2
Na SO 易被氧化;BaSO 难溶于水,可溶于稀HCl;BaSO 难溶于水,难溶于稀HCl;硝酸、硫
2 3 3 4
酸、盐酸等性质比较可知;
(2)根据亚硫酸钠易被氧化生成硫酸钠分析;
(3)根据重结晶的适用范围分析.
解答:解:(1)仪器a的名称是分液漏斗;E中的试剂是NaOH溶液,目的是吸收剩余的二氧化硫,因
为二氧化硫能与氢氧化钠溶液反应,与稀H SO 和饱和NaHSO 溶液不反应,
2 4 3故答案为:分液漏斗;B;
(3)将Na S O 结晶析出的操作应为:蒸发、结晶、过滤、洗涤、干燥,故答案为:蒸发;
2 2 3
Ⅲ.【探究与反思】
(1)根据:Na S O •5H O是无色透明晶体,易溶于水,其稀溶液与BaCl 溶液混合无沉淀生成;
2 2 3 2 2
Na SO 易被氧化;BaSO 难溶于水,可溶于稀HCl;BaSO 难溶于水,难溶于稀HCl,以及硝酸具
2 3 3 4
有强氧化性、加入硫酸会引入硫酸根离子可知,取适量产品配成稀溶液,滴加足量BaCl 溶液,
2
有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸,若沉淀未完全溶解,并
有刺激性气味的气体产生,则可以确定产品中含有Na SO 和Na SO ,
2 3 2 4
故答案为:过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸;
(2)因为亚硫酸钠易被氧化生成硫酸钠,所以为减少装置C中生成Na SO 的量,改进后的操作
2 4
是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳
酸钠的混合溶液,故答案为:先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再
向C中烧瓶加入硫化钠和碳酸钠的混合溶液;
(3)Na S O •5H O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯,故答案为:
2 2 3 2
重结晶.
点评:本题以某兴趣小组拟制备硫代硫酸钠晶体(Na S O •5H O)为载体,考查了物质的分离提纯、检
2 2 3 2
验、设计优化等,综合性较强.
10.(16分)(2014•四川)A是一种有机合成中间体,其结构为:
A的合成路线如图,其中B~H分别代表一种有机物.
已知: R、R′代表烃基.
请回答下列问题:
(1)A中碳原子的杂化轨道类型有 s p 2 、 s p 3 ;A的名称(系统命名)是 3 , 4﹣ 二乙基﹣ 2 , 4﹣ 己二
烯 ;第⑧步反应的类型是
消去反应 .
(2)第①步反应的化学方程式是 C H OH+HBr C H Br+H O .
2 5 2 5 2
(3)C物质与CH =C(CH )COOH按物质的量之比1:1反应,其产物经加聚得到可作隐形眼镜的镜片
2 3
材料I.I的结构简式是 .
(4)第⑥步反应的化学方程式是 .
(5)写出含有六元环,且一氯取代物只有2种(不考虑立体异构)的A的同分异构体的结构简式:
.
考点:真题集萃;有机物的推断.
菁优网版权所有
专题:有机物的化学性质及推断.分析:B为C H OH,C H OH与浓的氢溴酸发生取代反应生成C H Br;C H Br与镁反应生成
2 5 2 5 2 5 2 5
C H MgBr;C能发生2次催化氧化,故C为HOCH CH 0H,HOCH CH 0H发生2次催化氧化生
2 5 2 2 2 2
成D,故D为HOOC﹣COOH,HOOC﹣COOH与甲醇发生酯化反应生成E,E为 ;根据
已知信息可知, 与C H MgBr发生取代反应生成F和G,FCH OMgBr,G为
2 5 3
; 发生水解生成H,H为
, 在氢氧化钠/醇、加热条件下发生消去反应生成
A.依此进行分析,得出正确结论.
解答:解:(1)A中甲基碳原子含有4个σ键,所以C原子的杂化轨道类型为sp3,碳碳双键中C原子
的杂化轨道类型为sp2;A的系统命名法为:3,4﹣二乙基﹣2,4﹣己二烯;第⑧步反应为
在氢氧化钠/醇、加热条件下发生消去反应生成A,
故答案为:sp2、sp3;3,4﹣二乙基﹣2,4﹣己二烯;消去反应;
(2)第①步反应为:C H OH浓的氢溴酸发生取代反应生成C H Br,方程式为:C H OH+HBr
2 5 2 5 2 5
C H Br+H O,
2 5 2
故答案为:C H OH+HBr C H Br+H O;
2 5 2 5 2
(3)C为HOCH CH 0H,HOCH CH 0H与CH =C(CH )COOH按物质的量之比1:1发生酯化
2 2 2 2 2 3
反应生成CH =C(CH )COOCH CH 0H,CH =C(CH )COOCH CH 0H发生加聚反应生成I,I
2 3 2 2 2 3 2 2
为 ,
故答案为: ;
(4)第⑥步反应为: 与C H MgBr发生取代反应生成F和G,F为CH OMgBr,G为
2 5 3
,方程式为:
,
故答案为: ;
(5)A的同分异构体中含有六元环,且一氯取代物只有2种的结构简式为 ,
故答案为: .
点评:本题考查有机物的推断及相关方程式的书写,运用信息来推断物质是解答的关键,题目难度中等.
11.(16分)(2014•四川)污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题.某研
究小组利用软锰矿(主要成分为MnO ,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下
2
流程既脱除燃煤尾气中的SO ,又制得电池材料MnO (反应条件已省略).
2 2
请回答下列问题:
(1)上述流程脱硫实现了 A 、 C (选填下列字母编号).
A.废弃物的综合利用 B.白色污染的减少 C.酸雨的减少
(2)用MnCO 能除去溶液中Al3+和Fe3+,其原因是 消耗溶液中的酸,促进 A l 3 + 和 F e 3 + 水解生成氢氧化
3
物沉淀 .
(3)已知:25℃、101kPa时,
Mn(s)+O (g)═MnO (s)△H=﹣520kJ•mol﹣1
2 2
S(s)+O (g)═SO (g)△H=﹣297kJ•mol﹣1
2 2
Mn(s)+S(s)+2O (g)═MnSO (s)△H=﹣1065kJ•mol﹣1
2 4
SO 与MnO 反应生成无水MnSO 的热化学方程式是 MnO ( s ) +SO ( g ) =MnSO ( s )△ H=﹣
2 2 4 2 2 4
248kJ/mol .
(4)MnO 可作超级电容器材料.用惰性电极电解MnSO 溶液可制得MnO ,其阳极的电极反应式是
2 4 2
Mn 2+ +2H O﹣2e ﹣ =MnO +4H + .
2 2
(5)MnO 是碱性锌锰电池的正极材料.碱性锌锰电池放电时,正极的电极反应式是 MnO +H O+e ﹣
2 2 2
=MnO ( OH ) +OH ﹣ .
(6)假设脱硫的SO 只与软锰矿浆中MnO 反应.按照图示流程,将a m3(标准状况)含SO 的体积分
2 2 2
数为b%的尾气通入矿浆,若SO 的脱除率为89.6%,最终得到MnO 的质量为c kg,则除去铁、铝、铜、
2 2
镍等杂质时,所引入的锰元素相当于MnO kg.
2
考点:真题集萃;热化学方程式;原电池和电解池的工作原理;物质分离和提纯的方法和基本操作综合
应用;制备实验方案的设计.
菁优网版权所有
专题:实验设计题.
分析:二氧化硫能与二氧化锰反应生成硫酸锰,用MnCO 能除去溶液中Al3+和Fe3+,MnS将铜、镍离子
3
还原为单质,高锰酸钾能与硫酸锰反应生成二氧化锰.
(1)脱硫能减少酸雨;
(2)MnCO 消耗溶液中的酸,促进Al3+和Fe3+水解;
3
(3)根据盖斯定律解题;
(4)锰离子在阳极失电子;
(5)二氧化锰得电子生成MnO(OH);
(6)SO +MnO =MnSO ,根据方程式结合元素守恒解题.
2 2 4
解答:解:(1)脱硫能减少酸雨和废物在利用,故答案为:AC;
(2)MnCO 消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀,故答案为:消耗溶液中的
3
酸,促进Al3+和Fe3+水解生成氢氧化物沉淀;
(3)Mn(s)+O (g)═MnO (s)△H=﹣520kJ•mol﹣1
2 2
S(s)+O (g)═SO (g)△H=﹣297kJ•mol﹣1
2 2
Mn(s)+S(s)+2O (g)═MnSO (s)△H=﹣1065kJ•mol﹣1
2 4
将③﹣②﹣①可得MnO (s)+SO (g)=MnSO (s)△H=﹣248kJ/mol,故答案为:MnO (s)
2 2 4 2
+SO (g)=MnSO (s)△H=﹣248kJ/mol;
2 4(4)锰离子在阳极失电子:Mn2++2H O﹣2e﹣=MnO +4H+,故答案为:Mn2++2H O﹣2e﹣
2 2 2
=MnO +4H+;
2
(5)二氧化锰得电子生成MnO(OH),MnO +H O+e﹣=MnO(OH)+OH﹣,故答案为:
2 2
MnO +H O+e﹣=MnO(OH)+OH﹣;
2 2
(6)反应的二氧化硫的物质的量为 ×b%×89.6%=0.4abmol,根据SO +MnO =MnSO 可
2 2 4
知生成硫酸锰的物质的量为0.4abmol,最终生成的二氧化锰为c kg,设消耗硫酸锰的物质的量为
x.
2KMnO +3MnSO +2H O═5MnO +2H SO +K SO
4 4 2 2 2 4 2 4
3 87×5
x 1000c
x=
除去铁、铝、铜、镍等杂质时,所引入的锰元素( ﹣0.4ab)mol,
相当于MnO 的质量( ﹣0.4ab)mol×87g/mol=(600c﹣0.4ab×87)g= kg,故
2
答案为: .
点评:本题考查热化学方程式、原电池、电解池和化学计算等,侧重于学生的分析能力和实验能力的考
查,难度中等.