文档内容
2021 年普通高等学校招生全国统一考试(全国乙卷)
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,并将自己的姓
名、准考证号、座位号填写在本试卷上。
2.回答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标
号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案标号,涂写在本试卷上
无效。
3.作答非选择题时,将答案书写在答题卡上,书写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 Cl35.5 Fe
56
一、选择题
1. 我国提出争取在2030年前实现碳达峰,2060年实现碳中和,这对于改善环境,实现绿
色发展至关重要。碳中和是指CO 的排放总量和减少总量相当。下列措施中能促进碳中和
2
最直接有效的是
A. 将重质油裂解为轻质油作为燃料
B. 大规模开采可燃冰作为清洁燃料
C. 通过清洁煤技术减少煤燃烧污染
D. 研发催化剂将CO 还原为甲醇
2
【答案】D
【解析】
【分析】
【详解】A.将重质油裂解为轻质油并不能减少二氧化碳的排放量,达不到碳中和的目
的,故A不符合题意;
B.大规模开采可燃冰做为清洁燃料,会增大二氧化碳的排放量,不符合碳中和的要求,
故B不符合题意;
C.通过清洁煤技术减少煤燃烧污染,不能减少二氧化碳的排放量,达不到碳中和的目的,故C不符合题意;
D.研发催化剂将二氧化碳还原为甲醇,可以减少二氧化碳的排放量,达到碳中和的目
的,故D符合题意;
故选D。
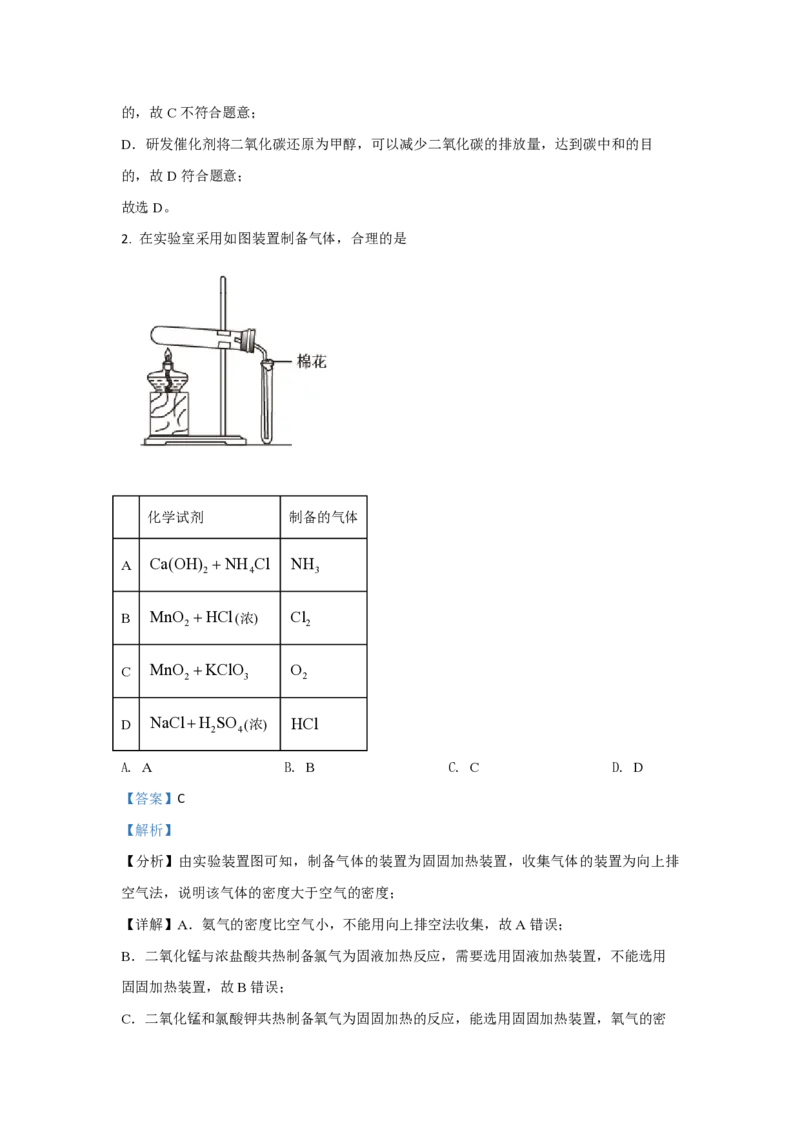
2. 在实验室采用如图装置制备气体,合理的是
化学试剂 制备的气体
A Ca(OH) NH Cl NH
2 4 3
B MnO HCl(浓) Cl
2 2
C MnO KClO O
2 3 2
D NaClH SO (浓) HCl
2 4
A. A B. B C. C D. D
【答案】C
【解析】
【分析】由实验装置图可知,制备气体的装置为固固加热装置,收集气体的装置为向上排
空气法,说明该气体的密度大于空气的密度;
【详解】A.氨气的密度比空气小,不能用向上排空法收集,故A错误;
B.二氧化锰与浓盐酸共热制备氯气为固液加热反应,需要选用固液加热装置,不能选用
固固加热装置,故B错误;
C.二氧化锰和氯酸钾共热制备氧气为固固加热的反应,能选用固固加热装置,氧气的密度大于空气,可选用向上排空气法收集,故C正确;
D.氯化钠与浓硫酸共热制备为固液加热反应,需要选用固液加热装置,不能选用固固加
热装置,故D错误;
故选C。
3. 下列过程中的化学反应,相应的离子方程式正确的是
A. 用碳酸钠溶液处理水垢中的硫酸钙:CO2 CaSO CaCO SO2
3 4 3 4
B. 过量铁粉加入稀硝酸中:Fe4H NO Fe3 NO2H O
3 2
C 硫酸铝溶液中滴加少量氢氧化钾溶液:Al3 4OH AlO 2H O
. 2 2
D. 氯化铜溶液中通入硫化氢:Cu2 S2 CuS
【答案】A
【解析】
【分析】
【详解】A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方
程式为:CO2+CaSO =CaCO +SO2,故A正确;
3 4 3 4
B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:
3Fe+8H++2NO=3Fe2++2NO↑+4H O,故B错误;
3 2
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:
Al3++3OH-=Al(OH) ↓,故C错误;
3
D.硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:
Cu2++H S=CuS↓+2H+,故D错误;
2
答案选A。
4. 一种活性物质的结构简式为 ,下
列有关该物质的叙述正确的是
A. 能发生取代反应,不能发生加成反应
B. 既是乙醇的同系物也是乙酸的同系物C. 与 互为同分异构体
D. 1mol该物质与碳酸钠反应得44gCO
2
【答案】C
【解析】
【分析】
【详解】A.该物质含有羟基、羧基、碳碳双键,能发生取代反应和加成反应,故 A错
误;
B.同系物是结构相似,分子式相差1个或n个CH 的有机物,该物质的分子式为
2
C H O ,而且与乙醇、乙酸结构不相似,故B错误;
10 18 3
C.该物质的分子式为C H O , 的分子式为
10 18 3
C H O ,所以二者的分子式相同,结构式不同,互为同分异构体,故C正确;
10 18 3
D.该物质只含有一个羧基,1mol该物质与碳酸钠反应,生成0.5mol二氧化碳,质量为
22g,故D错误;
故选C。
5. 我国嫦娥五号探测器带回1.731kg的月球土壤,经分析发现其构成与地球士壤类似土壤
中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15,X、
Y、Z为同周期相邻元素,且均不与W同族,下列结论正确的是
A. 原子半径大小顺序为W X Y Z
B. 化合物XW中的化学键为离子键
C. Y单质的导电性能弱于Z单质的
D. Z的氧化物的水化物的酸性强于碳酸
【答案】B
【解析】
【分析】由短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15, X、
Y、Z为同周期相邻元素,可知 W所在主族可能为第ⅢA族或第ⅥA族元素,又因 X、
Y、Z为同周期相邻元素,且均不与W同族,故W一定不是第ⅢA族元素,即W一定是第ⅥA族元素,进一步结合已知可推知 W、X、Y、Z依次为 O、Mg、Al、Si,据此答
题。
【详解】A.O原子有两层,Mg、Al、Si均有三层且原子序数依次增大,故原子半径大小
顺序为Mg>Al>Si>O,即X>Y>Z>W,A错误;
B.化合物XW即MgO为离子化合物,其中的化学键为离子键,B正确;
C.Y单质为铝单质,铝属于导体,导电性很强,Z单质为硅,为半导体,半导体导电性介
于导体和绝缘体之间,故Y单质的导电性能强于Z单质的,C错误;
D.Z的氧化物的水化物为硅酸,硅酸酸性弱于碳酸,D错误;
故选B。
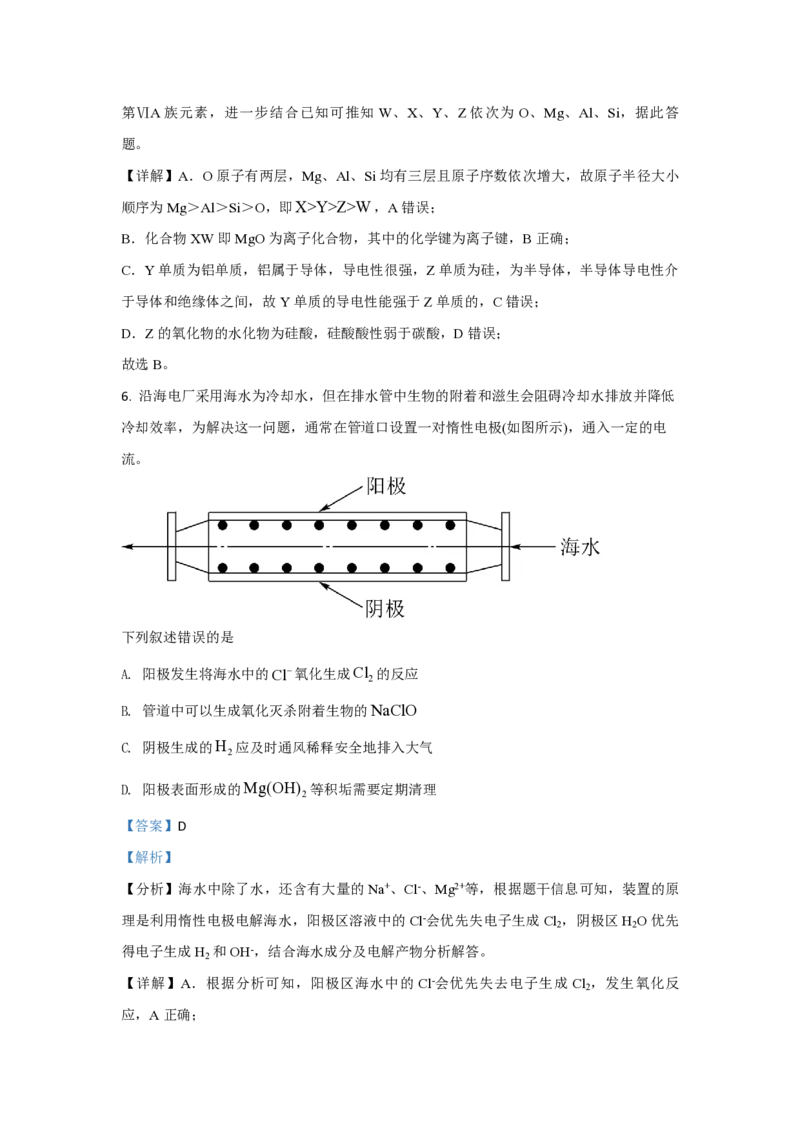
6. 沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并降低
冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电
流。
下列叙述错误的是
A. 阳极发生将海水中的Cl氧化生成Cl 的反应
2
B. 管道中可以生成氧化灭杀附着生物的NaClO
C. 阴极生成的H 应及时通风稀释安全地排入大气
2
D. 阳极表面形成的Mg(OH) 等积垢需要定期清理
2
【答案】D
【解析】
【分析】海水中除了水,还含有大量的Na+、Cl-、Mg2+等,根据题干信息可知,装置的原
理是利用惰性电极电解海水,阳极区溶液中的Cl-会优先失电子生成Cl ,阴极区H O优先
2 2
得电子生成H 和OH-,结合海水成分及电解产物分析解答。
2
【详解】A.根据分析可知,阳极区海水中的 Cl-会优先失去电子生成 Cl ,发生氧化反
2
应,A正确;B.设置的装置为电解池原理,根据分析知,阳极区生成的Cl 与阴极区生成的OH-在管道
2
中会发生反应生成NaCl、NaClO和H O,其中NaClO具有强氧化性,可氧化灭杀附着的
2
生物,B正确;
C.因为H 是易燃性气体,所以阳极区生成的H 需及时通风稀释,安全地排入大气,以
2 2
排除安全隐患,C正确;
D.阴极的电极反应式为:2H O+2e-=H ↑+2OH-,会使海水中的Mg2+沉淀积垢,所以阴极
2 2
表面会形成Mg(OH) 等积垢需定期清理,D错误。
2
故选D。
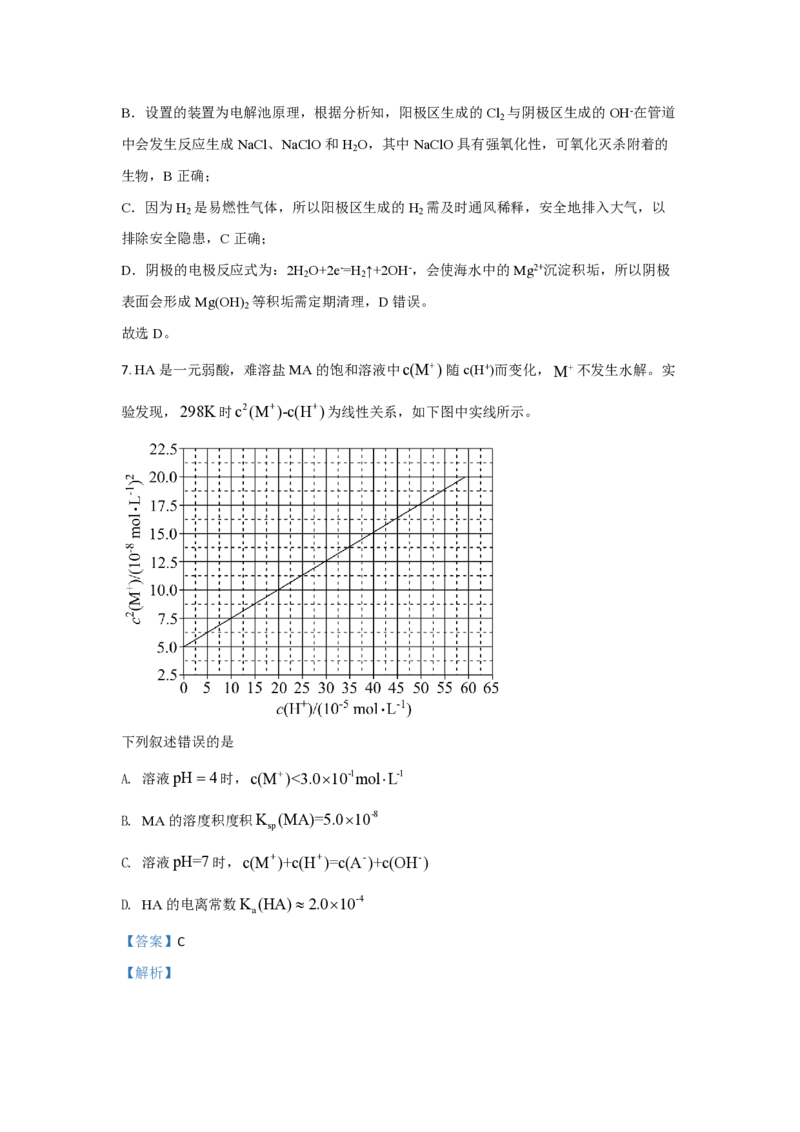
7. HA是一元弱酸,难溶盐MA的饱和溶液中c(M)随c(H+)而变化,M不发生水解。实
验发现,298K时c2(M+)-c(H+)为线性关系,如下图中实线所示。
下列叙述错误的是
A. 溶液pH4时,c(M)<3.010-1molL-1
B. MA的溶度积度积K (MA)=5.010-8
sp
C. 溶液pH=7时,c(M+)+c(H+)=c(A-)+c(OH-)
D. HA的电离常数K (HA)2.010-4
a
【答案】C
【解析】c(H+)c(A-)
【 分 析 】 由 题 意 可 知 HA是 一 元 弱 酸 , 其 电 离 常 数 K (HA)= ;
a
c(HA)
K (MA)
K (MA)=c(M+)×c(A-),联立二式可得线性方程c2(M+)=c(H+) sp +K (MA)。
sp K (HA) sp
a
【详解】A.由图可知 pH=4,即 c(H+)=10×10-5mol/L时,c2(M+)=7.5×10-8mol2/L2,c(M+)=
7.510-8mol/L= 7.510-4mol/L<3.0×10-4mol/L,A正确;
B.当c(H+)=0mol/L时,c2(M+)=5.0×10-8,结合分析可知5.0×10-8=
K (MA)
0 sp +K (MA)=K (MA),B正确;
K (HA) sp sp
a
C.设调pH所用的酸为H X,则结合电荷守恒可知c(M+)+c(H+)=c(A-)+c(OH-)+
n
nc(Xn-),题给等式右边缺阴离子部分nc(Xn-),C错误;
D.当c(H+)=20×10-5mol/L时,c2(M+)=10.0×10-8mol2/L2,结合K (MA)=5.010-8 B代入
sp
5.010-8
线性方程有10.0×10-8=210-4 +5.010-8,解得K (HA)2.010-4,D正
K (HA) a
a
确;
选C。
三、非选择题:共 174分。第 22~32 为必考题,每个试题考生都必须作答。第
33~38 题为选考题,考生根据要求作答。
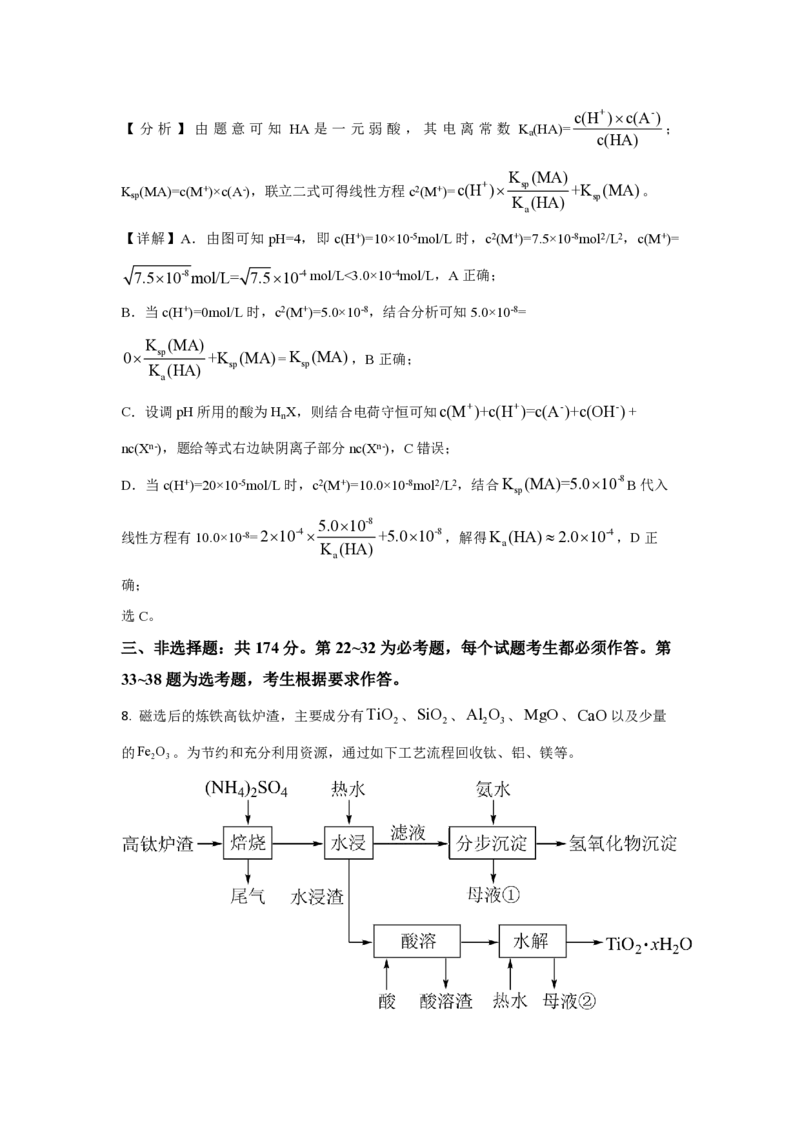
8. 磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、CaO以及少量
2 2 2 3
的Fe O 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3 Al3 Mg2 Ca2
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全
c=1.0105molL1
的pH 3.2 4.7 11.1 13.8
回答下列问题:
(1)“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、MgO、CaO、Fe O 转化为相应
2 2 2 3 2 3
的硫酸盐,写出Al O 转化为NH AlSO 的化学方程式_______。
2 3 4 4 2
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析出
的金属离子是_______。
(3)“母液①"中Mg2+浓度为_______molL-1。
(4)“水浸渣”在160℃“酸溶”最适合的酸是_______。“酸溶渣”的成分是_______、_______。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2水解析出TiO xH O沉淀,该反应的离子
2 2
方程式是_______。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得_______,循环利用。
焙烧
【答案】 (1). Al O 4MH SO 2NH AlSO 6NH 3H O
2 3 4 2 4 4 4 2 3 2
(2). Fe3+、Al3+、Mg2+ (3). 1.0106 (4). 硫酸 (5). SiO (6). CaSO
2 4
(7). TiO2++(x+1)H 2 O TiO 2 xH 2 O+2H (8). (NH 4 ) 2 SO 4
【解析】
【分析】由题给流程可知,高钛炉渣与硫酸铵混合后焙烧时,二氧化钛和二氧化硅不反
应,氧化铝、氧化镁、氧化钙、氧化铁转化为相应的硫酸盐,尾气为氨气;将焙烧后物质
加入热水水浸,二氧化钛、二氧化硅不溶于水,微溶的硫酸钙部分溶于水,硫酸铁、硫酸
镁和硫酸铝铵溶于水,过滤得到含有二氧化钛、二氧化硅、硫酸钙的水浸渣和含有硫酸
铁、硫酸镁、硫酸铝铵和硫酸钙的滤液;向pH约为2.0的滤液中加入氨水至11.6,溶液中铁离子、铝离子和镁离子依次沉淀,过滤得到含有硫酸铵、硫酸钙的母液①和氢氧化物沉
淀;向水浸渣中加入浓硫酸加热到160℃酸溶,二氧化硅和硫酸钙与浓硫酸不反应,二氧
化钛与稀硫酸反应得到 TiOSO ,过滤得到含有二氧化硅、硫酸钙的酸溶渣和 TiOSO 溶
4 4
液;将TiOSO 溶液加入热水稀释并适当加热,使TiOSO 完全水解生成TiO ·x H O沉淀
4 4 2 2
和硫酸,过滤得到含有硫酸的母液②和TiO ·x H O。
2 2
【详解】(1)氧化铝转化为硫酸铝铵发生的反应为氧化铝、硫酸铵在高温条件下反应生成硫
焙烧
酸 铝 铵 、 氨 气 和 水 , 反 应 的 化 学 方 程 式 为 Al O +4(NH ) SO
2 3 4 2 4
焙烧
NH Al(SO ) +4NH ↑+3H O, 故 答 案 为 : Al O +4(NH ) SO
4 4 2 3 2 2 3 4 2 4
NH Al(SO ) +4NH ↑+3H O;
4 4 2 3 2
(2)由题给开始沉淀和完全沉淀的pH可知,将pH约为2.0的滤液加入氨水调节溶液pH为
11.6时,铁离子首先沉淀、然后是铝离子、镁离子,钙离子没有沉淀,故答案为:Fe3+、
Al3+、Mg2+;
(3)由镁离子完全沉淀时,溶液pH为11.1可知,氢氧化镁的溶度积为1×10—5×(1×10—
110-10.8
2.9)2=1×10—10.8,当溶液pH为11.6时,溶液中镁离子的浓度为 =1×10—
(110-2.4)2
6mol/L,故答案为:1×10—6;
(4)增大溶液中硫酸根离子浓度,有利于使微溶的硫酸钙转化为沉淀,为了使微溶的硫酸钙
完全沉淀,减少TiOSO 溶液中含有硫酸钙的量,应加入浓硫酸加热到160℃酸溶;由分析
4
可知,二氧化硅和硫酸钙与浓硫酸不反应,则酸溶渣的主要成分为二氧化硅和硫酸钙,故
答案为:硫酸;SiO 、CaSO ;
2 4
(5)酸溶后将TiOSO 溶液加入热水稀释并适当加热,能使TiOSO 完全水解生成TiO ·x
4 4 2
H O沉淀和硫酸,反应的离子方程式为TiO2++(x+1)H OΔTiO ·xH O+2H+,故答案
2 2 2 2
为:TiO2++(x+1)H OΔTiO ·xH O+2H+;
2 2 2
(6)由分析可知,尾气为氨气,母液①为硫酸铵、母液②为硫酸,将母液①和母液②混合后
吸收氨气得到硫酸铵溶液,可以循环使用,故答案为:(NH ) SO 。
4 2 4
9. 氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重要的应用前景,通过氧化
剥离石墨制备氧化石墨烯的一种方法如下(转置如图所示):Ⅰ.将浓H SO 、NaNO 、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢
2 4 3
加入KMnO 粉末,塞好瓶口。
4
Ⅱ.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加H O 至悬浊液由紫色
2 2
变为土黄色。
Ⅳ.离心分离,稀盐酸洗涤沉淀。
Ⅴ.蒸馏水洗涤沉淀。
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
回答下列问题:
(1)装置图中,仪器a、c的名称分别是_______、_______,仪器b的进水口是_______(填字
母)。
(2)步骤Ⅰ中,需分批缓慢加入KMnO 粉末并使用冰水浴,原因是_______。
4
(3)步骤Ⅱ中的加热方式采用油浴,不使用热水浴,原因是_______。
(4)步骤Ⅲ中,H O 的作用是_______(以离子方程式表示)。
2 2
(5)步骤Ⅳ中,洗涤是否完成,可通过检测洗出液中是否存在SO2来判断。检测的方法是
4
_______。
(6)步骤Ⅴ可用pH试纸检测来判断Cl是否洗净,其理由是_______。
【答案】 (1). 滴液漏斗 (2). 三颈烧瓶 (3). d (4). 反应放热,使反应过快
(5). 反 应 温 度 接 近 水 的 沸 点 , 油 浴 更 易 控 温 (6).2MnO 5H O 6H 2Mn2 8H O5O (7). 取少量洗出液,滴加BaCl
4 2 2 2 2 2
,没有白色沉淀生成 (8). H+与Cl-电离平衡,洗出液接近中性时,可认为Cl-洗净
【解析】
【分析】
【详解】(1)由图中仪器构造可知,a的仪器名称为滴液漏斗,c的仪器名称为三颈烧瓶;
仪器b为球形冷凝管,起冷凝回流作用,为了是冷凝效果更好,冷却水要从d口进,a口
出,故答案为:分液漏斗;三颈烧瓶;d;
(2)反应为放热反应,为控制反应速率,避免反应过于剧烈,需分批缓慢加入KMnO 粉末
4
并使用冰水浴,故答案为:反应放热,使反应过快;
(3)油浴和水浴相比,由于油的比热容较水小,油浴控制温度更加灵敏和精确,该实验反应
温度接近水的沸点,故不采用热水浴,而采用油浴,故答案为:反应温度接近水的沸点,
油浴更易控温;
(4)由滴加H O 后发生的现象可知,加入的目的是除去过量的KMnO ,则反应的离子方程
2 2 4
式为:2MnO+5H O +6H+=2Mn2++5O ↑+8H O,故答案为:2MnO
4 2 2 2 2 4
+5H O +6H+=2Mn2++5O ↑+8H O ;
2 2 2 2
(5)该实验中为判断洗涤是否完成,可通过检测洗出液中是否存在SO2来判断,检测方法
4
是:取最后一次洗涤液,滴加BaCl 溶液,若没有沉淀说明洗涤完成,故答案为:取少量
2
洗出液,滴加BaCl ,没有白色沉淀生成;
2
(6)步骤IV用稀盐酸洗涤沉淀,步骤V洗涤过量的盐酸,H+与Cl-电离平衡,洗出液接近
中性时,可认为Cl-洗净,故答案为:H+与Cl-电离平衡,洗出液接近中性时,可认为
Cl-洗净。
10. 一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有机
合成中的碘化剂。回答下列问题:
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而错
过了一种新元素的发现,该元素是_______。
(2)氯铂酸钡(BaPtCl )固体加热时部分分解为BaCl 、Pt和Cl ,376.8℃时平衡常数
6 2 2
K′1.0104Pa2,在一硬质玻璃烧瓶中加入过量BaPtCl
,抽真空后,通过一支管通入
p 6碘蒸气(然后将支管封闭),在376.8℃,碘蒸气初始压强为20.0kPa。376.8℃平衡时,测得
烧瓶中压强为32.5kPa,则p =_______kPa,反应2ICl(g)Cl (g)I (g)的平衡常数
ICl 2 2
K=_______(列出计算式即可)。
(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数K 。
p
2NO(g)+2ICl(g)
2NOCl(g)+I
2
(g) K
p1
2NOCl(g)
2NO(g)+Cl
2
(g) K
p2
1 1
得到lgK ~ 和lgK ~ 均为线性关系,如下图所示:
p1 T p2 T
①由图可知,NOCl分解为NO和Cl 反应的ΔH_______0(填“大于”或“小于”)
2
②反应2ICl(g)Cl (g)I (g)的K=_______(用K 、K 表示):该反应的ΔH
2 2 p1 p2
_______0(填“大于”或“小于”),写出推理过程_______。
(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
NOClhvNOCl
NOClNOCl 2NOCl
2
其中hv表示一个光子能量,NOCl*表示NOCl的激发态。可知,分解1mol的NOCl需要
吸收_______mol光子。1007.6103
【答案】 (1). 溴(或Br) (2). 24.8 (3). (4). 大于 (5).
(24.8103)2
1 1
K K (6). 大 于 (7). 设 T T, 即 < , 由 图 可 知 :
p1 p2 T′ T
lgK (T')lgK (T)> lgK (T')lgK (T) lgK (T)lgK (T')则 :
p2 p2 p1 p1 p1 p1
lgK (T')K (T') lgK (T)K (T),即k(T')>k(T),因此该反应正反应为吸热
p2 p1 p2 p1
反应,即ΔH大于0 (8). 0.5
【解析】
【分析】
【详解】(1)红棕色液体,推测为溴单质,因此错过发现的元素是溴(或Br);
(2)由题意玻376.8℃时璃烧瓶中发生两个反应:BaPtCl
6
(s) BaCl
2
(s)+Pt(s)+2Cl
2
(g)、
Cl
2
(g)+I
2
(g)2ICl(g)。BaPtCl
6
(s) BaCl
2
(s)+Pt(s)+2Cl
2
(g)的平衡常数
K′1.0104Pa2,则平衡时p2(Cl )=1.0104Pa2,平衡时p(Cl )=100Pa,设到达平衡时
p 2 2
Cl (g)+ I (g) 2ICl(g)
2 2
开始/(kPa) 20.0 0
I (g)的分压减小pkPa,则 ,376.8℃平衡时,测得
2 变化/(kPa) p 2p
平衡/(kPa) 0.1 20.0-p 2p
烧瓶中压强为32.5kPa,则0.1+20.0+p=32.5,解得p=12.4,则平衡时p =2pkPa
ICl
=2×12.4kPa=24.8kPa;则平衡时,I (g)的分压为(20.0-p)kPa=7.6kPa=7.6×103Pa,p =
2 ICl
24.8kPa=24.8×103Pa,p(Cl )=0.1kPa=100Pa,因此反应2ICl(g)Cl (g)I (g)的平衡常数
2 2 2
1007.6103
K= ;
(24.8103)2
1
(3)①结合图可知,温度越高, 越小,lgKp 越大,即Kp 越大,说明升高温度平衡
2 2
T
2NOCl(g) 2NO(g)+Cl 2 (g)正向移动,则NOCl分解为NO和Cl 2 反应的大于0;
②Ⅰ.2NO(g)+2ICl(g)
2NOCl(g)+I
2
(g) K
p1
Ⅱ.2NOCl(g)
2NO(g)+Cl
2
(g) K
p2
Ⅰ+Ⅱ得2ICl(g)Cl (g)I (g),则2ICl(g)Cl (g)I (g)的K=K K ;该反应的
2 2 2 2 p1 p21 1
ΔH大于0;推理过程如下:设T T,即 < ,由图可知:
T′ T
lgK (T')lgK (T)> lgK (T')lgK (T) lgK (T)lgK (T')则:
p2 p2 p1 p1 p1 p1
lgK (T')K (T') lgK (T)K (T),即k(T')>k(T),因此该反应正反应为吸热
p2 p1 p2 p1
反应,即ΔH大于0;
(4)Ⅰ.NOClhvNOCl
Ⅱ.NOClNOCl 2NOCl
2
Ⅰ+Ⅱ得总反应为2NOCl+hv=2NO+Cl ,因此2molNOCl分解需要吸收1mol光子能量,则
2
分解1mol的NOCl需要吸收0.5mol光子。
11. 过渡金属元素铬
Cr
是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应
用。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是_______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。CrNH H O Cl 2 中提供电子对形成配位
3 3 2 2
键的原子是_______,中心离子的配位数为_______。
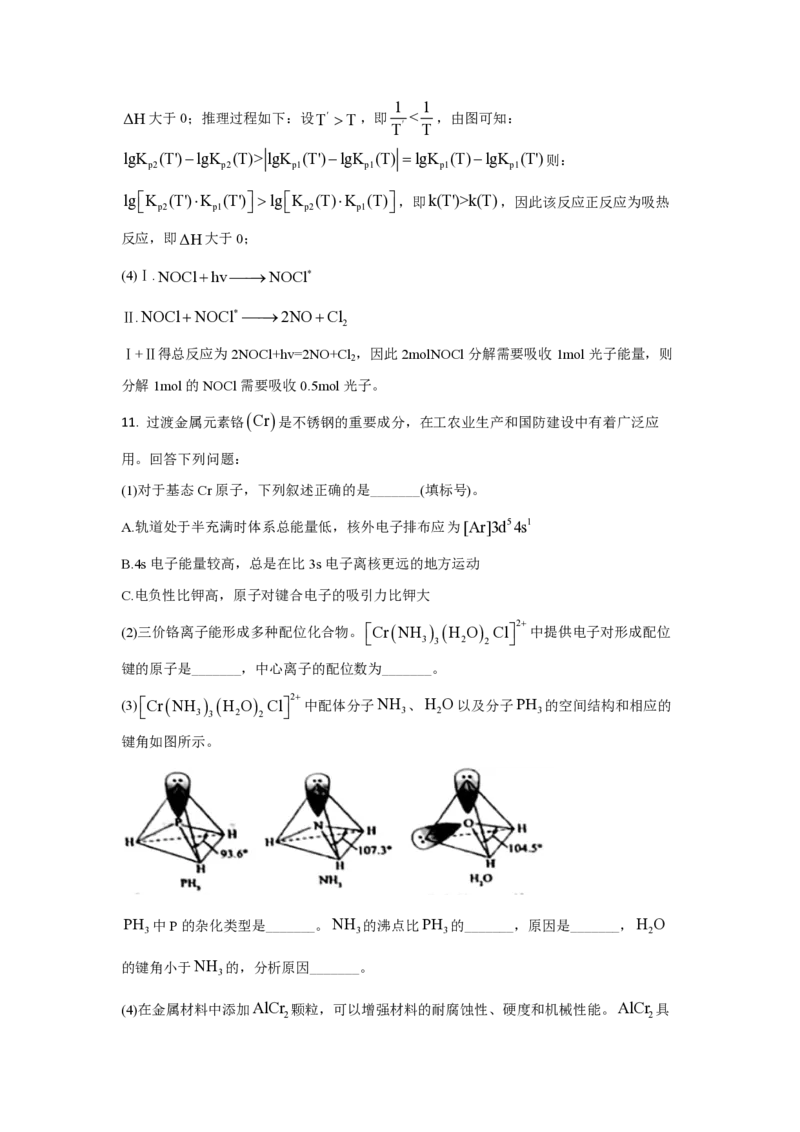
(3)CrNH H O Cl 2 中配体分子NH 、H O以及分子PH 的空间结构和相应的
3 3 2 2 3 2 3
键角如图所示。
PH 中P的杂化类型是_______。NH 的沸点比PH 的_______,原因是_______,H O
3 3 3 2
的键角小于NH 的,分析原因_______。
3
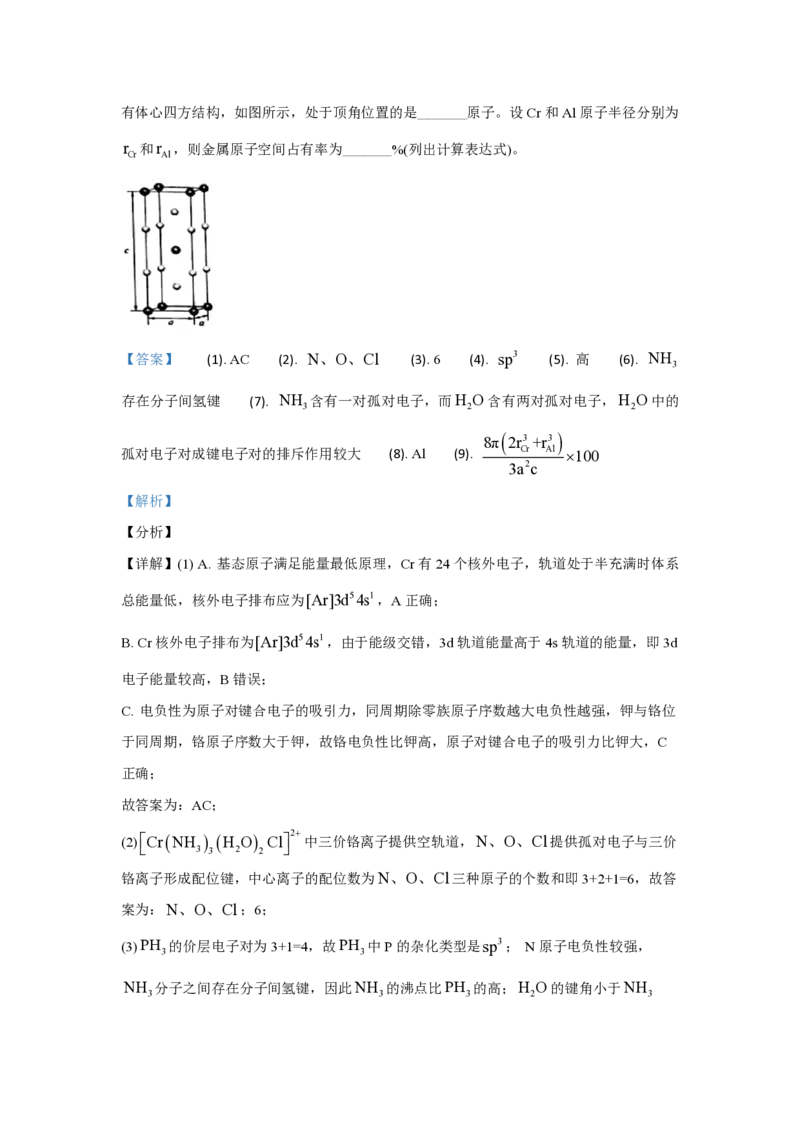
(4)在金属材料中添加AlCr 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr 具
2 2有体心四方结构,如图所示,处于顶角位置的是_______原子。设Cr和Al原子半径分别为
r 和r ,则金属原子空间占有率为_______%(列出计算表达式)。
Cr Al
【答案】 (1). AC (2). N、O、Cl (3). 6 (4). sp3 (5). 高 (6). NH
3
存在分子间氢键 (7). NH 含有一对孤对电子,而H O含有两对孤对电子,H O中的
3 2 2
8π 2r3 +r3
孤对电子对成键电子对的排斥作用较大 (8). Al (9). Cr Al 100
3a2c
【解析】
【分析】
【详解】(1) A. 基态原子满足能量最低原理,Cr有24个核外电子,轨道处于半充满时体系
总能量低,核外电子排布应为[Ar]3d54s1,A正确;
B. Cr核外电子排布为[Ar]3d54s1,由于能级交错,3d轨道能量高于4s轨道的能量,即3d
电子能量较高,B错误;
C. 电负性为原子对键合电子的吸引力,同周期除零族原子序数越大电负性越强,钾与铬位
于同周期,铬原子序数大于钾,故铬电负性比钾高,原子对键合电子的吸引力比钾大,C
正确;
故答案为:AC;
(2)CrNH H O Cl 2 中三价铬离子提供空轨道,N、O、Cl提供孤对电子与三价
3 3 2 2
铬离子形成配位键,中心离子的配位数为N、O、Cl三种原子的个数和即3+2+1=6,故答
案为:N、O、Cl;6;
(3)PH 的价层电子对为3+1=4,故PH 中P的杂化类型是sp3; N原子电负性较强,
3 3
NH 分子之间存在分子间氢键,因此NH 的沸点比PH 的高;H O的键角小于NH
3 3 3 2 3的,原因是:NH 含有一对孤对电子,而H O含有两对孤对电子,H O中的孤对电子对
3 2 2
成键电子对的排斥作用较大,故答案为:sp3;高;NH 存在分子间氢键;NH 含有一对
3 3
孤对电子,而H O含有两对孤对电子,H O中的孤对电子对成键电子对的排斥作用较
2 2
大;
1
(4)已知AlCr 具有体心四方结构,如图所示,黑球个数为8 +1=2,白球个数为
2 8
1
8 +2=4,结合化学式AlCr 可知,白球为Cr,黑球为Al,即处于顶角位置的是Al原
4 2
子。设Cr和Al原子半径分别为r 和r ,则金属原子的体积为
Cr Al
8π(2r3 +r3 )
4πr3 4πr3 8π(2r3 +r3 ) Cr Al
Cr 4+ Al 2= Cr Al ,故金属原子空间占有率= 3
3 3 3 100%=
a2c
8π 2r3 +r3 8π 2r3 +r3
Cr Al 100%,故答案为:Al; Cr Al 100。
3a2c 3a2c
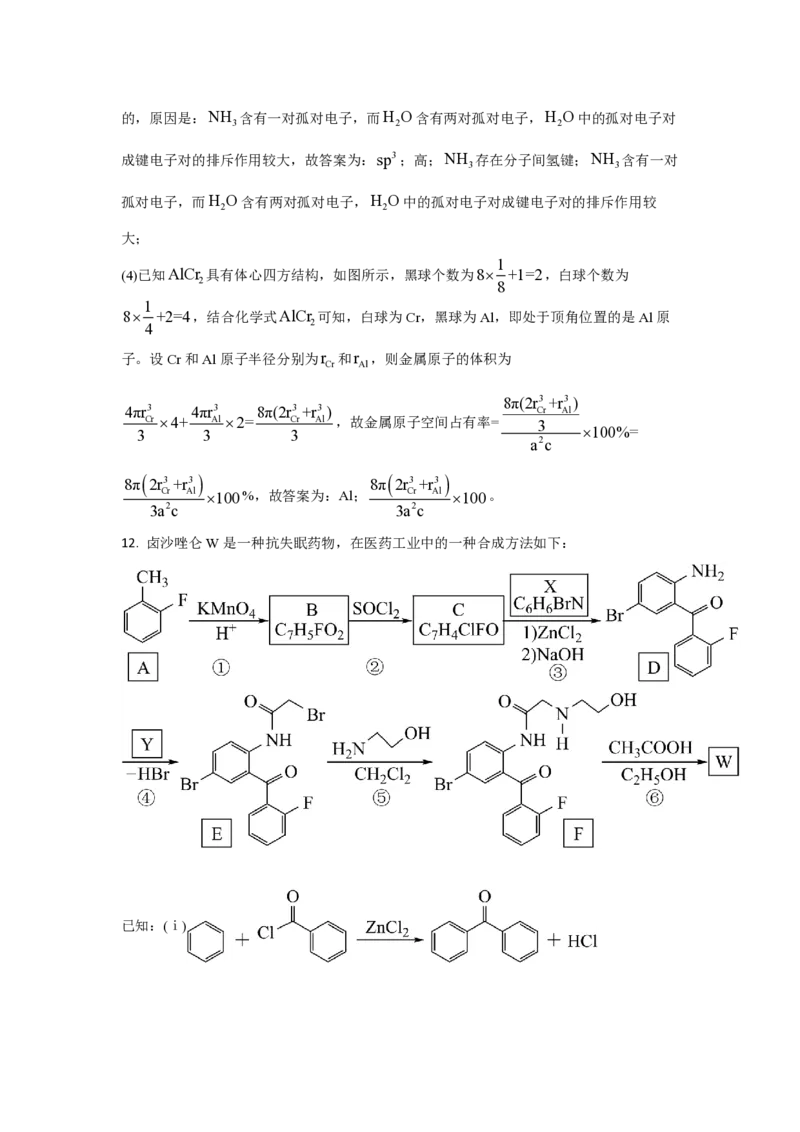
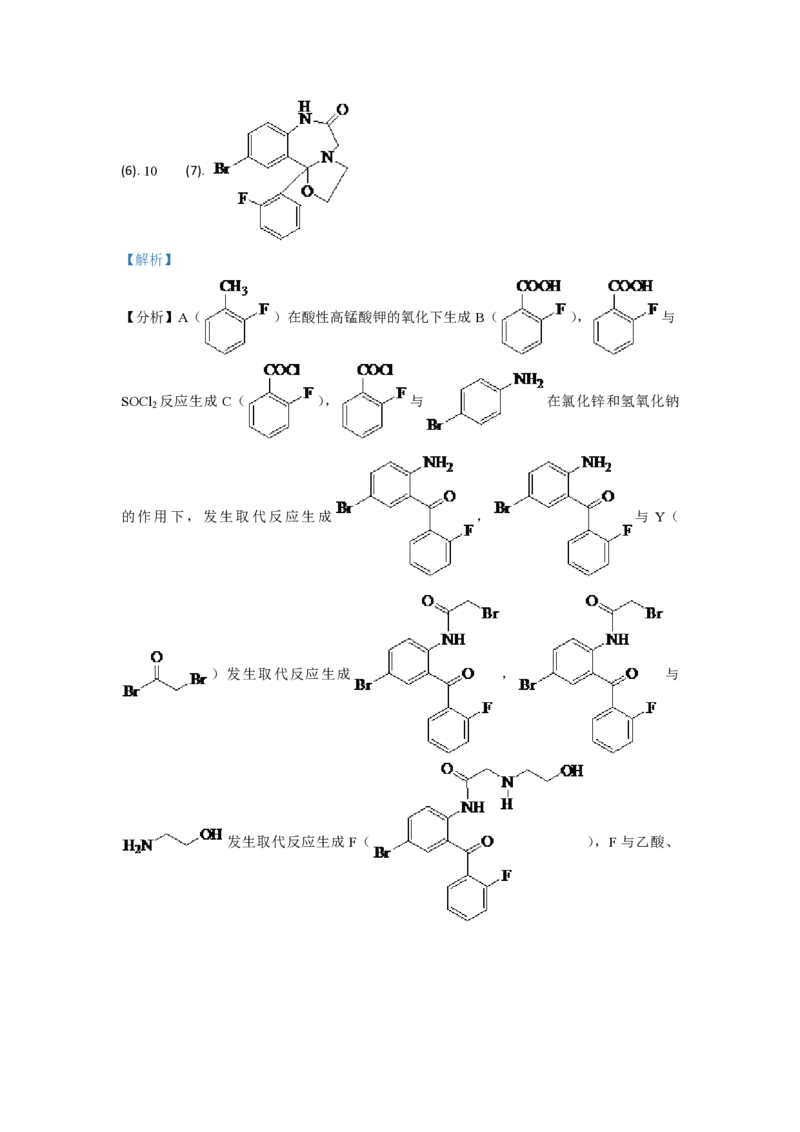
12. 卤沙唑仑W是一种抗失眠药物,在医药工业中的一种合成方法如下:
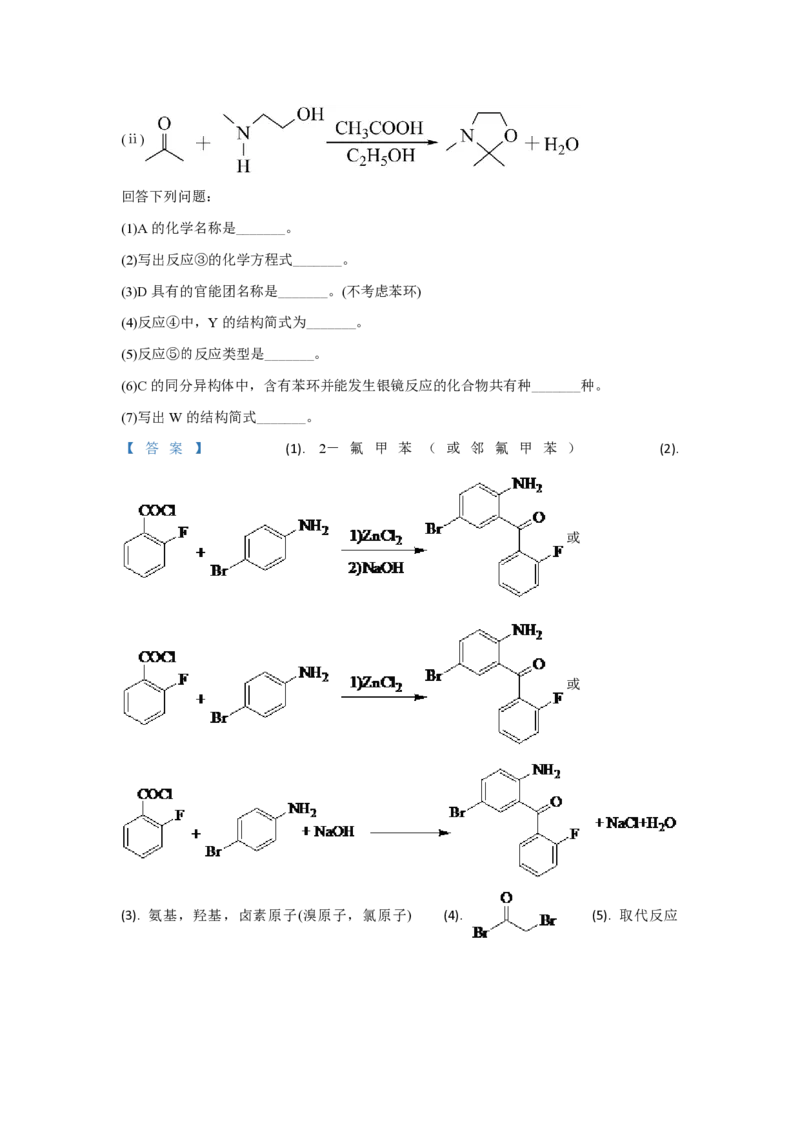
已知:(ⅰ)(ⅱ)
回答下列问题:
(1)A的化学名称是_______。
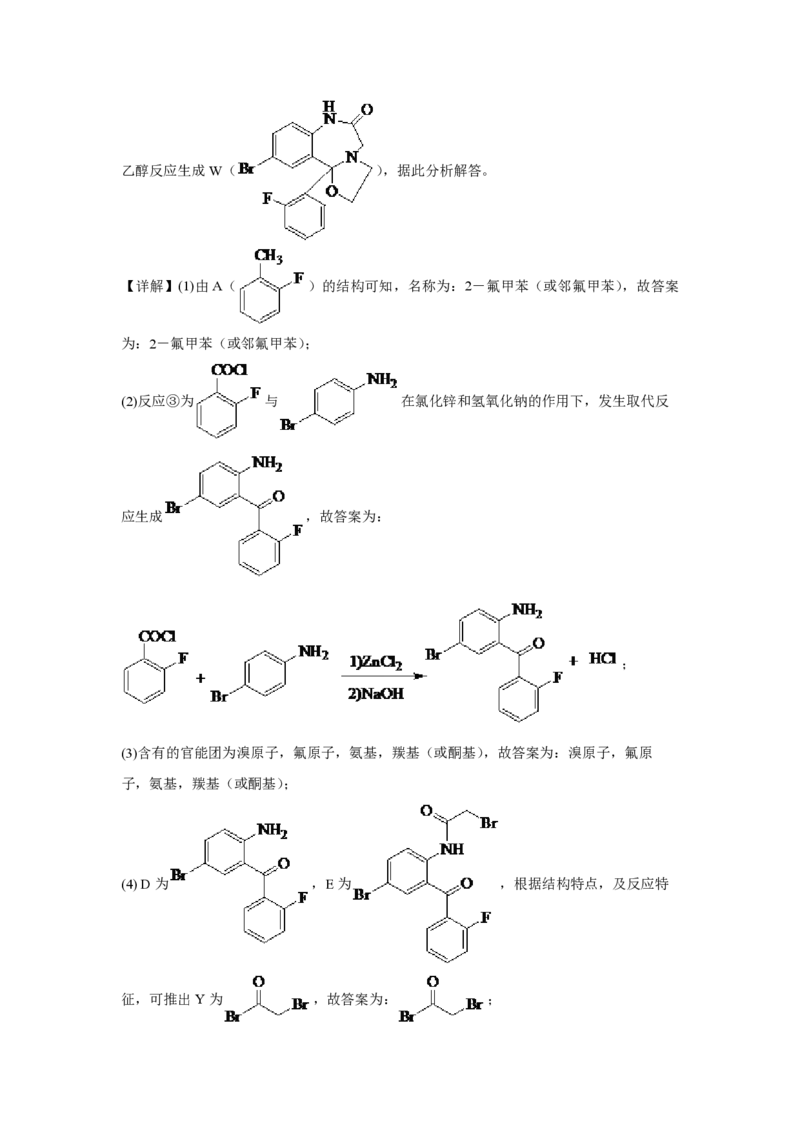
(2)写出反应③的化学方程式_______。
(3)D具有的官能团名称是_______。(不考虑苯环)
(4)反应④中,Y的结构简式为_______。
(5)反应⑤的反应类型是_______。
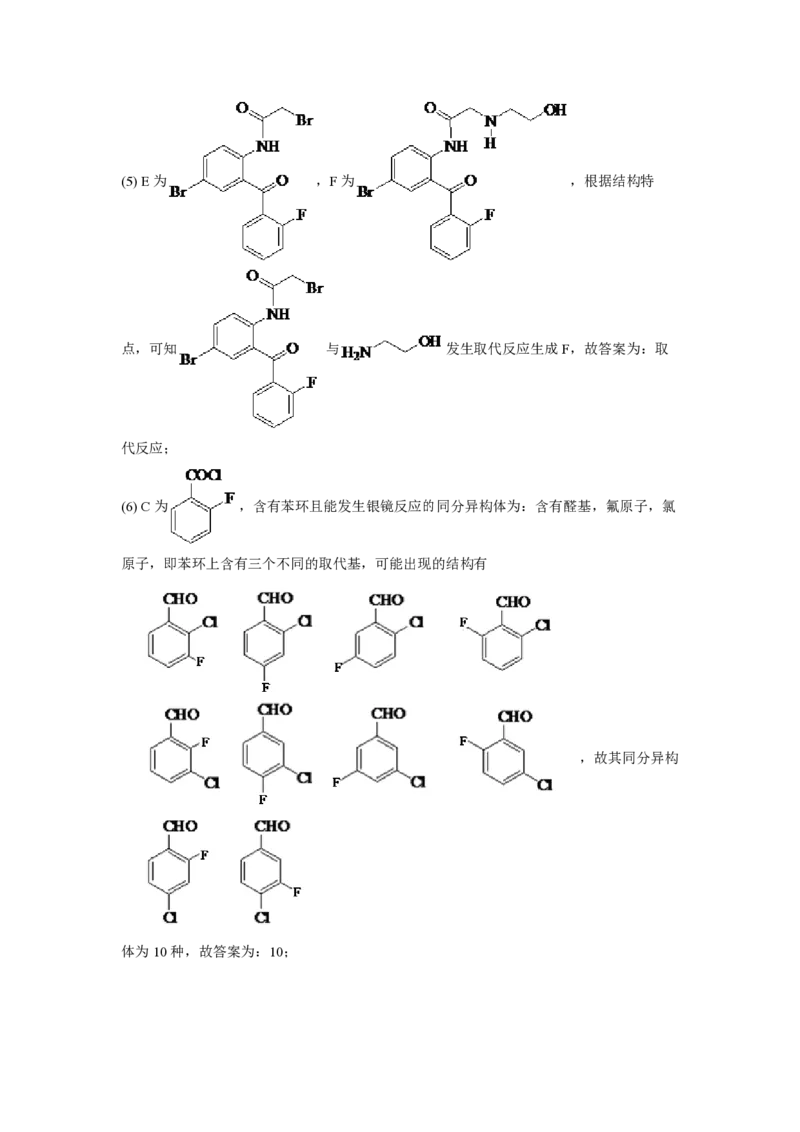
(6)C的同分异构体中,含有苯环并能发生银镜反应的化合物共有种_______种。
(7)写出W的结构简式_______。
【 答 案 】 (1). 2- 氟 甲 苯 ( 或 邻 氟 甲 苯 ) (2).
或
或
(3). 氨基,羟基,卤素原子(溴原子,氯原子) (4). (5). 取代反应(6). 10 (7).
【解析】
【分析】A( )在酸性高锰酸钾的氧化下生成B( ), 与
SOCl 反应生成 C( ), 与 在氯化锌和氢氧化钠
2
的作用下,发生取代反应生成 , 与 Y(
)发生取代反应生成 , 与
发生取代反应生成 F( ),F与乙酸、乙醇反应生成W( ),据此分析解答。
【详解】(1)由A( )的结构可知,名称为:2-氟甲苯(或邻氟甲苯),故答案
为:2-氟甲苯(或邻氟甲苯);
(2)反应③为 与 在氯化锌和氢氧化钠的作用下,发生取代反
应生成 ,故答案为:
;
(3)含有的官能团为溴原子,氟原子,氨基,羰基(或酮基),故答案为:溴原子,氟原
子,氨基,羰基(或酮基);
(4) D为 ,E为 ,根据结构特点,及反应特
征,可推出Y为 ,故答案为: ;(5) E为 ,F为 ,根据结构特
点,可知 与 发生取代反应生成F,故答案为:取
代反应;
(6) C为 ,含有苯环且能发生银镜反应的同分异构体为:含有醛基,氟原子,氯
原子,即苯环上含有三个不同的取代基,可能出现的结构有
,故其同分异构
体为10种,故答案为:10;(7)根据已知及分析可知, 与乙酸、乙醇反应生成
,故答案为: ;