文档内容
第 5 讲 氧化还原反应(下)
达标练习01.
★★☆☆☆
已知反应:H S+Fe (SO ) =S↓+2FeSO +H SO ,下列说法正确的是( )
2 2 4 3 4 2 4
A.H S是氧化剂
2
B.该反应中有三种元素化合价改变
C.氧化性强弱顺序:Fe3+<S
D.还原性强弱顺序:H S>Fe2+
2
【考点】氧化性与还原性的比较
【答案】D
【解答】解:A.H S 中 S 的化合价由﹣2 价→0 价,化合价升高,即 H S 为还
2 2
原剂,故A错误;B.该反应中H S 中S的化合价由﹣2价→0价,化合价升高,
2
Fe (SO ) 中Fe 的化合价由+3 价→+2 价,化合价降低,该反应中S 和Fe 两种元
2 4 3
素发生变化,故B 错误;C.利用氧化还原反应中,氧化剂的氧化性强于氧化产
物的氧化性进行判断,Fe (SO ) 中 Fe 的化合价降低,即 Fe (SO ) 为氧化剂,
2 4 3 2 4 3
H S 中S的化合价升高,S为氧化产物,因此有氧化性:Fe3+>S,故C错误;D.
2
还原剂为H S,其还原性大于氧化产物Fe2+,故D正确;故选:D。
2
达标练习02.
★★☆☆☆
根据反应式:(1)2Fe3++2I-===2Fe2++I ,(2)Br +2Fe2+===2Fe3++2Br-,可判断
2 2
离子的还原性从强到弱的顺序是 ( )
A.Br-、Fe2+、I- B.I-、Fe2+、Br- C.Br-、I-、Fe2+ D.Fe2+、I-、Br-
【考点】氧化性与还原性的比较
【答案】B
【解答】解:2Fe3++2I-=2Fe2++I 中,I 元素的化合价升高,由还原剂的还
2
原性大于还原产物的还原性,则还原性 I->Fe2+,Br +2Fe2+=2Fe3++2Br-
2
中,Fe 元素的化合价升高,由还原剂的还原性大于还原产物的还原性,
则还原性 Fe2+>Br-,所以离子的还原性由强到弱的顺序为 I->Fe2+>Br-,
故选:B。
第1页(共10页)达标练习03.
★★☆☆☆
已知常温下在溶液中可发生如下两个离子反应:
Ce4++Fe2+═Fe3++Ce3+
Sn2++2Fe3+═2Fe2++Sn4+
由此可以确定Fe 2+、Ce 3+、Sn 2+三种离子的还原性由强到弱的顺序是( )
A.Sn2+、Fe2+、Ce3+ B.Sn2+、Ce3+、Fe2+
C.Ce3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ce3+
【考点】氧化性与还原性的比较
【答案】A
【解答】解:根据反应:Ce4++Fe2+=Fe3++Ce3+,还原性是Fe2+>Ce3+,根据反应:
Sn2++2Fe3+=2Fe2++Sn4+,还原性是 Sn2+>Fe2+,所以还原性顺序是:Sn2+>Fe2+
>Ce3+。故选:A。
达标练习04.
★★☆☆☆
已知:2Fe3++SO +2H O═2Fe2++SO 2﹣+4H+
2 2 4
3Fe2++4H++NO ﹣═3Fe3++NO↑+2H O
3 2
由此得出:在酸性条件下,氧化性由强到弱的关系正确的是( )
A.NO ﹣>Fe3+>SO 2﹣ B.NO ﹣>SO 2﹣>Fe3+
3 4 3 4
C.SO 2﹣>Fe3+>NO ﹣ D.Fe3+>NO ﹣>SO 2﹣
4 3 3 4
【考点】氧化性与还原性的比较
【答案】A
【解答】解:2Fe3++SO +2H O═2Fe2++SO 2﹣+4H+中氧化剂是 Fe3+、氧化产物是
2 2 4
SO 2﹣,所以氧化性 Fe3+>SO 2﹣;3Fe2++4H++NO ﹣═3Fe3++NO↑+2H O 中氧化剂
4 4 3 2
是NO ﹣、氧化产物是 Fe3+,所以氧化性 NO ﹣>Fe3+;通过以上分析可知,氧化
3 3
性强弱顺序是NO ﹣>Fe3+>SO 2﹣,故选:A。
3 4
达标练习05.
★★☆☆☆
根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是( )
①Cl +2KI═I +2KCl
2 2
②2FeCl +2HI═I +2FeCl +2HCl
3 2 2
第2页(共10页)③2FeCl +Cl ═2FeCl
2 2 3
④I +SO +2H O═2HI+H SO
2 2 2 2 4
A.Cl >I >Fe3+>SO 2﹣ B.Fe3+>Cl >I >SO 2﹣
2 2 4 2 2 4
C.Cl >Fe3+>I >SO 2﹣ D.Cl >Fe3+>SO 2﹣>I
2 2 4 2 4 2
【考点】氧化性与还原性的比较
【答案】C
【解答】解:①反应 Cl +2KI═I +2KCl,氧化剂为 Cl ,氧化产物为 I ,氧化性
2 2 2 2
Cl >I ;②2FeCl +2HI═I +2FeCl +2HCl,氧化剂为 FeCl ,氧化产物为I ,氧化
2 2 3 2 2 3 2
性 Fe3+>I ;③2FeCl +Cl ═2FeCl ,氧化剂为 Cl ,氧化产物为 FeCl ,氧化性
2 2 2 3 2 3
Cl >Fe3+;④I +SO +2H O═2HI+H SO ,氧化剂为 I ,SO 2﹣为氧化产物,氧化
2 2 2 2 2 4 2 4
性I >SO 2﹣。所以氧化性Cl >Fe3+>I >SO 2﹣。故选:C。
2 4 2 2 4
达标练习06.
★★☆☆☆
根据如下反应:
①Fe+Cu2+═Fe2++Cu
②2Fe3++Cu═Cu2++2Fe2+
③2Fe2++Cl ═2Fe3++2Cl﹣
2
④HClO+H++Cl﹣═Cl ↑+H O
2 2
可以判断出各微粒的氧化性或还原性由强到弱的顺序正确的是( )
A.氧化性:HClO>Cl >Fe3+>Cu2+>Fe2+
2
B.氧化性:Cl >HClO>Fe3+>Cu2+>Fe2+
2
C.还原性:Fe>Cu2+>Fe2+>Cl﹣>Cl
2
D.还原性:Fe2+>Cu2+>Fe3+>Cl﹣>Cl
2
【考点】氧化性与还原性的比较
【答案】A
【解答】解: ①反应Fe+Cu2+=Fe2++Cu 中铜离子是氧化剂,亚铁离子是氧化产
物,铁是还原剂,铜是还原产物,则还原性Fe>Cu,氧化性为Cu2+>Fe2+;
②反应2Fe3++Cu=Cu2++2Fe2+中铁离子是氧化剂,铜离子是氧化产物,铜是还原
剂,亚铁离子是还原产物,则还原性Cu>Fe2+,氧化性为Fe3+>Cu2+;
③反应2Fe2++Cl =2Fe3++2Cl﹣中氯气是氧化剂,铁离子是氧化产物,亚铁离子是
2
第3页(共10页)还原剂,氯离子是还原产物,则还原性Fe2+>Cl﹣,氧化性为Cl >Fe3+;
2
④反应 HClO+H++Cl﹣=Cl +H O 中次氯酸是氧化剂,氯气是氧化产物,氯离子
2 2
是还原剂,氯气是还原产物,则还原性Cl﹣>Cl ,氧化性为HClO>Cl ;
2 2
由此可以判断出各微粒的氧化性由强到弱的顺序正确的是 HClO>Cl >Fe3+>
2
Cu2+>Fe2+,还原性由强到弱的顺序正确的是Fe>Cu>Fe2+>Cl﹣>Cl ,故选:A。
2
达标练习07.
★★☆☆☆
已知I﹣、Fe2+、SO 和H O 均有还原性,它们在酸性溶液中还原性的强弱顺序
2 2 2
为:Fe2+<H O <I﹣<SO ,则下列反应不能发生的是( )
2 2 2
A.2Fe3++SO +2H O═2Fe2++SO 2﹣+4H+
2 2 4
B.H O +H SO ═SO ↑+O ↑+2H O
2 2 2 4 2 2 2
C.I +SO +2H O═H SO +2HI
2 2 2 2 4
D.2Fe3++H O ═2Fe2++O ↑+2H+
2 2 2
【考点】氧化性与还原性的比较
【答案】B
【解答】解: A.因该反应中S元素的化合价升高,Fe 元素的化合价降低,则
SO 为还原剂,还原性强弱为 SO >Fe2+,与已知的还原性强弱一致,能发生,
2 2
故A不选;
B.若该反应发生,S 元素的化合价降低,O元素的化合价升高,则H O 为还原
2 2
剂,还原性强弱为 H O >SO ,与已知的还原性强弱矛盾,不可能发生,故 B
2 2 2
选;
C.因该反应中 S 元素的化合价升高,I 元素的化合价降低,则 SO 为还原剂,
2
还原性强弱为SO >I﹣,与已知的还原性强弱一致,能发生,故C 不选;
2
D.因该反应中 Fe 元素的化合价降低,O元素的化合价升高,则H O 为还原剂,
2 2
还原性强弱为 H O >Fe2+,与已知的还原性强弱一致,能发生,故 D 不选;故
2 2
选:B。
达标练习08.
★★☆☆☆
已知氧化性:Cl >Fe3+>Cu2+>H+,下列化学反应或离子反应不能发生的是
2
( )
第4页(共10页)A.Cu+2H+═Cu2++H ↑ B.Cl +2FeCl ═2FeCl
2 2 2 3
C.Cu+Cl CuCl D.2Fe3++Cu═2Fe2++Cu2+
2 2
【考点】氧化性与还原性的比较
【答案】A
【解答】解:A.由于氧化性Cu2+>H+,H+不能氧化Cu,反应不能进行,故A
选;
B.氧化性:Cl >Fe3+,氯气可以氧化亚铁离子,反应能进行,故B 不选;
2
C.氧化性:Cl >Cu2+,氯气可以氧化Cu,反应能进行,故C 不选;
2
D.氧化性Fe3+>Cu2+,铁离子和铜反应生成铜离子,反应能进行,故D 不选;
故选:A。
达标练习09.
★★★☆☆
常温下,下列三个反应均能发生:
X +2W2+═2X﹣+2W3+;Z +2X﹣═2Z﹣+X ;2W3++2Y﹣═2W2++Y 。
2 2 2 2
则在相同条件下,下列三个反应:
①Y +2X﹣═2Y﹣+X ;②Z +2Y﹣═2Z﹣+Y ;③2W3++2Z﹣═2W2++Z ,
2 2 2 2 2
能发生的是( )
A.只有① B.只有② C.①和② D.②和③
【考点】氧化性与还原性的比较
【答案】B
【解答】解: 反应 X +2W2+═2X﹣+2W3+,则得出氧化性关系 X >W3+;Z +2X﹣
2 2 2
═2Z﹣+X ,则得出氧化性关系 Z >X ;2W3++2Y﹣═2W2++Y ,则得出氧化性关系
2 2 2 2
W3+>Y ,所以物质的氧化性顺序是:Z >X >W3+>Y ,
2 2 2 2
①Y +2X﹣═2Y﹣+X ,则得出氧化性关系 Y >X ;与已知氧化性顺序不同,则反
2 2 2 2
应不能发生,故错误;
②Z +2Y﹣═2Z﹣+Y ,则得出氧化性关系 Z >Y ;与已知氧化性顺序相同,则反
2 2 2 2
应能发生,故正确;
③2W3++2Z﹣═2W2++Z ,则得出氧化性关系 W3+>Z ;与已知氧化性顺序不同,
2 2
则反应不能发生,故错误;故选:B。
第5页(共10页)达标练习10.
★★☆☆☆
由相同条件下的三个反应:
①2A﹣+B →2B﹣+A ②2C﹣+A →2A﹣+C ③2B﹣+D →2D﹣+B
2 2 2 2 2 2
由此可以判断( )
A.氧化性:A >B >C >D
2 2 2 2
B.还原性:C﹣>A﹣>B﹣>D﹣
C.反应2A﹣+D →2D﹣+A 不能进行
2 2
D.反应2C﹣+B →2B﹣+C 不能进行
2 2
【考点】氧化性与还原性的比较
【答案】B
【解答】解:根据氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于
还原产物的还原性来判断,那么氧化性 D >B >A >C ,还原性 C﹣>A﹣>B﹣
2 2 2 2
>D﹣,故 A 错误,B 正确。根据氧化性强的物质易与还原性强的物质反应,氧
化性:D >A ,还原性:A﹣>D﹣,故 A﹣和 D 能反应;同理 B 和C﹣可以进行
2 2 2 2
反应,故C、D错误;故选:B。
达标练习11.
★★☆☆☆
下列电子转移的表示方法中正确的是 ( )
【考点】氧化还原反应的表示
【答案】D
【解答】解:按照步骤,Fe O 是氧化剂,被还原,转移电子数为2×3e-,CO是
2 3
还原剂,被氧化,转移电子数为 3×2e-,正确的表示方式为:(本题根据题意:条
件写加热,一般会写高温)
第6页(共10页)达标练习12.
★★☆☆☆
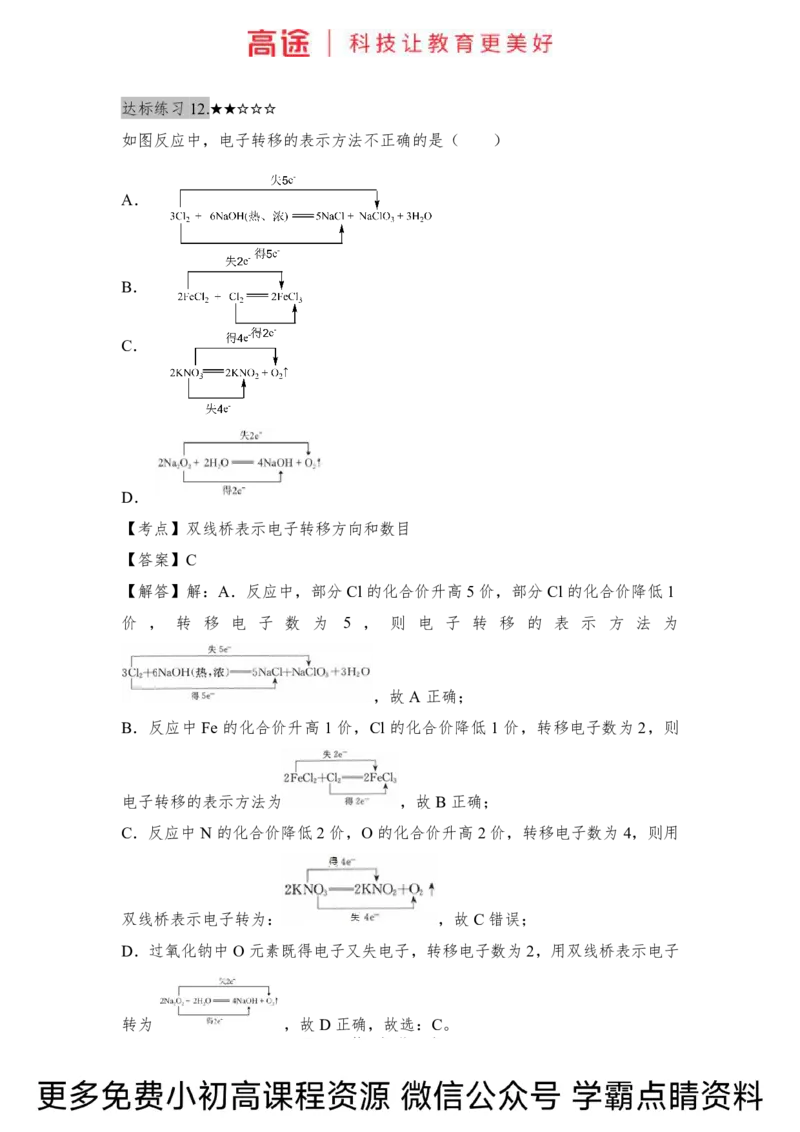
如图反应中,电子转移的表示方法不正确的是( )
A.
B.
C.
D.
【考点】双线桥表示电子转移方向和数目
【答案】C
【解答】解:A.反应中,部分Cl 的化合价升高5价,部分Cl 的化合价降低1
价 , 转 移 电 子 数 为 5 , 则 电 子 转 移 的 表 示 方 法 为
,故A 正确;
B.反应中 Fe 的化合价升高 1 价,Cl 的化合价降低 1 价,转移电子数为 2,则
电子转移的表示方法为 ,故B 正确;
C.反应中N的化合价降低2价,O 的化合价升高2价,转移电子数为4,则用
双线桥表示电子转为: ,故C 错误;
D.过氧化钠中O元素既得电子又失电子,转移电子数为2,用双线桥表示电子
转为 ,故D正确,故选:C。
第7页(共10页)达标练习13.
★★☆☆☆
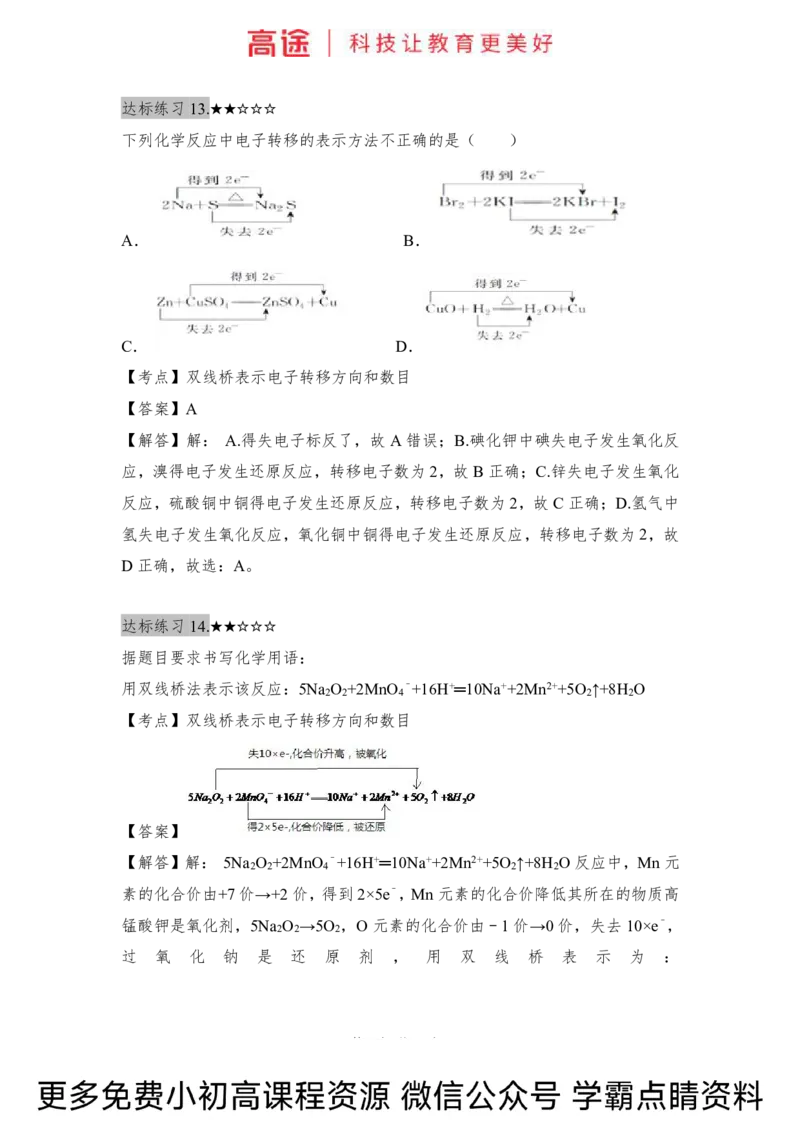
下列化学反应中电子转移的表示方法不正确的是( )
A. B.
C. D.
【考点】双线桥表示电子转移方向和数目
【答案】A
【解答】解: A.得失电子标反了,故 A错误;B.碘化钾中碘失电子发生氧化反
应,溴得电子发生还原反应,转移电子数为2,故B 正确;C.锌失电子发生氧化
反应,硫酸铜中铜得电子发生还原反应,转移电子数为2,故C 正确;D.氢气中
氢失电子发生氧化反应,氧化铜中铜得电子发生还原反应,转移电子数为2,故
D正确,故选:A。
达标练习14.
★★☆☆☆
据题目要求书写化学用语:
用双线桥法表示该反应:5Na O +2MnO ﹣+16H+═10Na++2Mn2++5O ↑+8H O
2 2 4 2 2
【考点】双线桥表示电子转移方向和数目
【答案】
【解答】解: 5Na O +2MnO ﹣+16H+═10Na++2Mn2++5O ↑+8H O 反应中,Mn 元
2 2 4 2 2
素的化合价由+7 价→+2 价,得到 2×5e﹣,Mn 元素的化合价降低其所在的物质高
锰酸钾是氧化剂,5Na O →5O ,O 元素的化合价由﹣1价→0价,失去10×e﹣,
2 2 2
过 氧 化 钠 是 还 原 剂 , 用 双 线 桥 表 示 为 :
第8页(共10页);
故答案为: 。
达标练习15.
★★☆☆☆
分析下列氧化还原反应中化合价变化的关系,用双线桥法标出电子转移的方向和
数目,并指出氧化剂和还原剂。
(1)Fe+H SO ==FeSO +H ↑:氧化剂是 ;还原剂是 。
2 4 4 2
用双线桥法标出电子转移的方向和数目:
Fe+H SO ==FeSO +H ↑
2 4 4 2
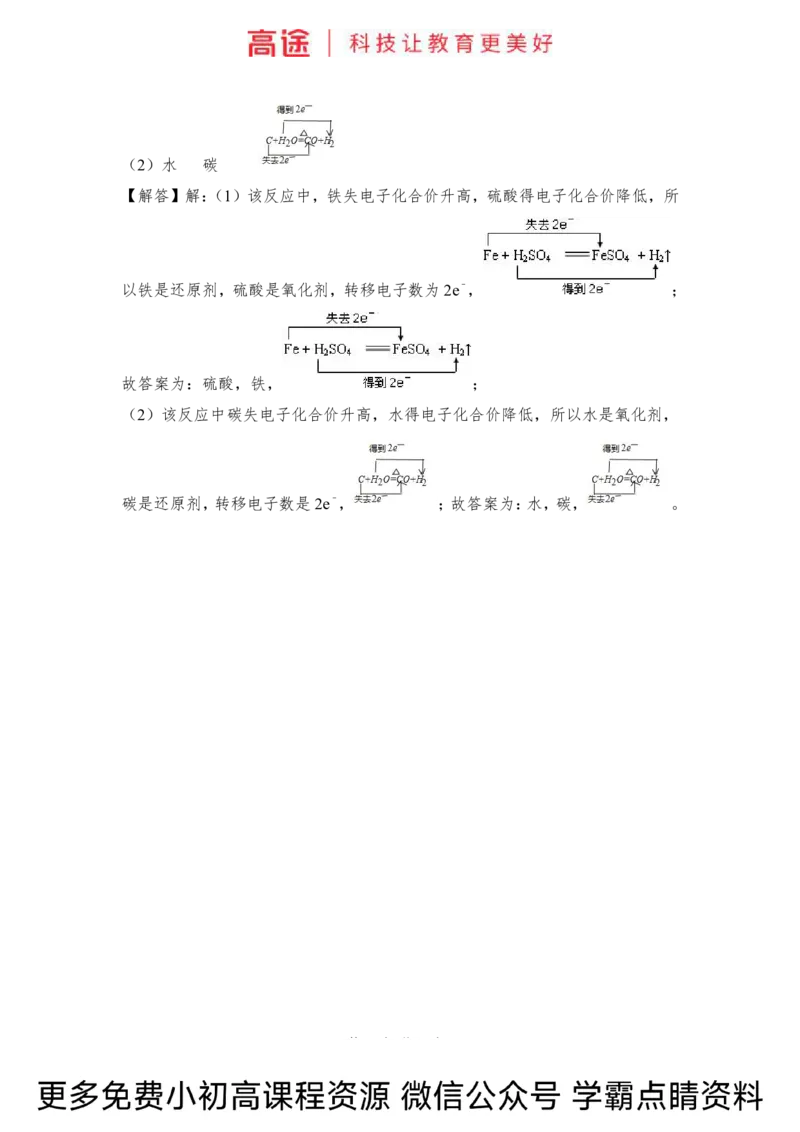
(2)C+H O(g) CO+H :氧化剂是 ;还原剂是 。
2 2
用双线桥法标出电子转移的方向和数目:
C+H O(g) CO+H
2 2
【考点】双线桥表示电子转移方向和数目
【答案】(1)硫酸 铁
第9页(共10页)(2)水 碳
【解答】解:(1)该反应中,铁失电子化合价升高,硫酸得电子化合价降低,所
以铁是还原剂,硫酸是氧化剂,转移电子数为 2e﹣, ;
故答案为:硫酸,铁, ;
(2)该反应中碳失电子化合价升高,水得电子化合价降低,所以水是氧化剂,
碳是还原剂,转移电子数是2e﹣, ;故答案为:水,碳, 。
第10页(共10页)