文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
题型 03 工艺流程题
►类型1 日常用品生产............................................................................................................................................1
►类型2 以矿石为原料生产....................................................................................................................................7
►类型3 以海水为原料生产..................................................................................................................................18
►类型4 废物利用再生产......................................................................................................................................23
►类型5 其他综合制备..........................................................................................................................................30
►类型1 日常用品生产
1.(2024·江苏无锡节选)造纸。竹子造纸的流程如下:
(1)“浸泡”的目的是软化纤维。竹子含有纤维素[(C H O )],纤维素中碳、氢、氧的原子个数比为
6 10 5
。
(2)“蒸煮”时,利用石灰浆[主要成分为Ca(OH) ]和草木灰水的碱性,达到除去木素的目的。将石灰浆
2
和草木灰水混合后效果更好,原因是 。
(3)“捞纸”与化学实验中物质分离的 (填字母)操作相似。
a.溶解 b.过滤 c.蒸发
2.(2024·四川成都)皮蛋是成渝等地人们喜爱的食品,制作流程如图。
资料:1.草木灰(含K CO )中常含有砂石和未燃尽的秸秆等固体。
2 3
2.碱,有涩味,可与蛋白质作用,使其凝固。
回答下列问题。
(1)选料:“过筛”的目的是 。
(2)调浆:调浆过程发生的复分解反应的化学方程式为 ,料浆浸出液中一定含有的阴离子有
(填离子符号)。
(3)裹泥:裹泥时,不慎皮肤接触料浆,处理方法为 。
(4)封存:需要“密封”的主要原因是减少水分蒸发和 。
(5)食用皮蛋时加醋能去除涩味的原因是 。
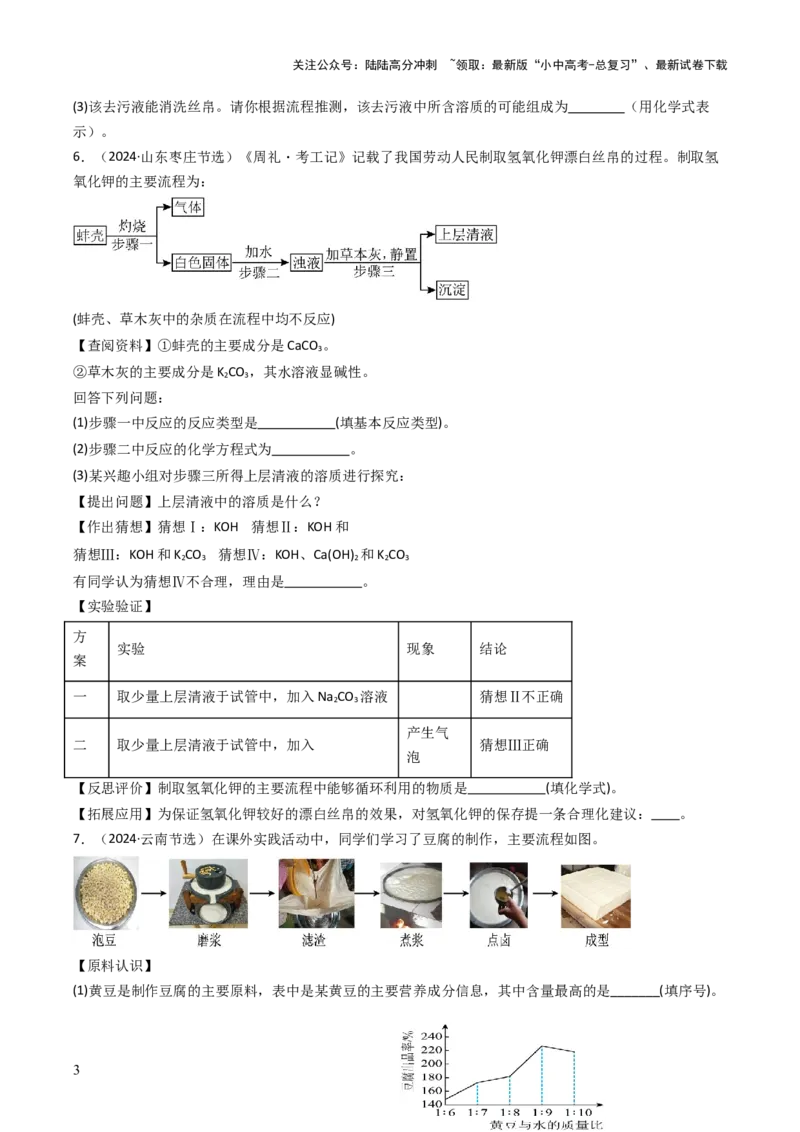
3.(2024·西藏)酥油茶色泽淡黄,味道鲜美,香气扑鼻,既能止渴,又能充饥,还能暖身,确是高原佳
饮。酥油茶制作流程如图,请完成下列问题。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)操作①在化学实验操作中的名称: 。
(2)酥油茶属于 (填“纯净物”或“混合物”)。
(3)生活中将硬水软化的方法是 。
(4)用洗涤剂清洗茶杯除去残余油污,这是利用洗涤剂的 作用。
(5)下列物质加入水中能形成溶液的是_____。
A.糌粑 B.白糖 C.酥油
4.(2024·湖南)酱油是我国传统调味品之一,已有3000多年历史。天然晒露法是传统的老法酱油的生产
方法。以初夏开始制作为例,主要流程如下:
回答下列问题:
(1)“发酵”过程中,所取缸内样品呈 (填“酸”“中”或“碱”)性。
(2)“压榨”与化学基本实验操作中的 (填操作名称)有相似之处。
(3)下列有关说法正确的是 (多选,填字母)。
a“浸泡”目的是泡胀大豆,并除去杂物
b.铁强化酱油中“铁”可以预防佝偻病
c.天然晒露法得到成品的时间会受天气影响
5.(2024·湖南长沙)《周礼·考工记》中记载,古人曾在草木灰(含 )的水溶液中加入贝壳烧成的
灰(主要成分为 ),利用生成物中能够去污的成分来清洗丝帛。为了得到该去污液,某兴趣小组同学
在老师的指导下设计了以下实验流程。回答下列问题:
(1)操作I的名称为 ;
(2)该流程中涉及到所有的基本反应类型有分解反应、 ;
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)该去污液能消洗丝帛。请你根据流程推测,该去污液中所含溶质的可能组成为 (用化学式表
示)。
6.(2024·山东枣庄节选)《周礼・考工记》记载了我国劳动人民制取氢氧化钾漂白丝帛的过程。制取氢
氧化钾的主要流程为:
(蚌壳、草木灰中的杂质在流程中均不反应)
【查阅资料】①蚌壳的主要成分是CaCO 。
3
②草木灰的主要成分是K CO ,其水溶液显碱性。
2 3
回答下列问题:
(1)步骤一中反应的反应类型是 (填基本反应类型)。
(2)步骤二中反应的化学方程式为 。
(3)某兴趣小组对步骤三所得上层清液的溶质进行探究:
【提出问题】上层清液中的溶质是什么?
【作出猜想】猜想Ⅰ:KOH 猜想Ⅱ:KOH和
猜想Ⅲ:KOH和K CO 猜想Ⅳ:KOH、Ca(OH) 和K CO
2 3 2 2 3
有同学认为猜想Ⅳ不合理,理由是 。
【实验验证】
方
实验 现象 结论
案
一 取少量上层清液于试管中,加入Na CO 溶液 猜想Ⅱ不正确
2 3
产生气
二 取少量上层清液于试管中,加入 猜想Ⅲ正确
泡
【反思评价】制取氢氧化钾的主要流程中能够循环利用的物质是 (填化学式)。
【拓展应用】为保证氢氧化钾较好的漂白丝帛的效果,对氢氧化钾的保存提一条合理化建议: 。
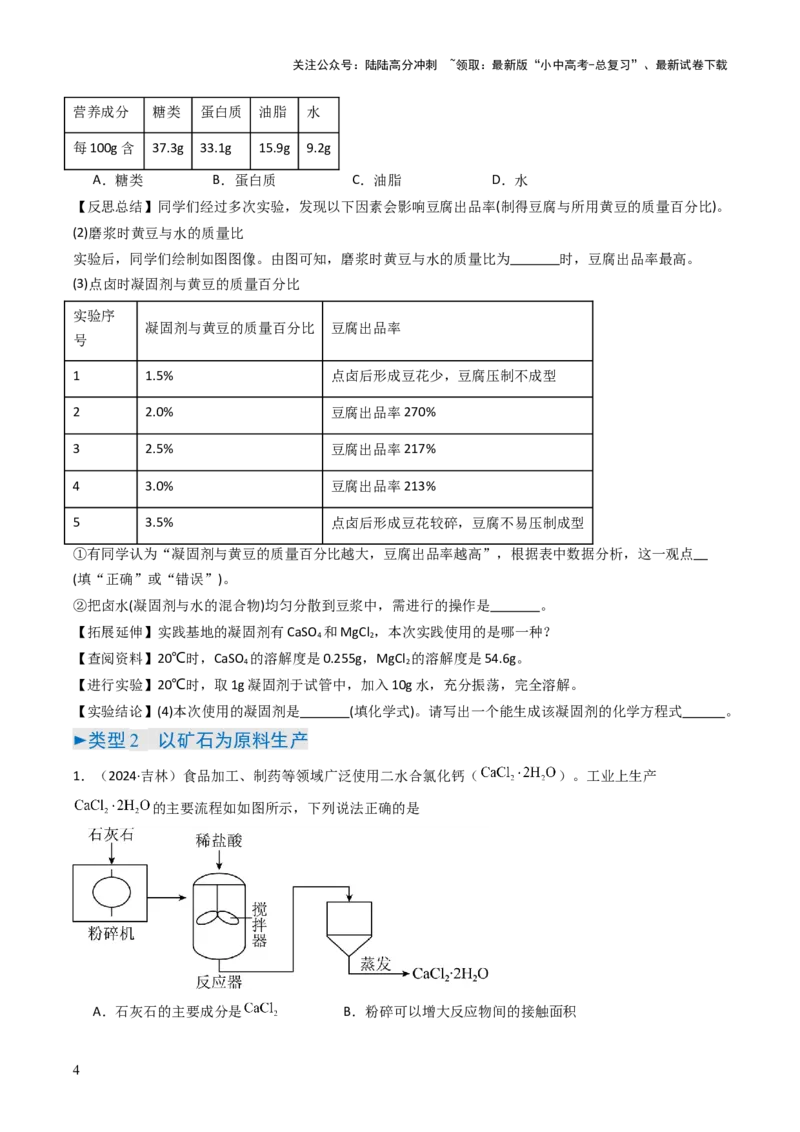
7.(2024·云南节选)在课外实践活动中,同学们学习了豆腐的制作,主要流程如图。
【原料认识】
(1)黄豆是制作豆腐的主要原料,表中是某黄豆的主要营养成分信息,其中含量最高的是_______(填序号)。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
营养成分 糖类 蛋白质 油脂 水
每100g含 37.3g 33.1g 15.9g 9.2g
A.糖类 B.蛋白质 C.油脂 D.水
【反思总结】同学们经过多次实验,发现以下因素会影响豆腐出品率(制得豆腐与所用黄豆的质量百分比)。
(2)磨浆时黄豆与水的质量比
实验后,同学们绘制如图图像。由图可知,磨浆时黄豆与水的质量比为 时,豆腐出品率最高。
(3)点卤时凝固剂与黄豆的质量百分比
实验序
凝固剂与黄豆的质量百分比 豆腐出品率
号
1 1.5% 点卤后形成豆花少,豆腐压制不成型
2 2.0% 豆腐出品率270%
3 2.5% 豆腐出品率217%
4 3.0% 豆腐出品率213%
5 3.5% 点卤后形成豆花较碎,豆腐不易压制成型
①有同学认为“凝固剂与黄豆的质量百分比越大,豆腐出品率越高”,根据表中数据分析,这一观点
(填“正确”或“错误”)。
②把卤水(凝固剂与水的混合物)均匀分散到豆浆中,需进行的操作是 。
【拓展延伸】实践基地的凝固剂有CaSO 和MgCl ,本次实践使用的是哪一种?
4 2
【查阅资料】20℃时,CaSO 的溶解度是0.255g,MgCl 的溶解度是54.6g。
4 2
【进行实验】20℃时,取1g凝固剂于试管中,加入10g水,充分振荡,完全溶解。
【实验结论】(4)本次使用的凝固剂是 (填化学式)。请写出一个能生成该凝固剂的化学方程式 。
►类型2 以矿石为原料生产
1.(2024·吉林)食品加工、制药等领域广泛使用二水合氯化钙( )。工业上生产
的主要流程如如图所示,下列说法正确的是
A.石灰石的主要成分是 B.粉碎可以增大反应物间的接触面积
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.搅拌可以提高 的产量 D.反应器中生成的气体具有可燃性
2.(2024·山东济南)菱锌矿是工业上制备硫酸锌的原料。菱锌矿的主要成分是 ,还含有 和
等。如图是用碳酸锌样品(杂质为 和 ; 难溶于水,也不与稀硫酸反应)模拟工业制备
的流程。下列有关说法中,合理的是
A.滤液 为无色溶液B.滤渣甲是 C.滤渣乙是单质铁 D.步骤Ⅱ有气体生成
3.(2024·四川德阳)金属钼(Mo)制成的合金有良好的机械性能,利用钼矿石(主要成分为MoS )制
2
备金属钼的简易流程如图所示。
回答下列问题:
(1)“灼烧”时,MoS 发生反应的化学方程式为 .
2
(2)中间产物(NH ) MoO 中钼元素的化合价为 。
4 2 4
(3)“高温”发生反应所属的化学反应类型是 (填标号)。
a.化合反应 b.分解反应 c.置换反应 d.复分解反应
4.(2024·四川广安)铁红(Fe O )可用于制备红色颜料,以菱铁矿(主要成分为FeCO )为原料制备铁
2 3 3
红的一种流程如下图所示:
已知:流程中“沉淀”时主要反应为: 。
回答下列问题:
(1)FeO(OH)中Fe的化合价为 。
(2)“酸浸”时,FeCO 与盐酸反应生成的盐为 (填化学式)。
3
(3)“过滤”时,会用到的玻璃仪器有玻璃棒、烧杯、 。
(4)“沉淀”过程中,应始终保持溶液的pH为3.0~4.5,需加入物质X消耗H+。物质X可能是______(填字
母)。
A.NaCl B.NaOH C.Cu
(5)高温下,“煅烧”只生成两种氧化物,该反应的化学方程式为 。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
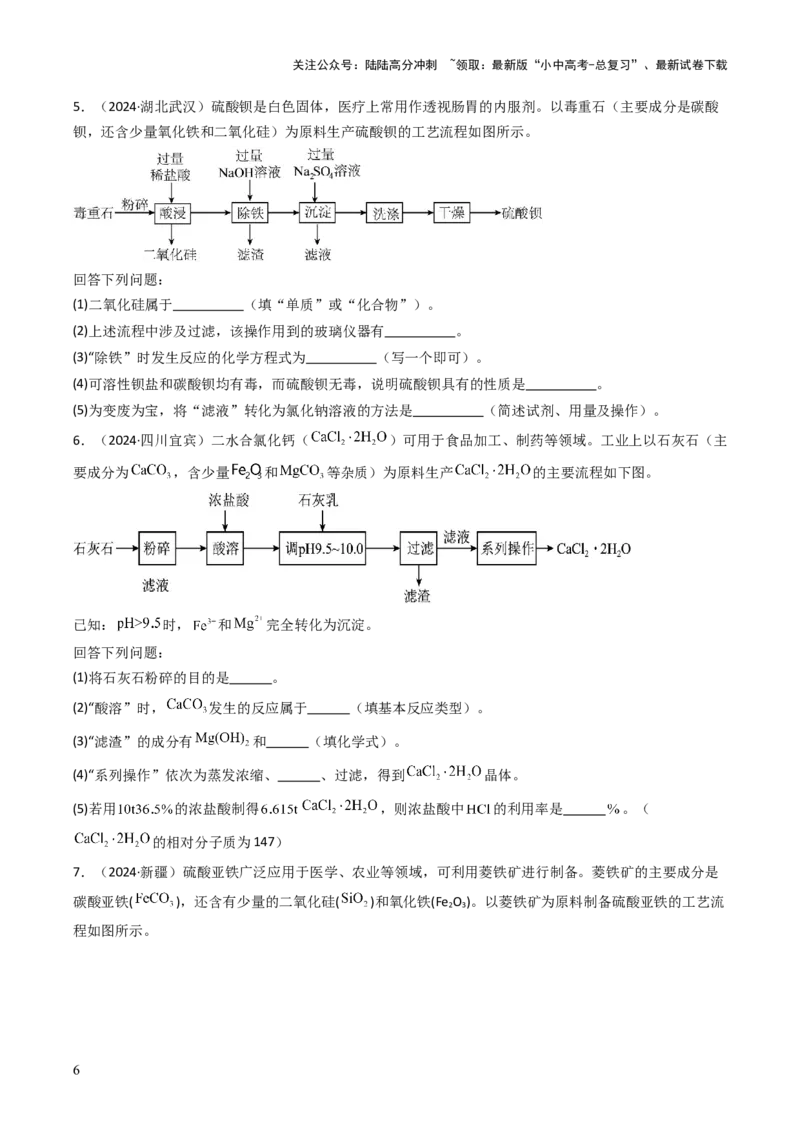
5.(2024·湖北武汉)硫酸钡是白色固体,医疗上常用作透视肠胃的内服剂。以毒重石(主要成分是碳酸
钡,还含少量氧化铁和二氧化硅)为原料生产硫酸钡的工艺流程如图所示。
回答下列问题:
(1)二氧化硅属于 (填“单质”或“化合物”)。
(2)上述流程中涉及过滤,该操作用到的玻璃仪器有 。
(3)“除铁”时发生反应的化学方程式为 (写一个即可)。
(4)可溶性钡盐和碳酸钡均有毒,而硫酸钡无毒,说明硫酸钡具有的性质是 。
(5)为变废为宝,将“滤液”转化为氯化钠溶液的方法是 (简述试剂、用量及操作)。
6.(2024·四川宜宾)二水合氯化钙( )可用于食品加工、制药等领域。工业上以石灰石(主
要成分为 ,含少量 和 等杂质)为原料生产 的主要流程如下图。
已知: 时, 和 完全转化为沉淀。
回答下列问题:
(1)将石灰石粉碎的目的是 。
(2)“酸溶”时, 发生的反应属于 (填基本反应类型)。
(3)“滤渣”的成分有 和 (填化学式)。
(4)“系列操作”依次为蒸发浓缩、 、过滤,得到 晶体。
(5)若用 的浓盐酸制得 ,则浓盐酸中 的利用率是 。(
的相对分子质为147)
7.(2024·新疆)硫酸亚铁广泛应用于医学、农业等领域,可利用菱铁矿进行制备。菱铁矿的主要成分是
碳酸亚铁( ),还含有少量的二氧化硅( )和氧化铁(Fe O )。以菱铁矿为原料制备硫酸亚铁的工艺流
2 3
程如图所示。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
回答下列问题:
(1)硫酸亚铁可为人体补充铁元素,在医学上可用于治疗 (填病症名称)。
(2)菱铁矿属于 (填“纯净物”或“混合物”)。
(3)Fe O 中铁元素的化合价为 ,其中铁元素与氧元素的质量比为 。
2 3
(4)由此流程可推知 的性质有______(填字母)。
A.难溶于水 B.化学性质很活泼 C.不能与稀硫酸反应
(5)溶液甲中,属于盐类的两种溶质为 (填化学式)。
8.(2024·重庆) 可用于食品加工,制药等领域,某工厂就地取用矿石(主要含石灰石和氧化铜)制取
,其主要流程如下图所示。
(1)粉碎机和搅拌器所起的作用是 。
(2)反应器中生成的气体的化学式为 ,流程中X可以为 (填序号)。
A.稀盐酸 B.氢氧化钠 C.生石灰 D.氢氧化钙
(3)写出生成沉淀的化学方程式 。
(4)该流程存在缺陷,请提出改进措施 。
9.(2024·江苏徐州)铝的应用涉及生产、生活的各个方面。工业上用铝土矿(主要成分为Al O ,含沙石
2 3
等杂质)制备铝的主要流程如图所示:
(1)过程①、②都包含固液分离的操作,该操作名称是 。
(2)为加快铝土矿与NaOH溶液反应的速率,可采取的措施是 。
(3)生成Al(OH) 的反应中,反应物除了有NaAlO ,CO ,还有一种氧化物为 。
3 2 2
(4)写出电解氧化铝获得铝的化学方程式: 。
10.(2024·山东菏泽)碳酸锰 是制造电信器材的软磁铁氧体,也可用作脱硫的催化剂。工业上
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
利用软锰矿(主要成分是 ,还含有 、 、 杂质)制取 的流程如图所示。
已知:①
②在酸性条件下, 可将 氧化为 ,而自身转化为 。
请回答下列问题:
(1)操作a的名称 。
(2)固体A中金属单质的化学式为 。
(3)查阅资料:
氢氧化物
开始沉淀 2.7 8.3
完全沉淀 3.7 9.8
在溶液C到固体D的转化过程中,用 溶液调节 ,其目的是 。发生反应
的化学方程式为 。
11.(2024·山东临沂)钛白粉( )作为白色颜料广泛应用于油漆、塑料等工业生产中。工业上以钛
铁矿(主要成分 )和硫酸为原料生产钛白粉,其主要工艺流程如图(部分流程未标出):
请回答:
(1)该工艺流程中将矿石粉碎的目的是 。
(2)该工艺流程中可循环使用的物质为 。
(3)在钛铁矿粉中加入硫酸可制得硫酸氧钛( ),其反应的化学方程式为:
。请推断X的化学式为 。
(4)偏钛酸 高温煅烧生成钛白粉( )和一种常见氧化物,请写出该反应的化学方程式
。
12.(2024·山东济宁)某化学兴趣小组模拟工厂苛化法制备烧碱的流程如下
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
请回答:
(1)X常用作食品干燥剂,其化学式为 ;
(2)写出反应池中发生反应的化学方程式 ;
(3)实验室中将滤液A盛装在 仪器中完成操作2;
(4)滤液B可加入反应池中循环利用,目的是 。
13.(2024·贵州节选)贵州蕴藏丰富的铝、锰、锌、铁、铜等矿产资源。合理开采、充分利用这些矿产资
源,可实现“富矿精开”。
(3)用某菱锰矿为原料制备高附加值新型电池材料 的流程如图1。
已知:菱锰矿中除 外,还有 ; 能与稀硫酸发生复分解反应, 不溶于水也不与稀硫
酸反应;氨水呈碱性。
①过滤器中得到的滤渣是 。
②反应器中, 溶液与 反应可生成锰的氧化物,如 、 、 。发生的反应之一是
,X的化学式是 。
③70℃时,在反应器中保持通入的 和 溶液的质量不变,只改变 溶液的溶质质量分数,测
得生成含锰元素的固体中锰元素的质量分数与 溶液的溶质质量分数之间的关系如图2。由图可知,
当 溶液的溶质质量分数为5.1%时,可获得高纯度的 ,当 溶液的溶质质量分数为其它
数值时, 纯度降低,原因可能是 。
14.(2024·山东潍坊)钼(Mo)是制作特种钢的重要添加剂。工业以辉钼矿(主要成分为 及少量的
)为原料制备金属钼的主要流程如下。回答下列问题。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)在焙烧炉中,矿石要粉碎处理并从上部加入,其目的是 。炉内主要反应
,X的化学式为 。
(2)反应器1中浓氨水可以溶解粗产品 。搅拌器相当于实验室中的 (填一种仪器名称)。要实
现废渣和溶液的分离,需要进行的主要操作是 (填操作名称)。
(3)反应器2中发生复分解反应,Y溶液中溶质的主要成分为 (填化学式)。
(4)反应器3中发生反应的化学方程式为 。
(5)为减少废气X对环境的影响,可用上述流程中的 溶液进行吸收。
►类型3 以海水为原料生产
1.(2024·山东青岛)分离提纯是获取物质的重要方法,其思路有两种:一是除去杂质,二是提取目标产
物。如图是海水综合利用的部分流程(操作已省略),下列说法不正确的是
已知:该粗盐中含泥沙、 、 、 等杂质。
A.流程Ⅰ中X、Y溶液的顺序不能颠倒
B.流程Ⅱ中的石灰乳可用生石灰替代
C.流程Ⅱ中提纯氯化镁是通过“提取目标产物”的思路实现的
D.混合物分离提纯的方法是由混合物中各组分的性质差异决定的
2.(2024·四川达州)海水中含有丰富的化学资源,可提取食盐。下图是粗盐提纯的部分流程,粗盐中的
杂质有泥沙、氯化钙、氯化镁,回答下列问题。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)粗盐溶解时,玻璃棒的作用是 。
(2)过滤后,滤渣中除泥沙外,还含有 (填化学式);若滤液仍然浑浊,原因可能是 (任
写一条即可)。
(3)蒸发时,当蒸发皿中出现 时即停止加热。
3.(2024·甘肃兰州)镁被誉为“21世纪最具开发应用潜力、绿色的战略性原材料”。用海水晒盐得到苦
卤(含 、NaCl等物质),从苦卤中提取镁的部分流程如下图所示。
回答下列问题:
(1)“苦卤”属于 (填“纯净物”或“混合物”)。
(2)写出中和池中反应的化学方程式: 。
(3)上述获取金属镁的整个流程中,涉及到的化学反应的基本类型共有 种。
(4)该流程中循环使用的物质是 。
(5)镁用于火箭、飞机等领域,体现了镁的哪些物理性质? (答一点)。
4.(2024·四川巴中)海洋是一个巨大的资源宝库。广泛应用于火箭、导弹和飞机制造业的金属镁,就是
利用从海水中提取的镁盐制取的。下图是模拟从海水中制取镁的简易流程。
根据流程回答下列问题:
(1)步骤①得到的母液是氯化钠的 (选填“饱和”或“不饱和”)溶液。
(2)步骤②操作中用到的玻璃仪器有烧杯、玻璃棒和 。
(3)步骤②中加入氢氧化钠溶液需过量的目的是 。
(4)写出步骤③中反应的化学方程式 。
(5)市场调研发现, 的价格远低于NaOH,更适用于实际工业生产。在步骤②中,若要制得
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
580t ,理论上至少需要加入 的质量是多少?(写出计算过程)
5.(2024·山东济南)海水中含有大量的氯化钠,可用于制取纯碱等工业原料。
(1)结合材料,回答问题:
材料一:我国化学家侯德榜在氨碱法的基础上创立了侯氏制碱法。主要流程如下:
上述过程的化学反应原理为 ;
。
材料二: 在水中的溶解度不大,常温常压下,每升水能溶解 。 极易溶于水,常温常压下,
每升水能溶解 。
①纯碱的主要成分是 ,从物质分类的角度看, 属于 (填“酸”“碱”“盐”之一)。
②侯氏制碱法在制得纯碱的同时还得到的一种氮肥是 (填化学式)。
③综合分析上述制碱流程中,要先向饱和食盐水中通 制成饱和氨盐水之后,再通 的原因是
。
(2)如图为 、 和 的溶解度曲线。下列说法中,正确的是______(填选项序号)。
A. 时, 的溶解度小于 的溶解度
B.当 中混有少量 时,可采用降温结晶的方法提纯
C. 时, 饱和溶液中溶质与溶液的质量比为
D. 时,各取相同质量的 和 固体,分别加水至恰好完全溶解,然后降温至 ,此时
所得 溶液的质量小于 溶液的质量
(3)工业上制得的纯碱中常混有少量氯化钠。为测定某纯碱样品(杂质为氯化钠)中 的质量分数,
某兴趣小组称取该样品 ,放入烧杯中,加入 水配成溶液,然后向其中逐滴加入溶质质量分数为
的 溶液至恰好完全反应,过滤并干燥,称得沉淀的质量为 ,实验过程如下图所示。请回答:
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①过程Ⅲ过滤后,所得滤液的质量是 。
②计算该样品中 的质量分数。(写出计算过程,结果精确至 )
►类型4 废物利用再生产
1.(2024·江苏连云港)一种以黄铜渣(含Zn、Cu、ZnO、CuO)为原料获取Cu和ZnSO 溶液的实验流程
4
如下。下列说法正确的是
A.加入H SO 生成H 的化学方程式为
2 4 2
B.根据流程可以判断Zn的金属活动性比Cu的强
C.判断加入的Zn如已过量的依据是溶液中有固体剩余
D.流程中涉及的化学反应类型均为置换反应
2.(2024·江苏常州节选)兴趣小组利用某种脱氧剂开展项目式学习。
任务三:回收设计
已知使用过的脱氧剂中含有氧化铁、氯化钠、碳酸钠、硅藻土、碳、铁。甲同学设计了以下回收铁的流程。
资料卡:
i.硅藻土不溶于水和酸。
ii. 溶液与Fe、Zn均能反应生成 。
(4)步骤②中氧化物发生反应的化学方程式为 。
(5)乙同学认为上述回收流程可以省略步骤①,原因是 。
3.(2024·江苏无锡)以黄铜废料为原料制备石绿[Cu (OH) CO ]的一种流程如下:
2 2 3
【查阅资料】
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①黄铜废料中含铜84%~86%,含锌14%~16%,杂质总量≤0.3%。
②59℃时,向5%的碳酸钠溶液中加入8%的硫酸铜溶液,可制得产率较高的石绿固体。
(1)“预处理”包括粉碎、酸浸等过程。“粉碎”的目的是 。使用稀硫酸酸浸的目的是 。
(2)写出铜与稀硫酸、过氧化氢溶液反应生成硫酸铜和水的化学方程式: 。
(3)步骤2获得的溶液中含有的阳离子有Cu2+和 (填离子符号)。
(4)“系列操作”包括过滤、洗涤、干燥等。干燥时温度过高会发生如下反应:
,R的化学式为 。
(5)本实验中,提高石绿产率采取的措施有① ;② 。
4.(2024·江西)研究小组利用炭粉与氧化铜反应后的剩余固体(含Cu、 、CuO和C)为原料制备胆
矾(硫酸铜晶体),操作流程如图:
资料:
(1)步骤①中进行反应时用玻璃棒搅拌的目的是 。
(2)步骤②中反应的化学方程式为 ,则X的化学式为 。
(3)步骤③中生成蓝色沉淀的化学方程式为 。
(4)下列分析不正确的是________(填字母,双选)。
A.操作1和操作2的名称是过滤
B.固体N的成分是炭粉
C.步骤④中加入的溶液丙是 溶液
D.“一系列操作”中包含降温结晶,说明硫酸铜的溶解度随温度的升高而减小
5.(2024·江苏苏州节选)柠檬酸亚铁(FeC H O )是一种补血剂,易溶于水,难溶于乙醇。某科研小组在实
6 6 7
验室研究制备柠檬酸亚铁。
I.制碳酸亚铁
用预处理后的硫铁矿烧渣(主要成分Fe O ,含少量不溶性杂质)制备碳酸亚铁的流程如图:
2 3
已知:a.Na CO 溶液呈碱性;
2 3
b.FeSO 在碱性条件下生成Fe(OH) 沉淀。
4 2
(1)“酸浸”时,为提高铁元素的浸出率,可采取的措施是 (任写一条)。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)“还原”时,加入铁粉,溶液由黄色变为浅绿色,同时有无色气体生成。“酸浸”所得溶液中含有的阳
离子是 (填离子符号)。
(3)“操作X”是为了除去过量铁粉和不溶性杂质。“操作X”是 (填操作名称)。
(4)“沉铁”时,反应原理为FeSO +Na CO =FeCO ↓+Na SO 。
4 2 3 3 2 4
①该反应的基本类型为 。
②实验时需将Na CO 溶液滴入FeSO 溶液中,而不能反向滴加,其原因是 。
2 3 4
③待FeSO 完全反应后,过滤,洗涤。洗涤前,FeCO 沉淀表面吸附的主要杂质是 (填化学式)。
4 3
6.(2024·内蒙古呼和浩特)作为基建强国,我国在建筑和水利工程中大量使用到水泥。生产水泥时,加
入适量 可调节水泥硬化速率。工厂利用电石渣[主要成分为 、MgO]制备 的主要流程
如下:
已知:MgO难溶, 易溶, 微溶。
(1)电石渣粉碎的目的是 。
(2)加入反应器中的试剂X的名称是 。
(3)反应器中发生的主要反应为 (写1个方程式即可),反应的基本类型是 。
(4)上述流程中,用于分离提纯的设备有 和洗涤槽。
7.(2024·江苏镇江节选)铁及其化合物在生产生活中有广泛应用。
(2)工业上冶炼钢铁的主要工艺流程如图。
①以赤铁矿为原料炼铁反应的化学方程式为 。
②炼钢炉中存在转化:Fe FeO Fe+CO,目的为降低 元素含量。
(3)铁及其化合物在现代多种领域发挥着重要作用。
①纳米零价铁(Fe)用于废水处理,可用H 和Fe(OH) 在高温下反应获得,反应的化学方程式为
2 3
。
②Fe O 是合成氨催化剂铁触媒的主要成分,可用CH 和Fe O 在高温下反应获得,同时生成CO 和H O的
3 4 4 2 3 2 2
质量比为 。
二、制备硫酸亚铁铵晶体
用废铁屑制备硫酸亚铁铵晶体[(NH ) Fe(SO ) •6H O]的实验流程如下。
4 2 4 2 2
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)“洗涤”是用蒸馏水洗去铁屑表面残留的Na CO 等杂质,判断铁屑已洗净的方法是:取最后一次洗涤后
2 3
的滤液,测定其pH= ,则已洗净。
(5)“酸溶”时控温75℃加热至不再产生气泡。
①加热的目的是 。
②产生的气体为H ,用点燃法检验H 前必须 。
2 2
(6)“反应”后冷却至20℃过滤。
①“反应”的化学方程式为 。
表:“反应”中相关物质的溶解度
温度/℃ 20℃
FeSO •7H O 48.0
4 2
溶解度S/g (NH 4 ) 2 SO 4 75.4
(NH ) Fe(SO ) •6H O 21.2
4 2 4 2 2
②“反应”过程中析出硫酸亚铁铵晶体,参考表中数据分析其原因 。
8.(2024·江苏镇江)一种用炼铜烟灰(主要含CuO、ZnO)制备Cu和ZnSO •7H O的流程如图。
4 2
(1)溶液X应选用 (选填序号)。
a.稀HCl b.稀H SO c.稀HNO
2 4 3
(2)“置换”发生反应的化学方程式为 。
(3)“过滤”操作用到的玻璃仪器有 、烧杯、玻璃棒等。
(4)“过滤”后滤液制备ZnSO •7H O晶体的实验方案:将滤液 (填操作名称),过滤,洗涤并干燥。
4 2
►类型5 其他综合制备
1.(2024·江苏镇江节选)(2)CO 的捕集:工业上可用氨水、K CO 溶液等化学物质捕集烟气中的CO 。氨
2 2 3 2
水捕集CO 的实验流程如下。
2
①转化中可循环使用的物质X的化学式为 。
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
②氨水吸收室中反应温度不宜过高,原因是 。
2.(2024·黑龙江大庆)氢气作为新能源。被认为具理相的清洁高能燃料。如图是用硫化氢H S气体制备
2
氢气的模拟工艺流程图。
(1)将图中S、H S、H SO 、SO 四种物质按硫元素化合价由低到高排序: 。
2 2 4 2
(2)HCl、HNO 是一元酸,H S、H SO 是二元酸,写出H S与足量NaOH溶液反应的化学方程式 。
3 2 2 4 2
(3)如图流程中可循环利用的物质有 (写出化学式)。
(4)人体缺碘会引起甲状腺肿大,碘是人体必需的 元素(填“常量”或“微量”)。
(5)如图为HI转化为I 的示意图,请写出如图中反应的化学方程式 。
2
3.(2024·北京)硫化钠( )广泛应用于染料、造纸等工业、以 为原料制备 的部分流程
如图所示。
已知: 为副产物,直接排放会造成环境污染。
(1)配平化学方程式:
(2) 中S的化合价为 。
(3)图中标示出的物质中,属于单质的是 。
(4)设备2中,加入NaOH溶液的目的是 。
4.(2024·山东烟台)电动汽车的兴起对金属镁和碳酸锂( )的需求增大。以盐湖卤水(主要成分
是 、 、 )为原料,制备金属镁和碳酸锂的主要物质转化流程如下:
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
资料:①碳酸钠能与氯化镁发生复分解反应;②部分物质的溶解度如下表:
物质
时溶解度 1.32 0.039 12.8 77 54.8 难溶
(1)为避免引入新杂质,过程Ⅰ中加入的适量物质X是 。
(2)制镁过程中发生中和反应的化学方程式是 。
(3)过程Ⅱ的目的是浓缩含锂溶液。这个过程中,氯化钠的结晶方法是 (填“蒸发结晶”或“降温结
晶”)。
(4)过程Ⅲ发生了复分解反应,其反应的化学方程式是 。
(5)用盐湖卤水制取碳酸锂,要先除去卤水中的氯化镁,其原因是 。
36.(2024·河南)粗食盐中含有泥沙和MgCl 、CaCl 、Na SO 杂质。某同学将粗食盐样品溶解、过滤,除
2 2 2 4
去泥沙后,取粗食盐水按以下流程进行提纯。
(1)溶解、过滤、蒸发操作中都用到的一种玻璃仪器是 。
(2)固体X中所含的难溶物有BaSO 、Mg(OH) 、 和BaCO 。
4 2 3
(3)加入盐酸的目的是除去溶液Y中的两种杂质,这两种杂质是 。
18