文档内容
2022 届高三化学二轮复习有机合成的综合应用专题练习
一、选择题(共17题)
1.2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖。由植物黄花蒿叶中提取的青蒿素还可合成
用于抗氯喹恶性疟及凶险型疟疾的蒿甲醚,其合成路线如下:
下列说法不正确的是
A.青蒿素的分子式是C H O,属于烃的衍生物
15 22 5
B.青蒿素难溶于水,而易溶于有机溶剂
C.反应②为取代反应,有HO生成
2
D.青蒿素遇湿润的淀粉碘化钾试纸立刻显蓝色,是因为分子结构中含有酯基
2.现有烃的含氧衍生物A,还原A时形成醇B,氧化A时形成酸C。由B、C反应可制造高分子化合物
。下列叙述中错误的是
A.A属于醛类,其相对分子质量为58,1 mol A与足量的银氨溶液反应可生成4 mol Ag
B.B在一定条件下可通过缩聚反应得到一种新的高聚物
C.B、C生成高聚物的反应为缩聚反应
D.高分子化合物的组成与B、C等物质的量混合时的组成相同
3.有机物X、Y、M的转化关系为: ,下列说法错误的是
A.X可用新制的氢氧化铜检验 B.Y有同分异构体
C.M含有两种碳氧共价键 D.Y可发生加成反应
4.金丝桃苷是从中药材中提取的一种具有抗病毒作用的黄酮类化合物,结构式如下:下列关于金丝桃苷的叙述,错误的是
A.可与氢气发生加成反应 B.分子含21个碳原子
C.能与乙酸发生酯化反应 D.不能与金属钠反应
5.有机物M的结构简式如图,下列叙述正确的是
A.1mol M与氢氧化钠溶液反应完全,消耗3molNaOH
B.M既能与乙酸反应,又能与乙醇反应
C.M不能与碳酸钠溶液反应
D.1mol M分别与Na和NaHCO 完全反应时,产生气体的物质的量之比为3∶1
3
6.下列关于烃 的说法正确的是
A.共面的C原子最多为14个
B.共直线的C原子只有为4个
C.1mol该烃最多可以和6molH 发生加成反应
2
D.1mol该烃最多可以消耗6molBr
2
7.新型冠状病毒肺炎疫情发生以来,科学和医学界积极寻找能够治疗病毒的药物。4-去甲基表鬼臼毒素具
有抗肿瘤抗菌、抗病毒等作用,分子结构如图所示,下列说法错误的是A.该有机物遇FeCl 溶液显紫色
3
B.该有机物可以与金属钠反应
C.该有机物可以与氢氧化钠反应
D.1 mol该有机物最多可以和1 mol NaOH、7 mol H 反应
2
8.某有机化合物D的结构为 ,是一种常见的有机溶剂,它可以通过下列三步反应制得:烃A
B C D,下列相关说法中不正确的是( )
A.烃A为乙烯
B.反应①②③的反应类型依次为加成反应、取代反应、取代反应
C.反应③为了加快反应速率可以快速升温至170 ℃
D.化合物D属于醚
9.CPAE是蜂胶的主要活性成分,也可由咖啡酸合成,下列说法不正确的是
A.1mol CPAE与足量的溴水反应,最多消耗4mol Br
2
B.咖啡酸可发生聚合反应,而且其分子中含有3种官能团
C.与苯乙醇互为同分异构体的酚类物质共有9种
D.可用金属Na检测上述反应是否残留苯乙醇
10.室温下,一气态烃与过量氧气混合完全燃烧,恢复到室温,使燃烧产物通过浓硫酸,体积比反应前减
少50mL,再通过NaOH溶液,体积又减少了40mL,原烃的分子式是
A.CH B.C H C.C H D.C H
4 4 10 2 6 3 8
11.普伐他汀是一种调节血脂的药物,其结构如下所示。下列关于普伐他汀的性质描述不正确的是
A.该分子的分子式为C H O
23 36 7B.不能与FeCl 溶液发生显色反应
3
C.能发生加成、取代、消去反应
D.1mol该物质最多可与3mol NaOH反应
12.断肠草为中国古代毒药之一,现代查明它是葫蔓藤科植物葫蔓藤,下列是分离出来的四种毒素的结构
式,下列推断不正确的是
A.①与②、③与④分别互为同分异构体
B.①、③互为同系物
C.等物质的量②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者多
D.①、②、③、④均能与氢氧化钠溶液反应
13.等质量的下列烃完全燃烧时,消耗氧气的量最多的是
A.CH B.C H C.C H D.C H
4 2 4 3 4 6 6
14.甲酸香叶酯是一种食品香料.可以由香叶醇与甲酸发生酯化反应制得。
下列说法中正确的是
A.香叶醇的分子式为C H O
ll l8
B.香叶醇在浓硫酸、加热条件下可发生消去反应
C.1 mol甲酸香叶酯可以与2 molH 发生加成反应
2
D.甲酸香叶酯分子中所有碳原子均可能共平面
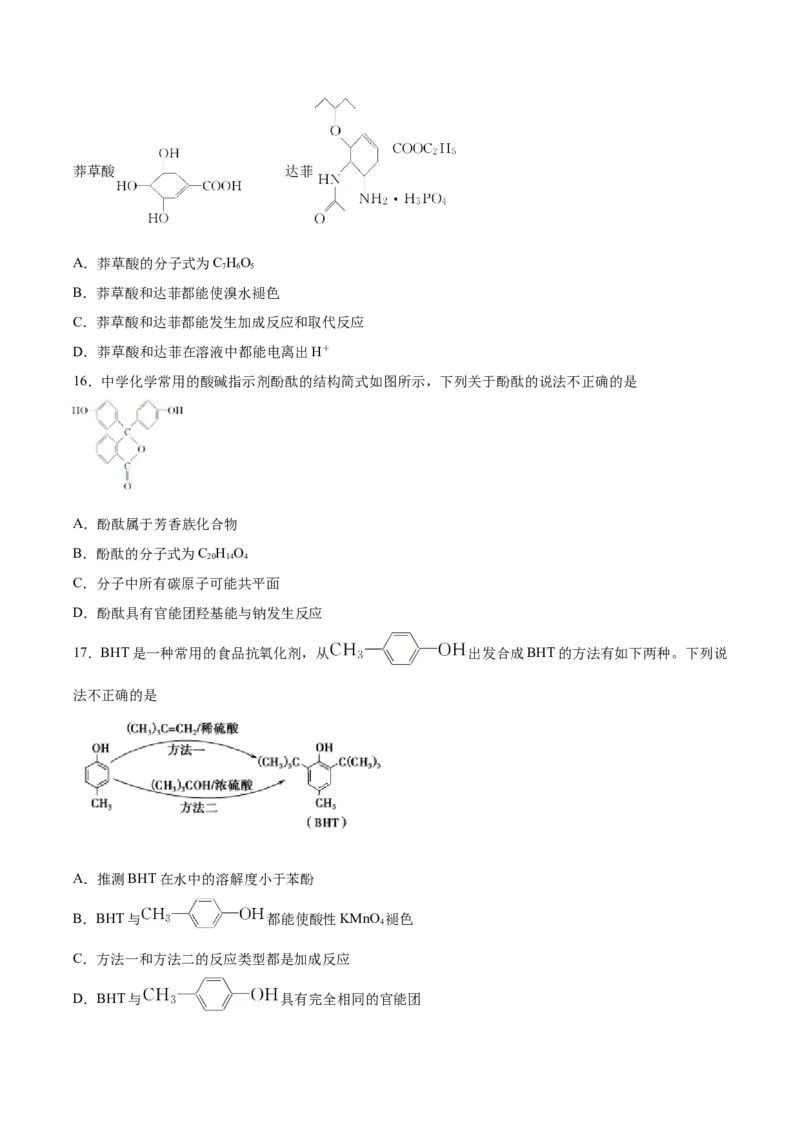
15.达菲是一种治疗甲型和乙型流感的药物,工业上可用莽草酸合成达菲,两者结构简式如下,下列有关
莽草酸和达菲的说法不正确的是莽草酸 达菲
A.莽草酸的分子式为C HO
7 6 5
B.莽草酸和达菲都能使溴水褪色
C.莽草酸和达菲都能发生加成反应和取代反应
D.莽草酸和达菲在溶液中都能电离出H+
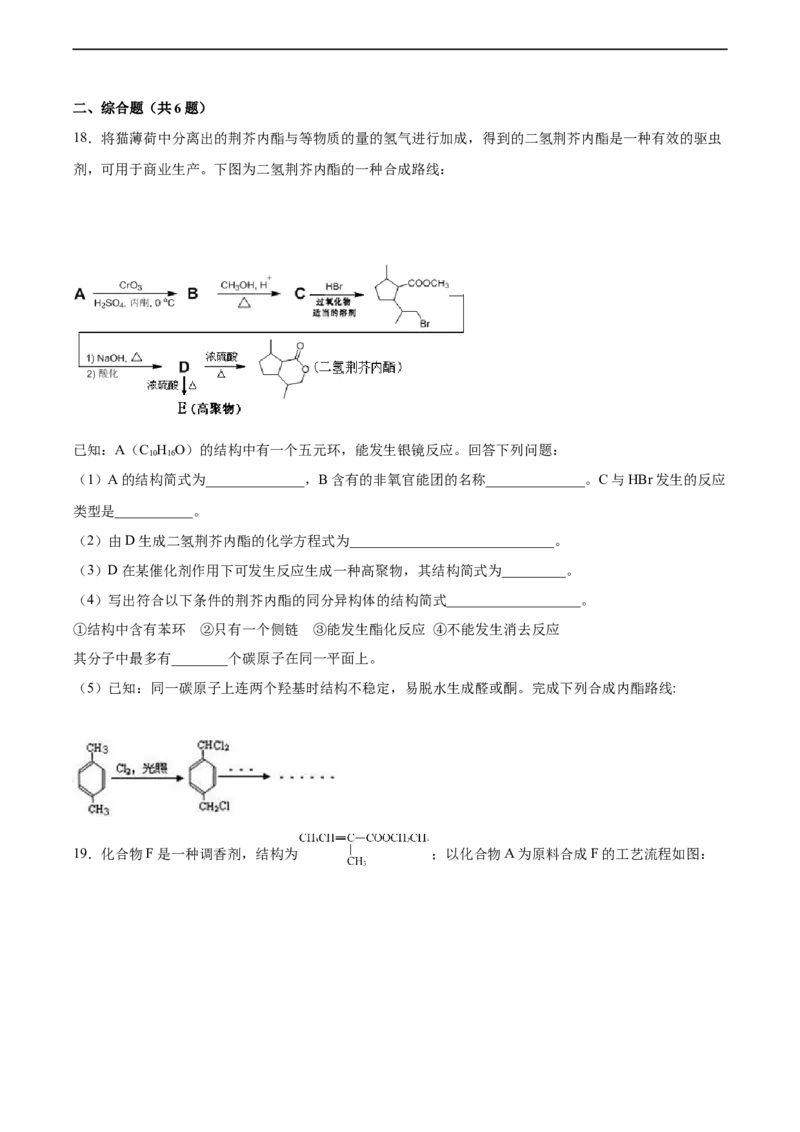
16.中学化学常用的酸碱指示剂酚酞的结构简式如图所示,下列关于酚酞的说法不正确的是
A.酚酞属于芳香族化合物
B.酚酞的分子式为C H O
20 14 4
C.分子中所有碳原子可能共平面
D.酚酞具有官能团羟基能与钠发生反应
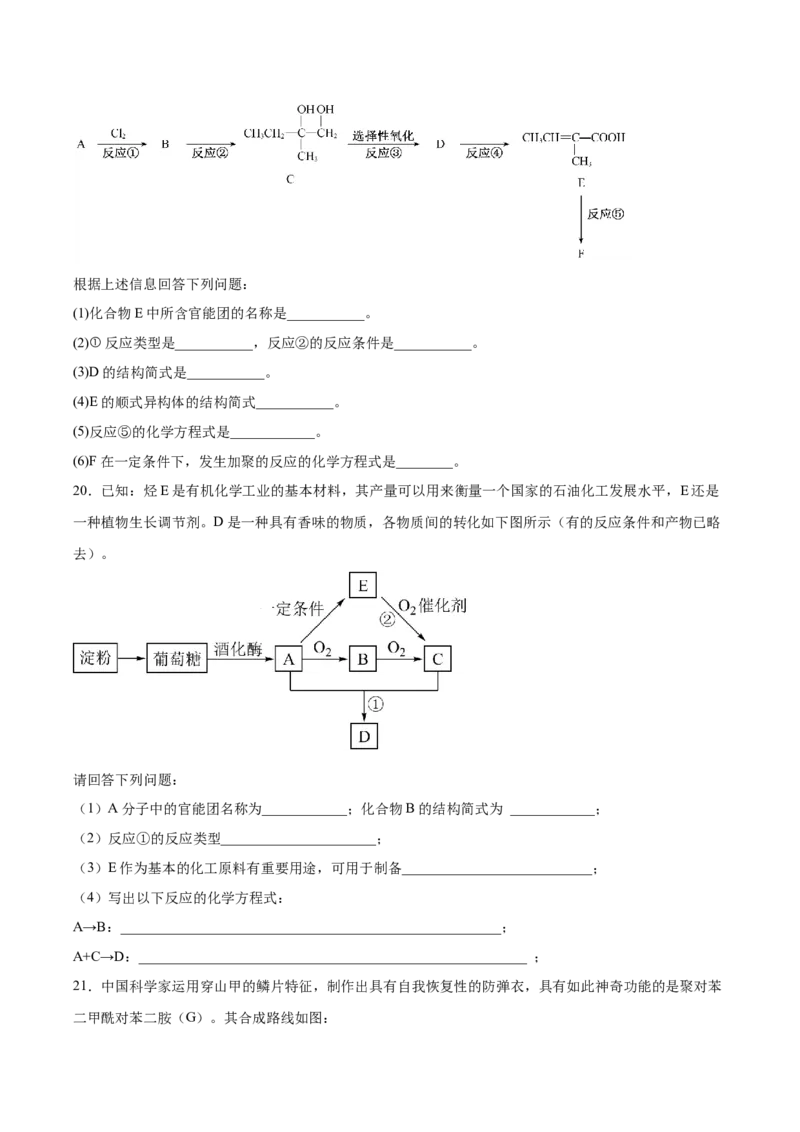
17.BHT是一种常用的食品抗氧化剂,从 出发合成BHT的方法有如下两种。下列说
法不正确的是
A.推测BHT在水中的溶解度小于苯酚
B.BHT与 都能使酸性KMnO 褪色
4
C.方法一和方法二的反应类型都是加成反应
D.BHT与 具有完全相同的官能团二、综合题(共6题)
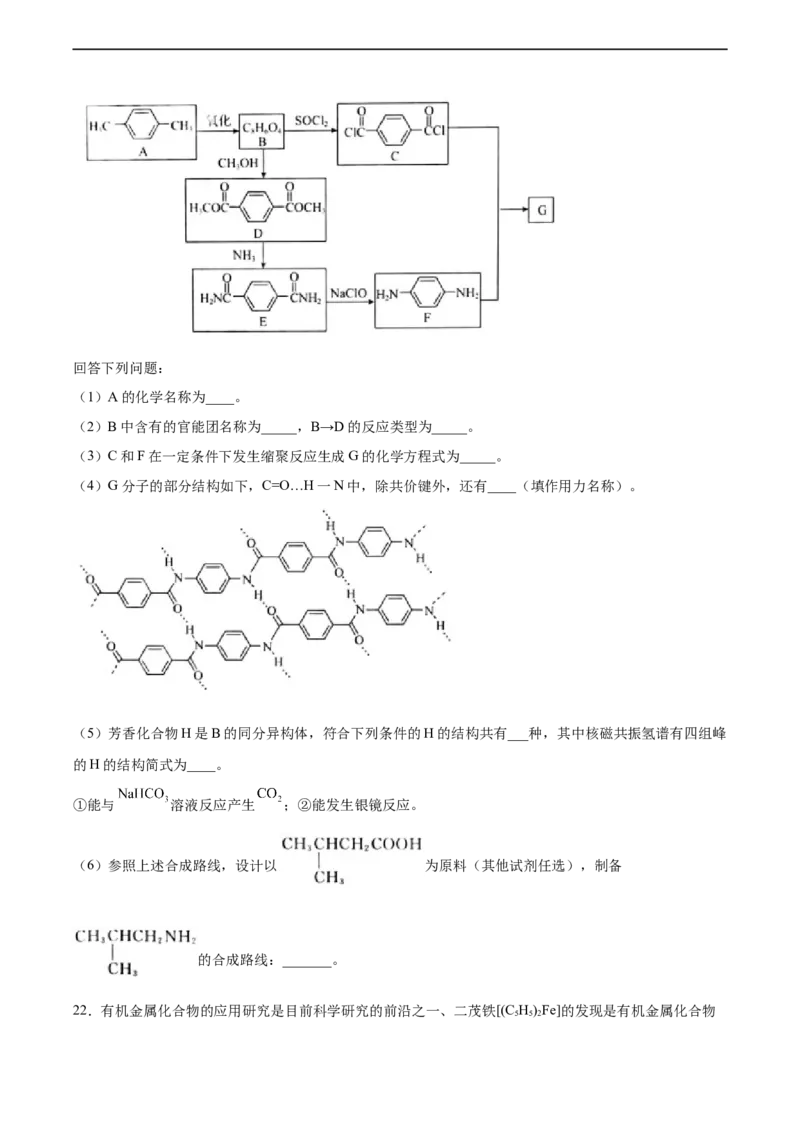
18.将猫薄荷中分离出的荆芥内酯与等物质的量的氢气进行加成,得到的二氢荆芥内酯是一种有效的驱虫
剂,可用于商业生产。下图为二氢荆芥内酯的一种合成路线:
已知:A(C H O)的结构中有一个五元环,能发生银镜反应。回答下列问题:
10 16
(1)A的结构简式为______________,B含有的非氧官能团的名称______________。C与HBr发生的反应
类型是___________。
(2)由D生成二氢荆芥内酯的化学方程式为_____________________________。
(3)D在某催化剂作用下可发生反应生成一种高聚物,其结构简式为_________。
(4)写出符合以下条件的荆芥内酯的同分异构体的结构简式___________________。
①结构中含有苯环 ②只有一个侧链 ③能发生酯化反应 ④不能发生消去反应
其分子中最多有________个碳原子在同一平面上。
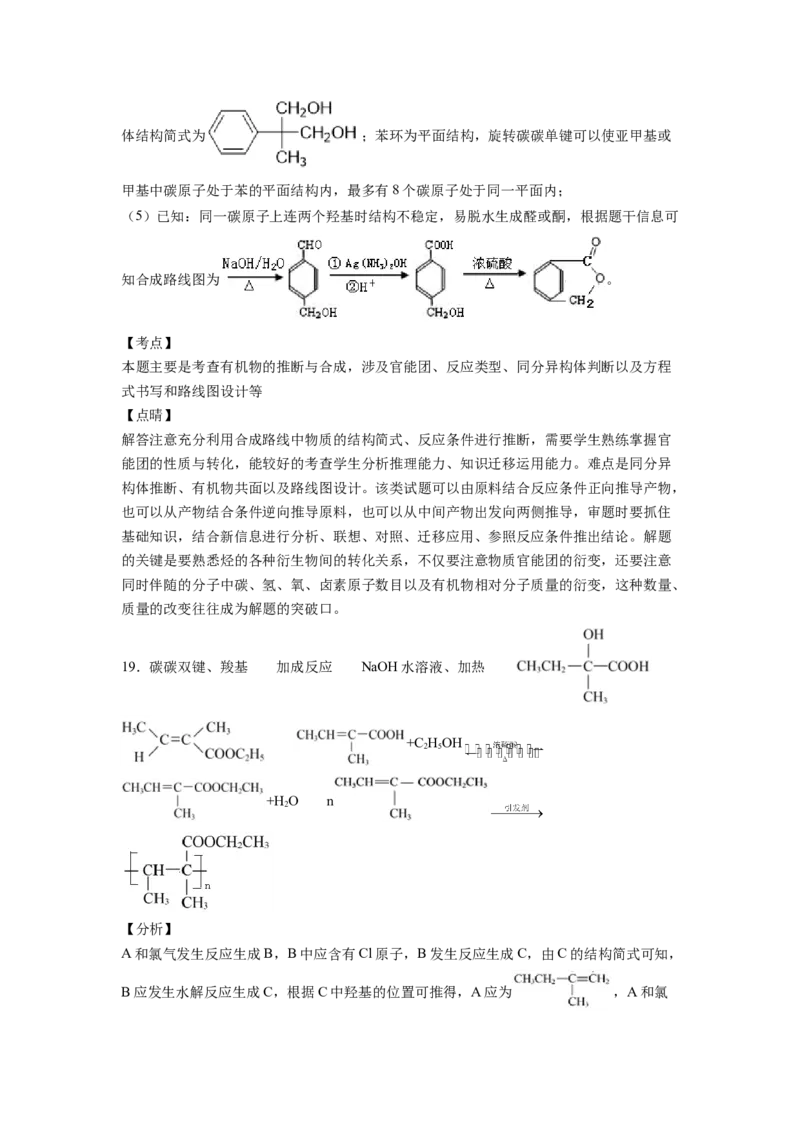
(5)已知:同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮。完成下列合成内酯路线:
19.化合物F是一种调香剂,结构为 ;以化合物A为原料合成F的工艺流程如图:根据上述信息回答下列问题:
(1)化合物E中所含官能团的名称是___________。
(2)①反应类型是___________,反应②的反应条件是___________。
(3)D的结构简式是___________。
(4)E的顺式异构体的结构简式___________。
(5)反应⑤的化学方程式是____________。
(6)F在一定条件下,发生加聚的反应的化学方程式是________。
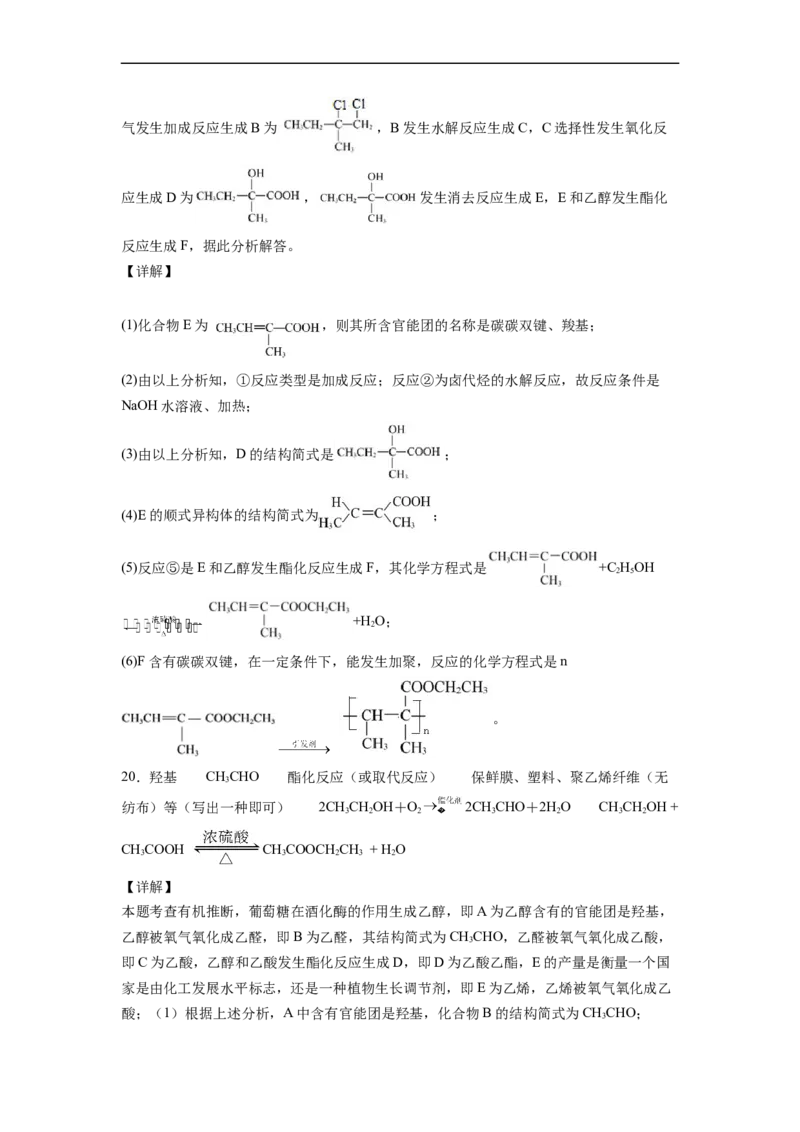
20.已知:烃E是有机化学工业的基本材料,其产量可以用来衡量一个国家的石油化工发展水平,E还是
一种植物生长调节剂。D是一种具有香味的物质,各物质间的转化如下图所示(有的反应条件和产物已略
去)。
请回答下列问题:
(1)A分子中的官能团名称为____________;化合物B的结构简式为 ____________;
(2)反应①的反应类型______________________;
(3)E作为基本的化工原料有重要用途,可用于制备___________________________;
(4)写出以下反应的化学方程式:
A→B:______________________________________________________;
A+C→D:_______________________________________________________ ;
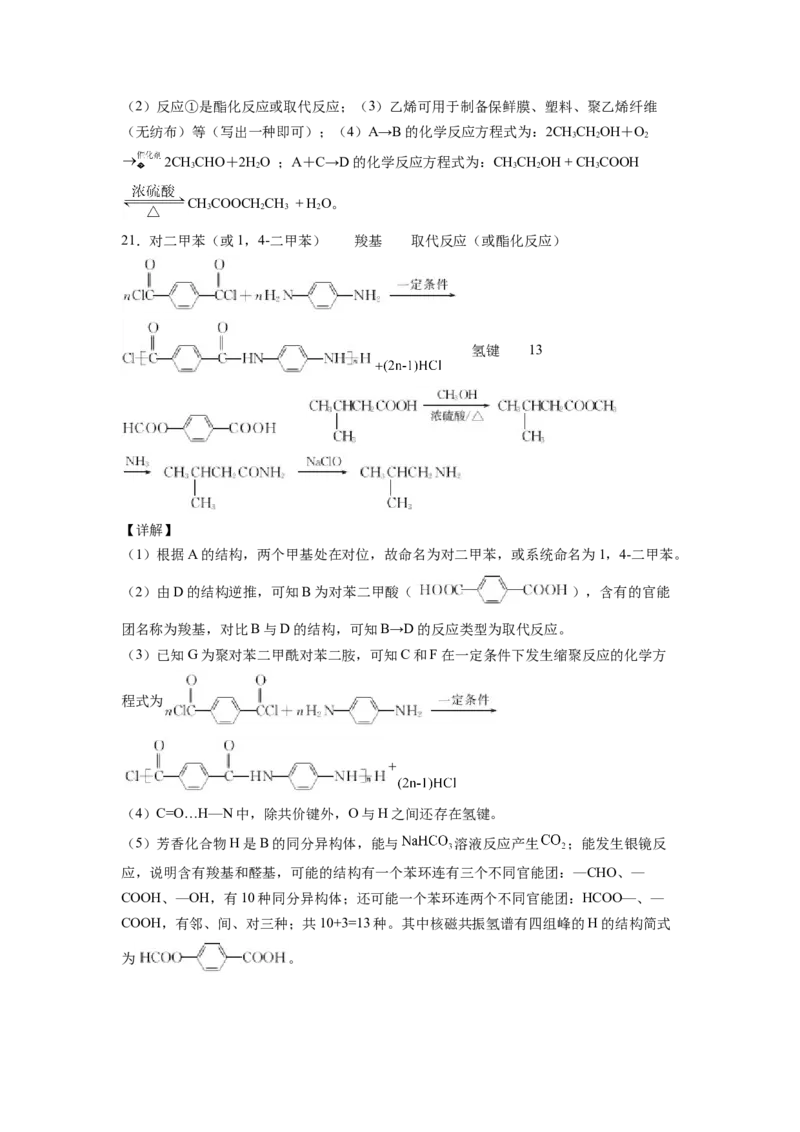
21.中国科学家运用穿山甲的鳞片特征,制作出具有自我恢复性的防弹衣,具有如此神奇功能的是聚对苯
二甲酰对苯二胺(G)。其合成路线如图:回答下列问题:
(1)A的化学名称为____。
(2)B中含有的官能团名称为_____,B→D的反应类型为_____。
(3)C和F在一定条件下发生缩聚反应生成G的化学方程式为_____。
(4)G分子的部分结构如下,C=O…H一N中,除共价键外,还有____(填作用力名称)。
(5)芳香化合物H是B的同分异构体,符合下列条件的H的结构共有___种,其中核磁共振氢谱有四组峰
的H的结构简式为____。
①能与 溶液反应产生 ;②能发生银镜反应。
(6)参照上述合成路线,设计以 为原料(其他试剂任选),制备
的合成路线:_______。
22.有机金属化合物的应用研究是目前科学研究的前沿之一、二茂铁[(C H)Fe]的发现是有机金属化合物
5 5 2研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。二茂铁分子是一种金属有机配合
物,熔点173℃,沸点249℃,100℃以上能升华;不溶于水,易溶于苯、乙醚、汽油等有机溶剂。环戊二
烯和二茂铁的结构如图所示。回答下列问题。
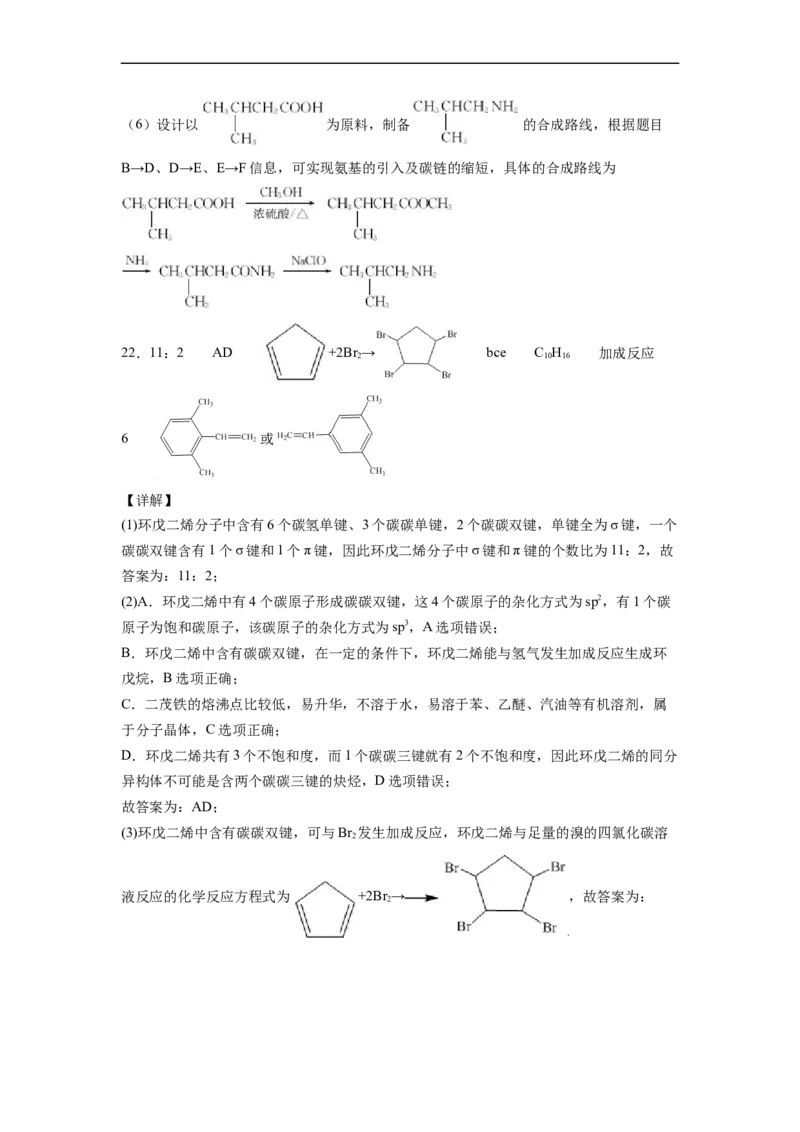
(1)环戊二烯分子中σ键和π键的个数比为___________。
(2)下列关于环戊二烯和二茂铁的说法不正确的是___________ (填字母序号)。
A.环戊二烯分子中五个碳原子均发生sp2杂化
B.在一定的条件下,环戊二烯能与氢气发生加成反应生成环戊烷
C.二茂铁晶体是分子晶体
D.环戊二烯的同分异构体可能是含两个碳碳三键的炔烃
(3)环戊二烯能使溴的四氯化碳溶液褪色。写出环戊二烯与足量的溴的四氯化碳溶液反应的化学方程式
___________。
(4)已知环戊二烯阴离子(C H )的结构与苯分子相似,具有芳香性。二茂铁[(C H)Fe]晶体中存在的微粒间
5 5 5 2
的作用力有___________(填字母序号)。
a.离子键 b.σ键 c.π键 d.氢键 e.配位键
(5)金刚烷可用于抗病毒、抗肿瘤等特效药物的合成。工业上用环戊二烯合成金刚烷的流程如图所示:
①金刚烷的分子式为___________,反应①的反应类型是___________。
②金刚烷的二氯代物有___________种(不考虑立体异构)。
③二聚环戊二烯有多种同分异构体。写出一种符合下列条件的二聚环戊二烯的同分异构体的结构简式
___________。
(a)属于芳香烃且能使溴的四氯化碳溶液褪色;
(b)苯环上有三个取代基;
(c)苯环上的一氯代物有2种。23.人体必需的元素包括常量元素与微量元素,常量元素包括碳、氢、氧、氮、钙、镁等,微量元素包括
铁、铜、锌、氟、碘等,这些元素形成的化合物种类繁多,应用广泛。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出Fe2+的核外电子排布式___________。
(2)1个Cu2+与2个HN—CH —COO−形成含两个五元环结构的内配盐(化合物),其结构简式为
2 2
___________(用→标出配位键),在HN—CH —COO−中,属于第二周期的元素的第一电离能由大到小的顺
2 2
序是___________(用元素符号表示),N、C原子存在的相同杂化方式是___________杂化。
(3)碳酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径r(Mg2+)=66 pm,r(Ca2+)=99
pm,r(Sr2+)=112 pm,r(Ba2+)=135 pm;碳酸盐分解温度T(MgCO)=402℃,T(CaCO )=825℃,
3 3
T(SrCO)=1172℃,T(BaCO )=1360℃。分析数据得出的规律是___________,解释出现此规律的原因是
3 3
___________。
(4)自然界的氟化钙矿物为萤石或氟石,CaF 的晶体结构呈立方体形,其结构如下:
2
①两个最近的F−之间的距离是___________pm(用含m的代数式表示)。
②CaF 晶胞体积与8个F−形成的立方体的体积比为___________。
2
③CaF 晶胞的密度是___________g·cm−3(化简至带根号的最简式,N 表示阿伏加德罗常数的值)。
2 A参考答案
1.D
【解析】试题分析:淀粉碘化钾试纸立刻显蓝色,是因为青蒿素中含有过氧键,具有强氧
化性将碘离子氧化,而酯基没有强氧化性,D符合题意。
考点:有机物机构及常见官能团的性质考查
2.D
【分析】
B、C反应可制造高分子化合物 ,该高聚物是缩聚产物,其单体
是乙二醇和乙二酸,则A是乙二醛,B是乙二醇,C是乙二酸,据此解答。
【详解】
A. A是乙二醛,属于醛类,其相对分子质量为58,A是二元醛,1molA与足量的银氨溶液
反应可生成4molAg,故A正确;
B. B是乙二醇,在一定条件下可以发生分子间脱水反应,即通过缩聚反应得到一种新的高
聚物 ,故B正确;
C. 乙二醇和乙二酸通过缩聚反应生成高分子化合物 ,故C正确;
D. 高分子化合物 是缩聚反应的产物,发生缩聚反应时还有水生
成,故其组成与B、C等物质的混合物的组成不同,故D错误;
答案选D。
3.D
【分析】
淀粉水解生成葡萄糖(X),葡萄糖在酒化酶的作用下分解生成乙醇(Y),乙醇可与乙酸
(M)反应生成乙酸乙酯。
【详解】
A、X为葡萄糖,含有醛基,可用新制的氢氧化铜检验,故A正确;
B、Y为乙醇,有同分异构体二甲醚,故B正确;
C、M为乙酸,有碳氧单键和碳氧双键,故C正确;
D、Y为乙醇,不能发生加成反应,故D错误;
故选D。
4.D
【详解】
A.该物质含有苯环和碳碳双键,一定条件下可以与氢气发生加成反应,故A正确;
B.根据该物质的结构简式可知该分子含有21个碳原子,故B正确;
C.该物质含有羟基,可以与乙酸发生酯化反应,故C正确;D.该物质含有普通羟基和酚羟基,可以与金属钠反应放出氢气,故D错误;
故答案为D。
5.B
【详解】
A.该分子中含有1个酚羟基和1个羧基,所以1molM与氢氧化钠溶液反应完全,消耗
2molNaOH,故A错误;
B.M含有羟基能与乙酸发生酯化反应,含有羧基能与乙醇发生酯化反应,故B正确;
C.M中含有酚羟基和羧基,能与碳酸钠反应,故C错误;
D.羟基和羧基能与钠反应,则1molM与Na反应生成1.5mol氢气,羧基与NaHCO 反应
3
生成二氧化碳,则1molM与NaHCO 完全反应生成1mol二氧化碳,则产生气体的物质的
3
量之比为3:2,故D错误;
答案选B。
6.C
【详解】
A.该有机物分子中共面的碳原子最多为13个;A错误;
B.因苯基对称轴上碳原子在一直线上,共直线的C原子只有为6个,B错误;
C.分子中的苯基、碳碳叁键、碳碳双键都能与H 发生加成反应,则可以和6mol H 发生加
2 2
成反应,C正确;
D. 1mol该烃最多可以和3mol溴发生加成反应,如果发生取代反应:苯环、烃基的氢被取
代,消耗的Br 多于6 mol,D错误;
2
答案选C。
7.D
【详解】
A.该有机物分子中含有1个苯环,且苯环上连有1个-OH,属于酚类,遇FeCl 溶液显紫
3
色,A正确;
B.该有机物分子中含有酚羟基和醇羟基,它们都能与Na反应,B正确;
C.该有机物分子中含有酚羟基和酯基,都可以与氢氧化钠反应,C正确;
D.醇羟基与NaOH不能反应,酯基与H 不能反应,但能与NaOH发生反应,所以1 mol
2
该有机物最多可以和2 mol NaOH、6mol H 反应,D错误;
2
故选D。
8.C
【分析】
D的结构为 ,结合烃A B C D可知,C
为HOCH CHOH,B为BrCHCHBr,烃A为乙烯,反应①为加成、②为水解、③为取代
2 2 2 2
反应,以此来解答。
【详解】由上述分析可知,A为乙烯,B为BrCHCHBr,C为HOCH CHOH,则
2 2 2 2
A.A为CH=CH ,故A正确;
2 2
B.反应①为加成、②为水解、③为取代反应,水解反应属于取代反应,故B正确;
C.快速升温至170℃,醇发生消去反应,不能发生取代反应生成醚,故C错误;
D.D中含醚键,为环醚,故D正确;
故答案选C。
9.D
【分析】
CPAE中含酚-OH、-COOC-和碳碳双键;咖啡酸中含有酚羟基、碳碳双键和羧基;结合相
关官能团的结构和性质分析判断。
【详解】
A.CPAE含酚-OH、-COOC-和碳碳双键,其中酚-OH和碳碳双键能够与溴水反应,则
1mol最多可与含4mol溴发生反应,故A正确;
B.咖啡酸含C=C,酚-OH、-COOC-,共3种官能团,含C=C可发生加聚反应,故B正确;
C.与苯乙醇互为同分异构体的酚类物质,含酚-OH、乙基(或2个甲基),含酚-OH、乙基
存在邻、间、对三种,两个甲基处于邻位的酚2种,两个甲基处于间位的有3种,两个甲
基处于对位的有1种,共9种,故C正确;
D.CPAE中含酚-OH、苯乙醇中含-OH,均与Na反应生成氢气,则不能用金属Na检测上
述反应是否残留苯乙醇,故D错误;
答案选D。
10.C
【详解】
NaOH溶液吸收40mL为燃烧生成CO 的体积,产物通过浓硫酸,再恢复至室温,气体体
2
积减少了50mL,则:C H+(x+ )O xCO+ HO,则: ,整理
x y 2 2 2
可得:5x=y+4,若x=1,则y=1,不符合,若x=2,则y=6,则分子式为C H,若x=3,则
2 6
y=11,不符合,若x=4,则y=16,不符合,所以该烃的分子式为:C H,故C正确。
2 6
故选:C。
11.D
【详解】
A.由结构简式可知分子式为C H O,故A正确;
23 36 7
B.不含酚羟基,则不能与FeCl 溶液发生显色反应,故B正确;
3
C.含-OH、-COOH可发生酯化反应,含-COOC-可发生水解反应,含双键可发生加成、氧
化,羟基可发生消去反应,故C正确;
D.能与氢氧化钠反应的为酯基和羧基,则1 mol该物质最多可与2mol NaOH反应,故D
错误。故选:D。
12.B
【详解】
A.①与②分子式均为C H O,属于同分异构体,③与④分子式均为C HO,属于同分异
13 10 5 12 8 4
构体,A正确;
B.①、③的结构相似,但两者相差一个OCH ,因此不属于同系物,B错误;
2
C.1mol的②耗氧量为 ,1mol的④耗氧量为 ,故等物质
的量时,前者耗氧量大于后者耗氧量,C正确;
D.4种物质都含有酯基,都能与氢氧化钠发生反应,D正确;
答案选B。
13.A
【详解】
相同质量的碳和氢燃烧,氢消耗的氧气量更多。即等质量的烃完全燃烧时,氢的百分含量
越多,消耗氧气量越多;因此比较y/x:A为4,B为2,C为4/3,D为1, A选项符合题
意。
14.C
【详解】
试题分析:A.由结构简式可知分子式为C H O,故A错误;B.香叶醇中与-OH相连的
11 20
C的邻位C上没有H原子,则不能发生消去反应,故B错误;C.1 mol甲酸香叶酯中含
2molC=C,则可以与2 molH 发生加成反应,故C正确;D.甲酸香叶酯中含3个甲基、2
2
个亚甲基、1个CH,均为四面体结构,所以所有碳原子不可能共平面,故D错误;故选
C。
【考点定位】考查有机物的结构与性质
【名师点晴】本题考查有机物的结构与性质,注意把握结构中的官能团及性质的关系,熟
悉烯烃的性质即可解答,选项D为解答的难点。有机物中的原子共平面问题可以直接联想
甲烷的正四面体结构、乙烯的平面型结构、乙炔的直线型结构和苯的平面型结构,对有机
物进行肢解,分部分析,另外要重点掌握碳碳单键可旋转、双键和三键不可旋转。
15.A
【详解】
A.由结构简式可知,莽草酸的分子式为C H O,故A错误;
7 10 5
B.由结构简式可知,莽草酸和达菲都含有碳碳双键,能与溴水发生加成反应,使溴水褪
色,故B正确;
C.由结构简式可知,莽草酸和达菲都含有碳碳双键,能发生加成反应,莽草酸分子中含
有的羟基、羧基都能发生取代反应,达菲含有的酯基、酰胺基都能发生取代反应,则莽草
酸和达菲都能发生加成反应和取代反应,故C正确;
D.由结构简式可知,莽草酸中含有—COOH,达菲分子中含有HPO ,在溶液中都能电离
3 4出H+,故D正确;
故选A。
16.C
【分析】
A. 酚酞含有苯环;B. 由结构简式可知酚酞的分子式;D. 金属钠能置换羟基上的氢原子。
【详解】
A. 酚酞含有苯环,属于芳香族化合物,故A正确;
B. 由结构简式可知,酚酞的分子式为C H O,故B正确;
20 14 4
C. 分子中含有饱和碳原子,该饱和碳原子的其中三个键连着其它碳原子,所有碳原子不可
能共平面,故C错误;
D. 金属钠能置换羟基上的氢原子,酚酞具有羟基,故其能与钠发生反应,D正确;
答案选C。
17.C
【分析】
A.BHT中烃基数目比苯酚多,烃基为憎水基,溶解性一定小于苯酚;B.酚羟基具有还
原性,都能够被强氧化剂氧化;C.反应一为加成,反应二为取代;D.BHT中含有的官
能团是酚羟基.
【详解】
A.BHT中含有的憎水基烃基比苯酚多,在水中的溶解度小于苯酚,故A正确;B.BHT
和 中都会有酚羟基,都能够被酸性高锰酸钾溶液氧化,使酸性KMnO
4
褪色,故B正确;C、由方法二可知,酚-OH的邻位H被叔丁基取代,为取代反应,故C
错误;D、BHT中含有的官能团是酚羟基, 中含有的官能团也是酚羟基,
故D正确,故选C。
18. 碳碳双键 加成反应 +H O
2
【详解】
试题分析:A的分子式为C H O,不饱和度为 =3,A的结构中有一个五元
10 16环,结合 的结构可知A为 ,A发生氧化反应得到B为
,B与甲醇发生转化反应得到C为 ,C再与HBr反应加成反应
得到 ,在碱性条件下发生水解反应、酸化得到D为 ,D发生酯
化反应得到二氢荆芥内酯,D发生缩聚反应得到高聚物E为 。
(1)A的结构简式为 ,B为 ,含有的非氧官能团为碳碳双键,
C与HBr发生的反应类型是加成反应;
(2)由D生成二氢荆芥内酯的化学方程式为:
;
(3)D为 ,含有羧基、羟基,在某催化剂作用下可发生缩聚反应,生成一
种高聚物的结构简式为 ;
(4)符合以下条件的二氢荆芥内酯的同分异构体:①结构中含有苯环,则侧链没有不饱和
键;②只有一个侧链,③能发生酯化反应,含有羟基,④不能发生消去反应,该同分异构体结构简式为 ;苯环为平面结构,旋转碳碳单键可以使亚甲基或
甲基中碳原子处于苯的平面结构内,最多有8个碳原子处于同一平面内;
(5)已知:同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮,根据题干信息可
知合成路线图为 。
【考点】
本题主要是考查有机物的推断与合成,涉及官能团、反应类型、同分异构体判断以及方程
式书写和路线图设计等
【点晴】
解答注意充分利用合成路线中物质的结构简式、反应条件进行推断,需要学生熟练掌握官
能团的性质与转化,能较好的考查学生分析推理能力、知识迁移运用能力。难点是同分异
构体推断、有机物共面以及路线图设计。该类试题可以由原料结合反应条件正向推导产物,
也可以从产物结合条件逆向推导原料,也可以从中间产物出发向两侧推导,审题时要抓住
基础知识,结合新信息进行分析、联想、对照、迁移应用、参照反应条件推出结论。解题
的关键是要熟悉烃的各种衍生物间的转化关系,不仅要注意物质官能团的衍变,还要注意
同时伴随的分子中碳、氢、氧、卤素原子数目以及有机物相对分子质量的衍变,这种数量、
质量的改变往往成为解题的突破口。
19.碳碳双键、羧基 加成反应 NaOH水溶液、加热
+C HOH
2 5
+H O n
2
【分析】
A和氯气发生反应生成B,B中应含有Cl原子,B发生反应生成C,由C的结构简式可知,
B应发生水解反应生成C,根据C中羟基的位置可推得,A应为 ,A和氯气发生加成反应生成B为 ,B发生水解反应生成C,C选择性发生氧化反
应生成D为 , 发生消去反应生成E,E和乙醇发生酯化
反应生成F,据此分析解答。
【详解】
(1)化合物E为 ,则其所含官能团的名称是碳碳双键、羧基;
(2)由以上分析知,①反应类型是加成反应;反应②为卤代烃的水解反应,故反应条件是
NaOH水溶液、加热;
(3)由以上分析知,D的结构简式是 ;
(4)E的顺式异构体的结构简式为 ;
(5)反应⑤是E和乙醇发生酯化反应生成F,其化学方程式是 +C HOH
2 5
+H O;
2
(6)F含有碳碳双键,在一定条件下,能发生加聚,反应的化学方程式是n
。
20.羟基 CHCHO 酯化反应(或取代反应) 保鲜膜、塑料、聚乙烯纤维(无
3
纺布)等(写出一种即可) 2CHCHOH+O 2CHCHO+2HO CH CHOH +
3 2 2 3 2 3 2
CHCOOH CHCOOCH CH + H O
3 3 2 3 2
【详解】
本题考查有机推断,葡萄糖在酒化酶的作用生成乙醇,即A为乙醇含有的官能团是羟基,
乙醇被氧气氧化成乙醛,即B为乙醛,其结构简式为CHCHO,乙醛被氧气氧化成乙酸,
3
即C为乙酸,乙醇和乙酸发生酯化反应生成D,即D为乙酸乙酯,E的产量是衡量一个国
家是由化工发展水平标志,还是一种植物生长调节剂,即E为乙烯,乙烯被氧气氧化成乙
酸;(1)根据上述分析,A中含有官能团是羟基,化合物B的结构简式为CHCHO;
3(2)反应①是酯化反应或取代反应;(3)乙烯可用于制备保鲜膜、塑料、聚乙烯纤维
(无纺布)等(写出一种即可);(4)A→B的化学反应方程式为:2CHCHOH+O
3 2 2
2CHCHO+2HO ;A+C→D的化学反应方程式为:CHCHOH + CH COOH
3 2 3 2 3
CHCOOCH CH + H O。
3 2 3 2
21.对二甲苯(或1,4-二甲苯) 羧基 取代反应(或酯化反应)
氢键 13
【详解】
(1)根据A的结构,两个甲基处在对位,故命名为对二甲苯,或系统命名为1,4-二甲苯。
(2)由D的结构逆推,可知B为对苯二甲酸( ),含有的官能
团名称为羧基,对比B与D的结构,可知B→D的反应类型为取代反应。
(3)已知G为聚对苯二甲酰对苯二胺,可知C和F在一定条件下发生缩聚反应的化学方
程式为
+
(4)C=O…H—N中,除共价键外,O与H之间还存在氢键。
(5)芳香化合物H是B的同分异构体,能与 溶液反应产生 ;能发生银镜反
应,说明含有羧基和醛基,可能的结构有一个苯环连有三个不同官能团:—CHO、—
COOH、—OH,有10种同分异构体;还可能一个苯环连两个不同官能团:HCOO—、—
COOH,有邻、间、对三种;共10+3=13种。其中核磁共振氢谱有四组峰的H的结构简式
为 。(6)设计以 为原料,制备 的合成路线,根据题目
B→D、D→E、E→F信息,可实现氨基的引入及碳链的缩短,具体的合成路线为
22.11:2 AD +2Br → bce C H 加成反应
2 10 16
6 或
【详解】
(1)环戊二烯分子中含有6个碳氢单键、3个碳碳单键,2个碳碳双键,单键全为σ键,一个
碳碳双键含有1个σ键和1个π键,因此环戊二烯分子中σ键和π键的个数比为11:2,故
答案为:11:2;
(2)A.环戊二烯中有4个碳原子形成碳碳双键,这4个碳原子的杂化方式为sp2,有1个碳
原子为饱和碳原子,该碳原子的杂化方式为sp3,A选项错误;
B.环戊二烯中含有碳碳双键,在一定的条件下,环戊二烯能与氢气发生加成反应生成环
戊烷,B选项正确;
C.二茂铁的熔沸点比较低,易升华,不溶于水,易溶于苯、乙醚、汽油等有机溶剂,属
于分子晶体,C选项正确;
D.环戊二烯共有3个不饱和度,而1个碳碳三键就有2个不饱和度,因此环戊二烯的同分
异构体不可能是含两个碳碳三键的炔烃,D选项错误;
故答案为:AD;
(3)环戊二烯中含有碳碳双键,可与Br 发生加成反应,环戊二烯与足量的溴的四氯化碳溶
2
液反应的化学反应方程式为 +2Br → ,故答案为:
2+2Br → ;
2
(4)由题干信息,二茂铁分子中含有两个环戊二烯阴离子,环戊二烯阴离子的结构与苯分子
相似,所以含有σ键和π键,环戊二烯阴离子和Fe2+形成配位键,故答案为:bce;
(5)①由题干信息可知,金刚烷的结构式为 ,其分子式为C H ,反应①环戊二
10 16
烯中的一个碳碳双键的加成反应,故答案为:C H ;加成反应;
10 16
②金刚烷结构中共有二种等效氢如图 ,一氯代物有二种,当一个氯在①位
上时,另一个氯的位置可以有3种,当一个氯在②上时,另一个氯的位置3种,共6种,
故答案为:6;
③二聚环戊二烯的分子式为C H ,不饱和度为5,其同分异构体属于芳香烃,说明含有苯
10 12
环,其苯环上的一氯代物只有两种,说明该分子高度对称,能使溴的四氯化碳溶液褪色,
说明有碳碳双键,又苯环上有三个取代基,符合上述条件的同分异构体的可能的结构简式
为 、 ,故答案为 、 。
23.[Ar]3d6(或1s22s22p63s23p63d6) N>O>C sp3
随着这类金属阳离子半径的增大,碳酸盐的热分解温度逐渐升高 金属离子半径越小,
其与碳酸根离子中氧的作用力越强,与碳的作用力则减弱,对应的碳酸盐就越容易分解(或
其他合理答案) 8∶1
【详解】
(1)Fe的核电荷数为26,核外电子排布式[Ar]3d64s2或1s22s22p63s23p63d64s2,Fe2+的核外电子
排布式为[Ar]3d6或1s22s22p63s23p63d6。
(2)1个Cu2+与2个HN—CH —COO−形成的盐,因为含两个五元环结构,所以结构为
2 2;在HN—CH —COO−中,属于第二周期元素的是C、N、
2 2
O,第一电离能由大到小的顺序是N>O>C,在HN—CH —COO−中,N的杂化方式为
2 2
sp3、C的杂化方式为sp3和sp2,相同的是sp3杂化。
(3)随着金属离子半径的增大,碳酸盐的热分解温度逐步升高;一般认为,含氧酸盐热分解
的本质是金属离子争夺含氧酸根中的氧元素,金属离子的半径越小,夺取含氧酸根中的氧
的能力越强,含氧酸盐的热分解温度越低,越易分解。
(4)①根据侧面图可看出,2m pm为面对角线的长度,边长为 pm,两个最近的F−之间
的距离为立方体边长的一半,所以两个最近的F−之间的距离为 pm。
②观察晶胞,可看出8个F−形成的小立方体的边长为CaF 晶胞边长的 ,所以CaF 晶胞体
2 2
积与8个F−形成的立方体的体积比为(2∶1)3=8∶1。
③根据图示可知CaF 晶胞中含4个Ca2+和8个F−,它的边长为 pm= ×10−10 cm,利
2
用ρVN =4M得出ρ= g·cm−3= g·cm−3
A