文档内容
2022 届高三化学二轮复习镁及其化合物专项练习
一、选择题(共17题)
1.下列物质分别与100mL、2mol/L的盐酸恰好反应时,所得溶液的溶质的物质的量浓度的大小关系是:
①镁粉 ②氧化镁 ③氢氧化镁 ④碳酸镁
A.①>②>③>④ B.①>②=④>③ C.①>④>③=② D.④>①>②=③
2.下列有关物质的性质与用途具有对应关系且正确的是
A.由于镁很活泼,点燃镁条之前,应该用砂纸打磨掉表面氧化膜
B.明矾溶于水能形成胶体,可用于自来水的杀菌消毒
C.金属钠具有强还原性,可用其与TiCl 溶液反应制取金属Ti
4
D.Al O 具有很高的熔点,可用于制造熔融烧碱的坩埚
2 3
3.下列物质中属于镁条在空气中燃烧产物的是( )
①MgCO ②Mg(OH) ③MgO④C ⑤MgN ⑥CO
3 2 3 2
A.①②③
B.⑤⑥
C.③④⑤
D.②③
4.下列有关钠和镁的说法中,不正确的是( )
A.电解熔融NaCl可以得到金属钠
B.金属钠在高温下能将TiCl 中的钛置换出来
4
C.金属镁着火,可用氮气灭火
D.金属镁燃烧后会发出耀眼的白光,因此常用来制造信号弹和焰火
5.把镁粉中混有的少量铝粉除去,应选用的试剂是
A.稀盐酸 B.烧碱溶液
C.硫酸铝溶液 D.硫酸镁溶液
6.下列物质的转化在给定条件下能实现的是( )
①
②
③
④⑤
A.①②③ B.②③④ C.①③⑤ D.②④⑤
7.下列有关实验现象的描述,错误的是
A.硫在氧气中燃烧,火焰呈明亮的蓝紫色,生成有刺激性气味的气体
B.磷在空气中燃烧火焰呈黄色,生成大量白烟
C.木炭在氧气中燃烧发出白光而在空气中燃烧则灼热成红热
D.镁条在氧气中燃烧,火星四射,生成黑色固体
8.现代建筑的门窗框架常用电镀加工成的古铜色硬铝制造。取硬铝样品进行如下图所示的实验(每一步试
剂均过量),由此可推知,硬铝的组成为(已知Si与NaOH溶液反应产生H) ( )
2
样品
A.Al,Cu,Mg,Si B.Al,Mg,Si,Zn
C.Al,Fe,C,Cu D.Al,Si,Zn,Na
9.自然界中存在一种尖晶石,化学式可表示为MgAlO,它透明色美,可作为宝石。已知该尖晶石中混有
2 4
Fe O。取一定量样品5.4g,恰好完全溶解在一定浓度100 mL盐酸溶液中,盐酸浓度可能是( )
2 3
A.2.8 mol·L-1 B.3.8 mol·L-1 C.4.3 mol·L-1 D.4.9 mol·L-1
10.下列氧化物的性质与用途具有对应关系的是
A. 具有漂白性,可用作溴蒸气的吸收剂
B.CaO具有碱性氧化物的性质,燃煤中加入CaO可以减少酸雨的形成
C. 是两性氧化物,可以用作防腐涂层
D.MgO熔融状态下能导电,可以用作耐火材料
11.将2.6g金属混合物的粉末跟足量的盐酸反应,生成2.24 LH(标况),则此金属混合物可能是( )
2
A.Mg和Al B.Al和Fe C.Fe和Zn D.Zn和Cu
12.下列说法正确的是
A.铁制容器可以盛装冷的浓硫酸,因为常温下铁和浓HSO 不反应
2 4
B.金属镁的熔点高,是优质的耐高温材料C.木材、纺织品浸过水玻璃后,具有防腐性能且不易燃烧
D.氢气是一种清洁能源,但热值低,因而目前没有被广泛应用
13.在给定条件下,下列选项所示的物质间转化均能实现的是 ( )
A.
B.
C.
D.
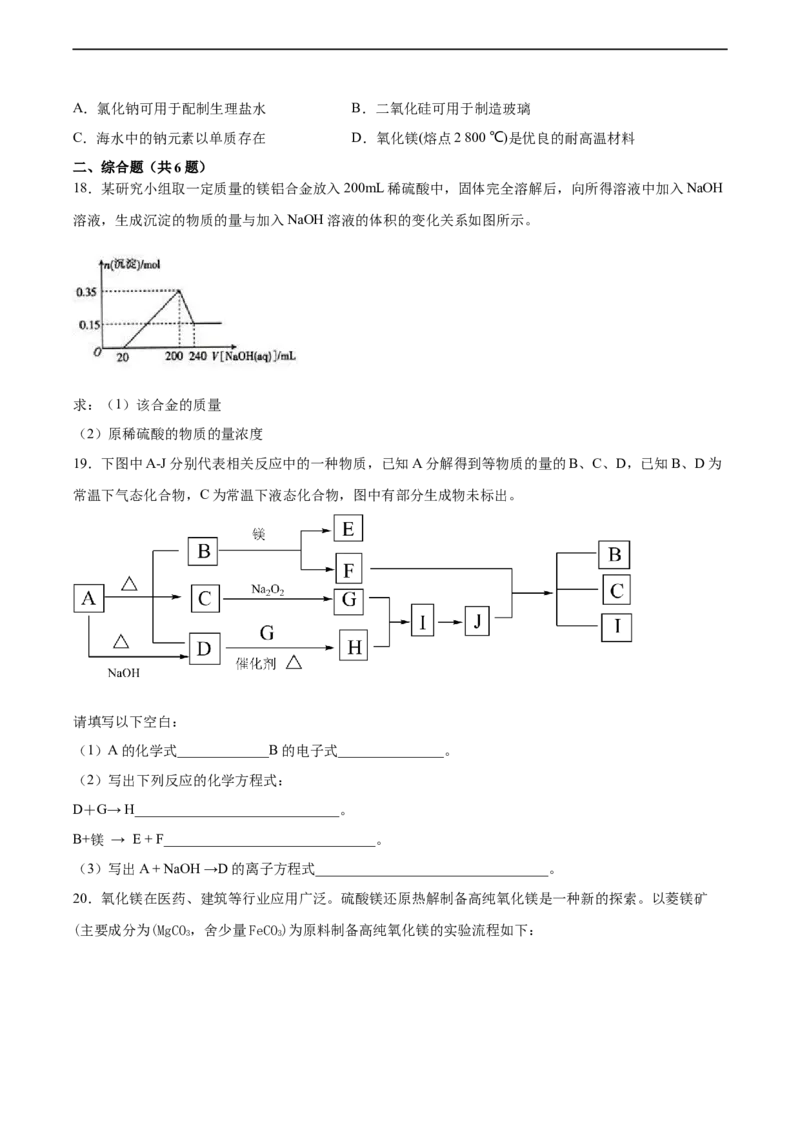
14.镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反
应中镁和铝的
A.物质的量之比为3︰2 B.质量之比为3︰2
C.摩尔质量之比为2︰3 D.反应速率之比为2︰3
15.下表中的各组物质之间通过一步反应就能实现如图所示转化的是( )
编号 a b c d
① NaO NaO Na NaOH
2 2 2
② Al O NaAlO Al Al(OH
2 3 2 )3
③ FeCl FeCl Fe CuCl
2 3 2
④ MgO MgCl Mg Mg(OH
2 )2
A.①②④ B.①③④ C.①②③ D.②③④
16.甲、乙、丙、丁分别是NaOH、AlCl 、BaCl 、MgCl 四种物质中的一种,若将乙溶液滴入丁溶液中,
3 2 2
发现有白色沉淀生成,继续滴加则沉淀消失;乙溶液滴入丙溶液中,无明显现象发生。据此可推断甲物质
是
A.BaCl B.NaOH C.AlCl D.MgCl
2 3 2
17.下列说法不正确的是( )A.氯化钠可用于配制生理盐水 B.二氧化硅可用于制造玻璃
C.海水中的钠元素以单质存在 D.氧化镁(熔点2 800 ℃)是优良的耐高温材料
二、综合题(共6题)
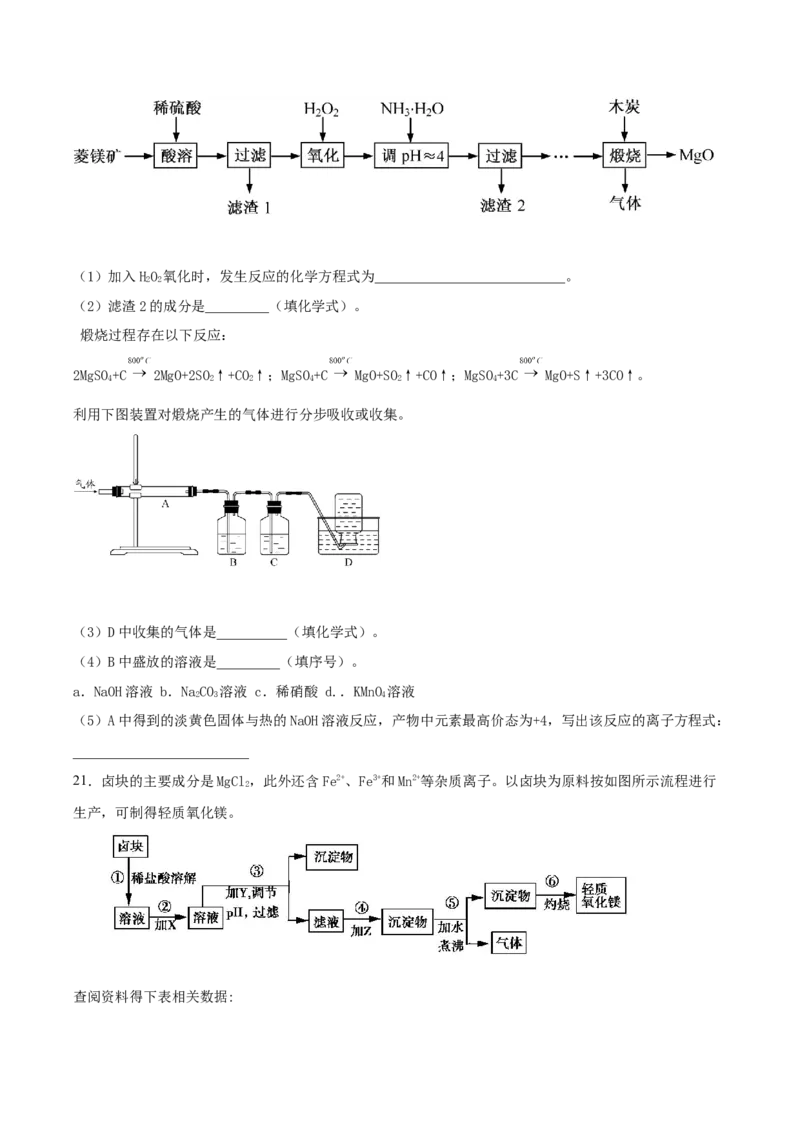
18.某研究小组取一定质量的镁铝合金放入200mL稀硫酸中,固体完全溶解后,向所得溶液中加入NaOH
溶液,生成沉淀的物质的量与加入NaOH溶液的体积的变化关系如图所示。
求:(1)该合金的质量
(2)原稀硫酸的物质的量浓度
19.下图中A-J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为
常温下气态化合物,C为常温下液态化合物,图中有部分生成物未标出。
请填写以下空白:
(1)A的化学式_____________B的电子式_______________。
(2)写出下列反应的化学方程式:
D+G→ H_____________________________。
B+镁 → E + F______________________________。
(3)写出A + NaOH →D的离子方程式_________________________________。
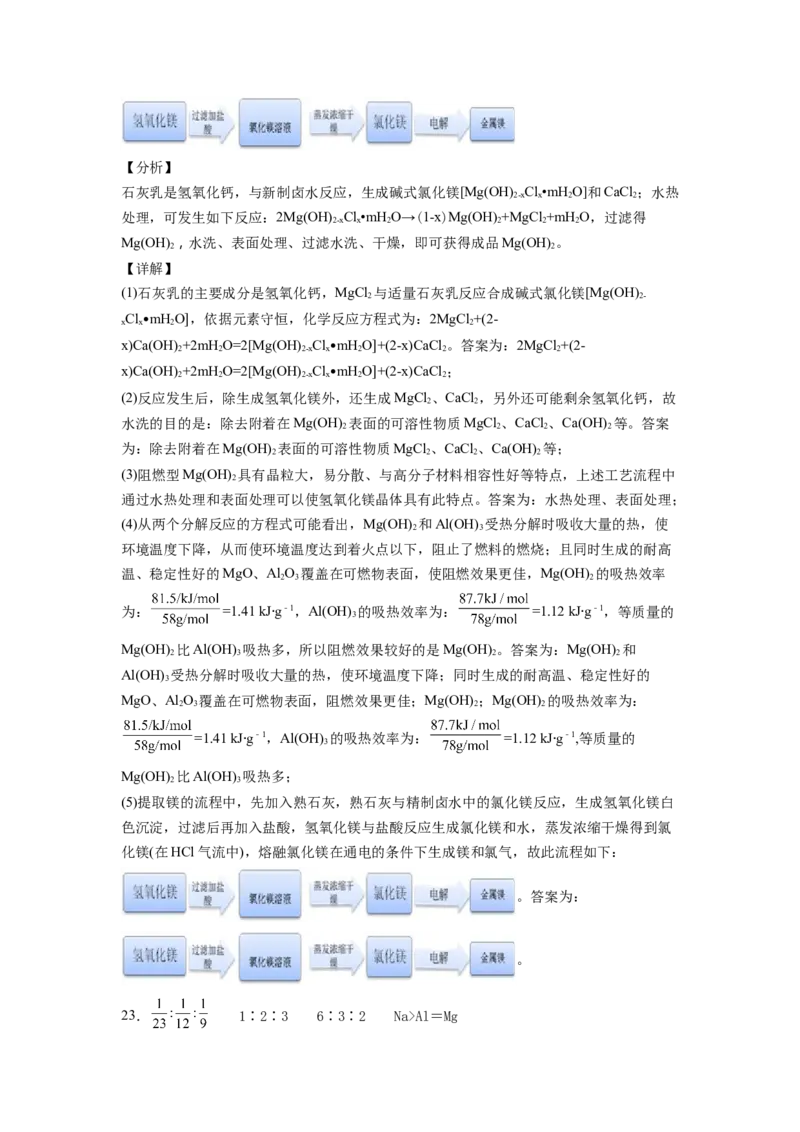
20.氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿
(主要成分为(MgCO,舍少量FeCO)为原料制备高纯氧化镁的实验流程如下:
3 3(1)加入HO 氧化时,发生反应的化学方程式为___________________________。
2 2
(2)滤渣2的成分是_________(填化学式)。
煅烧过程存在以下反应:
2MgSO+C 2MgO+2SO↑+CO↑;MgSO+C MgO+SO↑+CO↑;MgSO+3C MgO+S↑+3CO↑。
4 2 2 4 2 4
利用下图装置对煅烧产生的气体进行分步吸收或收集。
(3)D中收集的气体是__________(填化学式)。
(4)B中盛放的溶液是_________(填序号)。
a.NaOH溶液 b.NaCO 溶液 c.稀硝酸 d..KMnO 溶液
2 3 4
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:
_________________________
21.卤块的主要成分是MgCl,此外还含Fe2+、Fe3+和Mn2+等杂质离子。以卤块为原料按如图所示流程进行
2
生产,可制得轻质氧化镁。
查阅资料得下表相关数据:表1: 生成氢氧化物沉淀的pH 表2: 原料价格表
开始 沉淀完 价格
物质 试剂
沉淀 全 (元/吨)
Fe(OH) 2.7 3.7 a.漂液(含25.2%NaClO) 450
3
Fe(OH) 7.6 9.6 b.双氧水(含30%HO) 1500
2 2 2
Mn(OH) 8.3 9.8 c.烧碱(含98%NaOH) 2200
2
Mg(OH) 9.6 11.1 d.纯碱(含99.5%NaCO) 800
2 2 3
已知Fe2+氢氧化物呈絮状,不易从溶液中除去,必须将它氧化后以Fe(OH) 沉淀形式才能除尽。若要求产品
3
尽量不含杂质且生产成本较低,请根据上表提供的资料回答:
(1)流程中加入的试剂X、Y、Z的最佳选择依次是表2中的_____(选填试剂编号)。
(2)步骤②发生反应的离子方程式为__________;步骤⑤中发生反应的化学方程式为______。
(3)为尽量除去杂质,步骤③调节pH为____时,停止加入Y。调节为该pH的目的是____。
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是____。
A.酒精喷灯 B.铁三脚 C.坩埚 D.蒸发皿 E.泥三角 F.烧杯 G.石棉网
(5)向装有少量Mg(OH) 浊液的试管中加入适量CHCOONH 晶体,充分振荡后溶液会变澄清,请用化学平
2 3 4
衡的原理解释浊液变澄清的原因______。
22.往有机聚合物中添加阻燃剂,可增加聚合物的使用安全性,扩大其应用范围。Mg(OH) 是一种常用的
2
阻燃剂,生产工艺如下:
完成下列填空:
(1)精制卤水中的MgCl 与适量石灰乳反应合成碱式氯化镁[Mg(OH) Cl•mH O],反应的化学方程式为___。
2 2-x x 2
(2)合成反应后,继续在393K~523K下水热处理8h,发生反应:Mg(OH) Cl•mH O→(1- )Mg(OH) +
2-x x 2 2
MgCl +mH O,水热处理后,进行过滤、水洗。水洗的目的是___。
2 2
(3)阻燃型Mg(OH) 具有晶粒大,易分散、与高分子材料相容性好等特点。上述工艺流程中与此有关的步骤
2
是___。
(4)已知热化学方程式:Mg(OH) (s)→MgO(s)+H O(g)-81.5kJ•mol-1
2 2
Al(OH)(s)→ Al O(s)+ HO(g)-87.7kJ•mol-1
3 2 3 2
Mg(OH) 和Al(OH) 起阻燃作用的主要原因是___。等质量Mg(OH) 和Al(OH) 相比,阻燃效果较好的是___,
2 3 2 3原因是___。
(5)该工业生产的原料还可以用来提取金属镁。请设计提取金属镁的工艺流程(框内写产物名称,箭头上标
明转化条件):___
六、结构与性质
23.(1)分别取W g钠、镁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是_______。
(2)分别取0.1 mol钠、镁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是___________。
(3)若产生相同体积(同温同压下)的氢气,所需钠、镁、铝(与足量的盐酸反应)的物质的量之比为
____________。
(4)若将0.2 mol钠、镁、铝分别投入10 mL 1 mol·L-1的盐酸中,在标准状况下,产生氢气的体积大
小顺序是________。参考答案
1.B
【解析】
【详解】
n(HCl)=0.2mol,①镁粉不会产生水,②氧化镁 ③氢氧化镁 ④碳酸镁都会产生水,③氢氧
化镁产生的水最多;因此所得溶液的溶质的物质的量浓度最大的是①;最小的是③,②和
④浓度相等。故所得溶液的溶质的物质的量浓度的大小关系是①>②=④>③;
答案选B。
2.A
【详解】
A项,氧化镁熔点高,金属镁的表面有一层氧化膜,因此点燃镁条之前,应该用砂纸打磨
掉表面氧化膜,故A正确;
B项,明矾可水解,生成具有吸附性的氢氧化铝胶体,但不具有氧化性,不能用于杀菌消
毒,故不选B项;
C项,钠是活泼金属,具有还原性,可与熔融TiCl 反应制取金属Ti,溶液中钠与水剧烈反
4
应,不能用钠与溶液反应制备金属,故不选C项;
D项,高温下,氧化铝能与NaOH反应,氧化铝不能用于制造熔融烧碱的坩埚,故不选D项。
综上所述,本题选A。
3.C
【详解】
镁条在空气中燃烧,与空气中的氧气、氮气、二氧化碳反应,生成物为MgO、Mg N 、
3 2
C,只有C项符合题意。故选C。
4.C
【详解】
:A.电解熔融NaCl时阳极上氯离子失电子生成氯气,阴极上钠离子放电生成金属钠,A
正确;
B.Na的活泼性大于Ti,在熔融状态下,钠能置换出Ti,所以金属钠在高温下能将TiCl 中
4
的钛置换出来,B正确;
C.在点燃条件下,镁在氮气燃烧生成氮化镁,所以金属镁着火不可用氮气灭火,C错误;
D.镁燃烧时发生耀眼的白光,并放出大量的热,因此常用来制造信号弹和焰火,D正确;
答案选C。
5.B
【详解】
A、镁和铝都是活泼的金属,都能和酸反应,选项A不正确;
B、铝能溶解在强碱氢氧化钠溶液中,镁与氢氧化钠溶液不反应,因此把镁粉中混有少量
的铝粉除去,应选用的试剂是氢氧化钠溶液,即烧碱溶液,选项B正确;
C、镁能和硫酸铝发生置换反应生成硫酸镁和铝,是消耗镁生成铝而无法除去铝,选项C不正确;
D、硫酸镁溶液与铝不反应,无法除去铝,选项D不正确。
答案选B。
6.C
【详解】
①氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠溶液中通入二氧化碳生成氢氧化铝和碳
酸氢钠,故①能实现;②硫和氧气点燃生成二氧化硫,二氧化硫和氧气在催化剂加热的条
件下反应生成三氧化硫,故②不能实现;③在饱和食盐水中通入氨气,形成饱和氨盐水,
再向其中通入二氧化碳,在溶液中就有了大量的钠离子、铵根离子、氯离子和碳酸氢根离
子,其中NaHCO 溶解度最小,析出NaHCO 晶体,加热NaHCO 分解生成碳酸钠,故③
3 3 3
能实现;④氧化铁与盐酸反应生成氯化铁,氯化铁中Fe3+水解Fe3++3H
2
O
⇌
Fe(OH)
3
+3HCl,
加热HCl易挥发,平衡向右移动,因此加热得不到无水FeCl ,故④不能实现;⑤氯化镁与
3
石灰乳转化为更难溶的氢氧化镁,氢氧化镁煅烧分解生成氧化镁,故⑤能实现;因此
①③⑤能实现,故C符合题意。
综上所述,答案为C。
7.D
【详解】
A项,硫在氧气中燃烧,比在空气中更剧烈,发出明亮的蓝紫色火焰,产生一种具有刺激
性气味的气体,故A正确;B项,磷(白磷或红磷)容易在空气中燃烧,剧烈燃烧时火焰呈
黄色,生成大量白烟(这和白磷在暗处自燃产生绿色磷光不同),故B正确;C项,木炭
在氧气中燃烧比在空气中更剧烈,在氧气中燃烧发出白光而在空气中燃烧则灼热成红热,
故C正确;D项,镁条在氧气中燃烧,发出耀眼的白光,生成白色固体,故D错误。
8.A
【详解】
钠是一种极为活泼的金属,不能在空气中稳定存在,不能制作合金,D错误;加入稀盐酸
后,C项中的Al、Fe与盐酸完全反应,剩余的两种成分都不能与NaOH溶液反应,不符合
实验事实,又可排除C项,C错误;如果是A项,在合金样品与盐酸完全反应后,只剩余
Si和Cu,而Si能与NaOH溶液反应,放出氢气,Cu不反应,有不溶物剩余,A正确;如
果是B项,在合金样品与盐酸完全反应后,只剩余Si,而Si与氢氧化钠溶液反应生成硅酸
钠和氢气,没有不溶物,不合题意,B错误;正确选项A。
9.A
【详解】
假设全部是MgAlO 时,5.4gMgAlO 的物质的量为 =0.038mol,与盐酸反应最终
2 4 2 4
生成MgCl 和AlCl,1molMgAlO 消耗8molHCl,故消耗HCl的物质的量为
2 3 2 4
8mol×0.038mol/1mol=0.304mol,故100 mL盐酸溶液中盐酸的浓度为3.04mol/L;假如全部是FeO 时,5.4gFeO 的物质的量为 =0.0338mol,1molFeO 消耗
2 3 2 3 2 3
6molHCl,故消耗盐酸的物质的量为0.0338mol×6=0.203mol,故盐酸的物质的量浓度为
=2.03mol/L;
实际盐酸的物质的量浓度应介于二者之间,故选A。
10.B
【详解】
A.二氧化硫与溴蒸气发生氧化还原反应,体现了二氧化硫的还原性,A项错误;
B.燃煤中加入氧化钙可以减少酸雨的形成,当煤燃烧放出的二氧化硫,就会与氧化钙反
应,故可以减少酸雨的形成,B项正确;
C.三氧化二铝做防腐涂层利用了它的在常温下稳定的性质,C项错误;
D.氧化镁作耐火材料主要是因为其稳定性,熔点高,价格低,不是其熔融状态下的导电
性,D项错误;
答案选B。
11.B
【分析】
2.24 LH(标况)即0.1mol,根据电子守恒可知转移电子0.2mol,即2.6g金属混合物完全反映
2
转移电子0.2mol。
【详解】
A.2.6g镁约0.11mol,转移电子0.22mol,2.6g铝约0.08mol,转移电子0.24mol,因此2.6g
镁和铝的混合物转移电子0.22-0.24mol,不可能是0.2mol,故A不选;
B. 2.6g铁约0.05mol,与盐酸反应生成亚铁离子转移电子约0.1mol,2.6g铝约0.08mol,转
移电子0.24mol,因此2.6g铁和铝的混合物转移电子0.1-0.24mol,可能是0.2mol,故B选;
C. 2.6g铁约0.05mol,与盐酸反应生成亚铁离子转移电子约0.1mol,2.6g锌为0.04mol,转
移电子0.08mol,因此2.6g铁和锌的混合物转移电子0.1-0.08mol,不可能是0.2mol,故C
不选;
D.铜与盐酸不反应,2.6g锌为0.04mol,转移电子0.08mol,因此2.6g铜和锌的混合物转移
电子0-0.08mol,不可能是0.2mol,故D不选;
故选B。
12.C
【详解】
A.因为铁和浓硫酸发生了钝化反应,钝化时发生了氧化还原反应,生成致密的氧化物阻止
反应的进一步发生,所以铁制容器可盛装冷的浓硫酸,故A错误; B. 金属镁是活泼的金属,
容易被氧化,所以不能做耐高温材料,故B错误;C.木材、纺织品浸过水玻璃后,具有防
腐性能且不易燃烧,故C正确;D氢气难储存,生产成本高,所以制约氢气作为优质能源不
能大力推广的关键因素,故D错误;答案:C。13.B
【详解】
A.蔗糖不是还原性糖,不能发生银镜反应,故A错误;
B.氯化镁和氢氧化钙发生反应生成氯化钙和氢氧化镁沉淀,氢氧化镁沉淀受热分解生成
氧化镁和水,故B正确;
C.铁和盐酸反应生成氯化亚铁和氢气,故C错误;
D.NH +HO+CO+NaCl=NaHCO ↓+NH Cl,得NaHCO 沉淀,不是NaCO,故D错
3 2 2 3 4 3 2 3
误;
故选B。
14.A
【详解】
由题意可知,酸过量,产生氢气体积相等,转移电子数相等,3mol镁和2mol铝转移电子
数相等,所以物质的量之比为3:2,A 正确,B 错误,摩尔质量之比为24:27,C 错误,镁
比铝活泼,反应速率镁比铝快,D错误。故选A。
15.D
【详解】
① NaOH加热不能分解,NaOH不能一步转化为NaO,故不选①;Al O 与氢氧化钠反应
2 2 3
生成NaAlO ,NaAlO 与二氧化碳反应生成Al(OH) ,Al(OH) 加热分解为Al O,Al与氧气
2 2 3 3 2 3
反应生成Al O,Al与氢氧化钠反应生成NaAlO ,故选②;FeCl 与氯气反应生成FeCl ,
2 3 2 2 3
Fe与盐酸反应生成FeCl 、Fe与氯气反应生成FeCl ;FeCl 与Cu反应生成CuCl ,CuCl 与
2 3 3 2 2
铁反应生成FeCl 和铜,故选③;MgO与盐酸反应生成MgCl ,单质Mg与氧气反应生成
2 2
MgO,单质Mg与盐酸反应生成MgCl ,MgCl 和氢氧化钠反应生成Mg(OH ,加热
2 2 )2
Mg(OH 分解为MgO,故选④;
)2
选D。
16.D
【详解】
根据将乙溶液滴入丁溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,确定乙是
NaOH溶液,丁是AlCl 溶液;由于乙溶液滴入丙溶液中,无明显现象发生说明丙为BaCl
3 2
溶液,所以甲物质是MgCl 溶液;故答案选D。
2
17.C
【分析】
【详解】
A.NaCl易溶于水,食盐水可使细菌中细胞脱水,则氯化钠可用于配制生理盐水,故A正
确;
B.二氧化硅与碳酸钠反应,则高温下二氧化硅可用于制造玻璃,故B正确;
C.海水中存在大量NaCl,钠元素以离子存在,不能以单质存在,且Na与水剧烈反应,故C错误;
D.MgO的熔点高,熔点高的物质可作耐火材料,则氧化镁(熔点2800℃)是良好的耐高
温材料,故D正确;
故选C。
18.∵加入过量NaOH溶液,最终生成的沉淀只有Mg(OH) ,
2
故Mg(OH) 为0.15mol(1分)
2
∴生成的Al(OH) 最多为0.35mol-0.15mol=0.2mol(1分)
3
合金中含有0.15molMg和0.2molAl
合金的质量为 (1分)
(2)由于加入200mL~240mLNaOH溶液时,发生反应:
NaOH+Al(OH) =NaAlO +2H O
3 2 2
得c(NaOH)= (2分)
根据图示知:加入200mLNaOH溶液时,所得溶液中只含有NaSO 。
2 4
溶液中含有NaSO : ,即SO 2-为0.5mol
2 4 4
所以原稀硫酸中含HSO 0.5mol(2分)
2 4
c(HSO )= (1分)
2 4
答:合金的质量为9g;原稀硫酸的物质的量浓度为2.5mol/L
【解析】
试题分析:根据图像分析,镁铝溶于硫酸后溶液中有硫酸镁和硫酸铝和硫酸,所以先加入
氢氧化钠没有沉淀生成,当氢氧化钠的体积为20毫升时开始出现氢氧化镁和氢氧化铝沉淀,
沉淀最大值为0.35摩尔,然后氢氧化铝沉淀溶于氢氧化钠,最后剩余0.15摩尔氢氧化镁沉
淀,所以氢氧化铝沉淀的物质的量为0.35-0.15=0.20摩尔,从而计算合金的质量。根据200
到240只有氢氧化铝和氢氧化钠反应,所以可以计算氢氧化钠的物质的量或浓度,当氢氧
化钠的体积为200毫升时,溶液中只有硫酸钠,所以根据硫酸钠的化学式找硫酸和氢氧化
钠的关系即可计算硫酸的浓度。
考点:金属的性质,氢氧化铝的两性。
19.(1) NHHCO
4 3
(2) 4NH+5O 4NO + 6H O CO+ 2Mg ="==" 2MgO+C
3 2 2 2
(3) NH+ + HCO - +2OH- = NH +CO 2- +2H O
4 3 3 3 2
【分析】
已知A与碱反应生成气体化合物,则A含有铵根离子;A加热分解生成等物质的量的2种气体和1种液体,液体与过氧化钠反应则为水,可确定A为碳酸氢铵,D为氨气,C为水,
B为二氧化碳;二氧化碳与镁反应生成氧化镁和碳;
【详解】
(1)分析可知,A为碳酸氢铵,化学式为:NH HCO ;B为二氧化碳,其电子式为:
4 3
;
(2)D与G分别为氨气、氧气,在一定条件下反应生成一氧化氮和水,方程式为:
4NH +5O 4NO+6H O;镁与二氧化碳反应生成氧化镁和碳,方程式为:CO+ 2Mg
3 2 2 2
2MgO+C;
(3)碳酸氢钠与NaOH反应生成氨气、水和碳酸钠,其反应的离子方程式为:NH + +
4
HCO -+2OH-= NH +CO 2-+2H O;
3 3 3 2
20.2FeSO +HO+HSO =Fe (SO )+2HO Fe(OH) CO d 3S+6OH-
4 2 2 2 4 2 4 3 2 3
2S2-+SO 2-+3HO
3 2
【详解】
(1)菱镁矿的主要成分为MgCO ,还含少量FeCO,当向其中加入过量的HSO 时,发生
3 3 2 4
反应:MgCO + H SO =MgSO +H O+CO↑;FeCO+ H SO =FeSO+H O+CO↑;把难溶性的
3 2 4 4 2 2 3 2 4 4 2 2
杂质过滤除去,在滤液中含有MgSO 、FeSO 、HSO ;然后向溶液中加入HO,由于亚铁
4 4 2 4 2 2
离子易被氧化,发生氧化还原反应:2FeSO +HO+HSO =Fe (SO )+2HO;(2)把加
4 2 2 2 4 2 4 3 2
入HO 后的溶液调整溶液的pH=4,Fe3+就会形成Fe(OH) 沉淀,把沉淀过滤除去,得到的
2 2 3
滤液2含有MgSO ,滤渣2的主要成分是氢氧化铁;(3)由于装置要对煅烧产生的气体进
4
行分步吸收或收集,据图示可知在反应过程中产生的气体可能含有CO、CO、SO ;SO 被
2 2 2
酸性KMnO 氧化变为HSO ,CO 被碱液吸收,最后得到的是CO,即D中收集的气体是
4 2 4 2
CO;(4)B的作用是吸收SO ,而不能吸收CO,SO 有还原性,所以吸收试剂是具有氧
2 2 2
化性的物质KMnO 溶液,而稀硝酸尽管有氧化性,可以氧化SO ,但是还会产生NO气体,
4 2
因此不能使用,答案选d;(5)A中得到的淡黄色固体是S与热的NaOH溶液反应,由于
产物中元素最高价态为+4,则根据电子转移守恒及原子守恒可得该反应的离子方程式是3S
+6OH- 2S2-+SO 2-+3HO。
3 2
21.a、c、d 2Fe2++ClO-+2H+=Cl-+2Fe3++H O MgCO +H O Mg(OH) +CO ↑
2 3 2 2 2
9.8 使Mg2+以外的杂质离子尽可能彻底地转化为沉淀除去 ABCE Mg(OH) (s)
2
Mg2+(aq)+2OH-(aq);CHCOONH 电离出的NH +与OH-结合成弱电解质NH ·HO,降低了
3 4 4 3 2
c(OH-),Mg(OH) 溶解平衡向右移动
2
【分析】
卤块的主要成分是MgCl ,此外还含Fe2+、Fe3+和Mn2+等杂质离子,由流程可知,加稀盐酸
2
溶解后,为除去Fe2+,先将Fe2+氧化成Fe3+,漂液和HO 都可采用,但对比表2提供的原
2 2料价格可以看出,漂液比HO 的价格低得多,所以选漂液最合理,故X为漂液;步骤③的
2 2
目的在于使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀,以便通过过滤而除去,
应加入NaOH,如加入纯碱,不能达到较高的pH,由表1提供的数据可知,除去杂质离子
合理的pH范围是3.7<pH<9.8,在此范围内,如果pH过高,就会有大量的Mg2+生成
Mg(OH) 而进入沉淀中,从而导致生产成本的提高;为了兼顾产品质量和生产成本,选择
2
pH=9.8最合理,当然此时Mg2+也会部分生成Mg(OH) 沉淀,但由于卤块价格低廉,这点不
2
可避免的损失可忽略,过滤后,分离出Mn(OH) 、Fe(OH) ,在滤液中加入Z为纯碱将
2 3
Mg2+从溶液中以MgCO 沉淀出来,然后加热煮沸可得到Mg(OH) ,气体为二氧化碳,
3 2
Mg(OH) 灼烧后得到MgO,以此来解答。
2
【详解】
(1)步骤②是为了将Fe2+氧化成Fe3+,并在控制合适的pH条件时生成Fe(OH) 沉淀而除之,
3
虽然漂液和HO 都可采用,但对比表2提供的原料价格可以看出,漂液比HO 的价格低得
2 2 2 2
多,所以选漂液最合理,故X为漂液;加入Y的目的是调节pH,选用氢氧化钠,故Y为
烧碱;加入Z的目的是使镁离子沉淀,Z为纯碱;故答案为a、c、d;
(2)流程中加入次氯酸钠在酸性溶液中会氧化亚铁离子为铁离子,反应的离子方程式为:
2Fe2++ClO-+2H+=2Fe3++Cl-+H O;加入的Z物质为纯碱,所以步骤④生成的沉淀物是
2
MgCO ,沉淀物MgCO 在煮沸的情况下发生水解,生成Mg(OH) 和CO 气体,反应的化学
3 3 2 2
方程式为:MgCO +H O Mg(OH) ↓+CO↑;
3 2 2 2
(3)步骤③的目的在于使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀,以便通过过
滤而除去,应加入NaOH,若加入纯碱,不能达到较高的pH,分析表1提供的数据:除去
杂质离子合理的pH范围是3.7<pH<9.8,在此范围内,如果pH过高,就会有大量的
Mg2+生成Mg(OH) 而进入沉淀中,从而导致生产成本的提高;为了兼顾产品质量和生产成
2
本,选择pH=9.8最合理,当然此时Mg2+也会部分生成Mg(OH) 沉淀,但由于卤块价格低
2
廉,这点不可避免的损失还是可以承受的,以此保证产品的纯度;
(4)灼烧需要的仪器有铁三脚、酒精喷灯、坩埚、泥三角,故答案为ABCE;
(5)向装有少量Mg(OH) 浊液的试管中加入适量CHCOONH 晶体,充分振荡后溶液会变澄
2 3 4
清,因Mg(OH)
2
(s)⇌Mg2+ (aq)+2OH-(aq),CH
3
COONH
4
电离出的NH
4
+与OH-结合成弱电解
质NH •HO,降低了c(OH-),Mg(OH) 溶解平衡向右移动。
3 2 2
22.2MgCl +(2-x)Ca(OH) +2mH O=2[Mg(OH) Cl•mH O +(2-x)CaCl 除去附着在
2 2 2 2-x x 2 2
Mg(OH) 表面的可溶性物质MgCl 、CaCl 、Ca(OH) 等 水热处理、表面处理
2 2 2 2 ]
Mg(OH) 和Al(OH) 受热分解时吸收大量的热,使环境温度下降;同时生成的耐高温、稳
2 3
定性好的MgO、Al O 覆盖在可燃物表面,阻燃效果更佳 Mg(OH) Mg(OH) ;
2 3 2 2
Mg(OH) 的吸热效率为: =1.41 kJg﹣1,Al(OH) 的吸热效率为:
2 3
∙
=1.12 kJg﹣1,等质量的Mg(OH) 比Al(OH) 吸热多
2 3
∙【分析】
石灰乳是氢氧化钙,与新制卤水反应,生成碱式氯化镁[Mg(OH) Cl•mH O]和CaCl ;水热
2-x x 2 2
处理,可发生如下反应:2Mg(OH) Cl•mH O→(1-x)Mg(OH) +MgCl +mH O,过滤得
2-x x 2 2 2 2
Mg(OH) ,水洗、表面处理、过滤水洗、干燥,即可获得成品Mg(OH) 。
2 2
【详解】
(1)石灰乳的主要成分是氢氧化钙,MgCl 与适量石灰乳反应合成碱式氯化镁[Mg(OH)
2 2-
Cl•mH O ,依据元素守恒,化学反应方程式为:2MgCl +(2-
x x 2 2
x)Ca(OH) +2mH O=2[Mg(OH) Cl•mH O +(2-x)CaCl 。答案为:2MgCl +(2-
2] 2 2-x x 2 2 2
x)Ca(OH) +2mH O=2[Mg(OH) Cl•mH O +(2-x)CaCl ;
2 2 2-x x 2 ] 2
(2)反应发生后,除生成氢氧化镁外,还生成MgCl 、CaCl ,另外还可能剩余氢氧化钙,故
] 2 2
水洗的目的是:除去附着在Mg(OH) 表面的可溶性物质MgCl 、CaCl 、Ca(OH) 等。答案
2 2 2 2
为:除去附着在Mg(OH) 表面的可溶性物质MgCl 、CaCl 、Ca(OH) 等;
2 2 2 2
(3)阻燃型Mg(OH) 具有晶粒大,易分散、与高分子材料相容性好等特点,上述工艺流程中
2
通过水热处理和表面处理可以使氢氧化镁晶体具有此特点。答案为:水热处理、表面处理;
(4)从两个分解反应的方程式可能看出,Mg(OH) 和Al(OH) 受热分解时吸收大量的热,使
2 3
环境温度下降,从而使环境温度达到着火点以下,阻止了燃料的燃烧;且同时生成的耐高
温、稳定性好的MgO、Al O 覆盖在可燃物表面,使阻燃效果更佳,Mg(OH) 的吸热效率
2 3 2
为: =1.41 kJg﹣1,Al(OH) 的吸热效率为: =1.12 kJg﹣1,等质量的
3
∙ ∙
Mg(OH) 比Al(OH) 吸热多,所以阻燃效果较好的是Mg(OH) 。答案为:Mg(OH) 和
2 3 2 2
Al(OH) 受热分解时吸收大量的热,使环境温度下降;同时生成的耐高温、稳定性好的
3
MgO、Al O 覆盖在可燃物表面,阻燃效果更佳;Mg(OH) ;Mg(OH) 的吸热效率为:
2 3 2 2
=1.41 kJg﹣1,Al(OH) 的吸热效率为: =1.12 kJg﹣1,等质量的
3
∙ ∙
Mg(OH) 比Al(OH) 吸热多;
2 3
(5)提取镁的流程中,先加入熟石灰,熟石灰与精制卤水中的氯化镁反应,生成氢氧化镁白
色沉淀,过滤后再加入盐酸,氢氧化镁与盐酸反应生成氯化镁和水,蒸发浓缩干燥得到氯
化镁(在HCl气流中),熔融氯化镁在通电的条件下生成镁和氯气,故此流程如下:
。答案为:
。
23. 1∶2∶3 6∶3∶2 Na>Al=Mg【分析】
发生反应:2Na+2HCl=2NaCl+H ↑、Mg+2HCl=MgCl +H ↑、2Al+6HCl=2AlCl +3H ↑,
2 2 2 3 2
根据方程式计算解答。
【详解】
(1)2Na+2HCl=2NaCl+H ↑、
2
46g 1mol
Wg mol
Mg+2HCl=MgCl +H ↑ 、
2 2
24g 1mol
Wg mol
2Al+6HCl=2AlCl +3H ↑,
3 2
54g 3mol
Wg mol
故在相同条件下产生氢气的体积比= mol : mol: mol= ,
因此,本题正确答案是: 。
(2)分别取0.1mol钠、镁、铝与足量盐酸反应,则:
2Na+2HCl=2NaCl+H ↑
2
0.1mol 0.05mol
Mg+2HCl=MgCl +H ↑
2 2
0.1mol 0.1mol
2Al+6HCl=2AlCl +3H ↑
3 2
0.1mol 0.15mol
故在相同条件下产生氢气的体积比=0.05mol:0.1mol:0.15mol=1:2:3,
因此,本题正确答案是:1:2:3。
(3)若产生相同体积(同温同压下)的H,说明三种金属提供电子的物质的量相同,设
2
三种金属都失去6mol的电子,需钠的物质的量为6mol,镁的物质的量为3mol,铝的物质
的量为2mol,所以所需的钠、镁、铝物质的量比为6:3:2。
因此,本题正确答案是:6:3:2。
(4)若将0.2 mol钠、镁、铝分别投入10 mL 1 mol·L-1的盐酸中,可以知道三种金属
都过量,但金属钠活泼,能与水反应生成氢气,则生成氢气最多的是钠,镁和铝生成氢气
的体积一样多,
因此,本题正确答案是:Na>Al=Mg。