文档内容
第三章 水溶液中离子反应与平衡 单元测试题
一、单选题
1.常温下,下列说法正确的是
A. 的氯化铵溶液,由水电离出
B. 溶液的 ,该溶液中
C.pH均为11的氨水和NaOH溶液,水电离产生的 后者更大
D.将 的醋酸溶液加水稀释100倍,pH变为5
2.下列事实一定能说明HClO是弱电解质的是
①25℃时,用pH试纸测0.01mol/L的HClO溶液的pH约为4
②HClO水溶液中含有HClO分子和 、
③10mL 0.01mol/L HClO溶液恰好与10mL 0.01mol/L NaOH溶液完全反应
④次氯酸不稳定,在光照条件下易分解
⑤用HClO溶液做导电性实验,灯泡很暗
⑥NaClO溶液显碱性
A.①②⑤⑥ B.②⑥ C.①③④⑥ D.②④⑤
3.化学与人类生活、生产息息相关。下列说法正确的是
A.用纯碱溶液清洗油污,加热可增强去污力
B.大规模开采可燃冰作为新能源有利于实现“碳中和”的目标
C.聚氯乙烯制品易造成白色污染,宜采用焚烧法处理
D.草木灰和铵态氮肥混合使用能使肥效增强
4.如图是常温下向 的盐酸中,逐滴加入 的 溶液时,溶液
的 随 溶液的体积 变化的曲线,根据图像所得的下列结论中正确的是A.原盐酸的浓度为
B.当 滴入 时,溶液依然显酸性,且
C. 的值为20.00
D.只能选用酚酞作指示剂,不能用甲基橙
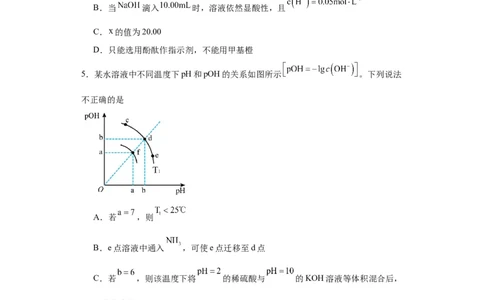
5.某水溶液中不同温度下pH和pOH的关系如图所示 。下列说法
不正确的是
A.若 ,则
B.e点溶液中通入 ,可使e点迁移至d点
C.若 ,则该温度下将 的稀硫酸与 的KOH溶液等体积混合后,
溶液显中性
D.f、d两点的 比较,前者大
6.25℃时, 的两种碱溶液各10mL,分别加水稀释到1000mL,其pH与溶液体
积(V)的关系如图所示,下列说法不正确的是A.若 ,则NOH为强碱
B.两种碱的物质的量浓度肯定不等
C.均稀释100倍以后,MOH溶液中水的电离程度大于NOH溶液
D.若两者均为弱碱,则 ,且NOH碱性强于MOH
7.在一定条件下,NaCO 溶液存在水解平衡: 。下列说
2 3
法正确的是
A.稀释溶液,各物质浓度均减小,平衡不移动
B.加入少量NaHCO 固体,平衡向正反应方向移动
3
C.升高温度, 减小
D.加入NaOH固体,溶液pH增大
8. 为阿伏加德罗常数的值。下列说法正确的是
A. 溶液水解生成的 胶体粒子数少于
B. 溶液中, 数目为
C. 的原子总数为
D.25℃, 溶液由水电离出的 为
9.25℃时,下列说法不正确的是
A.0.10mol/L、0.010mol/L的醋酸的电离常数Ka相同
B.中和pH和体积均相等的醋酸、HCl溶液,所需NaOH的物质的量前者多
C.1L pH=8的CHCOONa溶液中,由水电离出总的H+的物质的量为
3
D.同pH的盐酸、醋酸溶液,对水的抑制程度相等
10.氨氮是水体的污染物之一,工业上可用次氯酸钠作处理剂,反应方程式为:
。设阿伏加德罗常数的值为N ,下列说法正确的
A是
A.1 L 0.1mol/L NaClO 溶液中含有0.1N 个 ClO⁻
A
B.18 g HO 中含有的孤电子对数目为2N
2 A
C.生成11.2 L N,转移的电子数为 3N
2 A
D.0.5 L0.1 mol/L 氨水中含有
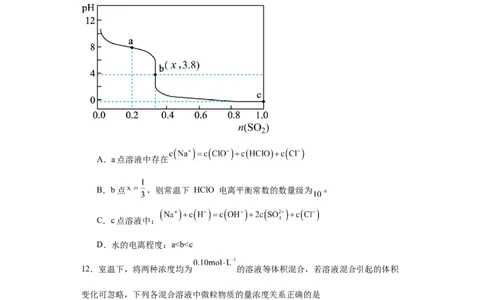
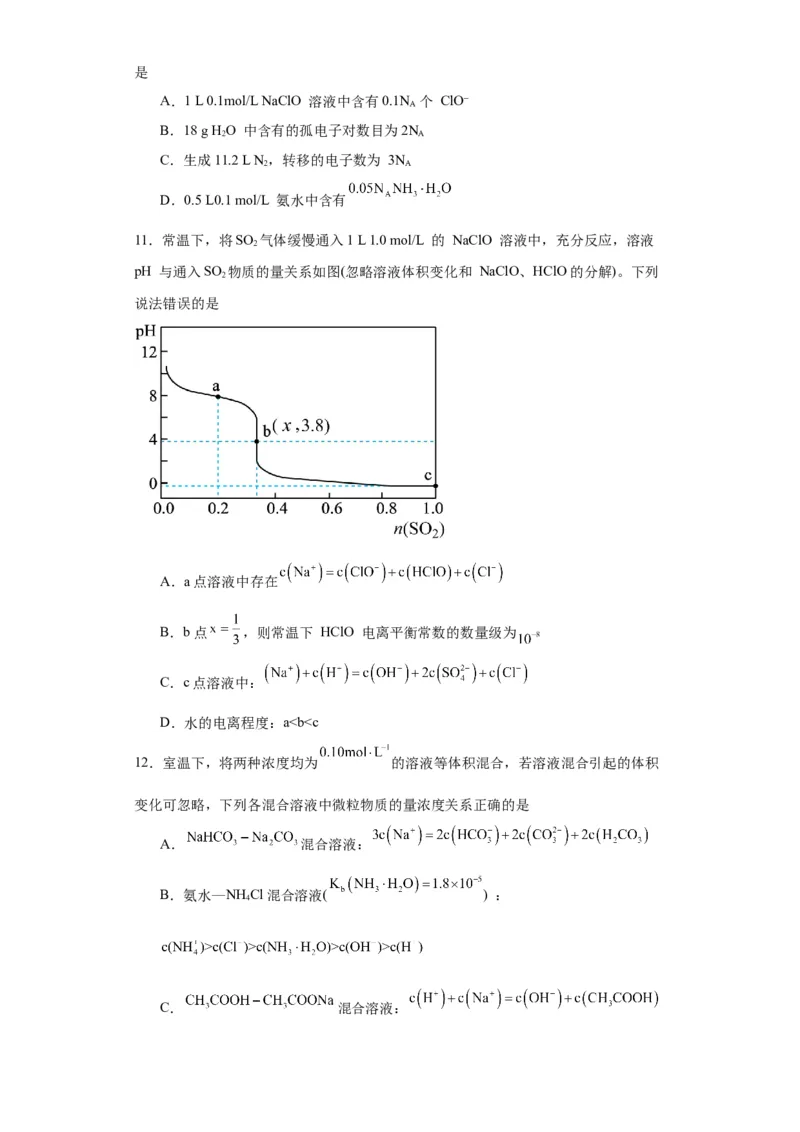
11.常温下,将SO 气体缓慢通入1 L 1.0 mol/L 的 NaClO 溶液中,充分反应,溶液
2
pH 与通入SO 物质的量关系如图(忽略溶液体积变化和 NaClO、HClO的分解)。下列
2
说法错误的是
A.a点溶液中存在
B.b点 ,则常温下 HClO 电离平衡常数的数量级为
C.c点溶液中:
D.水的电离程度:ab>c,故D错误;
故选D。
12.B
【详解】A.根据物料守恒, 等物质的量的混合溶液中存在:
,A错误;
B.由 可知 水解常数为 < , 水解
程度小于 的电离程度,则氨水—NH Cl混合溶液呈碱性,溶液中
4
,B正确;
C. 混合溶液中,根据电荷守恒存在:
,C错误;
D. 混合溶液,根据电荷守恒:
,和物料守恒:
,可得,D错误;
故选B。
13.C
【详解】A.常温下,测定0.1mol•L-1CHCOOH的pH值,若pH大于1,说明存在电离平
3
衡,醋酸为弱电解质,故A正确;
B.加水稀释氨水,c(OH-)均减小,而Kw不变,故 增加,故B正确;
C. 的盐酸其物质的量浓度为1×10-5mol/L,稀释1000倍,氢离子浓度约为10-
7mol•L-l,pH=-lg(10-7)≈7,不可能变为碱,故C错误;
D.盐酸为强酸、醋酸为弱酸,等pH时醋酸的浓度大,则相同温度下,中和相同pH、相
同体积的盐酸和醋酸溶液,消耗NaOH物质的量不同,故D正确。
答案选C。
14.B
【详解】A.次氯酸钠具有强氧化性,会使得pH试纸褪色,不能测其pH值,A错误;
B.含有酚酞的 溶液,因碳酸根离子水解显碱性: ,滴
有酚酞溶液变红,加入少量BaCl 固体,发生反应 ,导致水解平衡逆
2
向移动,则溶液颜色变浅,证明 溶液中存在水解平衡,B正确;
C.常温下, 均为7说明溶液中氢离子、氢氧根离子浓度相同,但是不能说明同温下,
不同浓度的 溶液中水的电离程度相同,C错误;
D. ,反应中高锰酸钾均过量,溶液不褪色,
D错误;
故选B。
15.(1)①
(2)由无色变为浅红色,半分钟不褪色
(3)22.60(4)0.2000
(5)2 KMnO +5H C O+3H SO =K SO +2MnSO +10CO ↑+8H O
4 2 2 4 2 4 2 4 4 2 2
(6) a 酸式滴定管
(7)0.2 mol•L-1
【详解】(1)碱式滴定管在装液前应用待装液进行润洗,否则标准液的浓度偏小,故答案
为:①;
(2)当滴入最后一滴NaOH溶液,溶液由无色变为粉红色,且半分钟内不褪色,即为终点,
故答案为:由无色变为浅红色,半分钟不褪色;
(3)根据滴定管的结构与精确度为0.01mL;滴定管中的液面读数为22.60mL,故答案为:
22.60;
(4)三次滴定消耗的体积为:20.00mL,22.10mL,20.00mL,22.10mL,偏差大舍弃,平
均用V(NaOH)=20.00mL, ═0.2000mol•L-1,故答案为:
0.2000;
(5)KMnO 与 HC O 反应,锰元素化合价降低了5,碳元素化合价升高了1,HC O 中2
4 2 2 4 2 2 4
个碳原子均变价,根据得失电子守恒,含锰元素的物质系数配2,含碳元素的物质系数配
5,由原子守恒可配平反应方程式为:2
KMnO +5H C O+3H SO =K SO +2MnSO +10CO ↑+8H O;
4 2 2 4 2 4 2 4 4 2 2
(6)酸性 KMnO 溶液具有强氧化性,能够氧化碱式滴定管的橡皮管;酸性 KMnO 溶液
4 4
应装在酸式滴定管中,故选a;
(7)三次滴定消耗标准液体积分别为:19.90mL,20.00mL,20.10mL,三次滴定的数据都
有效,消耗标准液的平均体积为: =20.00mL,高锰酸钾的物
质的量为0.1mol•L-1×0.020L=0.002mol,根据反应
2KMnO +5H C O+3H SO =K SO +10CO ↑+2MnSO +8H O可知,n(H C O)=
4 2 2 4 2 4 2 4 2 4 2 2 2 4
n(KMnO)=0.005mol,待测液草酸的物质的量浓度c(HC O)= =0.2 mol•L-1,故答案
4 2 2 4为:0.2 mol•L-1。
16.(1)抑制 水解
(2)丁达尔效应
(3) 可以氧化铜单质,但铜不与盐酸反应
(4)
(5)
(6) B D
【详解】(1)配制 溶液,需要 将固体先溶于浓盐酸,再稀释至指定浓度,原
因是抑制 水解。
(2)根据实验ⅰ中的现象,推测红褐色液体为胶体,胶体具有丁达尔效应,故可通过丁达
尔效应可快速判断其是否为胶体。
(3) 溶液与Cu反应的离子方程式为: ;实验ⅰ和ⅱ均先有
气体生成,后有溶液颜色的变化,甲同学认为产生该现象的原因可能是此实验条件下氧化
性: ,乙同学认为可以根据ⅲ判断氧化性: ,理由是: 可以氧化铜
单质,但铜不与盐酸反应。
(4)取红棕色溶液少许,加入 ,产生蓝色沉淀,可知此溶液中有亚铁离子,
推测 与 反应可生成亚铁离子和硫酸根离子,离子方程式为:
。
(5)另取红棕色溶液少许,检测其为胶体,向其中继续滴加 溶液,发现溶液红褐
色变深且产生刺激性气味的气体,说明铁离子和亚硫酸根离子发生双水解反应生成氢氧化铁胶体和二氧化硫,该气体是二氧化硫。
(6)结合(4)、(5),推测 溶液与 溶液反应同时存在氧化还原反应和双水解反
应。
17.(1)3 +Al3+=Al(OH) ↓+3CO ↑
3 2
(2)SO + +H O=HSO +HCO
2
(3)⑤
(4)c(Na+)>c(HCO )>c(CO )>c(OH-)>c(H+)
(5)a+b=13
(6)5
【详解】(1)碳酸氢根离子与铝离子发生双水解生成氢氧化铝沉淀和二氧化碳、水,离子
方程式:3 +Al3+=Al(OH) ↓+3CO ↑。
3 2
(2)由电离常数可知,酸性HSO >HCO>HSO >HCO ,故 溶液中通入足量
2 3 2 3
气体反应的离子方程式为SO + +H O=HSO +HCO 。
2
(3)酸和碱对水的电离起抑制作用,能水解的盐对水的电离起促进作用,则水的电离程度
最大的是能水解的盐,且水解程度最大的,其中CHCOONa、 溶液是单离子水解,
3
溶液是双离子互相促进水解,所以对水的电离促进程度更大,故答案为:⑤;
(4)0.1molCO 和0.15molNaOH反应生成0.05mol碳酸钠和0.05mol碳酸氢钠混合液,故
2
离子浓度大小为c(Na+)>c(HCO )>c(CO )>c(OH-)>c(H+)。
(5)25℃时, 的 的 溶液与 的 的 溶液混合后,溶液
呈中性,则 ,即 ,整理可得a和b满足的关系:a+b=13,故答案为:a+b=13;
(6)向 溶液中滴加 溶液至 ,
根据 ,解得 ,此时溶
液 5,故答案为:5。
18.(1)③>①>②
(2)向AgCl悬浊液中加入足量NaI溶液时,Ag+和I-反应生成AgI沉淀,平衡AgCl(s) Ag+
(aq)+Cl-(aq)正向移动,AgCl转化为黄色的AgI沉淀
(3)ClO-+CO +H O=HClO+HCO
2 2
(4) c(ClO-) c(HClO)
【详解】(1)①CHCOONH 溶液中CHCOO-的水解促进NH 水解而使NH 浓度减小;
3 4 3
②NH ClO溶液中ClO-的水解促进NH 水解而使NH 浓度减小,而酸性:CHCOOH>
4 3
HClO,则ClO-对NH 水解效果大于CHCOO-;③NH HSO 溶液中HSO 电离出H+抑制
3 4 4
NH 的水解,则常温下,相同浓度①CHCOONH、②NH ClO、③NH HSO 溶液中,[NH
3 4 4 4 4
]由大到小排列:③>①>②。
(2)向AgCl悬浊液中加入足量NaI溶液时,Ag+和I-反应生成AgI沉淀,平衡AgCl(s)
Ag+(aq)+Cl-(aq)正向移动,AgCl转化为黄色的AgI沉淀。
(3)由于酸性:HCO> HClO>HCO ,根据强酸制取弱酸的原理,向NaClO溶液中通入
2 3
少量CO 生成HClO和NaHCO ,离子方程式为:ClO-+CO +H O=HClO+HCO 。
2 3 2 2
(4)向饱和氯水中滴加NaOH溶液至溶液刚好为中性时,c(H+)=c(OH-),电荷守恒得:c(H+)+ c(Na+)=c(OH-)+c(Cl-)+c(ClO-),氯气与水反应生成氯化氢和次氯酸,依据物料守恒得
c(Cl-)= c(ClO-)+c(HClO),所以得c(Na+)=2c(ClO-)+c(HClO)。