文档内容
第1讲 钠及其重要化合物
[考纲要求]
1.了解钠及其重要化合物的制备方法。
2.掌握钠的主要性质及其应用。
3.掌握钠的重要化合物的主要性质及其应用。
考点一 钠的性质及用途
知识梳理
1.钠的物理性质
颜色:______色,有金属光泽;
密度:ρ(HO)____ρ(Na)____ρ(煤油);
2
硬度:质地________;
熔点:低于____ ℃。
2.钠的化学性质
(1)与非金属单质(如O、Cl)的反应
2 2
O
2
Cl:__________________
2
(2)与水反应
①离子方程式:__________________。
②钠与水(含酚酞)反应的实验现象及解释
(3)与盐酸反应
离子方程式:_______________________________________________________。
(4)钠与盐反应
①钠与盐溶液反应――→――→
如Na投入CuSO 溶液中,反应的离子方程式为__________________________。
4
②钠与熔融盐反应:
4Na+TiCl=====Ti+4NaCl
4
3.钠的制取及保存
(1)制取:化学方程式为 ______________。
(2)保存:密封保存,通常保存在____________中。
4.钠的用途
(1)制取NaO 等化合物。
2 2
(2)钠、钾合金(液态)可用于原子反应堆的导热剂。
(3)用作电光源,制作高压钠灯。
(4)冶炼某些金属,如制取金属钛。
[思考]
金属钠与氧气反应在不同条件下生成产物不同,据此回答下列问题。
(1)1 mol钠与足量氧气反应转移电子数为________。
(2)1 mol氧气与足量钠反应转移电子数范围为________。
(3) 金 属 钠 燃 烧 时 火 焰 为 黄 色 , 但 实 验 时 常 伴 有 黑 烟 , 原 因 是
________________________________________________________________________
________________________________________________________________________。
[判断] (正确的打“√”,错误的打“×”)
(1)钠表面自然形成的氧化层能够保护内层金属不被空气氧化( )
(2)钠与CuSO 溶液的反应:2Na+Cu2+===Cu↓+2Na+( )
4
(3)1 mol Na被完全氧化生成NaO,失去2N个电子( )
2 2 A
(4)钠与足量O 反应生成NaO,随着温度的升高,生成NaO的速率逐渐加快( )
2 2 2
(5)根据反应Na+KClNaCl+K↑,知Na的金属性强于K( )
(6)实验完毕后剩余的金属钠不能随意丢弃,应放回原试剂瓶( )
[提醒]
钠与盐溶液(除部分酸式盐溶液外,如NaHSO 溶液)反应时,先与水反应,生成的氢氧
4
化钠再与盐反应,故不会生成金属单质。如钠投入硫酸铜溶液中,生成氢氧化铜沉淀。
对点速练
练点一 钠的性质判断1.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,
则下列说法正确的是( )
A.第一块钠失去电子多
B.两块钠失去电子一样多
C.第二块钠的反应产物质量最大
D.两块钠的反应产物质量一样大
2.将金属钠放入盛有下列溶液的小烧杯中,既有气体,又有白色沉淀产生的是( )
①MgSO 溶液 ②NaSO 稀溶液 ③饱和澄清石灰水
4 2 4
④Ca(HCO) 溶液 ⑤CuSO 溶液 ⑥饱和NaCl溶液
3 2 4
A.①④⑤⑥ B.③④⑤⑥
C.②④⑤⑥ D.①③④⑥
3.向分别盛有100 mL水、100 mL 0.1 mol·L-1盐酸、100 mL 0.01 mol·L-1硫酸铜
溶液的X、Y、Z三个烧杯中各投入0.05 mol Na。下列有关说法正确的是( )
A.三个烧杯中均会发生的离子反应为2Na+2HO===2Na++2OH-+H↑
2 2
B.三个烧杯中钠均在液面上剧烈反应,且X烧杯中反应最剧烈
C.三个烧杯反应后,生成的溶质的物质的量浓度相同
D.三个烧杯反应后,生成的气体的质量一定相同
练后归纳
练点二 钠的探究性实验
4.为探究钠与盐反应的规律,某实验小组同学设计了下列两组实验:
实验1:如图,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水 CuSO
4
与熔化的钠接触。现象:瞬间产生耀眼的火花,同时有红色物质生成。
实验2:如图2,向盛有CuSO 溶液的小烧杯中加入一小块钠。
4
现象:钠浮在水面上,熔化成液态钠球并四处游动,生成蓝色沉淀。
问题:
(1)实验2中反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(2)比较实验1、实验2可知Na与CuSO 反应生成Cu的实验条件为
4
________________________________________________________________________
________________________________________________________________________。
5.如图甲是演示金属钠与水的反应的重要实验,为收集检验气体产物,某兴趣小组将
甲装置改进成如下乙或丙,请根据要求回答下列问题。
(1)写出钠与水反应的离子方程式:
________________________________________________________________________
________________________________________________________________________。
(2)按乙装置实验,液体添加完毕后,关闭活塞,打开右边胶塞,向煤油中加入一小块
钠,立即塞好胶塞,可观察到的现象是________(填字母)。
A.钠块始终保持在a处,直至完全消失
B.钠沉入U形管b处而后又慢慢浮到a处
C.钠处于煤油和水的交界处上下浮动
D.随反应的进行煤油与胶塞处液面下降,漏斗中液面上升E.最终钠块在煤油中燃烧起来
(3)乙装置中漏斗在反应过程中的主要作用是
________________________________________________________________________
________________________________________________________________________。
(4)用乙装置实验,点燃气体产物时,是否需要检验纯度________(填“是”或“否”)。
(5)按图丙所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按
下列两种情况收集产生的气体:①用铝箔包住钠;②用铜箔包住钠。在相同条件下体积的关
系是________(填字母)。
a.二者收集气体一样多 b.①收集气体体积较大
c.②收集气体体积较大
考点二 氧化钠与过氧化钠
知识梳理
1.氧化钠和过氧化钠的比较
物质 氧化钠(NaO) 过氧化钠(NaO)
2 2 2
色态 __________________ __________________
过氧化物
类别 __________________
(非碱性氧化物)
氧的价态 __________________ __________________
Na+ Na+
电子式 [\s\up2(×)O\s\up2(×)]2- [\s\up2(×)O\s\up3(·)O\s
Na+ \up2(×)]2-Na+
生成条件 常温 加热或点燃
热稳
__________________ 稳定
定性
与水
__________________ __________________
反应
化学性质
与CO
2
__________________ __________________
反应
与酸反应 2NaO+4HCl===4NaCl+2HO
__________________ 2 2 2
(盐酸) +O 2 ↑
主要性质 具有碱性氧化物通性 具有强氧化性用于制取少量Na 2 O 2 、 强氧化剂、漂白剂、供氧
主要用途
烧碱 剂、消毒剂
2.NaO 的强氧化性与还原性
2 2
从元素化合价角度分析NaO 的性质
2 2
(1)强氧化性的五个表现
(2)遇KMnO 等强氧化剂时,表现出还原性,氧化产物为O。
4 2
(3)遇CO、HO、H+则发生自身的氧化还原反应。
2 2
[判断] (正确的打“√”,错误的打“×”)
(1)氧化钠、过氧化钠均为碱性氧化物( )
(2)1 mol NaO 固体中含离子总数为4N( )
2 2 A
(3)NaO 溶于水产生O 的离子方程式为NaO+HO===2Na++2OH-+O↑( )
2 2 2 2 2 2 2
(4)NaO 的电子式为Na∶O∶O∶Na( )
2 2
(5)1 mol钠与氧气反应生成NaO或NaO 时,失去的电子数目均为N( )
2 2 2 A
(6)NaO 与HO反应时,NaO 既是还原剂又是氧化剂( )
2 2 2 2 2
(7)7.8 g NaO 与足量的CO 反应,转移电子的个数为0.2N( )
2 2 2 A
(8)NaO 在潮湿的空气中放置一段时间,最终产物是NaOH( )
2 2
[提醒]
金属钠露置在空气中会发生一系列变化,其过程:
银白色金属钠――→表面变暗――→出现白色固体接着表面变稀――→白色块状固
体――→白色粉末状物质
上述各步反应的化学方程式为:
①4Na+O===2NaO
2 2
②NaO+HO===2NaOH
2 2
③2NaOH+CO+9HO===NaCO·10HO
2 2 2 3 2
④NaCO·10HO===NaCO+10HO
2 3 2 2 3 2对点速练
练点一 钠的氧化物性质判断与计算
1.过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体质量
增加了28 g,反应中有关物质的物理量正确的是(N表示阿伏加德罗常数)( )
A
选项 二氧化碳 碳酸钠 转移的电子
A 1 mol 2N
A
B 22.4 L 1 mol
C 106 g 1 mol
D 106 g 2N
A
2.200 ℃时,11.6 g CO 和水蒸气的混合气体与足量的NaO 充分反应后固体质量增加
2 2 2
了3.6 g,则原混合气体的总物质的量是( )
A.0.125 mol B.0.25 mol
C.0.5 mol D.1 mol
3.如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。已知钠及其氧化
物的物质的量均为 0.1 mol,水的质量为100 g。下列说法正确的是( )
A.反应③最多能产生0.05 mol O
2
B.反应①的离子方程式为Na+2HO===Na++2OH-+H↑
2 2
C.NaO 中阴阳离子数目之比为1∶1
2 2
D.①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③
方法技巧
HO、CO 与NaO 反应的定量关系
2 2 2 2
1.物质的量的关系
无论是CO 或HO的单一物质还是二者的混合物,通过足量的NaO 时,CO 或HO与放出
2 2 2 2 2 2
O 的物质的量之比均为2∶1。
2
2.气体体积关系
若CO 和水蒸气的混合气体(或单一气体)通过足量的NaO,则气体体积减少的量等于
2 2 21
原混合气体体积的 ,且等于生成氧气的体积。
2
3.转移电子关系
2 mol的NaO 不论与HO还是与CO 反应均生成1 mol的O,转移2 mol的电子。
2 2 2 2 2
练点二 钠的氧化物的探究性实验
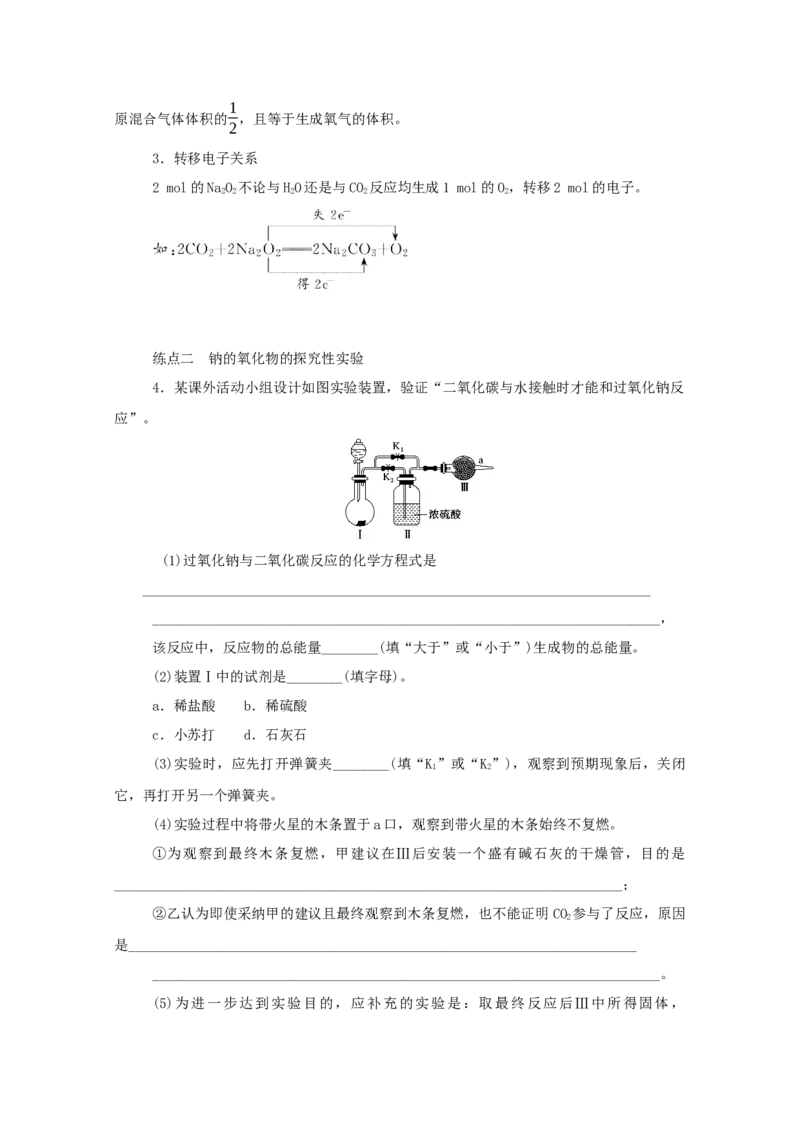
4.某课外活动小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反
应”。
(1)过氧化钠与二氧化碳反应的化学方程式是
________________________________________________________________________
________________________________________________________________________,
该反应中,反应物的总能量________(填“大于”或“小于”)生成物的总能量。
(2)装置Ⅰ中的试剂是________(填字母)。
a.稀盐酸 b.稀硫酸
c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹________(填“K”或“K”),观察到预期现象后,关闭
1 2
它,再打开另一个弹簧夹。
(4)实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃。
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是
________________________________________________________________________;
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明CO 参与了反应,原因
2
是________________________________________________________________________
________________________________________________________________________。
(5)为进一步达到实验目的,应补充的实验是:取最终反应后Ⅲ中所得固体,________________________________________________________________________。
△
5.NaO的制取可以通过如下反应完成:Na+NaNO NaO+N↑(未配平)。请回答下列
2 3 2 2
→
问题:
(1)上述反应的氧化剂是________(写化学式)。制取NaO时,若金属钠与NaNO 按质量
2 3
比23∶17投料,充分反应后收集到的气体体积为1.12 m3(标准状况下),则制得的NaO的质
2
量为________kg。
(2)制取NaO时由于设备密封性不好而进入了少量空气,导致制得的NaO产品中含有
2 2
NaO 杂质。现有NaO产品m g(假设只含有NaO 杂质),请从下面选用合适的仪器和试剂,设
2 2 2 2 2
计一种可选用的实验仪器组合,以完成样品中NaO含量的测定。
2
可选用的试剂:
a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH标准溶液 e.酚酞 f.碱石灰 g.
稀盐酸
实验需直接测定的有
实验过程中发生反应 实验所需仪器(用字 实验所需试剂(用字
关物理量(用文字说
的化学方程式 母表示) 母表示)
明)
(3)某学生设计了以下实验方案来测定该试样中NaO的质量分数,其操作流程和实验数
2
据如下:
该NaO产品中NaO的质量分数为 。
2 2
考点三 碳酸钠与碳酸氢钠
知识梳理
1.NaCO 和NaHCO 的性质
2 3 32.相互转化
NaCONaHCO
2 3 3
3.主要用途
(1)碳酸钠:用于造纸、制造玻璃、制皂、洗涤等。
(2)碳酸氢钠:用于发酵、医药、灭火剂等。
[思考]
NaCO 的制备——侯氏制碱法
2 3
(1)原料
食盐、氨气、二氧化碳——合成氨厂用水煤气制取氢气时的废气
其反应为C+HO(g)=====CO+H,CO+HO(g)=====CO+H。
2 2 2 2 2
(2)工艺流程
(3)反应原理
产生NaHCO 反应:
3________________________________________________________________________
________________________________________________________________________。
产生NaCO 反应:
2 3
________________________________________________________________________
________________________________________________________________________。
(4)循环使用的物质: 、 。
[判断] (正确的打“√”,错误的打“×”)
(1)用试管加热碳酸氢钠固体时,使试管口竖直向上( )
(2)分别加热NaCO 和NaHCO 固体,试管内壁均有水珠出现,则说明两种物质均受热
2 3 3
分解( )
(3)苏打是面包发酵粉的主要成分之一( )
(4)相同温度下溶解度:小苏打<苏打,热稳定性:NaCO>NaHCO( )
2 3 3
(5)向小苏打和苏打溶液中分别加入盐酸,均有气泡冒出,说明两者均能与盐酸反应
( )
(6)用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液( )
(7)确定NaCl溶液中是否混有NaCO 的方法是取少量溶液滴加CaCl 溶液,观察是否
2 3 2
出现白色浑浊( )
(8)向某溶液中加入稀盐酸,产生的气体通入澄清石灰水中,石灰水变浑浊,该溶液
一定是碳酸盐溶液( )
(9)用热的纯碱溶液洗去油污,是因为NaCO 可直接与油污反应( )
2 3
对点速练
练点一 NaCO、NaHCO 的性质判断
2 3 3
1.关于NaHCO 性质的有关叙述不正确的是( )
3
A.既能与强酸反应,又能与强碱反应
B.医疗上可用于治疗胃酸过多
C.与足量的酸反应时放出的CO 比与等质量的NaCO 要多
2 2 3
D.同温度时,NaHCO 的溶解度>NaCO 的溶解度
3 2 3
2.下列可以用来判定碳酸氢钠粉末中混有碳酸钠的实验方法是( )
A.加热时有无色气体放出
B.滴加盐酸时有气泡产生
C.溶于水后,滴加稀的氯化钡溶液有白色沉淀生成D.溶于水后,滴加澄清石灰水有白色沉淀生成
3.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
A.NaCO 溶液(NaHCO),选用适量的NaOH溶液
2 3 3
B.NaHCO 溶液(NaCO),应通入过量的CO 气体
3 2 3 2
C.NaO 粉末(NaO),将混合物在氧气中加热
2 2 2
D.NaCO 溶液(NaSO),加入适量Ba(OH) 溶液,过滤
2 3 2 4 2
方法总结
1.碳酸钠与碳酸氢钠的鉴别方法
(1)固体鉴别法
加热法,产生使澄清石灰水变浑浊的气体的是NaHCO。
3
(2)溶液鉴别法
①沉淀法:加入BaCl 或CaCl 溶液产生沉淀的是NaCO。
2 2 2 3
②气体法:滴入盐酸立即产生气体的是NaHCO。
3
③测pH法:用pH试纸测其相同浓度的稀溶液,pH大的是NaCO。
2 3
2.NaCO、NaHCO 的除杂方法
2 3 3
混合物(括号内为杂质) 除杂方法
NaCO(s)(NaHCO) 加热法
2 3 3
NaHCO(aq)(NaCO) 通入足量CO
3 2 3 2
NaCO(aq)(NaHCO) 滴加适量NaOH溶液
2 3 3
练点二 NaCO、NaHCO 的计算判断
2 3 3
4.有关NaHCO 和NaCO 的性质,以下叙述错误的是( )
3 2 3
A.等质量的NaHCO 和NaCO 与足量盐酸反应,在相同条件下NaCO 产生的CO 体积小
3 2 3 2 3 2
B.等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积 NaCO 是NaHCO 的
2 3 3
两倍
C.等质量NaHCO 和NaCO 与盐酸完全反应,前者消耗盐酸较多
3 2 3
D.等物质的量的NaHCO 和NaCO 与足量盐酸反应产生CO 一样多
3 2 3 2
5.(OH-、CO2− 、HCO− 与H+反应顺序的应用)分别取等物质的量浓度的氢氧化钠
3 3
溶液各 100 mL,再通入一定量的 CO ,随后分别各取 20 mL 溶液,向其中逐滴滴入 0.2
2
mol·L-1的盐酸,在标准状况下产生CO 的体积(y轴)与所加入盐酸的体积(x轴)的关系
2
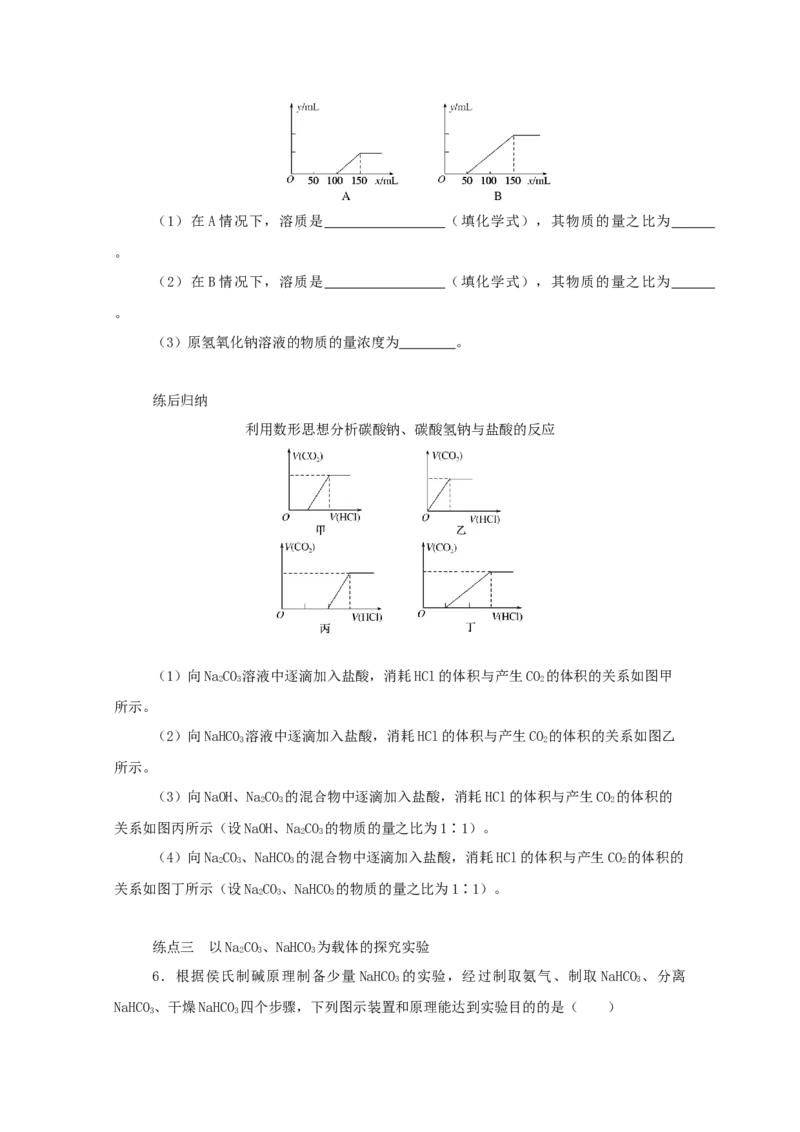
如下图(分A、B两种情况):(1)在A情况下,溶质是 (填化学式),其物质的量之比为
。
(2)在B情况下,溶质是 (填化学式),其物质的量之比为
。
(3)原氢氧化钠溶液的物质的量浓度为 。
练后归纳
利用数形思想分析碳酸钠、碳酸氢钠与盐酸的反应
(1)向NaCO 溶液中逐滴加入盐酸,消耗HCl的体积与产生CO 的体积的关系如图甲
2 3 2
所示。
(2)向NaHCO 溶液中逐滴加入盐酸,消耗HCl的体积与产生CO 的体积的关系如图乙
3 2
所示。
(3)向NaOH、NaCO 的混合物中逐滴加入盐酸,消耗HCl的体积与产生CO 的体积的
2 3 2
关系如图丙所示(设NaOH、NaCO 的物质的量之比为1∶1)。
2 3
(4)向NaCO、NaHCO 的混合物中逐滴加入盐酸,消耗HCl的体积与产生CO 的体积的
2 3 3 2
关系如图丁所示(设NaCO、NaHCO 的物质的量之比为1∶1)。
2 3 3
练点三 以NaCO、NaHCO 为载体的探究实验
2 3 3
6.根据侯氏制碱原理制备少量NaHCO 的实验,经过制取氨气、制取NaHCO 、分离
3 3
NaHCO、干燥NaHCO 四个步骤,下列图示装置和原理能达到实验目的的是( )
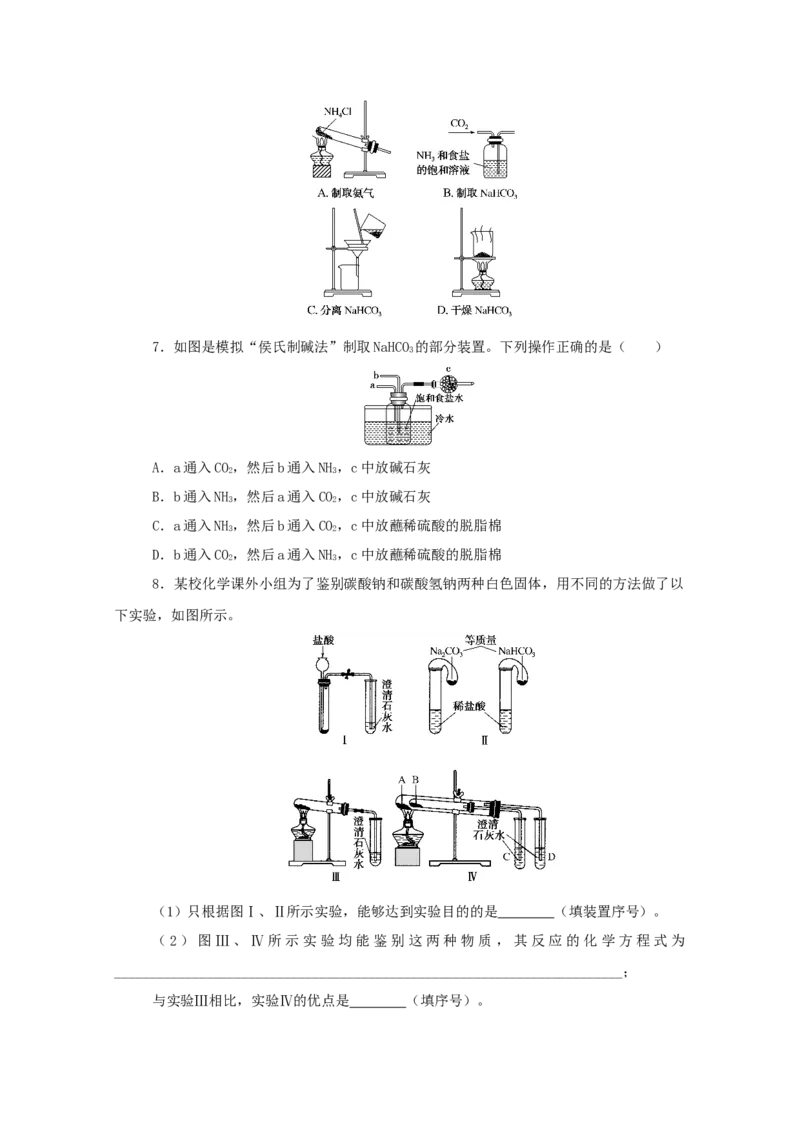
3 37.如图是模拟“侯氏制碱法”制取NaHCO 的部分装置。下列操作正确的是( )
3
A.a通入CO,然后b通入NH,c中放碱石灰
2 3
B.b通入NH,然后a通入CO,c中放碱石灰
3 2
C.a通入NH,然后b通入CO,c中放蘸稀硫酸的脱脂棉
3 2
D.b通入CO,然后a通入NH,c中放蘸稀硫酸的脱脂棉
2 3
8.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以
下实验,如图所示。
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是 (填装置序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
________________________________________________________________________;
与实验Ⅲ相比,实验Ⅳ的优点是 (填序号)。A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是
(填化学式)。
考点四 碱金属元素与焰色反应
知识梳理
1.碱金属
(1)相似性和递变性
相似性 递变性(由Li→Cs)
电子层数逐渐增多,核电荷数逐
原子结构 最外层均为1个电子
渐增大,原子半径逐渐增大
都具有较强的金属性,最高正价
元素性质 金属性逐渐增强
均为+1价
物理 (除Cs外)都呈银白色,密度较 密度逐渐增大(钾反常),熔、
性质 小,熔、沸点较低 沸点逐渐降低
单
质 具有较强的还原性
还原性逐渐增强。与O 反应越来
2
性 化学 ①与O 2 反应 越剧烈,产物越来越复杂。如
Li――→LiO。Na――→NaO;
质 性质 ②与H 2 O反应,反应方程式可表示 与HO反应越 2 来越剧烈,如 2 K 2 与水
为(用M代表碱金属)2M+ 2
反应可能会燃烧或轻微爆炸
2HO===2MOH+H↑
2 2
(2)特殊性
①碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠的小。
②碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度而将锂保存在石蜡中。
③碱金属跟氢气反应生成的碱金属氢化物都是离子化合物,其中氢以H-形式存在,碱
金属氢化物是强还原剂。
④试剂瓶中的药品取出后,一般不能放回原瓶,但Na、K等需放回原瓶。
⑤锂与O 反应与钠不同,只生成LiO。
2 2
2.焰色反应
(1)焰色反应的概念
某些金属或它们的化合物在灼烧时都会使火焰呈现出特殊的颜色,属于 变化,是
元素的性质。(2)焰色反应的操作
铂丝――→无色――→待测物――→观察火焰颜色――→铂丝――→无色
(3)常见元素的焰色
钠元素 色;钾元素 色(透过 观察);铜元素 色。
[判断] (正确的打“√”,错误的打“×”)
(1)ⅠA族元素又称碱金属元素( )
(2)碱金属元素Li、Na、K都可保存在煤油中( )
(3)焰色反应是一种复杂的化学变化( )
(4)钠、氧化钠、碳酸钠的焰色反应均显黄色( )
(5)焰色反应是大多数金属元素的性质,属于化学变化( )
(6)用洁净的铂丝对某溶液进行焰色反应,火焰呈黄色,则溶液中一定含有Na+,不
含K+( )
(7)无水硫酸铯的化学式为CsSO,它不易溶于水( )
2 4
(8)进行焰色反应时,使用稀硫酸清洗铂丝( )
(9)Li在空气中燃烧生成LiO( )
2 2
[提醒]
1.焰色反应是物理变化,可以是单质,也可以是化合物的固体或溶液。
2.用来清洗铂丝的是盐酸。
3.Li、Na、K在空气中燃烧主要产物分别是LiO、NaO、KO(超氧化钾)。
2 2 2 2
对点速练
练点一 碱金属元素的性质
1.下列有关铯及其化合物的说法不正确的是( )
A.CsOH的碱性比KOH的强
B.铯与水或稀盐酸反应剧烈,都生成H
2
C.Cs的还原性比Na的强,故Na+的氧化性强于Cs+
D.Li的金属性比Cs的强
2.碱金属元素单质及化合物有广泛用途。
回答下列问题:
(1)锂是最轻的活泼金属,常用于制造高效锂电池。电解池中的电解液不能用水作溶
剂 , 原 因 是
________________________________________________________________________________________________________________________________________________。
(2)金属钾是一种活泼的金属,下列有关其性质说法中正确的是( )
A.钾在空气中燃烧时,只生成KO
2
B.钾与水反应,由于反应剧烈可能会发生爆炸
C.1 mol·L-1 KOH溶液比1 mol·L-1 NaOH溶液碱性强
(3)KH是一种野外供氢剂,其电子式为 ,与水反应放出氢气,生成1 mol氢
气时,反应中转移电子数为 。
(4)工业上用钠制钾,反应方程式为 Na+KClK↑+NaCl,其原理为
________________________________________________________________________。
练后归纳
碱金属问题设置的六个方面:
(1)碱金属单质与水(或酸)反应的现象;
(2)碱金属单质的保存(注意碱金属的密度);
(3)碱金属单质与氧气反应产物的判断;
(4)碱金属对应的氢氧化物碱性强弱的比较;
(5)碱金属的碳酸盐性质的比较;
(6)与最新的科学技术相关的碱金属的应用。
练点二 焰色反应
3.《本草经集注》中对鉴别硝石(KNO )和朴硝(NaSO )的记载:“以火烧之,紫
3 2 4
青烟起,乃真硝石也”,与其相关的化学原理正确的是( )
A.焰色反应 B.丁达尔效应
C.颜色反应 D.热稳定性
4.做焰色反应实验时用到的铂丝,应该用下列哪种溶液洗涤( )
A.稀HCl B.浓HNO
3
C.稀HNO D.稀HSO
3 2 4
5.用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察到火焰呈黄色,下列各
判断正确的是( )
A.只含有Na+
B.一定含有Na+,可能含有K+
C.既含有Na+,又含有K+D.可能含有Na+,可能还含有K+
练后归纳
铂丝洗涤剂的选择
铂丝在使用前要用稀盐酸将其表面物质洗净,然后在火焰上灼烧至无色,这是因为金
属氯化物在灼烧时易挥发,若用稀HSO 洗涤铂丝,由于硫酸盐的熔、沸点较高难以挥发,会
2 4
对后面实验造成干扰。
本讲真题研练
1.[2019·全国卷Ⅱ,26(1)]立德粉ZnS·BaSO (也称锌钡白),是一种常用白色
4
颜料。回答下列问题:
利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧
立德粉样品时,钡的焰色为( )
A.黄色 B.红色 C.紫色 D.绿色
2.[2018·海南卷,1]下列食品添加剂中,常用作防腐剂的是( )
A.碘酸钾 B.碳酸氢钠
C.苯甲酸钠 D.磷酸氧钠
3.正误判断(正确的打“√”,错误的打“×”)。
(1)室温下Na与空气中O 反应制取NaO[2019·江苏卷,6D]( )
2 2 2
(2)盐碱地(含较多NaCO 等)不利于作物生长,可施加熟石灰进行改良[2019·天
2 3
津卷,3C]( )
(3)NaO 在空气中放置后由淡黄色变为白色原因的方程式是 2NaO===2NaO+
2 2 2 2 2
O↑[2019·全国卷Ⅲ,11C]( )
2
(4)2NaO+2CO===2NaCO+O 属于置换反应[2019·浙江4月,4C]( )
2 2 2 2 3 2
4.[2018·高考选项组合]下列说法不正确的是( )
A.NaHCO 受热易分解,可用于制胃酸中和剂[2018·江苏卷,3A]
3
B.NaO 可与CO 反应放出氧气,可用于制作呼吸面具[2018·海南卷,5A]
2 2 2
C.碳酸钠可用于去除餐具的油污[2018·全国卷Ⅱ,7A]
D.用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+[2018·全国卷
Ⅲ,10C]
5.[2017·海南卷,16]锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)用碳酸锂和 反应可制备氯化锂,工业上可由电解LiClKCl的熔融混合物
生产金属锂,阴极上的电极反应式为______________________________________。
(2)不可 使用二氧化 碳灭火器扑灭 因金属 锂引 起的火 灾,其原因是
________________________________________________________________________。
(3)硬脂酸锂是锂肥皂的主要成分,可作为高温润滑油和油脂的稠化剂。鉴别硬脂酸
锂与硬脂酸钠、硬脂酸钾可采用的实验方法和现象分别是
________________________________________________________________________
________________________________________________________________________。
(4)LiPF 易溶于有机溶剂,常用作锂离子电池的电解质。LiPF 受热易分解,其热分
6 6
解产物为PF 和________________________________________。
5
第1讲 钠及其重要化合物
考点一
1知识梳理
1.银白 > > 柔软 100
2.(1)4Na+O===2NaO 2Na+O=====NaO 2Na+Cl=====2NaCl (2)2Na+
2 2 2 2 2 2
2HO===2Na++2OH-+H↑ 小 低 放 H NaOH
2 2 2
(3)2Na+2H+===2Na++H↑
2
(4)2Na+2HO+Cu2+===2Na++Cu(OH)↓+H↑
2 2 2
3.(1)2NaCl(熔融)=====2Na+Cl↑ (2)石蜡油或煤油
2
思考 答案:(1)N (2)2N~4N (3)钠表面煤油未除尽,燃烧时冒黑烟
A A A
判断 答案:(1)× (2)× (3)× (4)× (5)× (6)√
2对点速练
1.解析:金属钠失电子均变为+1价的阳离子,等质量的两块钠,失电子是一样的。
根据4Na+O===2NaO,则1 mol金属钠完全反应得氧化钠的质量是 31 g,根据反应2Na+
2 2
O===NaO,则1 mol金属钠完全反应得过氧化钠的质量是39 g,等质量的两块钠,即金属钠
2 2 2
的物质的量是相等的,所以生成过氧化钠的质量大,即第一块钠的反应产物质量大。
答案:B2.解析:2Na+2HO===2NaOH+H↑,①中Mg2++2OH-===Mg(OH) ↓;③中反应消耗
2 2 2
水,溶液温度升高,Ca(OH) 的溶解度降低,析出Ca(OH)
沉淀;④中Ca2++HCO−
+OH
2 2 3
-===CaCO↓+HO;⑤生成的Cu(OH) 是蓝色沉淀,不符合题意;⑥水减少,c(Na+)增大,
3 2 2
使NaCl(s) Na+(aq)+Cl-(aq)平衡向左移动。
⇌
答案:D
3.解析:钠与盐酸反应时钠先与H+反应,离子方程式表示为2Na+2H+===2Na++
H↑,与CuSO 溶液反应会生成沉淀,A错误;X烧杯中,水中的氢离子浓度最小,反应最慢,
2 4
B错误;X烧杯中生成的溶质为NaOH,Y烧杯中生成的溶质为NaCl,Z烧杯中生成的溶质为
NaSO ,由于钠的物质的量相同,故Z烧杯中物质的量浓度最小,C错误;因向三个烧杯中加
2 4
入钠的物质的量相同且钠全部反应完,故生成H 的量相同,D正确。
2
答案:D
4.答案:(1)2Na+Cu2++2HO===2Na++Cu(OH)↓+H↑ (2)加热且无水
2 2 2
5.解析:(2)因钠的密度比水小,比煤油大,钠与水接触时反应产生氢气,生成的
气体将钠块带离水层,进入煤油层后停止反应又下沉,如此往复,直至钠反应完,反应过程
中没有氧气,钠不可能燃烧,所以钠处于煤油和水的交界处,上下浮动。(4)液体充满U形
管,反应过程中只产生氢气,不可能含有氧气,点燃时不会爆炸,因而不需要检验氢气的纯
度。(5)Na和HO反应产生H 的同时产生NaOH,NaOH可以和Al发生反应2Al+2NaOH+
2 2
6HO===2Na[Al(OH)]+3H↑,故用铝箔包住Na时产生的H 的体积较大。
2 4 2 2
答案:(1)2Na+2HO===2Na++2OH-+H↑
2 2
(2)CD (3)储存反应过程中排出的水 (4)否 (5)b
考点二
1知识梳理
1.白色固体 淡黄色固体 碱性氧化物 -2 -1 不稳定(2NaO+O=====2NaO )
2 2 2 2
NaO + HO===2NaOH 2NaO + 2HO===4NaOH + O↑ NaO + CO===NaCO 2NaO +
2 2 2 2 2 2 2 2 2 3 2 2
2CO===2NaCO+O NaO+2HCl===2NaCl+HO
2 2 3 2 2 2
判断 答案:(1)× (2)× (3)× (4)× (5)√ (6)√ (7)×
(8)×
2对点速练1.解析: +2CO===2NaCO+O Δm 转移电子
2 2 3 2
2 mol 2 mol 56 g 2 mol
1 mol 1 mol 28 g 1 mol
由上述关系,不难得出C项正确。B项中未指明标准状况,错误。
答案:C
2.解析:根据质量守恒定律可知,生成O 的质量为11.6 g-3.6 g=8 g,n(O )=
2 2
8 g
=0.25 mol,根据NaO 与HO(g)、CO 反应的物质的量的关系可知CO 和HO
32g·mol-1 2 2 2 2 2 2
(g)的物质的量之和为0.25 mol×2=0.5 mol。
答案:C
3.解析:0.1 mol Na O 与100 g H O反应,HO过量,反应③最多能产生0.05 mol
2 2 2 2
O ,选项A正确;反应①的离子方程式应为2Na+2HO===2Na++2OH-+H↑,选项B错误;
2 2 2
NaO 中阴阳离子数目之比为1∶2,选项C错误;①、②、③充分反应后所得溶液中溶质
2 2
(NaOH)的质量分数从大到小:③=②>①,选项D错误。
答案:A
4.解析:(1)此反应是放热反应。
(2)依据实验目的,需要干燥CO ,所以装置Ⅰ是制取CO 的装置,因为盐酸易挥发出
2 2
HCl,所以应选择稀硫酸、小苏打。
(3)先通干燥CO,然后再通湿润CO 进行对比。
2 2
(5)证明反应后固体中含有CO2−
。
3
答案:(1)2NaO+2CO===2NaCO+O 大于
2 2 2 2 3 2
(2)bc (3)K
2
(4)①除去未充分反应的CO ②水与NaO 反应生成O
2 2 2 2
(5)加入稀盐酸,将产生的气体通入澄清石灰水中(答案合理即可)
5.解析:(1)由N元素的化合价降低可知,NaNO 是氧化剂。配平方程式:10Na+
3
2NaNO=====6NaO+N↑,收集到 1.12 m3(标准状况下)N ,n(N )=50 mol,那么n
3 2 2 2 2
(NaO)=300 mol,故m(NaO)=18.6 kg。
2 2
(2)测定样品中氧化钠的含量有多种方法,可通过测生成 O 的体积来计算NaO 的量;
2 2 2也可测反应后锥形瓶和溶液的总质量与反应前锥形瓶、样品和水的总质量之差,还可以通过
滴定法测锥形瓶中生成NaOH的量来计算。
解析:(3)设试样中NaO的物质的量为x mol,NaO 的物质的量为y mol,则有:62x
2 2 2
0.1×62
+78y=7.75,78(x+y)=9.35,解得:x=0.1,那么NaO的质量分数为 ×100%
2 7.75
=80%。
答案:(1)NaNO 18.6
3
(2)(以下三种方法任选一种,其他合理方法亦可)
2Na 2 O 2 +2H 2 O===4NaOH ①反应前锥形瓶、样品和水的总
+O↑, A、D b 质量
2
NaO+HO===2NaOH ②反应后锥形瓶和溶液的总质量
2 2
2NaO+2HO===4NaOH
2 2 2
+O↑, G、C b 量筒中收集到的气体的体积
2
NaO+HO===2NaOH
2 2
2NaO+2HO===4NaOH
2 2 2
+O↑, 中和锥形瓶中样品与水反应后所
2
D、H b、c、e 得溶液使用的盐酸标准溶液的体
Na 2 O+H 2 O===2NaOH, 积
NaOH+HCl===NaCl+HO
2
(3)80%
考点三
1知识梳理
1.NaCO +2HCl===2NaCl+HO+CO↑ NaCO +Ca(OH) ===CaCO↓+2NaOH NaCO
2 3 2 2 2 3 2 3 2 3
+BaCl===BaCO↓+2NaCl 小 NaHCO +HCl===NaCl+HO+CO↑ HCO− +OH-+Ca2+
2 3 3 2 2 3
===CaCO↓+HO
Ca2++2OH-+2HCO===CaCO↓+CO2−
+2HO 无明显 2NaHCO=====NaCO
3 2 3 3 2 3 2 3
+HO+CO↑
2 2
思考 答案:(3)NH +NaCl+CO +HO===NaHCO↓+NHCl 2NaHCO=====NaCO +
3 2 2 3 4 3 2 3
CO↑+HO
2 2
(4)CO 饱和食盐水
2
判断 答案:(1)× (2)× (3)× (4)√ (5)√ (6)√ (7)√(8)× (9)×
2对点速练
1.解析:NaHCO 可与酸反应生成二氧化碳气体,如与盐酸反应生成二氧化碳、氯化钠
3
和水,也可与碱反应,如与氢氧化钠反应生成碳酸钠和水,故A正确;碳酸氢钠和盐酸反应,
可用于中和胃酸,故B正确;等质量的碳酸钠、碳酸氢钠,n(NaHCO )>n(NaCO ),分别
3 2 3
与足量的盐酸反应,NaHCO 生成的二氧化碳多,故C正确;常温下相同的溶剂时,NaCO 较
3 2 3
NaHCO 易溶,故D错误。
3
答案:D
2.解析:NaHCO 与BaCl 不反应,而NaCO 与BaCl 溶液反应产生白色BaCO 沉淀,C项
3 2 2 3 2 3
正确。
答案:C
3.解析:Ba(OH) 与NaCO 和NaSO 均发生化学反应生成白色沉淀,不符合除杂的要
2 2 3 2 4
求。
答案:D
4.解析:NaCO+2HCl===2NaCl+CO↑+HO
2 3 2 2
NaHCO+HCl===NaCl+CO↑+HO
3 2 2
1
解答此类题目用归“1”法。A项,假设二者都是1 g,则n(NaHCO )=n(CO )=
3 2 84
1
mol,n(NaCO )=n(CO )= mol,正确;B项,假设二者均为1 mol,则消耗的盐酸:
2 3 2 106
NaCO 为2 mol,NaHCO 为1 mol,正确;C项,假设二者均为1 g,NaCO 需盐酸的物质的量
2 3 3 2 3
1 1
为2× mol= mol,NaHCO 需盐酸 mol,错误。
106 3 84
答案:C
5.解析:CO 与NaOH溶液反应时,据CO 与NaOH量的相对多少,有这样两个阶段:
2 2
①CO +2NaOH===NaCO +HO,此时溶质可能为NaOH和NaCO 或只有NaCO (刚好反应);②
2 2 3 2 2 3 2 3
NaCO +CO +HO===2NaHCO ,此时溶质可能为NaCO 和NaHCO 或只有NaHCO ;据图分析:B
2 3 2 2 3 2 3 3 3
情况最终生成的CO(其实就是最初通入的与NaOH溶液反应的CO)是A情况的2倍。
2 2
(3)当加入150 mL盐酸时,恰好完全反应,此时溶液中溶质为NaCl。据物料守恒有n
(NaOH)=n(Na+)=n(Cl-)=0.2 mol·L-1×0.15 L=0.03 mol,所以原氢氧化钠溶液0.03mol
的物质的量浓度为 =1.5 mol·L-1。
0.02L
答案:(1)NaOH、NaCO 1∶1
2 3
(2)NaCO、NaHCO 1∶1
2 3 3
(3)1.5 mol·L-1
6.解析:NHCl在试管底部分解为NH 和HCl,温度一降低又会生成NHCl,无法得到
4 3 4
NH ,A错误;通入CO 的导管应长进短出,B错误;CO 通入氨化的饱和食盐水生成NaHCO 沉
3 2 2 3
淀:NH +NaCl+CO +HO===NaHCO↓+NHCl,可用过滤方法分离 NaHCO ,C 正确;加热
3 2 2 3 4 3
NaHCO 会分解:2NaHCO=====NaCO+CO↑+HO,同时对固体加热应在坩埚中进行,D错误。
3 3 2 3 2 2
答案:C
7.解析:由于CO 在水中的溶解度比较小,而NH 极易溶于水,所以在实验中要先通入
2 3
溶解度较大的NH ,再通入CO ,由于NH 极易溶于水,在溶于水时极易发生倒吸现象,所以
3 2 3
通入NH 的导气管的末端不能伸入到溶液中,即a先通入NH ,然后b通入CO ,A、B、D均错
3 3 2
误;因为NH 是碱性气体,所以过量的NH 要用稀硫酸来吸收,故答案选C。
3 3
答案:C
8.解析:(1)图Ⅰ不能达到实验目的,因为无论碳酸钠还是碳酸氢钠均可以与盐酸
反应产生二氧化碳,二氧化碳气体与澄清石灰水作用变浑浊,故不可以;图Ⅱ可以鉴别,因
为等质量的碳酸钠和碳酸氢钠与足量的稀盐酸反应,生成的二氧化碳气体的量不同,可根据
气球膨胀程度来判断。
(2)图Ⅲ、Ⅳ所涉及的化学方程式为 2NaHCO=====NaCO +HO+CO↑,CO +Ca
3 2 3 2 2 2
(OH)===CaCO↓+HO,实验Ⅳ的优点是可同时做对比实验。
2 3 2
解析:(3)试管B装入碳酸氢钠,试管A装入碳酸钠,这样直接加热的碳酸钠,温度
高,不分解,不能使澄清石灰水变浑浊,而间接加热的碳酸氢钠分解,使澄清石灰水变浑浊,
表明了碳酸氢钠很不稳定。
答案:(1)Ⅱ
(2)2NaHCO=====NaCO+HO+CO↑、CO+Ca(OH)===CaCO↓+HO D
3 2 3 2 2 2 2 3 2
(3)NaHCO
3
考点四
1知识梳理
2.(1)物理 (3)黄 紫 蓝色钴玻璃 绿判断 答案:(1)× (2)× (3)× (4)√ (5)× (6)× (7)×
(8)× (9)×
2对点速练
1.解析:根据元素周期律,Cs的金属性比K强,故CsOH的碱性比KOH强,A项正确;
Cs的性质与钠相似,Na能与水或稀盐酸反应产生H ,故Cs也能与水或稀盐酸反应产生H ,
2 2
且反应更剧烈,B项正确;Cs的还原性强于Na,则Na+得电子能力比Cs+强,即氧化性:Na+
>Cs+,C项正确;Li、Cs均为碱金属元素,Cs的电子层数多,更容易失去最外层电子,故金
属性:Cs>Li,D项错误。
答案:D
2.答案:(1)锂可以与水反应 (2)B (3)K+[H∶]- N
A
(4)高温下,K变为蒸汽逸出,浓度减小,平衡右移
3.解析:鉴别硝石(KNO )和朴硝(NaSO ),由信息可知,Na、K的焰色反应不同,
3 2 4
则“以火烧之,紫青烟起,乃真硝石也”,该方法应用了焰色反应,故A项正确。
答案:A
4.解析:铂丝应用盐酸洗涤,而不能利用硫酸洗涤,硫酸不挥发,不能利用浓硝酸,
浓硝酸容易分解。
答案:A
5.解析:钠元素的焰色为黄色,而钾元素的焰色为紫色,而且黄色会干扰紫色,所以
不能判断是否含有钾元素。
答案:B
本讲真题研练
1.解析:重要金属的焰色反应的颜色平时要注意识记。
答案:D
2.答案:C
3.答案:(1)× (2)× (3)× (4)×
4.答案:A
5.解析:(1)碳酸锂与盐酸反应生成LiCl,由电解LiClKCl的熔融混合物产生金属
锂,阴极上锂离子得到电子。
(2)Li是活泼的金属,与二氧化碳反应。
(3)阳离子不同、焰色反应不同。(4)在LiPF 和PF 中磷的化合价都是+5价,因而该分解反应为非氧化还原反应,根
6 5
据原子守恒,即可确定另一氟化物的化学式为LiF。
答案:(1)盐酸 Li++e-===Li
(2)Li与二氧化碳反应
(3)焰色反应,观察到黄色的为硬脂酸钠,透过蓝色钴玻璃观察到紫色的为硬脂酸钾
(4)LiF