文档内容
上海市金山区 2022-2023 学年高三上学期第一次质量调研
化学试题
式量:Fe—56; —232; —233; —197; —217
一、选择题(共40分,每小题2分。每小题只有一个正确答案)
1. 下列有热量放出的过程是
A. 浓硫酸稀释 B. 冰融化
C. 石灰石高温分解 D. 断开 中的H-H键
2. 反应 可除去 ( )污染。下列说法正确 是
的
A. 是极性分子 B. 电子式:
C. 中含有非极性键 D. 中子数为18的Cl原子: Cl
18
3. 以下事实可以判断元素的非金属性氧强于氮的是
A. 相对原子质量:O>N B. 空气中含量:
C. 沸点: D. 在 中燃烧生成
4. 环碳 (C )中碳原子是单键和三键交替连接的,结构如图所示。下列说法正确的是
18
A. 与 互为同系物 B. 和 互为同位素
C. 和金刚石互为同分异构体 D. 环碳中碳原子均达8电子稳定结构
5. 丹参醇具有抗心律失常作用,其合成路线中的一步反应如下。有关说法正确的是A. Y的分子式为 B. Y不能发生消除反应
C. X所有原子位于同一平面 D. X和Y可用 (H+)鉴别
6. NaCl是化学工业的最基本原料之一,下列说法符合工业生产实际的是
A. 电解饱和食盐水制金属钠
B. 在食盐中加入 制加碘食盐
C. 将 通入氨化的饱和食盐水中,析出 晶体
D. 采用电解饱和食盐水在阳极上同时获得 和烧碱
7. 实验室用盐酸和二氧化锰制备 ,有关说法正确的是
A. 增大盐酸的浓度能加快反应速率 B. 用稀盐酸则反应速率较慢
C. 增加 的用量可显著加快反应速率 D. 升高温度则减慢反应速率
8. 实验室用无水乙醇和浓硫酸制取乙烯的操作,错误是
A. 先注入无水乙醇再慢慢倒入浓硫酸 B. 放入几片碎瓷片
C. 加热,使温度慢慢升到170℃ D. 用排水法收集乙烯
9. 关于前四周期主族元素 、 、 、 的判断正确的是
A. 原子半径: B. 热稳定性:
C. 酸性: D. Ge位于第四周期ⅥA族
10. 有关铝及其化合物的说法正确的是
A. 铝片可与冷水剧烈反应 B. 铝热反应放出的热量使生成的铁熔化
C. 氧化铝是碱性氧化物 D. 氢氧化铝能溶于稀氨水
11. 实验室从碘的四氯化碳溶液中分离单质碘的主要步骤为:用浓 溶液进行反萃取、分液、酸化、
过滤及干燥等。下列说法正确的是A. 反萃取时 与 溶液反应的离子方程式:
B. 反萃取时倒转振荡过程中要适时旋开活塞放气
C. 分液时,先放出有机相,然后从下口放出水相
D. 酸化后过滤时,用玻璃棒搅拌可加快单质碘从酸化后的体系分离
12. 为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是
选项 被提纯的物质 除杂试剂 分离方法
A 溴化钠溶液(NaI) 氯水、CCl 萃取、分液
4
B 氯化铵溶液(FeCl ) 氢氧化钠溶液 过滤
3
C 二氧化碳(CO) 氧化铜粉末 通过灼热的氧化铜粉末
D 乙酸乙酯(CHCOOH) 乙醇、浓硫酸 加热蒸馏
3
A. A B. B C. C D. D
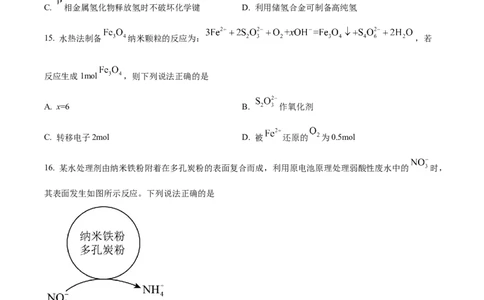
13. 已知锰酸钾(K MnO )在浓的强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO +2H O=2MnO
2 4 2
+MnO↓+4OH-。下列用Cl 氧化KMnO 制备KMnO 的实验原理和装置不能达到实验目的的是
2 2 2 4 4
A. 用装置甲制取Cl B. 用装置乙除去 Cl 中的HCl
2 2
C. 用装置丙使KMnO 转化成KMnO D. 用装置丁分离出溶液中的MnO
2 4 4 2
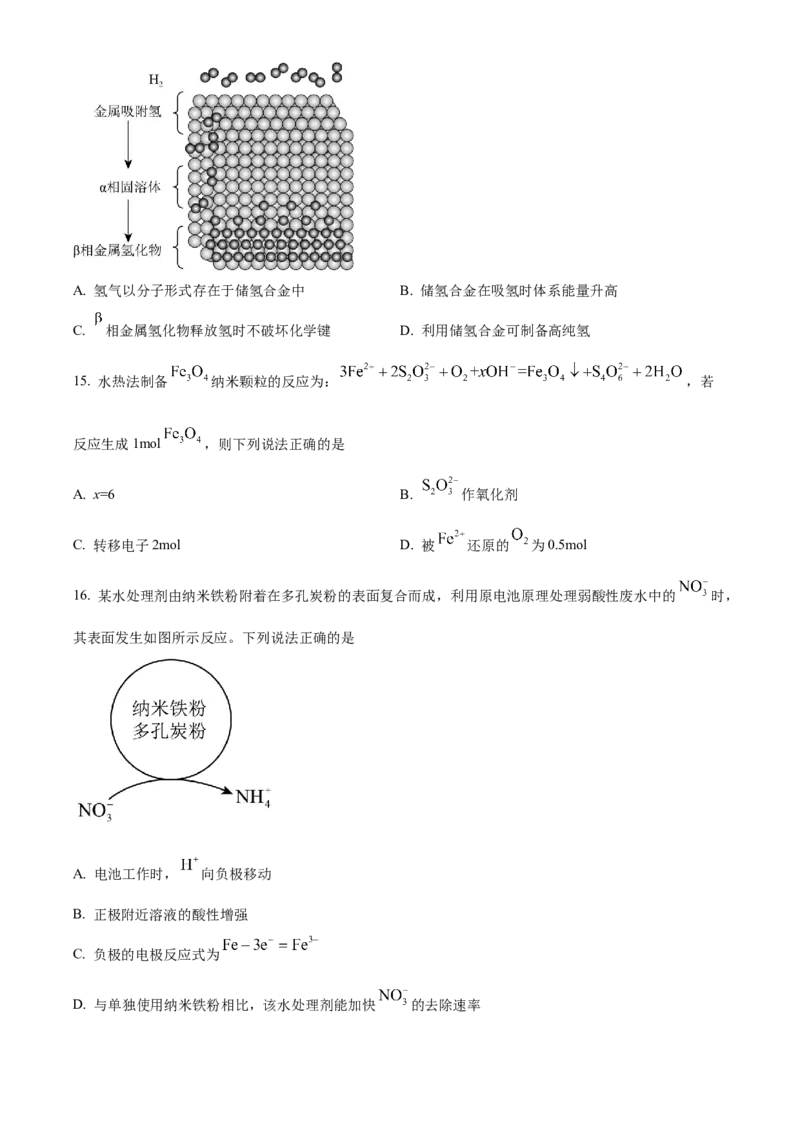
14. 图示为某储氢合金的吸氢过程,此过程放出大量热。下列说法正确的是A. 氢气以分子形式存在于储氢合金中 B. 储氢合金在吸氢时体系能量升高
C. 相金属氢化物释放氢时不破坏化学键 D. 利用储氢合金可制备高纯氢
15. 水热法制备 纳米颗粒的反应为: ,若
反应生成1mol ,则下列说法正确的是
A. x=6 B. 作氧化剂
C. 转移电子2mol D. 被 还原的 为0.5mol
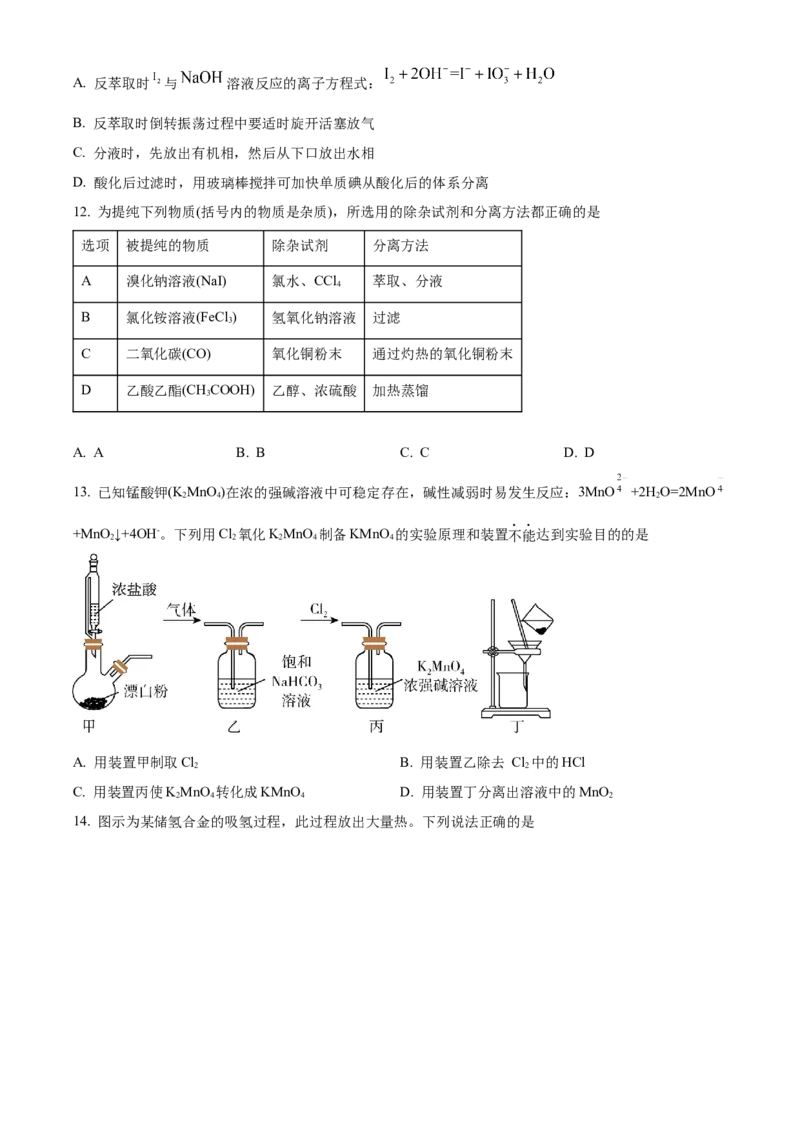
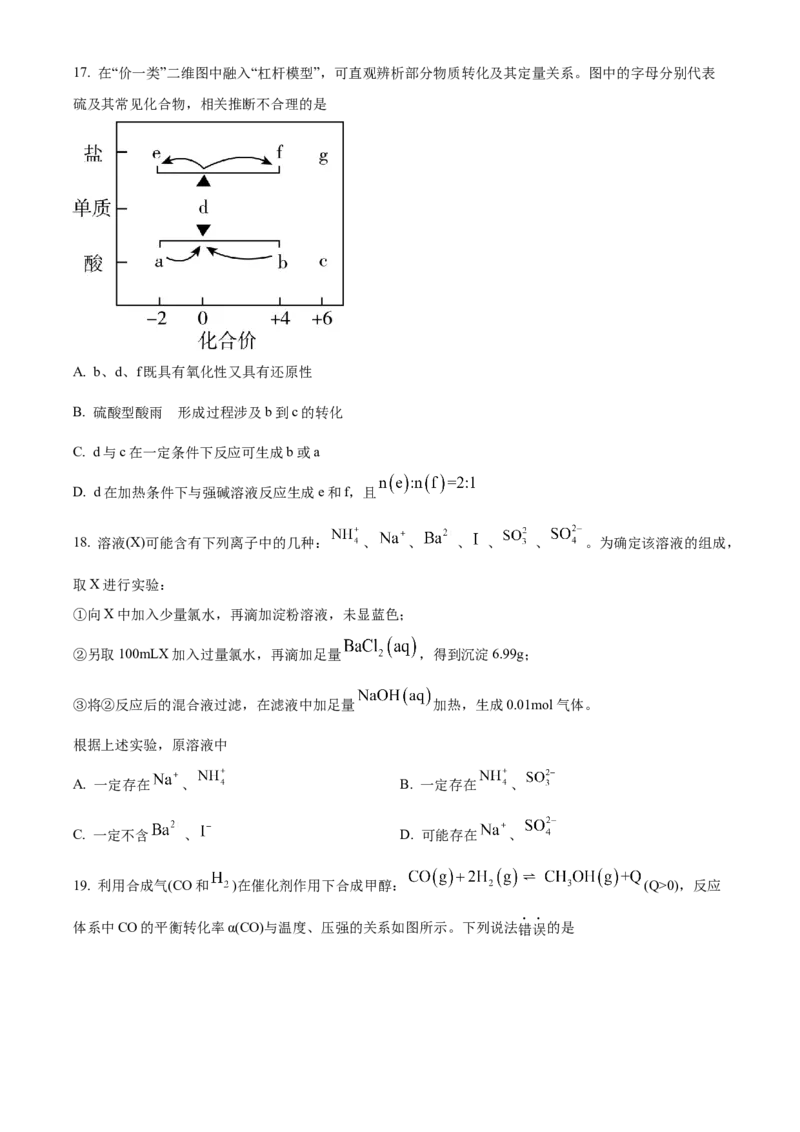
16. 某水处理剂由纳米铁粉附着在多孔炭粉的表面复合而成,利用原电池原理处理弱酸性废水中的 时,
其表面发生如图所示反应。下列说法正确的是
A. 电池工作时, 向负极移动
B. 正极附近溶液的酸性增强
C. 负极的电极反应式为
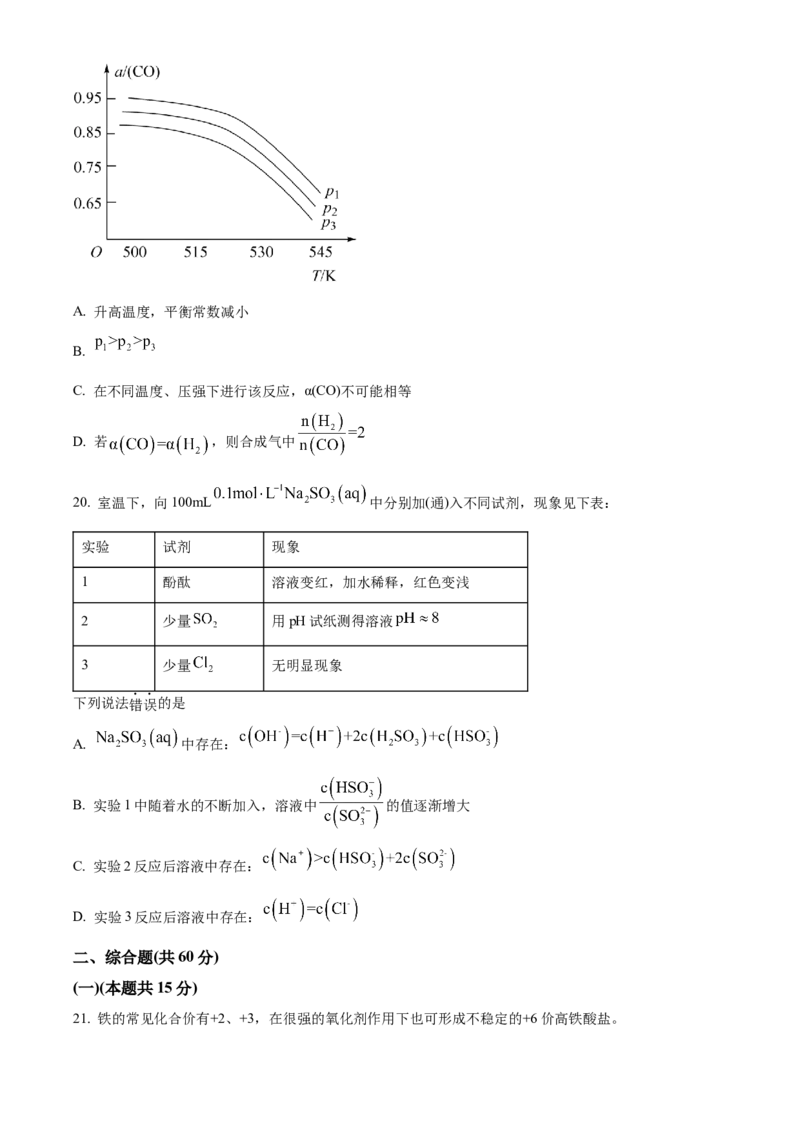
D. 与单独使用纳米铁粉相比,该水处理剂能加快 的去除速率17. 在“价一类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。图中的字母分别代表
硫及其常见化合物,相关推断不合理的是
A. b、d、f既具有氧化性又具有还原性
的
B. 硫酸型酸雨 形成过程涉及b到c的转化
C. d与c在一定条件下反应可生成b或a
D. d在加热条件下与强碱溶液反应生成e和f,且
18. 溶液(X)可能含有下列离子中的几种: 、 、 、 、 、 。为确定该溶液的组成,
取X进行实验:
①向X中加入少量氯水,再滴加淀粉溶液,未显蓝色;
②另取100mLX加入过量氯水,再滴加足量 ,得到沉淀6.99g;
③将②反应后的混合液过滤,在滤液中加足量 加热,生成0.01mol气体。
根据上述实验,原溶液中
A. 一定存在 、 B. 一定存在 、
C. 一定不含 、 D. 可能存在 、
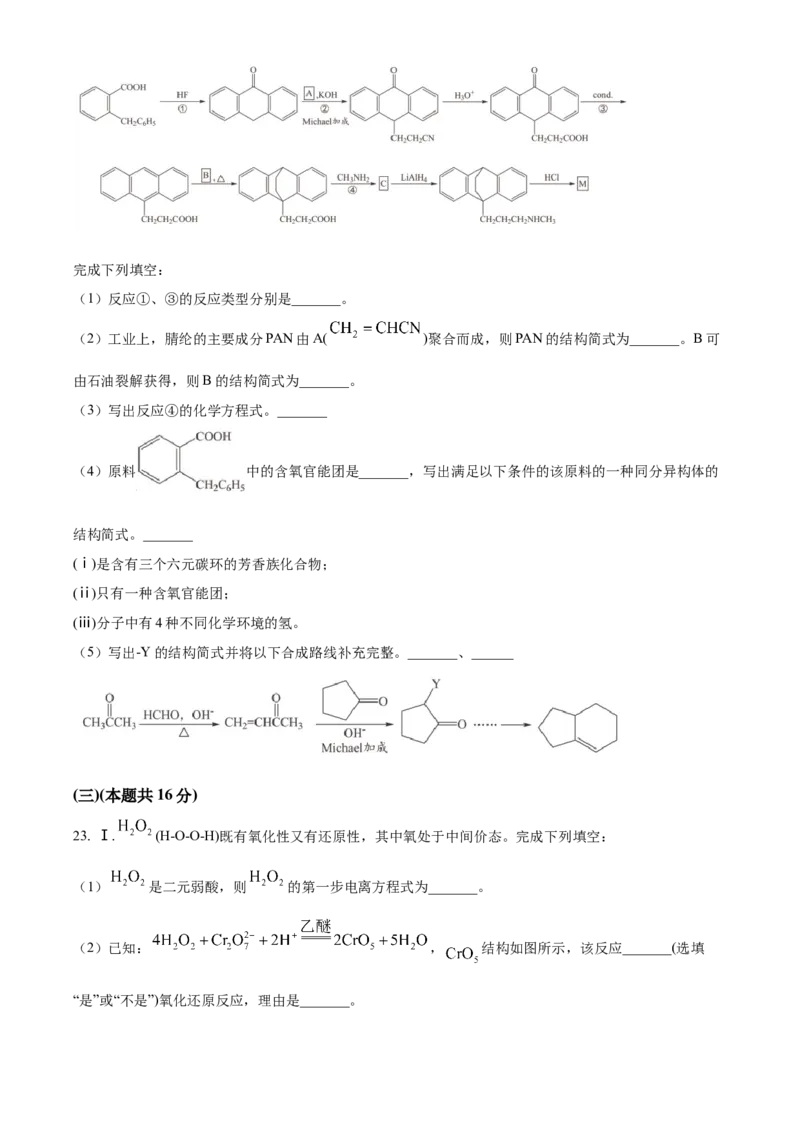
19. 利用合成气(CO和 )在催化剂作用下合成甲醇: (Q>0),反应
体系中CO的平衡转化率α(CO)与温度、压强的关系如图所示。下列说法错误的是A. 升高温度,平衡常数减小
B.
C. 在不同温度、压强下进行该反应,α(CO)不可能相等
D. 若 ,则合成气中
20. 室温下,向100mL 中分别加(通)入不同试剂,现象见下表:
实验 试剂 现象
1 酚酞 溶液变红,加水稀释,红色变浅
2 少量 用pH试纸测得溶液
3 少量 无明显现象
下列说法错误的是
A. 中存在:
B. 实验1中随着水的不断加入,溶液中 的值逐渐增大
C. 实验2反应后溶液中存在:
D. 实验3反应后溶液中存在:
二、综合题(共60分)
(一)(本题共15分)
21. 铁的常见化合价有+2、+3,在很强的氧化剂作用下也可形成不稳定的+6价高铁酸盐。Ⅰ.实验室以 为原料制备高密度磁记录材料Fe/ 复合物,装置如图所示。在氩气气氛中,
向装有50mL 的三颈烧瓶中逐滴加入100mL ,100℃下搅拌回流
3h,得到成分为Fe和 的黑色沉淀。
待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,40℃干燥后焙烧3h,得到Fe/ 复
合物产品3.24g。
完成下列填空:
(1)三颈烧瓶内发生反应的离子方程式为_______;检验反应是否进行完全的操作是_______。
的
(2)焙烧需在隔绝空气条件下进行,原因是_______,实验所得产品 产率为_______。
Ⅱ.已知: 为共价化合物,熔点是306℃,易水解:
的平衡常数 。
(3) 的晶体类型属于_______。
(4)向 中加入 以除去杂质 ,为使溶液中c(Fe3+)≤10-6mol/L,则溶液中
c(OH-)≥_____mol/L。用平衡移动原理解释除杂原理。_______。
(二)(本题共15分)
22. 抗抑郁药盐酸马普替林(M: )的一条合成路线如下:完成下列填空:
(1)反应①、③的反应类型分别是_______。
(2)工业上,腈纶的主要成分PAN由A( )聚合而成,则PAN的结构简式为_______。B可
由石油裂解获得,则B的结构简式为_______。
(3)写出反应④的化学方程式。_______
(4)原料 中的含氧官能团是_______,写出满足以下条件的该原料的一种同分异构体的
结构简式。_______
(ⅰ)是含有三个六元碳环的芳香族化合物;
(ⅱ)只有一种含氧官能团;
(ⅲ)分子中有4种不同化学环境的氢。
(5)写出-Y的结构简式并将以下合成路线补充完整。_______、______
(三)(本题共16分)
23. Ⅰ. (H-O-O-H)既有氧化性又有还原性,其中氧处于中间价态。完成下列填空:
(1) 是二元弱酸,则 的第一步电离方程式为_______。
(2)已知: , 结构如图所示,该反应_______(选填
“是”或“不是”)氧化还原反应,理由是_______。(3)少量 催化分解 的反应分两步进行,第一步: ;写出第二
步反应的离子方程式。_______
Ⅱ.称取1.023g ( )加入20.0mL 酸化后定容至
100mL,取出10.00mL用 的 滴定至终点,消耗 24.34mL。
已知:①
② (未配平)
(4)配平离子方程式。_______
(5)实验所需的定量仪器有电子天平、量筒、_______。
(6)滴定终点的现象为溶液变为_______色,且30s不变色。理论上消耗 _______mL,实验
过程操作正确,产生误差的原因可能是_______。
(四)(本题共14分)
24. 丙烯( )是石油化工的基础有机原料之一,主要用于生产聚丙烯、二氯丙烷、异丙醇等。制备方法
如下:
方法一 丙烷氧化脱氢法制备丙烯: (正反应放热)
在催化剂的作用下、相同的反应时间, 的转化率和 的产率随温度变化关系如图。完成下列填空:
(1) 的转化率随温度升高而上升的原因是_______,写出一条提高 产率的措施。_______
方法二 丙烷脱氢制备丙烯: 。
(2)已知: ;
用含a、b的代数式表示Q=_______。
(3)某温度下,在一恒容容器中充入 ,发生脱氢制丙烯反应,起始压强为10kPa,平衡时总压强为
14kPa, 的平衡转化率为_______。该反应的平衡常数 _______kPa(用平衡分压代替平衡浓度,分
压=总压×物质的量分数)
(4)将一定浓度的 与固定浓度的 通过含催化剂的恒容反应器发生脱氢反应:
,经相同时间,流出的 、 和 随初始 的变
化关系如图。结合化学方程式解释 和 变化差异的原因。_______
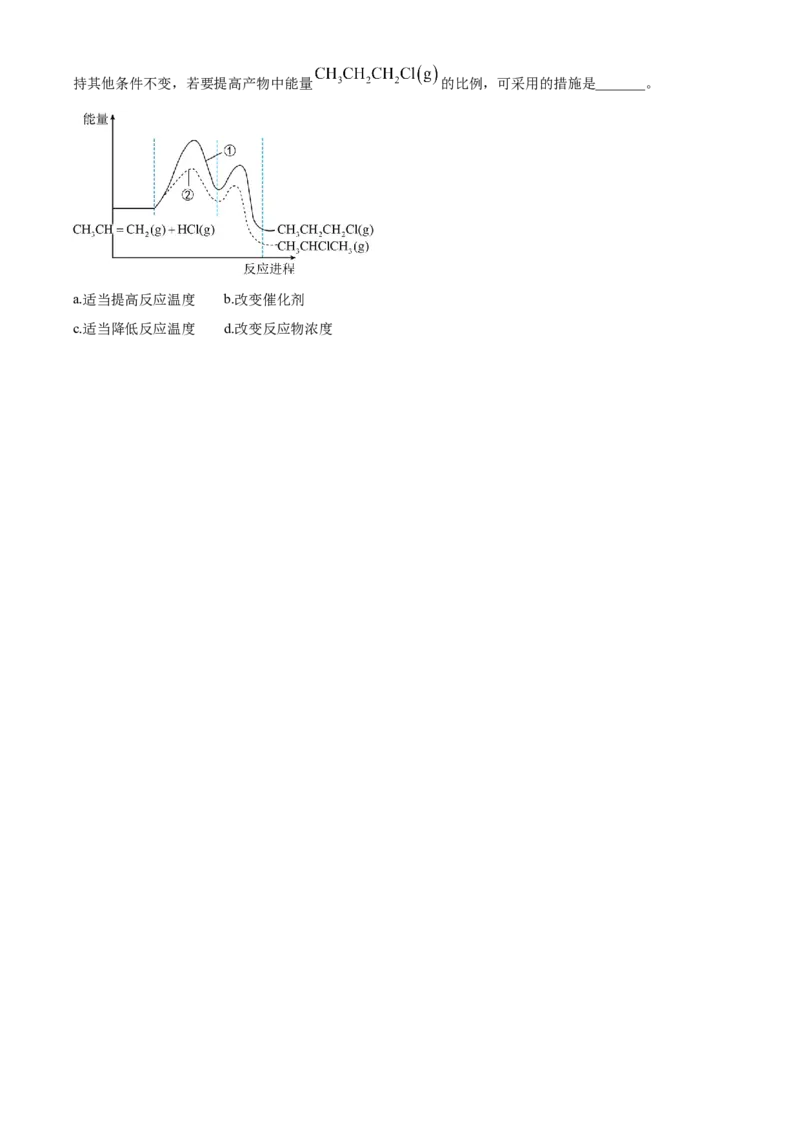
(5)一定条件下, 与HCl发生反应有①、②两种可能,反应进程中的能量变化如图。保持其他条件不变,若要提高产物中能量 的比例,可采用的措施是_______。
a.适当提高反应温度 b.改变催化剂
c.适当降低反应温度 d.改变反应物浓度上海市金山区 2022-2023 学年高三上学期第一次质量调研
化学试题
式量:Fe—56; —232; —233; —197; —217
一、选择题(共40分,每小题2分。每小题只有一个正确答案)
【1题答案】
【答案】A
【2题答案】
【答案】A
【3题答案】
【答案】D
【4题答案】
【答案】D
【5题答案】
【答案】A
【6题答案】
【答案】B
【7题答案】
【答案】A
【8题答案】
【答案】C
【9题答案】
【答案】B
【10题答案】
【答案】B
【11题答案】
【答案】B
【12题答案】
【答案】C
【13题答案】
【答案】B【14题答案】
【答案】D
【15题答案】
【答案】D
【16题答案】
【答案】D
【17题答案】
【答案】C
【18题答案】
【答案】AC
【19题答案】
【答案】C
【20题答案】
【答案】D
二、综合题(共60分)
(一)(本题共15分)
【21题答案】
【答案】(1) ①. ②. 取少量反应后溶液加入
KSCN溶液,溶液不变色,再加入新制氯水,溶液没有变红色,说明反应已经完全
(2) ①. 铁容易被空气中氧气氧化 ②.
(3)分子晶体 (4) ①. 3.42×10-11 ②. 溶液中加入 溶液,氢氧根离子浓度增大,平
衡向生成氢氧化铁沉淀的方向移动
(二)(本题共15分)
【22题答案】
【答案】(1)取代反应、还原反应
(2) ①. ②. CH=CH
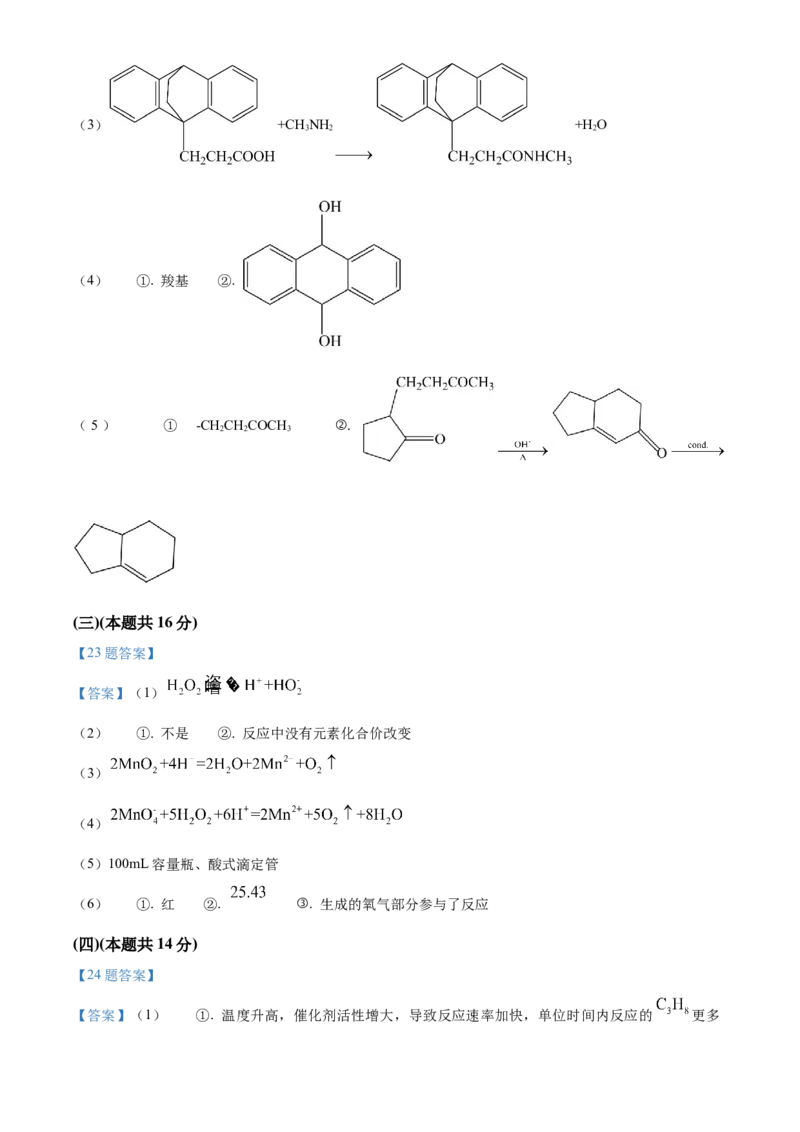
2 2(3) +CH NH +H O
3 2 2
(4) ①. 羧基 ②.
(5) ① -CHCHCOCH ②.
2 2 3
.
(三)(本题共16分)
【23题答案】
【答案】(1)
(2) ①. 不是 ②. 反应中没有元素化合价改变
(3)
(4)
(5)100mL容量瓶、酸式滴定管
(6) ①. 红 ②. ③. 生成的氧气部分参与了反应
(四)(本题共14分)
【24题答案】
【答案】(1) ①. 温度升高,催化剂活性增大,导致反应速率加快,单位时间内反应的 更多②. 适当降低反应温度
(2)a-b (3) ①. 40% ②.
(4)高温下二氧化碳会和氢气发生反应生成一氧化碳,且消耗氢气等于生成的一氧化碳:
,导致 、 的变化幅度出现差异
(5)ab