文档内容
特色练 6 “位、构、性”推断
1.原子序数依次增大的X、Y、Z、W四种元素形成化合物Z[W(XY) ],其中X、Y、Z为
3 6
主族元素。X最外层电子数是内层电子数的两倍,Y的简单气态氢化物能使酚酞溶液变红,
W3+的3d轨道电子数为半满。下列说法正确的是( )
A.Z和W一定位于同周期
B.原子半径:Z>X>Y
C.四种元素基态原子中未成对电子数最多的是Y
D.该化合物属于配合物,其内界σ键与π键的数目之比为1∶2
答案 B
解析 X最外层电子数是内层电子数的两倍,X是C元素,Y的简单气态氢化物能使酚酞溶
液变红,Y是N元素;W3+的3d轨道电子数为半满,W是Fe元素;Z显+1价,X、Y、
Z、W原子序数依次增大,Z是Na或K元素。Z是Na或K元素,W是Fe元素,不一定位
于同周期,故A错误;电子层数越多半径越大,电子层数相同,质子数越多半径越小,原
子半径:K>C>N,Na>C>N,故B正确;Fe原子中有4个未成对电子,C原子中有2个未成
对电子,N原子中有3个未成对电子,Na或K原子中都只有1个未成对电子,四种元素基
态原子中未成对电子数最多的是Fe,故C错误;该化合物属于配合物,其内界有6个配位
键、6个C≡N,配位键是σ键,三键中有1个σ键、2个π键,σ键与π键的数目之比为
1∶1,故D错误。
2.五种短周期元素X、Y、Z、W、M的原子序数依次增大且位于不同的主族,Y的最外层
电子数是次外层的2倍,M的原子序数等于Y和W的原子序数之和,只有Y、Z、W同周
期。下列说法错误的是( )
A.简单离子半径:Z>W
B.X、Y、W三种元素可形成多种化合物
C.M的最高价氧化物对应的水化物为强酸
D.Y、Z、W均可与X形成电子数相等的分子
答案 C
解析 五种短周期元素X、Y、Z、W、M的原子序数依次增大,Y的最外层电子数是次外
层的2倍,Y为C;只有Y、Z、W同周期,W为O或F,又所有元素不同主族,M的原子
序数等于Y和W的原子序数之和,故X为H、Y为C、Z为O、W为F、M为P,以此来解
答。具有相同电子排布的离子中原子序数大的离子半径小,则简单离子半径:r(O2-)>r(F
-),即Z>W,A项正确;X、Y、W三种元素可形成多种化合物,如氟代烃,B项正确;M
的最高价氧化物对应的水化物为磷酸,不属于强酸,C项错误;Y、Z、W均可与X形成电子数相等的分子,如甲烷、水、HF,均含10个电子,D项正确。
3.X、Y、Z、R、W为原子序数依次增大的短周期元素,Z、W为同族元素,R是短周期中
原子半径最大的主族元素。其中,X、Y、Z、W形成的化合物可表示为[YX ]+[XWZ ]-。下
4 4
列说法不正确的是( )
A.R与X、Y、Z、W均可形成离子化合物
B.简单气态氢化物的稳定性:Z>Y
C.X、Y、Z三种元素形成物质的水溶液只能呈酸性
D.[YX ]+为正四面体结构
4
答案 C
解析 R是短周期中原子半径最大的主族元素,R为Na;X、Y、Z、W形成的化合物可表
示为[YX ]+[XWZ ]-,由[YX ]+可知Y为N,X为H,Z、W为同族元素且能形成[XWZ ]
4 4 4 4
-,故Z为O,W为S。Na形成化合物时均失电子,和H、N、O、S均形成离子化合物,A
正确;Z、Y的简单氢化物为HO和NH ,O的非金属性大于N,故稳定性:HO>NH ,B
2 3 2 3
正确;H、N、O可形成一水合氨,水溶液显碱性,C错误;铵根离子的空间结构为正四面
体,D正确。
4.W、X、Y、Z是原子序数依次增大的短周期主族元素,其中 X和Z同主族,由W、X、
Y、Z形成的锂盐结构如图所示,下列说法正确的是( )
A.原子半径:W>X>Y>Z
B.最简单氢化物的稳定性:X<Y
C.Z的单质在过量X 中燃烧生成ZX
2 3
D.该锂盐所有原子最外层均满足8电子稳定结构
答案 B
解析 W、X、Y、Z是原子序数依次增大的短周期主族元素,由W、X、Y、Z形成的锂盐
结构所示,X、Z同主族,X可形成Z==X,Z有6条共价键,则二者位于第ⅥA族,则X
为O元素,Z是S元素;W形成4条共价键,Y形成一条共价键,则W为C元素,Y为F
元素,以此分析解答。W、X、Y、Z分别为C、O、F、S,原子半径:Z>W>X>Y,A项
错误;X、Y最简单氢化物分别为HO、HF,由于非金属性:F>O,稳定性:X<Y,B项正
2
确;Z为S,X为O,Z的单质在过量X 中燃烧生成SO ,C项错误;该锂盐中C、O、F、S
2 2
的最外层均有8个电子,而Li+最外层只有2个电子,D项错误。
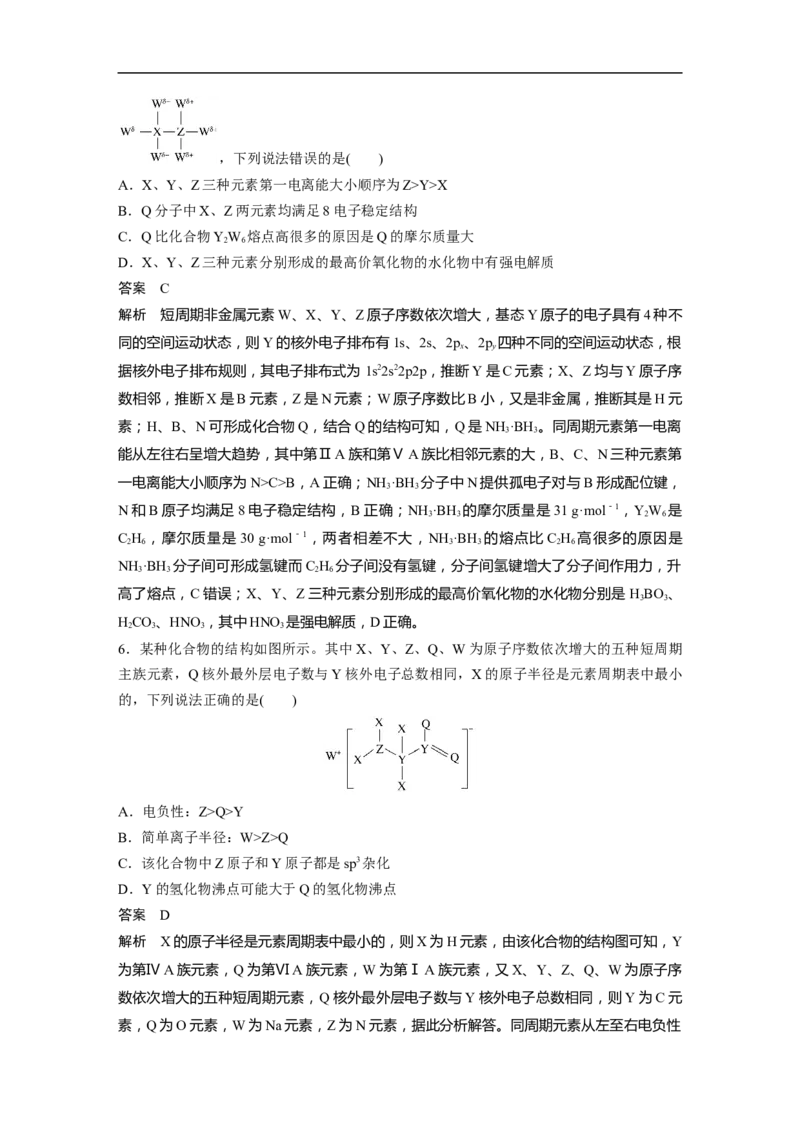
5.短周期非金属元素W、X、Y、Z原子序数依次增大,其中基态Y原子的电子具有4种不
同的空间运动状态,X、Z 均与 Y 原子序数相邻。W、X、Z 可形成化合物 Q:,下列说法错误的是( )
A.X、Y、Z三种元素第一电离能大小顺序为Z>Y>X
B.Q分子中X、Z两元素均满足8电子稳定结构
C.Q比化合物YW 熔点高很多的原因是Q的摩尔质量大
2 6
D.X、Y、Z三种元素分别形成的最高价氧化物的水化物中有强电解质
答案 C
解析 短周期非金属元素W、X、Y、Z原子序数依次增大,基态Y原子的电子具有4种不
同的空间运动状态,则Y的核外电子排布有1s、2s、2p、2p 四种不同的空间运动状态,根
x y
据核外电子排布规则,其电子排布式为 1s22s22p2p,推断Y是C元素;X、Z均与Y原子序
数相邻,推断X是B元素,Z是N元素;W原子序数比B小,又是非金属,推断其是H元
素;H、B、N可形成化合物Q,结合Q的结构可知,Q是NH ·BH 。同周期元素第一电离
3 3
能从左往右呈增大趋势,其中第ⅡA族和第ⅤA族比相邻元素的大,B、C、N三种元素第
一电离能大小顺序为N>C>B,A正确;NH ·BH 分子中N提供孤电子对与B形成配位键,
3 3
N和B原子均满足8电子稳定结构,B正确;NH ·BH 的摩尔质量是31 g·mol-1,YW 是
3 3 2 6
C H ,摩尔质量是30 g·mol-1,两者相差不大,NH ·BH 的熔点比C H 高很多的原因是
2 6 3 3 2 6
NH ·BH 分子间可形成氢键而C H 分子间没有氢键,分子间氢键增大了分子间作用力,升
3 3 2 6
高了熔点,C错误;X、Y、Z三种元素分别形成的最高价氧化物的水化物分别是 HBO 、
3 3
HCO、HNO,其中HNO 是强电解质,D正确。
2 3 3 3
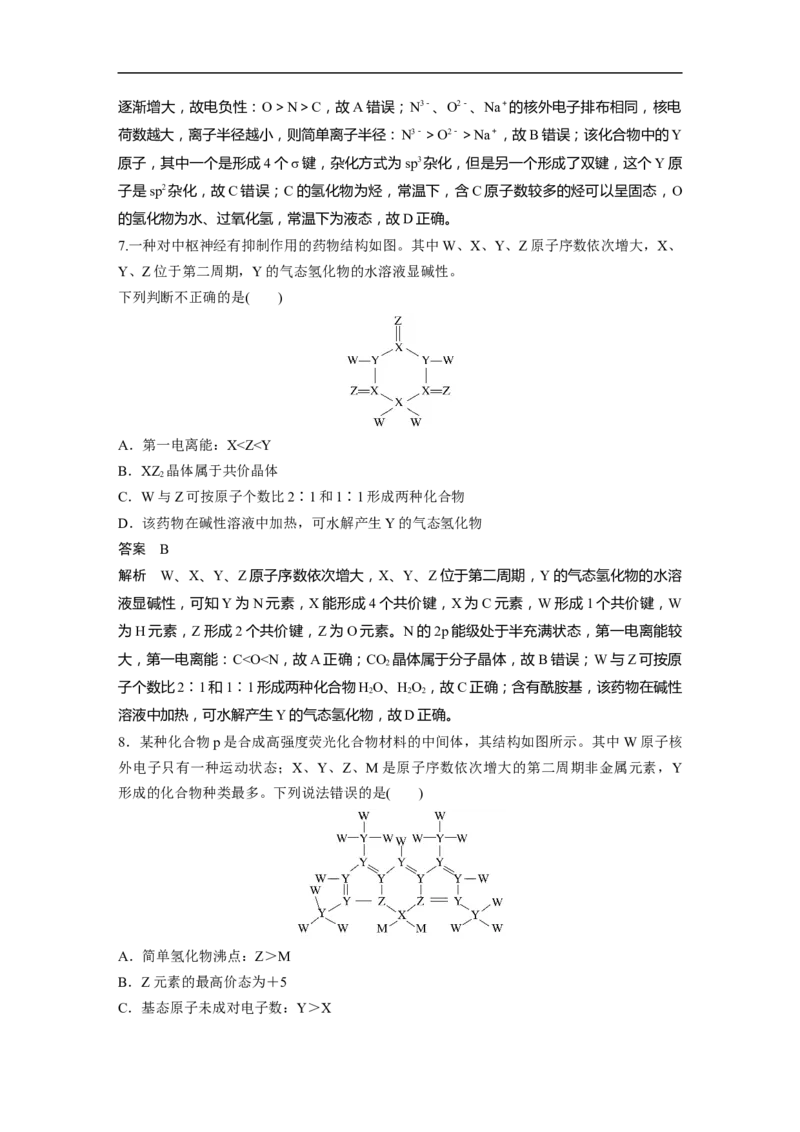
6.某种化合物的结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期
主族元素,Q核外最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小
的,下列说法正确的是( )
A.电负性:Z>Q>Y
B.简单离子半径:W>Z>Q
C.该化合物中Z原子和Y原子都是sp3杂化
D.Y的氢化物沸点可能大于Q的氢化物沸点
答案 D
解析 X的原子半径是元素周期表中最小的,则X为H元素,由该化合物的结构图可知,Y
为第ⅣA族元素,Q为第ⅥA族元素,W为第ⅠA族元素,又X、Y、Z、Q、W为原子序
数依次增大的五种短周期元素,Q核外最外层电子数与Y核外电子总数相同,则Y为C元
素,Q为O元素,W为Na元素,Z为N元素,据此分析解答。同周期元素从左至右电负性逐渐增大,故电负性:O>N>C,故A错误;N3-、O2-、Na+的核外电子排布相同,核电
荷数越大,离子半径越小,则简单离子半径:N3->O2->Na+,故B错误;该化合物中的Y
原子,其中一个是形成4个σ键,杂化方式为sp3杂化,但是另一个形成了双键,这个Y原
子是sp2杂化,故C错误;C的氢化物为烃,常温下,含C原子数较多的烃可以呈固态,O
的氢化物为水、过氧化氢,常温下为液态,故D正确。
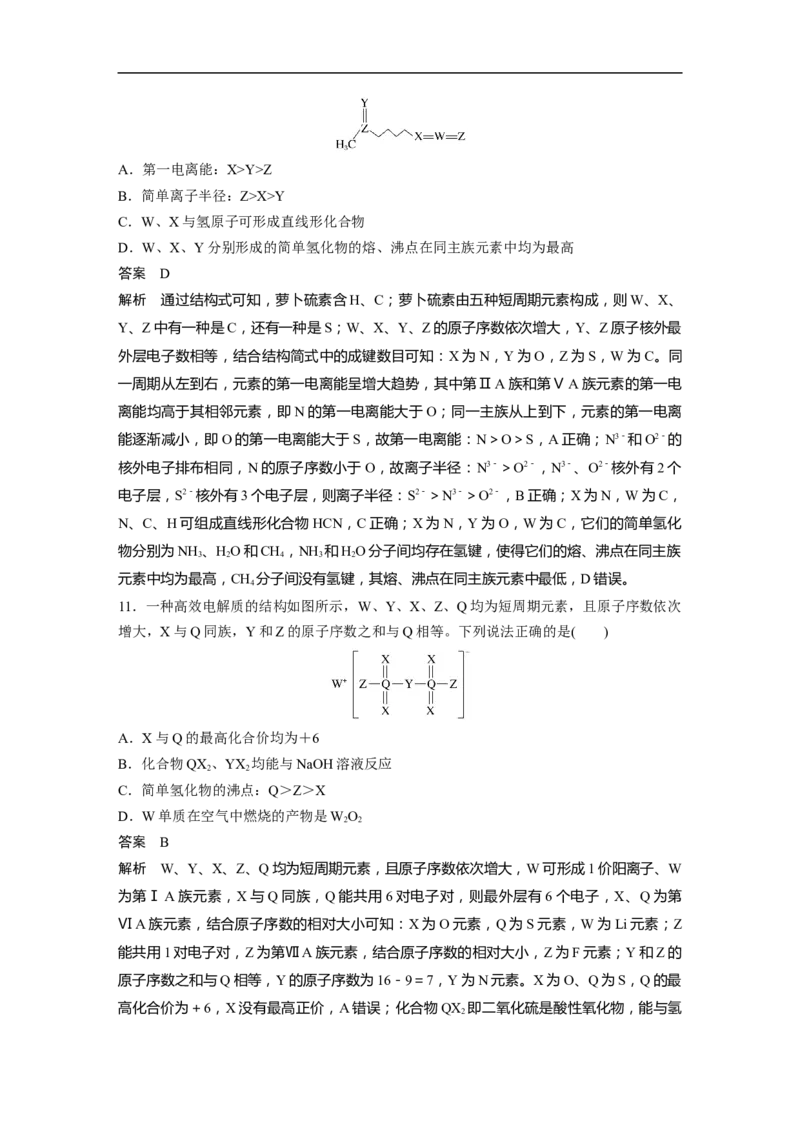
7.一种对中枢神经有抑制作用的药物结构如图。其中W、X、Y、Z原子序数依次增大,X、
Y、Z位于第二周期,Y的气态氢化物的水溶液显碱性。
下列判断不正确的是( )
A.第一电离能:XW>Z>Y
D.最简单氢化物的沸点:X>W>Z
答案 A
解析 W的最简单氢化物的水溶液呈碱性,可知W为N元素;Z的最外层电子数为内层电
子总数的两倍,可知Z为C元素;Y与其他元素不在同一周期且短周期元素Z、W、X、Y
的原子半径逐渐减小,可知Y为H元素;从图中可知,X共用两对电子达到稳定结构,可
知X为O元素,据此分析解题。同周期元素的第一电离能从左往右呈增大趋势,但由于 N
原子的2p轨道是半充满状态,较稳定,所以第一电离能:N>O>C;同时由于H的原子半径
比C小得多,核外电子受到原子核的引力大,电离需要消耗更多的能量,因此第一电离能:
H>C,所以四种元素中C的第一电离能最小,故A项错误;仅由W和X形成的化合物有
NO、NO、NO 、NO 、NO 等,不止四种,故B项正确;X的最简单氢化物为HO,W
2 2 2 4 2 5 2
的最简单氢化物为NH ,Z的最简单氢化物为CH ,由于HO和NH 分子间存在氢键,且
3 4 2 3
HO分子间氢键强度大于NH 分子,所以最简单氢化物的沸点:HO>NH >CH ,故D项正
2 3 2 3 4
确。
10.萝卜硫素是具有美容效果的天然产物,其结构如图所示,该物质由五种短周期元素构成,
其中W、X、Y、Z的原子序数依次增大,Y、Z原子核外最外层电子数相等,下列说法错误
的是( )A.第一电离能:X>Y>Z
B.简单离子半径:Z>X>Y
C.W、X与氢原子可形成直线形化合物
D.W、X、Y分别形成的简单氢化物的熔、沸点在同主族元素中均为最高
答案 D
解析 通过结构式可知,萝卜硫素含H、C;萝卜硫素由五种短周期元素构成,则W、X、
Y、Z中有一种是C,还有一种是S;W、X、Y、Z的原子序数依次增大,Y、Z原子核外最
外层电子数相等,结合结构简式中的成键数目可知:X为N,Y为O,Z为S,W为C。同
一周期从左到右,元素的第一电离能呈增大趋势,其中第ⅡA族和第ⅤA族元素的第一电
离能均高于其相邻元素,即N的第一电离能大于O;同一主族从上到下,元素的第一电离
能逐渐减小,即O的第一电离能大于S,故第一电离能:N>O>S,A正确;N3-和O2-的
核外电子排布相同,N的原子序数小于O,故离子半径:N3->O2-,N3-、O2-核外有2个
电子层,S2-核外有3个电子层,则离子半径:S2->N3->O2-,B正确;X为N,W为C,
N、C、H可组成直线形化合物HCN,C正确;X为N,Y为O,W为C,它们的简单氢化
物分别为NH 、HO和CH ,NH 和HO分子间均存在氢键,使得它们的熔、沸点在同主族
3 2 4 3 2
元素中均为最高,CH 分子间没有氢键,其熔、沸点在同主族元素中最低,D错误。
4
11.一种高效电解质的结构如图所示,W、Y、X、Z、Q均为短周期元素,且原子序数依次
增大,X与Q同族,Y和Z的原子序数之和与Q相等。下列说法正确的是( )
A.X与Q的最高化合价均为+6
B.化合物QX 、YX 均能与NaOH溶液反应
2 2
C.简单氢化物的沸点:Q>Z>X
D.W单质在空气中燃烧的产物是WO
2 2
答案 B
解析 W、Y、X、Z、Q均为短周期元素,且原子序数依次增大,W可形成1价阳离子、W
为第ⅠA族元素,X与Q同族,Q能共用6对电子对,则最外层有6个电子,X、Q为第
ⅥA族元素,结合原子序数的相对大小可知:X为O元素,Q为S元素,W为Li元素;Z
能共用1对电子对,Z为第ⅦA族元素,结合原子序数的相对大小,Z为F元素;Y和Z的
原子序数之和与Q相等,Y的原子序数为16-9=7,Y为N元素。X为O、Q为S,Q的最
高化合价为+6,X没有最高正价,A错误;化合物QX 即二氧化硫是酸性氧化物,能与氢
2氧化钠溶液反应,YX 为二氧化氮,能和氢氧化钠溶液反应生成硝酸钠、亚硝酸钠和水,B
2
正确;X为O、Z为F、Q为S,简单氢化物分别为HO、HF、HS,水和氟化氢分子之间都
2 2
有氢键,水分子间的氢键数大于氟化氢分子间的氢键数,硫化氢分子间只存在分子间作用力,
因此,沸点:X>Z>Q,C错误;W单质(Li)在空气中燃烧的产物是WO(Li O),D错误。
2 2