文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题09
1.下列离子方程式正确的是
A. 向CuSO 溶液中加入过量氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
4 3 2 2
B. 向Fe(NO ) 溶液中加入过量的HI溶液:2NO ++6I-=3I+2NO↑+4HO
3 3 +8H 2 2
C. NaHSO 溶液与Ba(OH) 溶液混合后呈中性:2H++SO+Ba2++2OH-=BaSO↓+2H O
4 2 4 2
D NaOH溶液与过量HC O 溶液反应:HC O+2OH-=C O+2HO
2 2 4 2 2 4 2 2
答案:C
解析:A.向CuSO 溶液中加入过量氨水:Cu2++4NH·H O=[Cu(NH )]2++ 4H O,故A错误;
4 3 2 3 4 2
B.向Fe(NO ) 溶液中加入过量的HI溶液:Fe3++3NO ++10I-=Fe2++5I +3NO↑+6HO,故B错
3 3 +12H 2 2
误;
C.NaHSO 溶液与Ba(OH) 溶液混合后呈中性,则氢离子与氢氧根离子恰好完全反应,反应离
4 2
子方程式为:2H++SO+Ba2++2OH-=BaSO↓+2H O,故C正确;
4 2
D.NaOH溶液与过量HC O 溶液反应:HC O+OH-=HC O+H O,故D错误;
2 2 4 2 2 4 2 2
2.化学与生活、科技、社会发展息息相关。下列说法正确的是
A.“天宫”空间站使用聚乳酸材料餐具,聚乳酸是化合物
B.富勒烯与石墨烯用途广泛,它们都属于新型无机非金属材料
C. 冬奥场馆建筑使用碲化镉发电玻璃,碲和镉均属于主族元素
D. 中国承建的卡塔尔首座光伏电站中的光伏材料为高纯度二氧化硅
答案:B
解析:A.聚乳酸是混合物,故A错误;
B.富勒烯与石墨烯属于新型无机非金属材料,故B正确;
C.镉为在元素周期表中位置为第五周期ⅡB族,故C错误;
D.光伏电池为Si单质,故D错误;
3.能正确表示下列反应的离子方程式的是
A. 用K[Fe(CN) ]溶液检验Fe2+:Fe2++K++[Fe(CN)]3-=KFe[Fe(CN) ]↓
3 6 6 6
B. 向二元弱酸亚磷酸(H PO )溶液中滴加足量的烧碱溶液:HPO +3OH-=PO O
3 3 3 3 +3H2
C. 用惰性电极电解氯化镁溶液:2Cl-+2H O=====Cl↑+H ↑+2OH-
2 2 2
D. 海水提溴工艺中用二氧化硫还原溴:SO +Br +2H O=2H++SO+2HBr
2 2 2
答案:A
解析:A.用K[Fe(CN) ]溶液检验Fe2+,离子方程式为Fe2++K++[Fe(CN)]3-=KFe[Fe(CN) ]↓,故
3 6 6 6
A正确;
B.向二元弱酸亚磷酸(H PO )溶液中滴加足量的烧碱溶液,离子方程式为HPO +2OH-=
3 3 3 3
HPO O,故B错误;
+2H2
C.用惰性电极电解氯化镁溶液,离子方程式为Mg2++2Cl-+2H O=====Cl↑+H ↑+2Mg(OH) ↓,
2 2 2 2
故C错误;D.海水提溴工艺中用二氧化硫还原溴,离子方程式为SO +Br +2H O=4H++SO+2Br-,故D错
2 2 2
误;
4.下列叙述不涉及氧化还原反应的是
A. 海水提溴 B. 苏打用作食用碱
C. 谷物发酵酿酒 D. 漂白粉久置空气中失效
答案:B
解析:A.海水提溴,是将化合态的溴转化为溴单质再分离出来的过程,涉及氧化还原反应,
故A错误;
B.苏打用作食用碱,是碳酸钠和酸反应的过程,其属于复分解反应,因而不涉及氧化还原反
应,故B正确;
C.谷物发酵酿造食醋的过程为:淀粉水解生成葡萄糖,葡萄糖在酶的作用下生成乙醇,乙醇
氧化生成醋酸的过程,涉及氧化还原反应,故C错误;
D.漂白粉久置与空气中时次氯酸钙与水、二氧化碳反应生成碳酸钙和次氯酸,次氯酸易分解,
分解后生成盐酸和氧气,从而变质,其过程中涉及氧化还原反应,故D错误;
5.下列消毒剂的有效成分属于盐的是
A. 高锰酸钾溶液 B. 过氧乙酸溶液 C. 双氧水 D. 医用酒精
答案:A
解析:A.高锰酸钾溶液的有效成分为KMnO ,其在水溶液中电离出K+和MnO KMnO 属于
4 ,故 4
盐,A符合题意;
B.过氧乙酸溶液的有效成分是CHCOOOH,在水溶液中电离出CHCOOO-和H+,即水溶液
3 3
中的阳离子全部为H+,故其属于酸,不合题意;
C.双氧水是由H和O组成的化合物,故其属于氧化物,C不合题意;
D.医用酒精的有效成分为CHCHOH,其属于有机物,不属于盐,D不合题意;
3 2
6.下列物质属于纯净物的是
A. 漂白粉 B. 氯水 C. 柴油 D. 冰醋酸
答案:D
解析:A.漂白粉是氯化钙和次氯酸钙的混合物,A不符合题意;
B.氯水是氯气溶于水的混合物,其中有水、氯气、次氯酸、盐酸,B不符合题意;
C.柴油是轻质石油,复杂烃类混合物,C不符合题意;
D.冰醋酸就是乙酸,属于纯净物,D符合题意;
7.下列物质属于电解质,且熔融状态下能导电的是
A. Cu B. HCl C. KNO D. 葡萄糖(C H O)
3 6 12 6
答案:C
解析:在水溶液或熔融状态能电离出自由移动的离子的化合物属于电解质,Cu是单质不属于
电解质;HCl在熔融状态不能电离出自由移动的离子;KNO 是盐在熔融状态可以电离出钾离子和
3
硝酸根离子,在熔融状态可以导电;葡萄糖(C H O)是非电解质,故答案为C;
6 12 68.下列表示不正确的是
A. 氯化钠的电子式: B. 二氧化碳的结构式:O=C=O
C. 乙烷分子的空间填充模型: D. 1,3-丁二烯的键线式:
答案:A
解析:A.氯化钠为离子化合物,钠离子用离子符号表示,氯离子需要标出最外层电子及所带
电荷,氯化钠正确的电子式为 ,故A错误;
B.二氧化碳为共价化合物,碳原子与两个氧原子各共用两对电子,用短线表示共用电子对即
为结构式,二氧化碳的结构式为O=C=O,故B正确;
C.乙烷的结构简式为CHCH,原子半径C>H,其空间填充模型为 ,故C正确;
3 3
D.键线式用短线表示化学键,交点、端点表示碳原子,一般C、H原子不标出,则1,3-丁二
烯的键线式应为: ,故D正确;
9.关于反应2NaNO +2KI+2H SO =2NO↑+I +Na SO +K SO +2HO,下列说法正确的是
2 2 4 2 2 4 2 4 2
A. KI发生还原反应
B. HSO 既不是氧化剂,也不是还原剂
2 4
C. 氧化产物与还原产物的物质的量之比为2:1
D. 消耗0.5molNaNO 时,转移1.0mol电子
2
答案:B
解析:A.该反应中,KI中的I失电子化合价升高,发生氧化反应,A错误;
B.反应中HSO 中的元素化合价既不升高也不降低,故HSO 既不是氧化剂也不是还原剂,B
2 4 2 4
正确;
C.NaNO 中N得电子化合价降低,NO为还原产物,KI中I失电子化合价升高,I 为氧化产物,
2 2
则氧化产物和还原产物的物质的量之比为1:2,C错误;
D.反应中NaNO 中N得电子化合价从+3价降低为+2价,则消耗0.5molNaNO 转移0.5mol电
2 2
子,D错误;
10.下列反应对应的方程式不正确的是
A. 大理石与醋酸反应:CaCO +2CH COOH=Ca2++2CH COO−+H O+CO↑
3 3 3 2 2
B. 铜的电解精炼的总反应(粗铜作阳极,纯铜作阴极,硫酸铜溶液作电解液):Cu(阳
极)=====Cu(阴极)
C. 钠与水反应生成气体:2Na+2HO=2NaOH+H ↑
2 2
D. 向Mg(HCO ) 溶液中加入过量NaOH溶液的反应:Mg2++2HCO−
3 2 3+4OH−=Mg(OH) ↓+2CO 2−+2HO
2 3 2
答案:B
解析:A.大理石与醋酸反应生成醋酸钙、水和二氧化碳,大理石是难溶物质,醋酸是弱酸,
书写时不拆,离子方程式书写正确,故A正确;
B.粗铜电解精炼(粗铜作阳极,纯铜作阴极,硫酸铜溶液作电解液)时,阳极上溶解的金属除
Cu外,还有Zn、Fe等活泼性比Cu强的金属,阴极上只有Cu2+得到电子变为Cu单质,故B错误;
C.钠与水反应生成氢氧化钠和氢气,化学方程式为2Na+2HO=2NaOH+H ↑,故C正确;
2 2
D.氢氧化镁比碳酸镁更难溶,Mg(HCO ) 溶液中加入过量NaOH溶液的反应生成氢氧化镁沉
3 2
淀和碳酸钠、水,反应的离子方程式为Mg2++2HCO−+4OH−=Mg(OH) ↓+2CO 2−+2H O,故D正确;
3 2 3 2
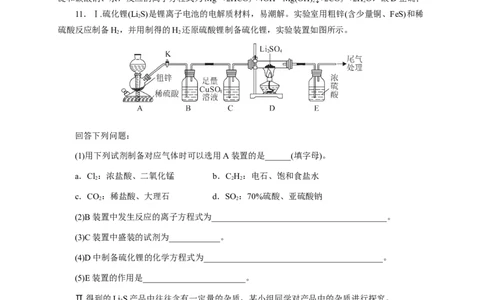
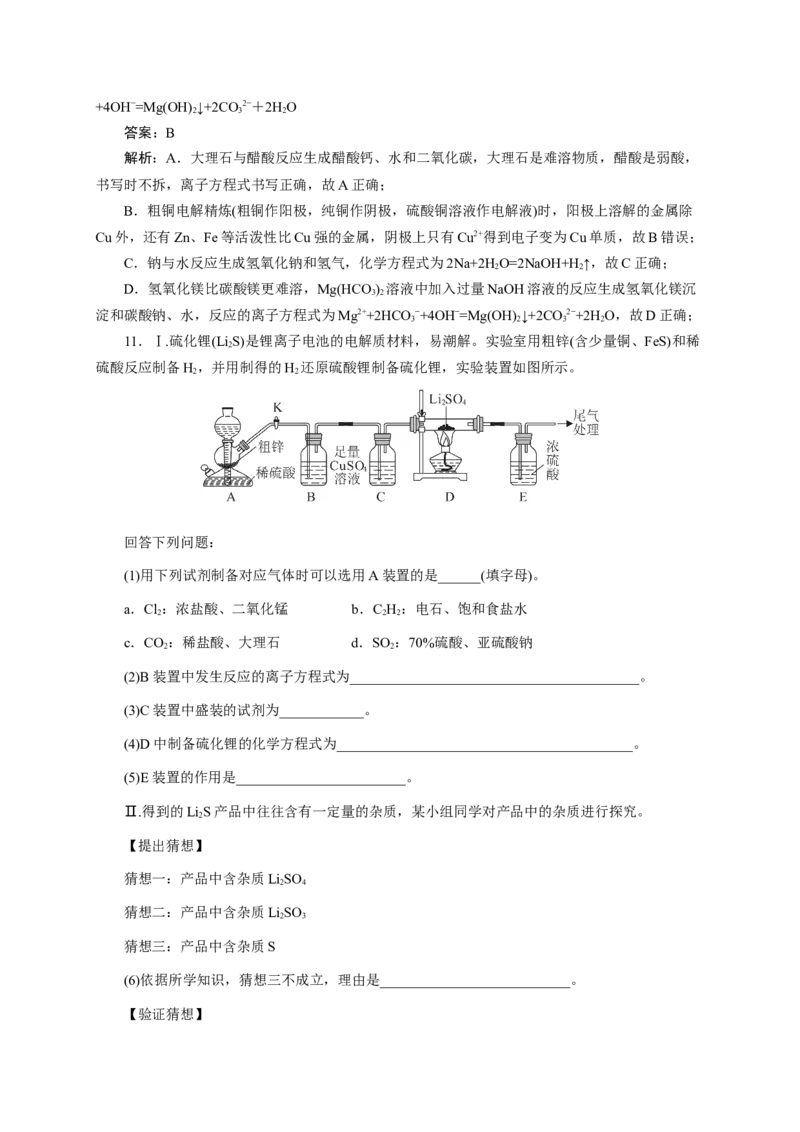
11.Ⅰ.硫化锂(Li S)是锂离子电池的电解质材料,易潮解。实验室用粗锌(含少量铜、FeS)和稀
2
硫酸反应制备H,并用制得的H 还原硫酸锂制备硫化锂,实验装置如图所示。
2 2
回答下列问题:
(1)用下列试剂制备对应气体时可以选用A装置的是______(填字母)。
a.Cl:浓盐酸、二氧化锰 b.C H:电石、饱和食盐水
2 2 2
c.CO:稀盐酸、大理石 d.SO :70%硫酸、亚硫酸钠
2 2
(2)B装置中发生反应的离子方程式为_________________________________________。
(3)C装置中盛装的试剂为____________。
(4)D中制备硫化锂的化学方程式为__________________________________________。
(5)E装置的作用是________________________。
Ⅱ.得到的LiS产品中往往含有一定量的杂质,某小组同学对产品中的杂质进行探究。
2
【提出猜想】
猜想一:产品中含杂质LiSO
2 4
猜想二:产品中含杂质LiSO
2 3
猜想三:产品中含杂质S
(6)依据所学知识,猜想三不成立,理由是___________________________。
【验证猜想】(7)完成表格:
限选试剂:稀盐酸、稀硫酸、蒸馏水、双氧水、氯化钡溶液、硝酸钡溶液
实验 操作与现象 结论
Ⅰ 取少量LiS样品溶于水,______ 样品中不含LiSO
2 2 3
Ⅱ 在实验Ⅰ反应后的溶液中,______ 样品中含LiSO
2 4
答案:(1)c (2)Cu2++HS=CuS↓+2H+ (3)浓硫酸
2
(4) LiSO +4H===LiS+4HO (5)排除空气中水蒸气干扰
2 4 2 2 2
(6)硫单质和氢气加热会生成硫化氢,且硫受热会生成硫蒸气随气流流走
(7)加入适量的稀盐酸,生成气体通入品红溶液中,溶液不褪色 滴加盐酸酸化的氯化
钡溶液,生成白色沉淀
解析:A装置中生成二氧化硫气体,通过B装置除去杂质气体,通过C干燥后进入D装置反应
生成LiS,装置E排除空气中水蒸气干扰,尾气吸收处理。
2
(1)A装置为固液不加热反应,且固体需要为块状固体,电石遇水变成糊状,故选c;
(2)A中生成的杂质气体硫化氢和硫酸铜反应生成硫化铜沉淀,反应为Cu2++HS=CuS↓+
2
2H+;
(3)硫化锂易潮解,故生成的氢气需要干燥后进入D装置进行反应,故C装置中盛装的试剂为
浓硫酸干燥剂;
D装置中H 还原硫酸锂制备硫化锂,根据质量守恒可知,还会生成水,反应为LiSO +
2 2 4
4H===LiS+4HO;
2 2 2
(5)硫化锂易潮解,E装置盛有浓硫酸防止空气中水蒸气进入装置D;
(6)硫单质和氢气加热会生成硫化氢,且硫受热会生成硫蒸气随气流流走;故猜想三错误;
(7)亚硫酸根离子会和酸生成具有漂白性的二氧化硫气体,故操作为:取少量LiS样品溶于水,
2
加入适量的稀盐酸,生成气体通入品红溶液中,溶液不褪色,说明不含LiSO ;
2 3
硫酸根离子会和钡离子生成不溶于酸的硫酸钡沉淀,故操作为:在实验Ⅰ反应后的溶液中,滴加盐
酸酸化的氯化钡溶液,生成白色沉淀,说明样品中含LiSO 。
2 4
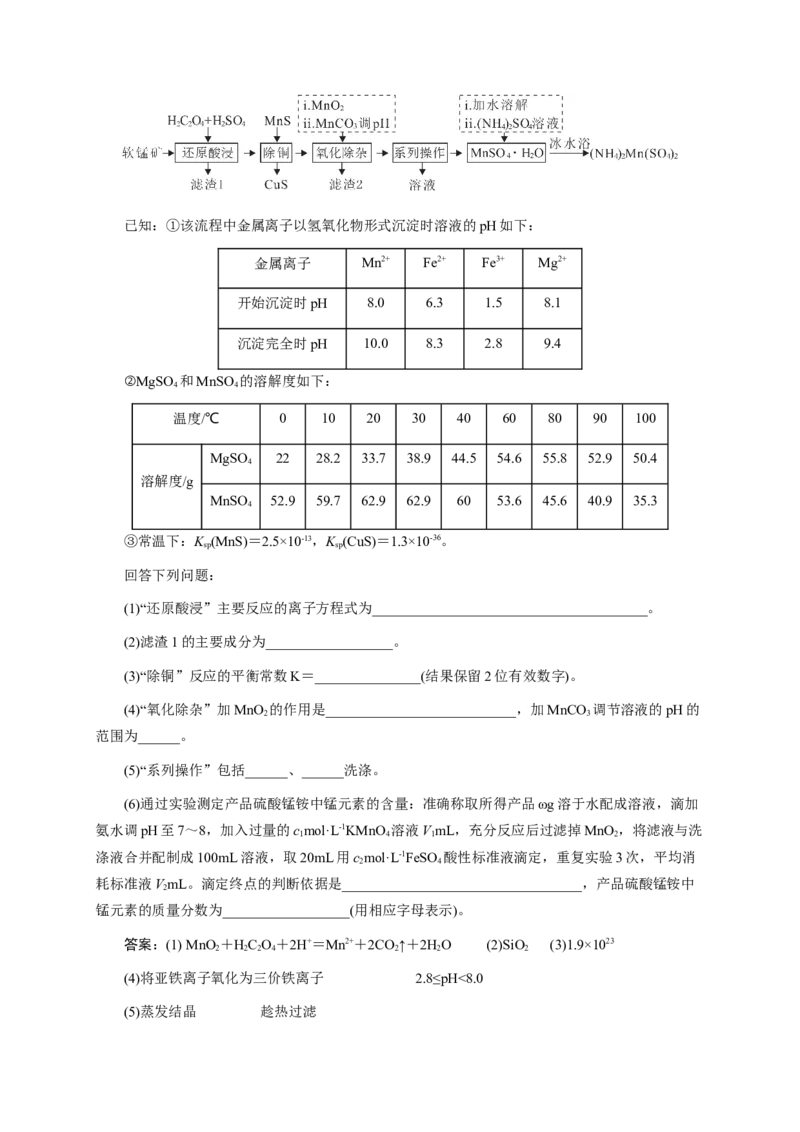
12.硫酸锰铵[(NH )Mn(SO )]是一种浅粉色固体,可溶于水,工业上可用于加工木材防火剂。
4 2 4 2
用软锰矿(主要含MnO ,还含有FeO、Fe O、CuO、MgO、SiO 等)制备硫酸锰铵的工艺流程如下:
2 2 3 2已知:①该流程中金属离子以氢氧化物形式沉淀时溶液的pH如下:
金属离子 Mn2+ Fe2+ Fe3+ Mg2+
开始沉淀时pH 8.0 6.3 1.5 8.1
沉淀完全时pH 10.0 8.3 2.8 9.4
②MgSO 和MnSO 的溶解度如下:
4 4
温度/℃ 0 10 20 30 40 60 80 90 100
MgSO 22 28.2 33.7 38.9 44.5 54.6 55.8 52.9 50.4
4
溶解度/g
MnSO 52.9 59.7 62.9 62.9 60 53.6 45.6 40.9 35.3
4
③常温下:K (MnS)=2.5×10-13,K (CuS)=1.3×10-36。
sp sp
回答下列问题:
(1)“还原酸浸”主要反应的离子方程式为_______________________________________。
(2)滤渣1的主要成分为__________________。
(3)“除铜”反应的平衡常数K=_______________(结果保留2位有效数字)。
(4)“氧化除杂”加MnO 的作用是___________________________,加MnCO 调节溶液的pH的
2 3
范围为______。
(5)“系列操作”包括______、______洗涤。
(6)通过实验测定产品硫酸锰铵中锰元素的含量:准确称取所得产品ωg溶于水配成溶液,滴加
氨水调pH至7~8,加入过量的cmol·L-1KMnO 溶液VmL,充分反应后过滤掉MnO ,将滤液与洗
1 4 1 2
涤液合并配制成100mL溶液,取20mL用cmol·L-1FeSO 酸性标准液滴定,重复实验3次,平均消
2 4
耗标准液VmL。滴定终点的判断依据是__________________________________,产品硫酸锰铵中
2
锰元素的质量分数为__________________(用相应字母表示)。
答案:(1) MnO+HC O+2H+=Mn2++2CO↑+2HO (2)SiO (3)1.9×1023
2 2 2 4 2 2 2
(4)将亚铁离子氧化为三价铁离子 2.8≤pH<8.0
(5)蒸发结晶 趁热过滤(6)溶液由紫色变为微红色,且半分钟不褪色 ×100%
解析:软锰矿(主要含MnO ,还含有FeO、Fe O、CuO、MgO、SiO 等),加入稀硫酸和草酸
2 2 3 2
进行还原酸浸,其中形成含有二价铁离子,三价铁离子,铜离子、镁离子溶液,二氧化硅不与稀硫
酸、草酸反应,因此滤渣1为二氧化硅,此步骤除掉硅元素;其次加入硫化锰的目的是除去铜离子,
以硫化铜的形式除掉;加入二氧化锰的目的是将亚铁离子氧化为三价铁离子,然后加入碳酸锰调节
PH,将三价铁离子以氢氧化铁的形式沉淀除掉,之后进行蒸发结晶、过滤、洗涤得到硫酸锰,随
后硫酸锰加水溶解,加入硫酸铵反应,在冰水浴的条件下,目的是增大硫酸锰的溶解度,最后得到
目标产物硫酸锰铵。
(1)“还原酸浸”主要反应是MnO 转化为锰离子,离子反应为MnO +HC O+2H+=Mn2++
2 2 2 2 4
2CO↑+2HO;
2 2
(2)软锰矿(主要含MnO ,还含有FeO、Fe O、CuO、MgO、SiO 等),加入稀硫酸和草酸进行
2 2 3 2
“还原酸浸”,其中形成含有二价铁离子,三价铁离子,铜离子、镁离子溶液,二氧化硅不与稀硫
酸、草酸反应,因此滤渣1为二氧化硅;
(3)“除铜”的反应离子方程式为:MnS+Cu2+ CuS+Mn2+,则常温下平衡常数为K===
1.9×1023;
(4)加入二氧化锰的目的是将亚铁离子氧化为三价铁离子,然后加入碳酸锰调节PH,使Fe3+沉
淀完全,而不能使Mn2+形成沉淀,则由金属离子以氢氧化物形式沉淀时溶液的pH可知,调节pH
的范围为2.8≤pH<8.0;
(5)进行蒸发结晶、趁热过滤、洗涤得到硫酸锰
(6)过量的KMnO 溶液与硫酸锰铵反应生成MnO ,过滤掉MnO 后溶液为紫色,反应剩余的
4 2 2
KMnO 用FeSO 滴定,生成Fe3+,故滴定终点现象为溶液由紫色变为微红色,且半分钟不褪色;由
4 4
题意得,加入的KMnO 物质的量为n=cV×10-3mol,用FeSO 滴定KMnO 的反应为MnO 2++
4 1 1 1 4 4 +5Fe
8H+=Mn2++5Fe3++4HO ,滴定20mL KMnO 消耗FeSO 的物质的量为n=cV×10-3mol,则剩余
2 4 4 2 2 2
的高锰酸钾的物质的量为cV×10-3mol××=cV×10-3mol,与硫酸锰铵反应完的KMnO 的物质的量
2 2 2 2 4
为:n-n,反应为2MnO 2++2HO=5MnO ↓+4H+,wg硫酸锰铵(即锰元素)的物质的量为:
1 2 +3Mn 2 2
×(n- n)mol,故锰元素的质量分数为 ×100%
1 2
= ×100%。