文档内容
第 5 讲 氧化还原反应方程式的书写与配平
[复习目标] 1.掌握氧化还原反应方程式的配平方法及技巧。2.能提取有效信息书写化学方
程式。
考点一 氧化还原反应方程式的配平
1.氧化还原反应方程式配平的基本原则
2.氧化还原反应方程式配平的一般步骤
1.正向配平
(1)______HCl(浓)+______MnO =====______Cl↑+______MnCl +______HO
2 2 2 2
(2)______Cu+______HNO(稀)===______Cu(NO )+______NO↑+______HO
3 3 2 2
(3)______KI+______KIO +______HSO ===______I+______KSO +______HO
3 2 4 2 2 4 2
(4)______MnO+______H++______Cl-===______Mn2++______Cl↑+______HO
2 2
答案 (1)4 1 1 1 2 (2)3 8 3 2 4
(3)5 1 3 3 3 3 (4)2 16 10 2 5 82.逆向配平
(1)____S+______KOH===______KS+______KSO +______HO
2 2 3 2
(2)______P +______KOH+______HO===______KPO +______PH ↑
4 2 3 4 3
答案 (1)3 6 2 1 3 (2)2 9 3 3 5
3.含有未知数的配平
(1)______FeS+____HCl===______S+______FeCl +______HS
x 2 2
(2)______Na S+______NaClO+______NaOH===______NaSO +______NaCl+______HO
2 x 2 4 2
答案 (1) 2 (-1) 1 1
(2)1 (3x+1) (2x-2) x (3x+1) (x-1)
4.有机物参与的氧化还原反应方程式的配平
(1)______KClO + ______HC O + ______HSO ===______ClO ↑ + ______CO↑ +
3 2 2 4 2 4 2 2
______KHSO+______HO
4 2
(2)______C HO + ______KMnO + ______HSO ===______KSO + ______MnSO +
2 6 4 2 4 2 4 4
______CO↑+______HO
2 2
答案 (1)2 1 2 2 2 2 2
(2)5 12 18 6 12 10 33
5.缺项配平
(1)______ClO-+______Fe(OH) +________===______Cl-+______FeO+______HO
3 2
(2)______MnO+______HO+________===______Mn2++______O↑+______HO
2 2 2 2
(3)某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有:Al O、C、N、CO。
2 3 2
请将AlN之外的反应物与生成物分别填入以下空格内,并配平。
++=====AlN+
(4)将NaBiO 固体(黄色,微溶)加入MnSO 和HSO 的混合溶液里,加热,溶液显紫色(Bi3+
3 4 2 4
无色)。配平该反应的离子方程式:
NaBiO+Mn2++____===Na++Bi3++____+____
3
答案 (1)3 2 4OH- 3 2 5
(2)2 5 6H+ 2 5 8
(3)AlO 3C N 2 3CO
2 3 2
(4)5 2 14 H+ 5 5 2 MnO 7 HO
2
解析 (3)根据氮元素、碳元素的化合价变化,N 是氧化剂,C是还原剂,AlN为还原产物,
2
CO为氧化产物。
“三步法”突破缺项型氧化还原反应方程式的配平
缺项方程式是指某些反应物或生成物在方程式中没有写出来,它们一般为水、酸(H+)或碱(OH-),其配平流程为
考点二 情景方程式的书写
“四步法”突破新情景下氧化还原反应方程式的书写
示例
KMnO 能与热的经硫酸酸化的NaC O 溶液反应,生成Mn2+和CO,该反应的离子方程式
4 2 2 4 2
是________________________________________________________________________
________________________________________________________________________。
分析 第一步:依题意,锰元素的化合价降低,故 KMnO 是氧化剂,Mn2+是还原产物;碳
4
元素的化合价升高,故NaC O(碳元素化合价为+3价)是还原剂,CO 是氧化产物。
2 2 4 2
第二步:按“氧化剂+还原剂―→还原产物+氧化产物”把离子方程式初步写成:MnO+
C O―→Mn2++CO↑。
2 2
由MnO→Mn2+,锰元素降了5价;由C O→CO ,碳元素升了1价,1 mol C O共失去2 mol
2 2 2
e-,故在C O前配5,在氧化产物CO 前配10;在MnO前配2,在还原产物Mn2+前配2,
2 2
即2MnO+5C O―→2Mn2++10CO↑。
2 2
第三步:反应在硫酸中进行,故在左边补充 H+,右边补充HO,2MnO+5C O+H+―→
2 2
2Mn2++10CO↑+HO。
2 2
第四步:依据电荷守恒及H、O原子守恒配平如下:2MnO+5C O+16H+=====2Mn2++10CO↑+8HO。
2 2 2
一、依据陈述信息书写方程式
1.[2021·全国甲卷,26(2)]以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的
3 2 3
NaHSO ,生成碘化物;再向混合溶液中加入NaIO 溶液,反应得到I 。上述制备I 的总反
3 3 2 2
应的离子方程式为______________________________________________________________。
答案 2IO+5HSO===I+5SO+3H++HO
2 2
解析 先向NaIO 溶液中加入计量的NaHSO ,生成碘化物,即含I-的物质;再向混合溶液
3 3
(含I-)中加入NaIO 溶液,反应得到I ,上述制备I 的两个反应中I-为中间产物,总反应为
3 2 2
IO与HSO发生氧化还原反应生成SO和I ,根据得失电子守恒、电荷守恒及元素守恒即可
2
得离子方程式:2IO+5HSO===I+5SO+3H++HO。
2 2
2.工业上可由天然二氧化锰粉和硫化锰矿用硫酸溶浸得硫单质和硫酸锰,写出该反应的化
学方程式:________________________________________________________________。
答案 MnO +MnS+2HSO ===2MnSO +S+2HO
2 2 4 4 2
二、依据流程信息书写方程式
3.NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示:
2
(1)写出“反应”步骤中生成ClO 的化学方程式:
2
________________________________________________________________________
________________________________________________________________________。
(2)“尾气吸收”是吸收电解过程中排出的少量ClO 。写出此吸收反应的化学方程式:
2
________________________________________________________________________
________________________________________________________________________。
答案 (1)2NaClO+SO +HSO ===2ClO +2NaHSO
3 2 2 4 2 4
(2)2ClO+HO+2NaOH===2NaClO+O+2HO
2 2 2 2 2 2
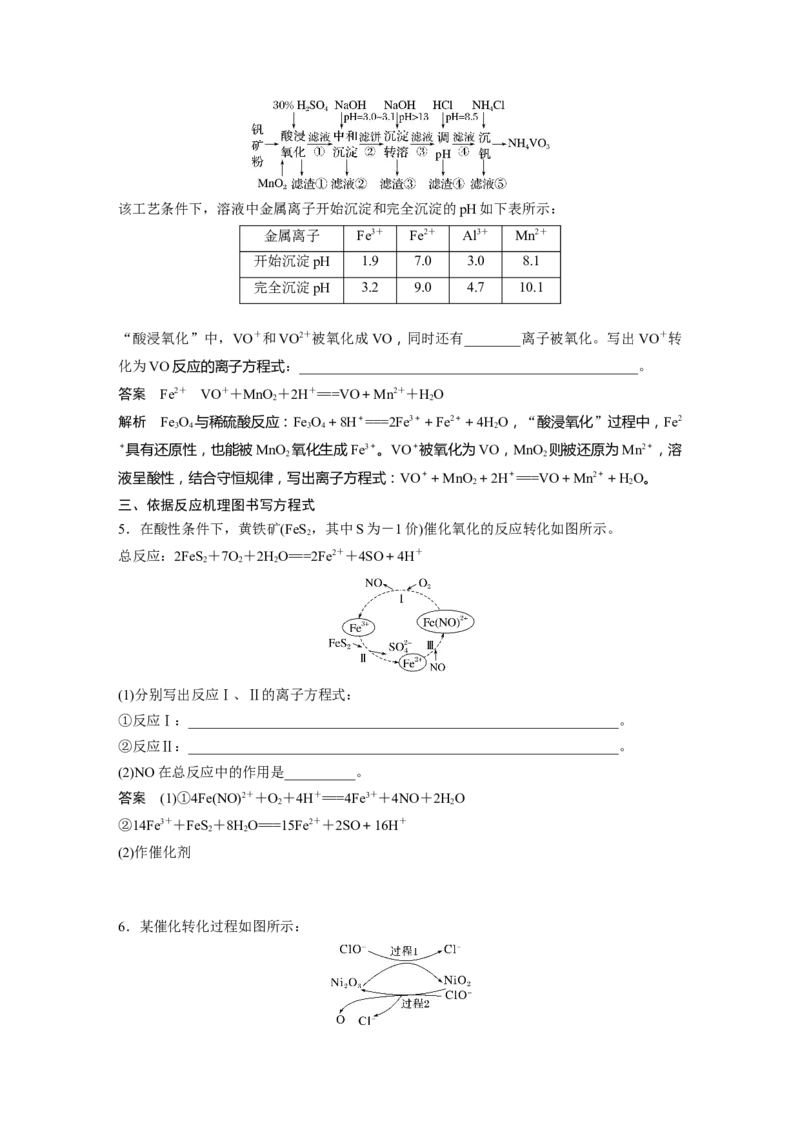
4.[2020·全国卷Ⅰ,26(2)]钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物
存在,还包括钾、镁的铝硅酸盐,以及 SiO 、Fe O 。采用以下工艺流程可由黏土钒矿制备
2 3 4
NH VO 。
4 3该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
“酸浸氧化”中,VO+和VO2+被氧化成VO,同时还有________离子被氧化。写出VO+转
化为VO反应的离子方程式:________________________________________________。
答案 Fe2+ VO++MnO +2H+===VO+Mn2++HO
2 2
解析 Fe O 与稀硫酸反应:Fe O +8H+===2Fe3++Fe2++4HO,“酸浸氧化”过程中,Fe2
3 4 3 4 2
+具有还原性,也能被MnO 氧化生成Fe3+。VO+被氧化为VO,MnO 则被还原为Mn2+,溶
2 2
液呈酸性,结合守恒规律,写出离子方程式:VO++MnO +2H+===VO+Mn2++HO。
2 2
三、依据反应机理图书写方程式
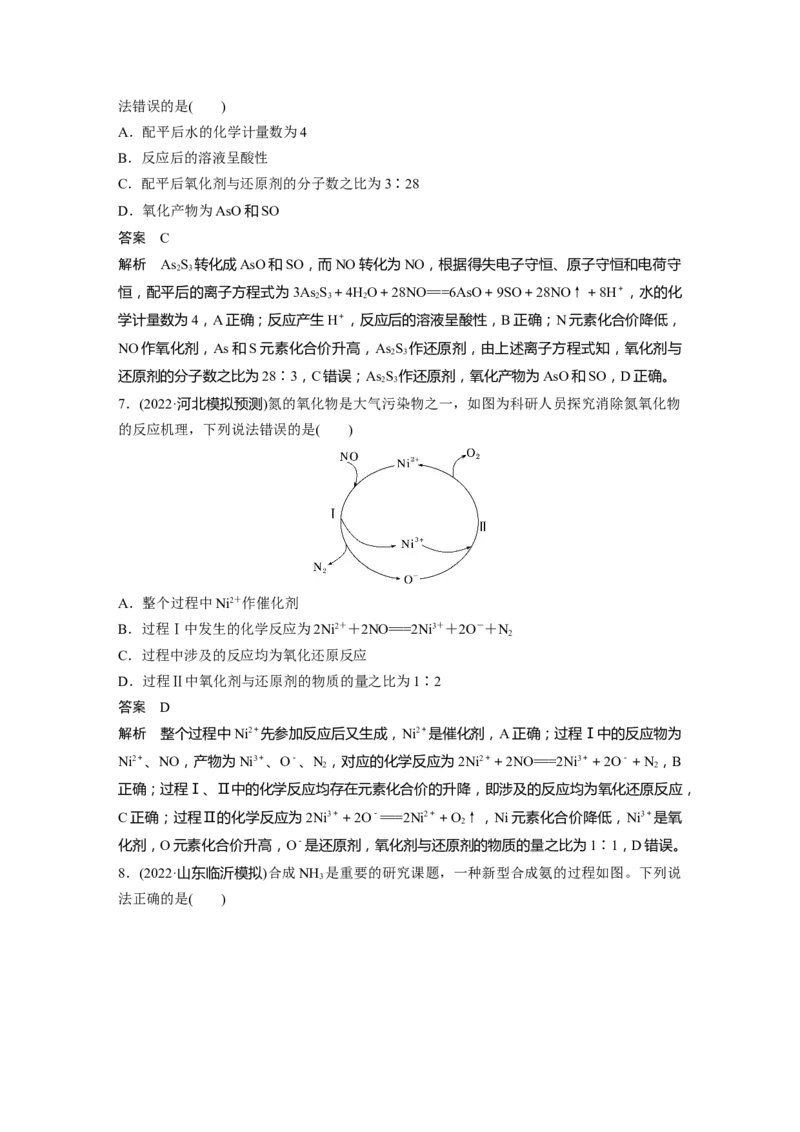
5.在酸性条件下,黄铁矿(FeS ,其中S为-1价)催化氧化的反应转化如图所示。
2
总反应:2FeS+7O+2HO===2Fe2++4SO+4H+
2 2 2
(1)分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:_____________________________________________________________。
②反应Ⅱ:_____________________________________________________________。
(2)NO在总反应中的作用是__________。
答案 (1)①4Fe(NO)2++O+4H+===4Fe3++4NO+2HO
2 2
②14Fe3++FeS+8HO===15Fe2++2SO+16H+
2 2
(2)作催化剂
6.某催化转化过程如图所示:过程1:Ni O+ClO-===2NiO+Cl-,
2 3 2
过程2的离子方程式:___________________________________________________。
答案 2NiO+ClO-===Ni O+Cl-+2O
2 2 3
7.NaClO氧化可除去氨氮,反应机理如图所示(其中HO和NaCl略去):
2
NaClO氧化NH 的总反应的化学方程式为___________________________________
3
________________________________________________________________________。
答案 2NH +3NaClO===N+3HO+3NaCl
3 2 2
循环转化关系图中物质变化分析思路
(1)根据示意图中的箭头方向分清反应物、生成物:箭头进入的是反应物,箭头出去的是生
成物。
(2)若上一步反应生成某物质,下一步该物质又参加反应,则该物质为中间产物。
(3)若某物质参加反应,后又生成该物质,则该物质为催化剂。
1.[2020·全国卷Ⅱ,26(3)(4)]化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合
物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(3)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该反应为
2 2
歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备ClO的化学方程式为
2
________________________________________________________________________
________________________________________________________________________。
(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为
2
NaClO 、NaHSO 、NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到
2 4 3
ClO 溶液。上述过程中,生成ClO 的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的
2 2 2 2
量为____________mol;产生“气泡”的化学方程式为_____________________________
________________________________________________________________________。
答案 (3)2Cl +HgO===HgCl +ClO
2 2 2
(4)1.25 NaHCO +NaHSO===CO↑+NaSO +HO
3 4 2 2 4 2
解析 (3)由新制的HgO和Cl 反应制备ClO,由于该反应为歧化反应,所以只有氯元素的
2 2
化合价发生变化,由 0 价变为+1 价和-1 价,所以反应的化学方程式为 2Cl +
2
HgO===HgCl +ClO。(4)由题意知,在NaClO 生成ClO 的过程中,发生歧化反应,NaClO
2 2 2 2 2既是氧化剂,又是还原剂,4NaClO―――→4ClO ,NaClO――→NaCl,每生成4 mol ClO ,需
2 2 2 2
消耗5 mol NaClO ,所以每生成1 mol ClO ,需消耗 mol(即1.25 mol)NaClO 。产生的气泡
2 2 2
的成分为CO,反应的化学方程式为NaHCO +NaHSO===CO↑+NaSO +HO。
2 3 4 2 2 4 2
2.[2022·全国甲卷,26(1)(4)]硫酸锌(ZnSO)是制备各种含锌材料的原料,在防腐、电镀、
4
医学上有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以
3 2
及Ca、Mg、Fe、Cu等的化合物。其制备流程如下:
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为___________________________________。
(4)向80~90 ℃的滤液①中分批加入适量KMnO 溶液充分反应后过滤,滤渣②中有MnO ,
4 2
该步反应的离子方程式为__________________________________________________。
答案 (1)ZnCO=====ZnO+CO↑
3 2
(4)3Fe2++MnO+7HO===3Fe(OH) ↓+MnO ↓+5H+
2 3 2
解析 (1)焙烧时,生成ZnO的反应为ZnCO =====ZnO+CO↑。(4)向80~90 ℃的滤液①
3 2
中加入KMnO 溶液,可氧化Fe2+,得到含Fe(OH) 和MnO 的滤渣②,反应的离子方程式为
4 3 2
3Fe2++MnO+7HO===3Fe(OH) ↓+MnO ↓+5H+。
2 3 2
课时精练
1.一定条件下,硝酸铵受热分解的化学方程式(未配平)为NH NO ―→HNO+N↑+HO,
4 3 3 2 2
下列说法错误的是( )
A.配平后HO的化学计量数为6
2
B.NH NO 既是氧化剂又是还原剂
4 3
C.该反应既是分解反应也是氧化还原反应
D.氧化产物和还原产物的物质的量之比为5∶3
答案 A
解析 由配平后的化学方程式可知,HO的化学计量数为9,A错误;NH NO 中NH所含N
2 4 3元素价态升高,部分NO所含N元素价态降低,则NH NO 既是氧化剂又是还原剂,B正确;
4 3
该反应中反应物只有一种,则属于分解反应,该反应中含有变价元素,则属于氧化还原反应,
C正确;氧化产物(5NH→N)和还原产物(3NO→N)的物质的量之比为∶=5∶3,D正确。
2 2
2.把图2中的物质补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平)。
对该氧化还原反应的离子方程式,下列说法不正确的是( )
A.IO是氧化剂,具有氧化性
B.氧化性:MnO>IO
C.氧化剂和还原剂的微粒个数之比为5∶2
D.若有2个Mn2+参加反应,则转移10个电子
答案 B
解析 由题干信息得到该离子方程式为5IO+2Mn2++3HO===2MnO+5IO+6H+,IO中的
2
碘元素在反应中化合价降低,得电子,作氧化剂,具有氧化性,故 A正确;根据反应方程
式可知,该反应的氧化剂是IO,氧化产物是MnO,根据氧化剂的氧化性大于氧化产物的氧
化性,则氧化性强弱顺序是IO>MnO,故B错误;根据方程式可知:氧化剂碘酸根离子和
还原剂锰离子的物质的量之比为5∶2,故C正确;根据反应方程式可知,有2个Mn2+参加
反应时,转移电子的个数是2×(7-2)=10个,故D正确。
3.钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三
铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到
130 ℃反应。其过程可以用如下化学方程式表示,下列说法不正确的是( )
①3Fe+NaNO +5NaOH===3NaFeO+HO+NH ↑
2 2 2 2 3
②NaFeO+NaNO +HO―→NaFe O+NH ↑+NaOH(未配平)
2 2 2 2 2 2 4 3
③NaFeO+NaFe O+2HO===Fe O+4NaOH
2 2 2 2 4 2 3 4
A.碱性条件下,NaNO 的氧化性比NaFeO、NaFe O 都强
2 2 2 2 2 4
B.反应①、②是氧化还原反应,③不是氧化还原反应
C.反应②配平后,HO的化学计量数是6
2
D.整个反应过程中,每有16.8 g Fe参加反应转移0.8 mol电子
答案 C
解析 根据反应①可知碱性条件下,NaNO 的氧化性比NaFe O 强,根据反应②可知碱性
2 2 2 2
条件下NaNO 的氧化性比NaFe O 强,A正确;反应①、②中N、Fe元素的化合价均发生
2 2 2 4
变化,为氧化还原反应,反应③中没有元素化合价发生变化,为非氧化还原反应,B正确;
反应②中NaFeO 中Fe元素化合价由+2价升高到 NaFe O 中的+3价,升高了 1价,
2 2 2 2 4NaNO 中N元素化合价由+3价降低到NH 中的-3价,降低了6价,根据得失电子守恒和
2 3
原子守恒配平方程式为6NaFeO +NaNO +5HO===3NaFe O +NH ↑+7NaOH,所以HO
2 2 2 2 2 2 4 3 2
的化学计量数是5,C错误;16.8 g Fe的物质的量为=0.3 mol,Fe元素最终均被氧化为
Fe O ,平均化合价升高价,整个过程中没有其他元素被氧化,且 Fe元素全部被氧化,所以
3 4
转移0.3 mol×=0.8 mol电子,D正确。
4.工业上常用绿矾(FeSO ·7H O)处理工业废水中含有的重铬酸根离子(CrO),反应的化学方
4 2 2
程式为FeSO +KCr O +HSO ―→Fe (SO ) +Cr (SO ) +HO+KSO (未配平),下列有关
4 2 2 7 2 4 2 4 3 2 4 3 2 2 4
说法正确的是( )
A.每有1 mol K Cr O 参加反应,转移3 mol电子
2 2 7
B.KCr O 中铬元素的化合价为+7价
2 2 7
C.参与反应的Fe2+与Cr O物质的量之比为6∶1
2
D.FeSO 是氧化剂
4
答案 C
解析 Cr元素化合价由+6价降低到+3价,转移电子关系为KCr O ~6e-,故每有1 mol
2 2 7
KCrO 参加反应,转移6 mol电子,A错误;K元素化合价为+1价,O元素化合价为-2价,
2 2 7
根据化合价代数和为0,知Cr元素化合价为+6价,B错误;根据得失电子守恒知,Fe2+与
Cr O物质的量之比为6∶1,C正确;FeSO 中Fe元素化合价升高,作还原剂,D错误。
2 4
5.已知反应:①SO +2Fe3++2HO―→SO+2Fe2++W;
2 2
②Cr O+aFe2++bH+―→Cr3++Fe3++HO (未配平)
2 2
下列有关说法正确的是( )
A.方程式①中W为4OH-
B.还原性强弱:SO >Fe2+
2
C.a=6,b=7
D.反应Cr O+3SO +2H+===2Cr3++3SO+HO不能发生
2 2 2
答案 B
解析 根据原子守恒并结合离子方程式两边离子所带电荷总数相等可知,反应①为SO +
2
2Fe3++2HO===SO+2Fe2++4H+,W为4H+,A错误;还原剂的还原性强于还原产物,由
2
反应①可知,还原性:SO >Fe2+,B正确;反应②中,Cr元素的化合价由+6降到+3,Fe
2
元素化合价由+2升高到+3,根据得失电子守恒可得,Cr O和Cr3+对应的化学计量数分别
2
为1、2,Fe2+和Fe3+对应的化学计量数均为6,则a=6,再结合离子方程两边离子所带电
荷总数相等可得,b=14,C错误;CrO具有强氧化性,SO 具有还原性,且由①、②可知氧
2 2
化性:CrO>SO,则CrO能将SO 氧化为SO,即反应CrO+3SO +2H+===2Cr3++3SO+
2 2 2 2 2
HO能发生,D错误。
2
6.已知离子方程式:As S +HO+NO―→AsO+SO+NO↑+________(未配平),下列说
2 3 2法错误的是( )
A.配平后水的化学计量数为4
B.反应后的溶液呈酸性
C.配平后氧化剂与还原剂的分子数之比为3∶28
D.氧化产物为AsO和SO
答案 C
解析 As S 转化成AsO和SO,而NO转化为NO,根据得失电子守恒、原子守恒和电荷守
2 3
恒,配平后的离子方程式为3As S +4HO+28NO===6AsO+9SO+28NO↑+8H+,水的化
2 3 2
学计量数为4,A正确;反应产生H+,反应后的溶液呈酸性,B正确;N元素化合价降低,
NO作氧化剂,As和S元素化合价升高,As S 作还原剂,由上述离子方程式知,氧化剂与
2 3
还原剂的分子数之比为28∶3,C错误;As S 作还原剂,氧化产物为AsO和SO,D正确。
2 3
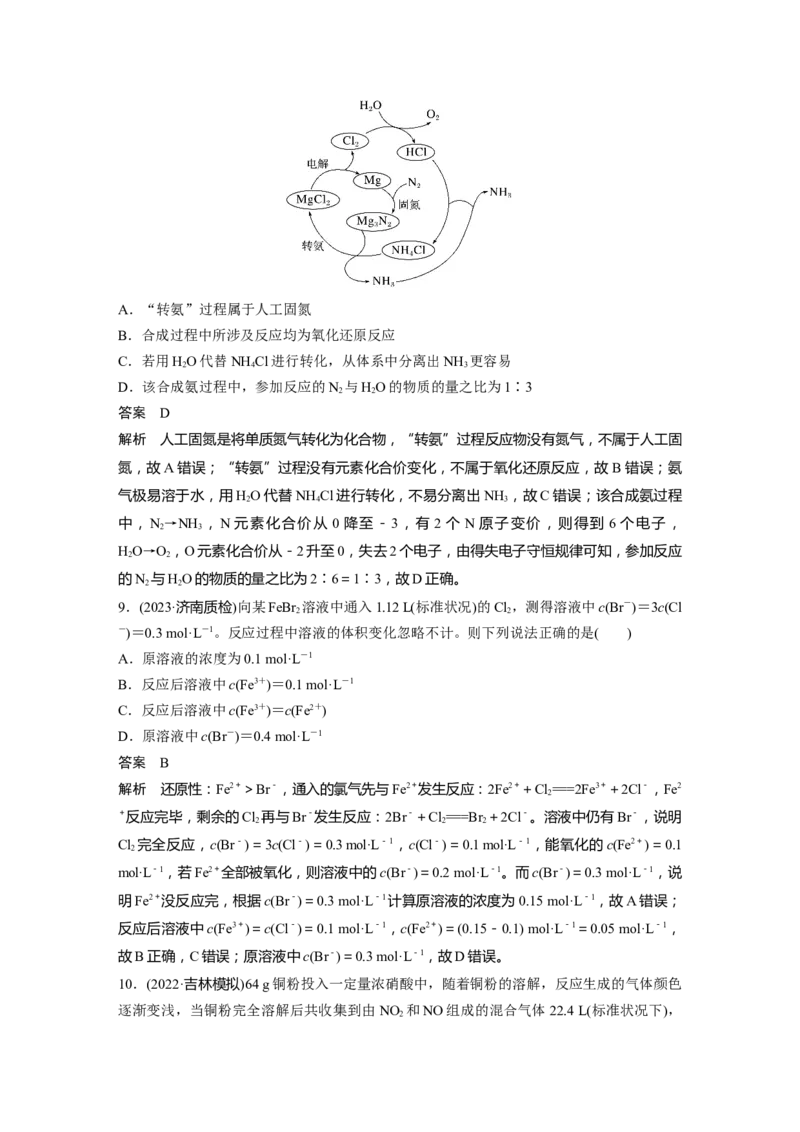
7.(2022·河北模拟预测)氮的氧化物是大气污染物之一,如图为科研人员探究消除氮氧化物
的反应机理,下列说法错误的是( )
A.整个过程中Ni2+作催化剂
B.过程Ⅰ中发生的化学反应为2Ni2++2NO===2Ni3++2O-+N
2
C.过程中涉及的反应均为氧化还原反应
D.过程Ⅱ中氧化剂与还原剂的物质的量之比为1∶2
答案 D
解析 整个过程中Ni2+先参加反应后又生成,Ni2+是催化剂,A正确;过程Ⅰ中的反应物为
Ni2+、NO,产物为Ni3+、O-、N ,对应的化学反应为2Ni2++2NO===2Ni3++2O-+N ,B
2 2
正确;过程Ⅰ、Ⅱ中的化学反应均存在元素化合价的升降,即涉及的反应均为氧化还原反应,
C正确;过程Ⅱ的化学反应为2Ni3++2O-===2Ni2++O↑,Ni元素化合价降低,Ni3+是氧
2
化剂,O元素化合价升高,O-是还原剂,氧化剂与还原剂的物质的量之比为1∶1,D错误。
8.(2022·山东临沂模拟)合成NH 是重要的研究课题,一种新型合成氨的过程如图。下列说
3
法正确的是( )A.“转氨”过程属于人工固氮
B.合成过程中所涉及反应均为氧化还原反应
C.若用HO代替NH Cl进行转化,从体系中分离出NH 更容易
2 4 3
D.该合成氨过程中,参加反应的N 与HO的物质的量之比为1∶3
2 2
答案 D
解析 人工固氮是将单质氮气转化为化合物,“转氨”过程反应物没有氮气,不属于人工固
氮,故A错误;“转氨”过程没有元素化合价变化,不属于氧化还原反应,故 B错误;氨
气极易溶于水,用HO代替NH Cl进行转化,不易分离出NH ,故C错误;该合成氨过程
2 4 3
中,N→NH ,N 元素化合价从 0 降至-3,有 2 个 N 原子变价,则得到 6 个电子,
2 3
HO→O,O元素化合价从-2升至0,失去2个电子,由得失电子守恒规律可知,参加反应
2 2
的N 与HO的物质的量之比为2∶6=1∶3,故D正确。
2 2
9.(2023·济南质检)向某FeBr 溶液中通入1.12 L(标准状况)的Cl ,测得溶液中c(Br-)=3c(Cl
2 2
-)=0.3 mol·L-1。反应过程中溶液的体积变化忽略不计。则下列说法正确的是( )
A.原溶液的浓度为0.1 mol·L-1
B.反应后溶液中c(Fe3+)=0.1 mol·L-1
C.反应后溶液中c(Fe3+)=c(Fe2+)
D.原溶液中c(Br-)=0.4 mol·L-1
答案 B
解析 还原性:Fe2+>Br-,通入的氯气先与Fe2+发生反应:2Fe2++Cl===2Fe3++2Cl-,Fe2
2
+反应完毕,剩余的Cl 再与Br-发生反应:2Br-+Cl===Br +2Cl-。溶液中仍有Br-,说明
2 2 2
Cl 完全反应,c(Br-)=3c(Cl-)=0.3 mol·L-1,c(Cl-)=0.1 mol·L-1,能氧化的c(Fe2+)=0.1
2
mol·L-1,若Fe2+全部被氧化,则溶液中的c(Br-)=0.2 mol·L-1。而c(Br-)=0.3 mol·L-1,说
明Fe2+没反应完,根据c(Br-)=0.3 mol·L-1计算原溶液的浓度为0.15 mol·L-1,故A错误;
反应后溶液中c(Fe3+)=c(Cl-)=0.1 mol·L-1,c(Fe2+)=(0.15-0.1) mol·L-1=0.05 mol·L-1,
故B正确,C错误;原溶液中c(Br-)=0.3 mol·L-1,故D错误。
10.(2022·吉林模拟)64 g铜粉投入一定量浓硝酸中,随着铜粉的溶解,反应生成的气体颜色
逐渐变浅,当铜粉完全溶解后共收集到由NO 和NO组成的混合气体22.4 L(标准状况下),
2则混合气体中NO的体积为( )
A.11.2 L B.33.6 L C.22.4 L D.44.8 L
答案 A
解析 已知HNO 与铜反应生成NO、NO ,根据反应的化学方程式:Cu+4HNO(浓)===
3 2 3
Cu(NO ) +2NO ↑+2HO、3Cu+8HNO(稀)===3Cu(NO ) +2NO↑+4HO 分析计算。
3 2 2 2 3 3 2 2
n(Cu)==1 mol,n(NO +NO)==1 mol,设NO 和NO组成的混合气体中n(NO)=x mol,
2 2
n(NO )=y mol,根据 Cu+4HNO(浓)===Cu(NO ) +2NO ↑+2HO,消耗的铜为 0.5y
2 3 3 2 2 2
mol,根据3Cu+8HNO(稀)===3Cu(NO ) +2NO↑+4HO,消耗的铜为1.5x mol,则有x
3 3 2 2
+y=1,1.5x+0.5y=1,解得:x=0.5,y=0.5,则V(NO)=0.5 mol×22.4 L·mol-1=11.2 L。
11.(2022·浙江模拟)已知酸性KMnO 溶液能被NaSO 溶液还原成Mn2+而使溶液褪色。欲
4 2 3
使20.00 mL 1.00×10-2 mol·L-1酸性KMnO 溶液恰好褪色,需消耗25.00 mL Na SO 溶液,
4 2 3
则该NaSO 溶液的物质的量浓度(单位:mol·L-1)为( )
2 3
A.2.00×10-2 B.3.00×10-2
C.4.00×10-2 D.5.00×10-2
答案 A
解析 酸性KMnO 溶液能被NaSO 溶液还原成Mn2+而使溶液褪色,发生的反应为2MnO
4 2 3
+5SO+6H+===2Mn2++5SO+3H O,则有关系式:2MnO~5SO,使20.00 mL 1.00×10-
2
2 mol·L-1酸性KMnO 溶液恰好褪色,需消耗25.00 mL Na SO 溶液,则该NaSO 溶液的物
4 2 3 2 3
质的量浓度为=2.00×10-2 mol·L-1,故选A。
12.(2022·山东模拟)玻璃仪器内壁残留的硫单质可用热NaOH溶液洗涤除去,发生如下反应:
①3S+6NaOH=====2NaS+NaSO +3HO
2 2 3 2
②(x-1)S+NaS=====NaS (x=2~6)
2 2 x
③S+NaSO =====NaSO
2 3 2 2 3
下列说法正确的是( )
A.反应①②③中,硫单质的作用相同
B.反应①中,每消耗1 mol硫单质转移4 mol电子
C.0.96 g硫单质与a mL 2 mol·L-1热NaOH溶液恰好完全反应,只生成NaS和NaSO ,
2 2 3
则a=60
D.1.28 g硫单质与10 mL 2 mol·L-1热NaOH溶液恰好完全反应,只生成NaS 和NaSO ,
2 x 2 2 3
则x=5
答案 D
解析 由题干方程式可知,反应①中S既是氧化剂又是还原剂,反应②中S是氧化剂,反应
③中S是还原剂,故反应①②③中,硫单质的作用不相同,A错误;分析反应①可知,每消
耗3 mol硫单质转移 4 mol电子,B错误;0.96 g即=0.03 mol硫单质与a mL 2 mol·L-1热
NaOH溶液恰好完全反应,只生成Na S和Na SO ,由反应①的方程式,则a=×1 000 L-
2 2 31=30,C 错误;1.28 g 即=0.04 mol 硫单质与 10 mL 2 mol·L-1即0.01 L×2 mol·L-1=
0.02 mol热NaOH溶液恰好完全反应,只生成a mol Na S 和b mol Na SO,则由Na原子守
2 x 2 2 3
恒有2a+2b=0.02,由S原子守恒有:ax+2b=0.04,由电子守恒有2a=4b,解得x=5,D
正确。
13.根据信息完成下列方程式。
(1)KMnO 氧化废水中Mn2+生成MnO 的离子方程式为________________________。
4 2
(2)NaAlH 与水发生氧化还原反应的化学方程式为_____________________________。
4
(3)在酸性条件下,NaClO 可发生反应生成NaCl并释放出ClO ,该反应的离子方程式为
2 2
________________________________________________________________________。
(4)PbO 可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为_______________
2
________________________________________________________________________。
(5)NaClO溶液与Ag反应的产物为AgCl、NaOH和O,该反应的化学方程式为
2
________________________________________________________________________。
(6)在45~50 ℃时向CuCl悬浊液中持续通入空气,得到碱式氯化铜[Cu (OH) Cl·3H O],该
2 2 2 2
反应的化学方程式为_____________________________________________________。
答案 (1)2MnO+3Mn2++2HO===5MnO ↓+4H+
2 2
(2)NaAlH +2HO===NaAlO +4H↑
4 2 2 2
(3)4H++5ClO===Cl-+4ClO ↑+2HO
2 2
(4)PbO+ClO-===PbO +Cl-
2
(5)4Ag+4NaClO+2HO===4AgCl+4NaOH+O↑
2 2
(6)4CuCl+O+8HO=======2Cu (OH) Cl·3H O
2 2 2 2 2 2
14.锰广泛存在于自然界中,工业可用软锰矿(主要成分是MnO )制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO 。
2 2 4
Ⅰ.制备
(1)写出铝热法还原MnO 制备锰的化学方程式:______________________________
2
________________________________________________________________________。
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度 SO 的烟气,可用
2
以下方法处理。
方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO
2
进行脱硫的化学方程式:__________________________________________________。
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如图所示:过程 Ⅰ:……
过程 Ⅱ:2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
过程 Ⅰ 的离子方程式是__________________________________________________。
方法二:
③用MnCO 进行脱硫,可提高脱硫率。结合化学用语解释原因:_______________
3
________________________________________________________________________。
Ⅱ.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO ,将溶液中的Mn2+氧化为Mn3+,用
4
c mol·L-1 (NH )Fe(SO ) 溶液进行滴定,达到滴定终点时,滴定管刻度由V mL变为V
4 2 4 2 0 1
mL,废水中锰的含量为________g·mL-1。
答案 (1)4Al+3MnO =====3Mn+2Al O (2)①MnO +SO ======MnSO ②2Fe2++MnO
2 2 3 2 2 4 2
+4H+===Mn2++2Fe3++2HO ③溶液中存在平衡:MnCO (s)Mn2+(aq)+CO(aq),CO
2 3
消耗溶液中的H+,促进SO 溶解:SO +HOHSO H++HSO,生成的Mn2+有催化
2 2 2 2 3
作用,可促进反应2SO +O+2HO=====2HSO 发生 (3)55c(V-V)×10-3
2 2 2 2 4 1 0
解析 (1)铝热法还原MnO 制备锰即高温条件下铝单质和MnO 反应得到氧化铝和Mn单质,
2 2
化学方程式为4Al+3MnO =====3Mn+2Al O 。(2)①根据题意可知MnO 会将SO 氧化得
2 2 3 2 2
到MnSO ,化学方程式应为MnO +SO ======MnSO 。②据图可知过程Ⅰ中MnO 被Fe2+
4 2 2 4 2
还原生成Mn2+,Fe2+被氧化为Fe3+,根据电子守恒和元素守恒可得离子方程式为2Fe2++
MnO +4H+===Mn2++2Fe3++2HO。(3)滴定时发生反应Fe2++Mn3+===Fe3++Mn2+,所以
2 2
n(Mn)=n(Mn3+)=c(V -V )×10-3 mol,所取废水为1 mL,所以废水中锰的含量为55c(V
1 0 1
-V )×10-3 g·mL-1。
0
15.亚氯酸钠(NaClO)是一种重要的含氯消毒剂,制备亚氯酸钠的工艺流程如下:
2
回答下列问题:
(1)亚氯酸钠用作纸浆、纸张和各种纤维的漂白剂,是一种高效漂白剂,主要原因是亚氯酸
钠具有________性。
(2)制备 ClO 气体的化学方程式为 2NaClO +HO +HSO ===2ClO ↑+O↑+NaSO +
2 3 2 2 2 4 2 2 2 4
2HO;制备时可用S代替HO,写出该反应的离子方程式:________。
2 2 2
(3)测定某亚氯酸钠样品的纯度:准确称取亚氯酸钠样品m g,加入适量蒸馏水和过量的碘
化钾晶体,再滴入适量稀硫酸(发生反应:ClO+4I-+4H+===2I +Cl-+2HO),配成250
2 2
mL待测液。移取25.00 mL待测液于锥形瓶中,加几滴淀粉溶液,用 c mol·L-1的NaSO
2 2 3
标准溶液进行滴定,消耗NaSO 标准溶液V mL (已知:I+2SO===2I-+SO)。
2 2 3 2 2 4
①移取25.00 mL待测液的仪器的名称是________。②该样品中NaClO 的质量分数为________(用含m、c、V的代数式表示);在滴定操作正确
2
无误的情况下,此实验测得结果偏高,其可能的原因是________。
答案 (1)氧化 (2)6ClO+S+4H+===6ClO ↑+SO+2HO (3)①酸式滴定管(或移液管)
2 2
②×100% 碘离子被空气中的氧气氧化成了碘单质
解析 制备时NaClO 和HO 以及HSO 反应生成ClO 和O 以及NaSO 、HO,生成的
3 2 2 2 4 2 2 2 4 2
ClO 再用NaOH碱性溶液吸收,同时利用HO 将其还原为NaClO ,将所得的溶液经过一系
2 2 2 2
列操作得到NaClO 晶体,据此分析解题。(3)②根据题意可得关系式:ClO~2I ~4SO,所
2 2 2
以样品中NaClO 的质量分数为×100%=×100%;由于碘离子具有较强的还原性,能够被
2
空气中的氧气氧化成为碘单质,导致消耗的NaSO 的量增多,进一步导致NaClO 的质量
2 2 3 2
分数偏高。