文档内容
第 26 讲 氨和铵盐
[复习目标] 1.掌握NH 及铵盐的性质与用途。2.掌握喷泉实验、NH 的实验室制法的原理
3 3
及操作。
考点一 氨
1.氨的分子结构和物理性质
电子式 密度 气味 水溶性
比空气的小 刺激性气味 极易溶于水(1∶700)
思考 试从结构和性质上解释NH 极易溶于水的原因。
3
提示 NH 、HO均为极性分子,NH 与HO之间可形成分子间氢键,并且NH 和HO反应。
3 2 3 2 3 2
2.氨的化学性质
提醒 ①NH 是中学化学中唯一的碱性气体,能使湿润的红色石蕊试纸变蓝,可在推断题
3
中作为解题突破口。
②氨水呈碱性,NH ·H O属于一元弱碱,计算氨水的浓度时,溶质按NH 进行计算。
3 2 3
3.喷泉实验
如图为氨喷泉实验的装置(夹持装置均已略去)。(1)用图1装置进行喷泉实验。
①引发“喷泉”的方法是_______________________________________________。
答案 打开止水夹,挤出胶头滴管中的水
②简述产生喷泉的原理:___________________________________________________。
答案 氨极易溶于水,使烧瓶内的压强迅速减小
(2)只使用图2所示装置进行喷泉实验。
①打开止水夹,水不能倒吸入烧瓶的原因是______________________________________
________________________________________________________________________。
答案 玻璃管中有空气,氨与水不接触,不能被水吸收,烧瓶内压强不减小,故不能产生倒
吸现象
②如何引发图2装置的“喷泉”?
________________________________________________________________________。
答案 打开止水夹,用手(或热毛巾等)将烧瓶捂热,使烧瓶内氨膨胀,将导管中的空气排出,
使氨与烧杯中的水接触
(3)指出下面几种常见的能形成喷泉的气体的吸收剂。
CO、Cl、 NO、O NO 、O
2 2 2 2 2
气体 HCl NH NO
3 2
SO 、HS (4∶3) (4∶1)
2 2
水、
NaOH
吸收剂 NaOH 水 水 水 水
溶液
溶液
4.喷泉实验产物的浓度计算
关键是确定所得溶液中溶质的物质的量和溶液的体积,标准状况下的气体进行喷泉实验后所
得溶液的物质的量浓度:
(1)HCl、NH 、NO 气体或它们与其他不溶于水的气体混合时,所得溶液的物质的量浓度为
3 2
mol·L-1。
(2)当是NO 和O 的混合气体且体积比为4∶1时,c(HNO)= mol·L-1。
2 2 3
1.液氨制冷、碘的升华、加热法分离NH Cl和NaCl都不涉及化学变化( )
4
2.现有1 mol·L-1的氨水,则该溶液中NH ·H O的浓度是1 mol·L-1( )
3 2
3.氨水具有弱碱性,说明氨水是弱电解质( )
4.浓氨水可检验氯气管道是否漏气( )
答案 1.× 2.× 3.× 4.√
一、从“类别”和“价态”的视角理解NH 的性质
31.下列根据实验现象得出的结论不正确的是( )
A.将集有氨的试管倒扣于盛有水的水槽中,液体迅速充满试管,说明氨极易溶于水
B.将湿润的红色石蕊试纸放入集有氨的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性
C.将蘸有浓氨水和浓硝酸的玻璃棒靠近,观察到白烟,说明氨具有碱性且易与酸化合生成
铵盐
D.将红热的Pt丝伸入盛有浓氨水的锥形瓶中,瓶口出现少量红棕色气体,说明氨的直接氧
化产物为NO
2
答案 D
解析 氨极易溶于水,将集有氨的试管倒扣于盛有水的水槽中,液体迅速充满试管,故A
正确;氨水呈碱性:NH +HONH ·H ONH+OH-,故B正确;氨被氧气直接氧化为
3 2 3 2
NO,NO被O 氧化为红棕色的NO ,故D错误。
2 2
2.氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的
制备和性质,设计了如图所示装置。下列说法错误的是( )
A.甲装置中的固体可以是NaOH或CaO
B.乙装置中的干燥剂可以是碱石灰
C.丙中发生的反应是4NH +5O=====4NO+6HO
3 2 2
D.若戊中观察到紫色石蕊溶液变红,则说明已制得HNO
3
答案 A
解析 甲装置需要提供氨气和氧气,如果甲装置中的固体是 NaOH或CaO ,只能提供氨气,
不能提供氧气,X应为过氧化钠等,故A错误;戊中观察到紫色石蕊溶液变红,说明生成
了酸性物质,可以说明一氧化氮、氧气与水反应生成了硝酸,故D正确。
氨的化学性质归纳
化学性质
二、喷泉实验原理的理解
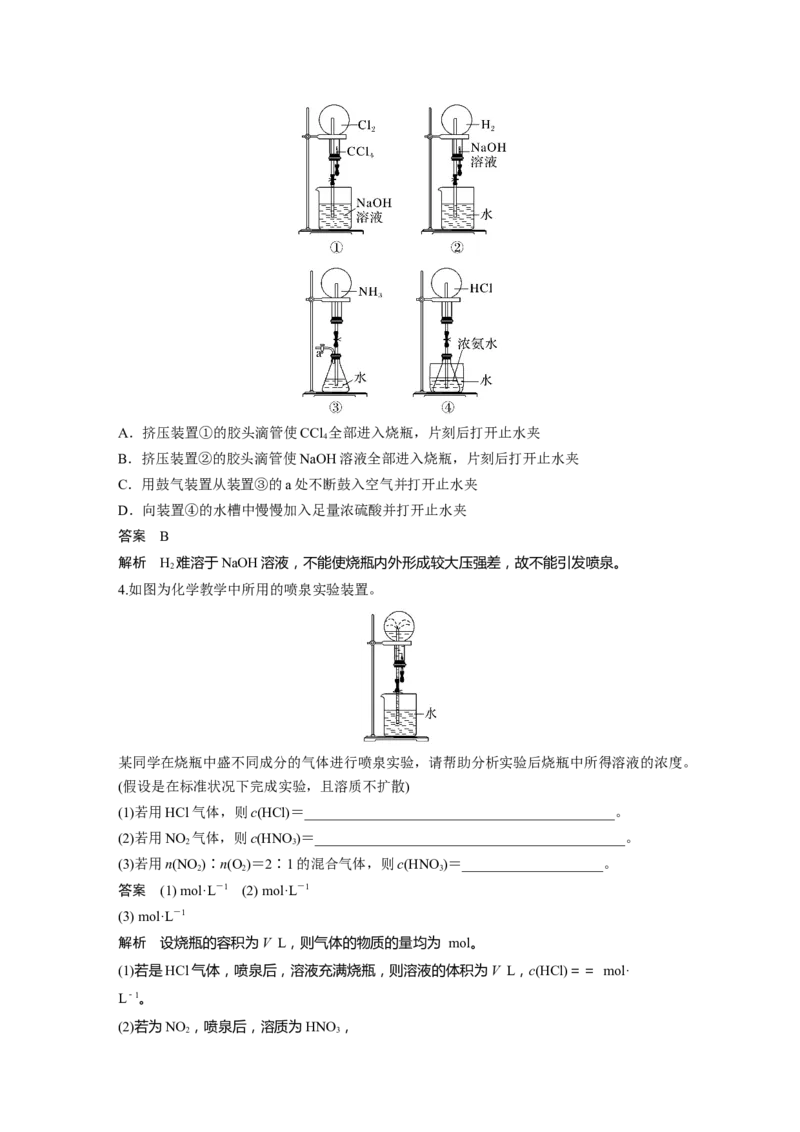
3.下图是课外活动小组的同学设计的4个喷泉实验方案,下列有关操作不可能引发喷泉的
是( )A.挤压装置①的胶头滴管使CCl 全部进入烧瓶,片刻后打开止水夹
4
B.挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹
C.用鼓气装置从装置③的a处不断鼓入空气并打开止水夹
D.向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹
答案 B
解析 H 难溶于NaOH溶液,不能使烧瓶内外形成较大压强差,故不能引发喷泉。
2
4.如图为化学教学中所用的喷泉实验装置。
某同学在烧瓶中盛不同成分的气体进行喷泉实验,请帮助分析实验后烧瓶中所得溶液的浓度。
(假设是在标准状况下完成实验,且溶质不扩散)
(1)若用HCl气体,则c(HCl)=____________________________________________。
(2)若用NO 气体,则c(HNO)=____________________________________________。
2 3
(3)若用n(NO )∶n(O )=2∶1的混合气体,则c(HNO)=____________________。
2 2 3
答案 (1) mol·L-1 (2) mol·L-1
(3) mol·L-1
解析 设烧瓶的容积为V L,则气体的物质的量均为 mol。
(1)若是HCl气体,喷泉后,溶液充满烧瓶,则溶液的体积为V L,c(HCl)== mol·
L-1。
(2)若为NO ,喷泉后,溶质为HNO,
2 33NO +HO===2HNO+NO
2 2 3
mol × mol
则喷泉后溶液的体积为V L,
c(HNO)== mol·L-1。
3
(3)若n(NO )∶n(O )=2∶1,发生反应:4NO +O +2HO===4HNO ,则反应剩余 L O ,溶
2 2 2 2 2 3 2
液的体积为V L,溶质为HNO,则c(HNO)== mol·L-1。
3 3
考点二 铵盐、NH 的检验
1.铵盐及NH的检验
(1)铵盐的物理性质
铵盐大多数是白色固体,绝大多数易溶于水。
(2)铵盐的化学性质
(3)NH的检验步骤
未知液――――→产生使湿润的红色石蕊试纸变蓝色的气体,则证明含NH
2.氨的实验室制法
(1)加热固态铵盐和碱的混合物
简易装置
干燥 用碱石灰
①将湿润的红色石蕊试纸置于试管口,试纸变蓝;
验满
②将蘸有浓盐酸的玻璃棒置于试管口,有白烟产生
(2)实验室制取氨的其他方法
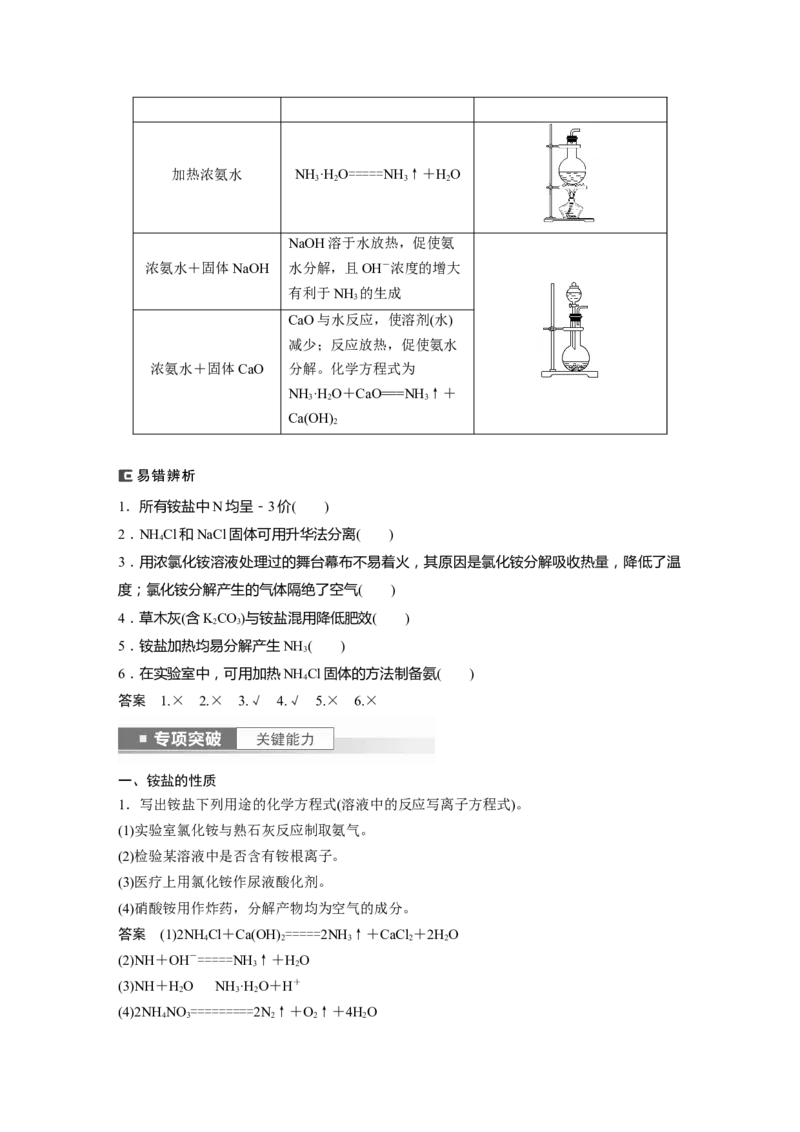
方法 化学方程式(或原理) 气体发生装置加热浓氨水 NH ·H O=====NH ↑+HO
3 2 3 2
NaOH溶于水放热,促使氨
浓氨水+固体NaOH 水分解,且OH-浓度的增大
有利于NH 的生成
3
CaO与水反应,使溶剂(水)
减少;反应放热,促使氨水
浓氨水+固体CaO 分解。化学方程式为
NH ·H O+CaO===NH ↑+
3 2 3
Ca(OH)
2
1.所有铵盐中N均呈-3价( )
2.NH Cl和NaCl固体可用升华法分离( )
4
3.用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是氯化铵分解吸收热量,降低了温
度;氯化铵分解产生的气体隔绝了空气( )
4.草木灰(含KCO)与铵盐混用降低肥效( )
2 3
5.铵盐加热均易分解产生NH ( )
3
6.在实验室中,可用加热NH Cl固体的方法制备氨( )
4
答案 1.× 2.× 3.√ 4.√ 5.× 6.×
一、铵盐的性质
1.写出铵盐下列用途的化学方程式(溶液中的反应写离子方程式)。
(1)实验室氯化铵与熟石灰反应制取氨气。
(2)检验某溶液中是否含有铵根离子。
(3)医疗上用氯化铵作尿液酸化剂。
(4)硝酸铵用作炸药,分解产物均为空气的成分。
答案 (1)2NH Cl+Ca(OH) =====2NH ↑+CaCl +2HO
4 2 3 2 2
(2)NH+OH-=====NH ↑+HO
3 2
(3)NH+HONH ·H O+H+
2 3 2
(4)2NH NO =========2N↑+O↑+4HO
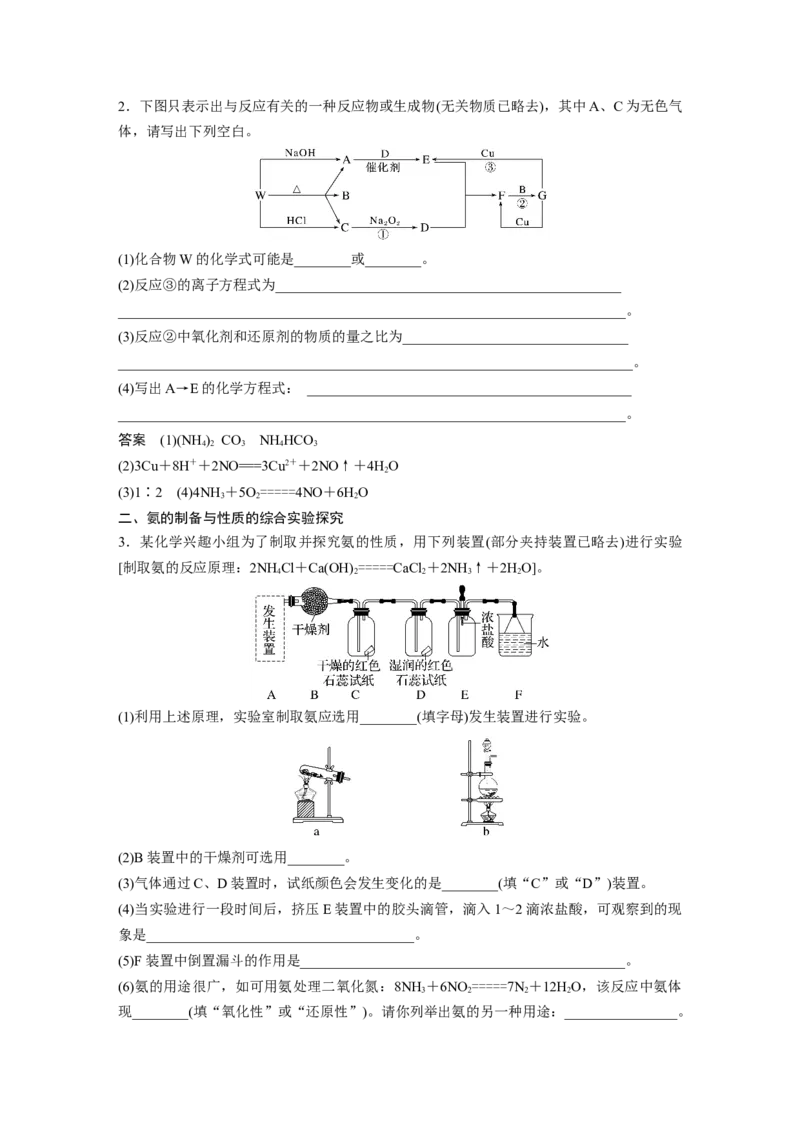
4 3 2 2 22.下图只表示出与反应有关的一种反应物或生成物(无关物质已略去),其中A、C为无色气
体,请写出下列空白。
(1)化合物W的化学式可能是________或________。
(2)反应③的离子方程式为_________________________________________________
________________________________________________________________________。
(3)反应②中氧化剂和还原剂的物质的量之比为________________________________
_________________________________________________________________________。
(4)写出A→E的化学方程式: ______________________________________________
________________________________________________________________________。
答案 (1)(NH ) CO NH HCO
4 2 3 4 3
(2)3Cu+8H++2NO===3Cu2++2NO↑+4HO
2
(3)1∶2 (4)4NH +5O=====4NO+6HO
3 2 2
二、氨的制备与性质的综合实验探究
3.某化学兴趣小组为了制取并探究氨的性质,用下列装置(部分夹持装置已略去)进行实验
[制取氨的反应原理:2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO]。
4 2 2 3 2
(1)利用上述原理,实验室制取氨应选用________(填字母)发生装置进行实验。
(2)B装置中的干燥剂可选用________。
(3)气体通过C、D装置时,试纸颜色会发生变化的是________(填“C”或“D”)装置。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现
象是______________________________________。
(5)F装置中倒置漏斗的作用是______________________________________________。
(6)氨的用途很广,如可用氨处理二氧化氮:8NH +6NO =====7N +12HO,该反应中氨体
3 2 2 2
现________(填“氧化性”或“还原性”)。请你列举出氨的另一种用途:________________。答案 (1)a (2)碱石灰 (3)D (4)产生白烟 (5)防止倒吸 (6)还原性 作制冷剂、制氮肥
(或化肥)、制硝酸、作化工原料(任答一点,其他合理答案也可)
1.正误判断,正确的打“√”,错误的打“×”。
(1)加热盛有少量NH HCO 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变
4 3
蓝,说明NH HCO 显碱性(2017·全国卷Ⅱ,13B)( × )
4 3
(2)用烧碱处理含高浓度NH的废水并回收利用氨(2017·天津,1D)( √ )
(3)NH HCO 受热易分解,因而可用作化肥(2019·江苏,3A)( × )
4 3
(4)氨气使AlCl 溶液产生白色沉淀,反应中氨气被还原(2017·北京,8D)( × )
3
2.(2021·江苏,7)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生
2 3
产HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条
3 3
件下,N 与O 反应生成NO,NO进一步氧化生成NO 。2NO(g)+O(g)===2NO (g) ΔH=
2 2 2 2 2
-116.4 kJ·mol-1。大气中过量的NO 和水体中过量的NH、NO均是污染物。通过催化还原
x
的方法,可将烟气和机动车尾气中的NO转化为N ,也可将水体中的NO转化为N 。在指
2 2
定条件下,下列选项所示的物质间转化能实现的是( )
A.NO(g)――→HNO(aq)
3
B.稀HNO(aq)――→NO (g)
3 2
C.NO(g)―――――→N(g)
2
D.NO(aq)――→N(g)
2
答案 C
解析 NO不溶于水也不与水反应,A错误;稀HNO 与Cu反应得到硝酸铜、水和NO,得
3
不到NO ,B错误;NO有氧化性,CO有还原性,在高温、催化剂条件下二者可发生氧化
2
还原反应转化为无毒的N 和CO ,C正确;O 有强氧化性,不能作还原剂将硝酸根离子还
2 2 3
原,D错误。
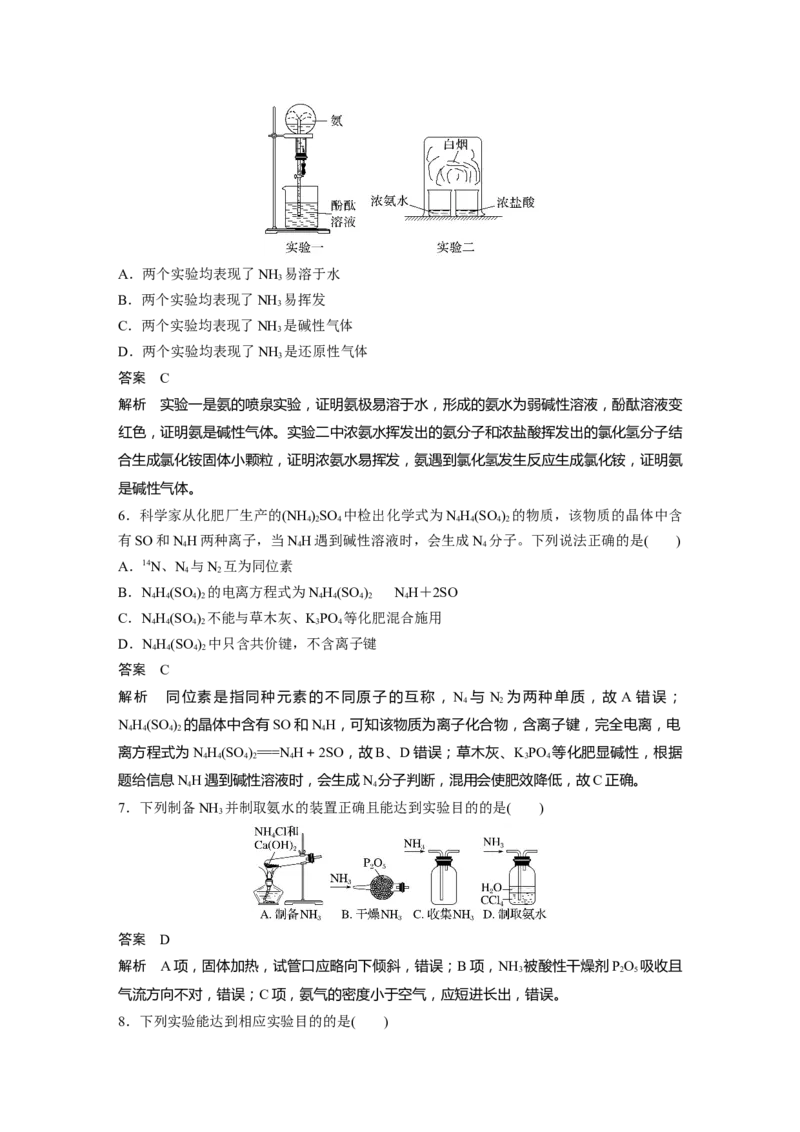
3.(2022·海南,17)磷酸氢二铵[(NH )HPO ]常用于干粉灭火剂。某研究小组用磷酸吸收氨
4 2 4
气制备(NH )HPO ,装置如图所示(夹持和搅拌装置已省略)。
4 2 4
回答问题:
(1)实验室用NH Cl(s)和Ca(OH) (s)制备氨气的化学方程式为____________________。
4 2(2)现有浓 HPO 质量分数为 85%,密度为 1.7 g·mL-1。若实验需 100 mL 1.7 mol·L-1的
3 4
HPO 溶液,则需浓HPO __________ mL(保留一位小数)。
3 4 3 4
(3)装置中活塞K 的作用为________________________________________________。
2
实验过程中,当出现__________________现象时,应及时关闭K,打开K。
1 2
(4)当溶液pH为8.0~9.0时,停止通NH ,即可制得(NH )HPO 溶液。若继续通入NH ,当
3 4 2 4 3
pH>10.0时,溶液中OH-、____________和__________(填离子符号)浓度明显增加。
(5)若本实验不选用 pH 传感器,还可选用______________作指示剂,当溶液颜色由
____________变为__________时,停止通NH 。
3
答案 (1)2NH Cl+Ca(OH) =====CaCl +2HO+2NH ↑ (2)11.5 (3)平衡气压防倒吸 倒
4 2 2 2 3
吸 (4)NH PO (5)酚酞 无色 浅红色
解析 本实验的实验目的为制备磷酸氢二铵[(NH )HPO ],实验原理为 2NH +
4 2 4 3
HPO ===(NH )HPO ,结合相关实验基础知识分析解答问题。(1)实验室用 NH Cl(s)和
3 4 4 2 4 4
Ca(OH) (s)在加热的条件下制备氨气,反应的化学方程式为2NH Cl+Ca(OH) =====CaCl +
2 4 2 2
2HO+2NH ↑。(2)设需浓HPO 的体积为V mL,则=0.1 L×
2 3 3 4
1.7 mol·L-1,V≈11.5。(3)由于NH 极易溶于水,因此可选择打开活塞K 以平衡气压,防止
3 2
发生倒吸,所以实验过程中,当出现倒吸现象时,应及时关闭K ,打开K 。(4)继续通入
1 2
NH ,(NH )HPO 继续反应生成(NH )PO ,当pH>10.0时,溶液中OH-、NH、PO的浓度
3 4 2 4 4 3 4
明显增加。(5)由(4)可知,当pH为8.0~9.0时,可制得(NH )HPO ,说明(NH )HPO 溶液显
4 2 4 4 2 4
碱性,因此若不选用pH传感器,还可以选用酚酞作指示剂,当溶液颜色由无色变为浅红色
时,停止通入NH ,即可制得(NH )HPO 溶液。
3 4 2 4
课时精练
1.清代《本草纲目拾遗》中关于“鼻冲水(氨水)”的记载明确指出:“鼻冲水,……贮以
玻璃瓶,紧塞其口,勿使泄气,则药力不减……唯以此水瓶口对鼻吸其气,即遍身麻颤出汗
而愈,虚弱者忌之。宜外用,勿服。”下列有关“鼻冲水”的推断不正确的是( )
A.鼻冲水是弱电解质
B.鼻冲水滴入酚酞溶液中,溶液变红色
C.鼻冲水中含有分子和离子的种类为6种
D.存在平衡:NH +HONH ·H ONH+OH-
3 2 3 2
答案 A
解析 鼻冲水为氨水,氨水本身为混合物,所以鼻冲水不是弱电解质,故 A错误;氨水中
含有的分子为NH 、HO、NH ·H O,离子有NH、 OH-、H+,共六种,故C正确。
3 2 3 2
2.下列关于氨的说法正确的是( )
A.氨是非电解质,氨水是电解质,NH具有金属阳离子的一些性质B.氨溶于水后,大部分以NH 分子形式存在,所以氨水显弱碱性
3
C.用碱石灰代替消石灰与氯化铵固体加热制取氨气,可使反应速率加快
D.用玻璃棒蘸取浓氨水靠近浓盐酸、浓硝酸和浓硫酸,都可看到有白烟生成
答案 C
解析 选项A,NH 在熔融态不导电,其水溶液导电是由于形成了NH ·H O,故NH 不是电
3 3 2 3
解质,氨水是电解质溶液,而不是电解质,NH能与阴离子形成盐,具有金属阳离子的一些
性质;选项B,氨水呈弱碱性的原因是NH ·H O电离出OH-;选项C,碱石灰中的CaO、
3 2
NaOH吸水能力强,能使反应温度迅速上升,从而加快反应速率;选项D,浓硫酸不是挥发
性酸,故玻璃棒蘸取浓氨水靠近浓硫酸看不到有白烟生成。
3.下列离子方程式书写正确的是( )
A.实验室用氯化铵和熟石灰制氨:NH+OH-=====NH ↑+HO
3 2
B.NaOH溶液与NH Cl溶液混合加热:NH+OH-=====NH ·H O
4 3 2
C.氨水中加盐酸:NH ·H O+H+===NH+HO
3 2 2
D.氨水中加入氯化铁溶液:Fe2++2NH ·H O===2NH+Fe(OH) ↓
3 2 2
答案 C
解析 A项,该反应属于固体间的加热反应,不能书写相应的离子方程式;B项,加热条件
下NH ·H O分解为NH 和HO,离子方程式应为NH+OH-=====NH ↑+HO;D项,向氨
3 2 3 2 3 2
水中滴加FeCl 溶液应生成Fe(OH) 沉淀,离子方程式为Fe3++3NH ·H O===Fe(OH) ↓+
3 3 3 2 3
3NH。
4.某同学探究氨气和铵盐的性质,对相关实验操作及现象描述正确的是( )
A.室温下测定等浓度的氨水和NaOH溶液的pH,比较NH ·H O和NaOH的碱性强弱
3 2
B.向试管中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,若试纸不变蓝,则原
溶液中无NH
C.液氨作为清洁能源的反应原理是4NH +5O=====4NO+6HO
3 2 2
D.加热可除去NH Cl中的少量NaHCO
4 3
答案 A
解析 NH ·H O是弱电解质,NaOH是强电解质,前者部分电离,后者完全电离,故通过室
3 2
温下测定等浓度的氨水和NaOH溶液的pH,可比较NH ·H O和NaOH的碱性强弱,A正确;
3 2
NH 极易溶于水,稀溶液中不加热,NH 不能逸出,无法确定是否含NH,B错误;NH 不
3 3 3
易燃烧,产生的NO是大气污染物,不能作清洁能源,C错误;NH Cl受热也会分解,故不
4
可采用加热法除杂,D错误。
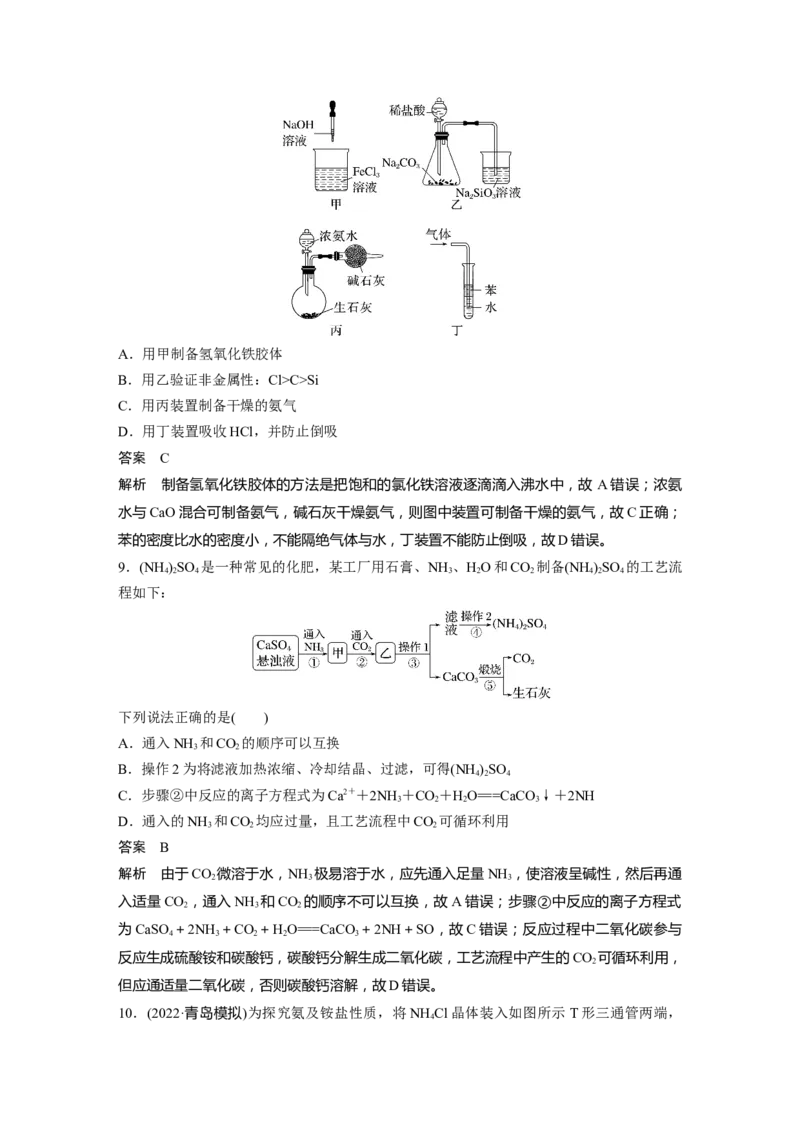
5.如图所示是NH 的两个性质实验,下列有关说法正确的是( )
3A.两个实验均表现了NH 易溶于水
3
B.两个实验均表现了NH 易挥发
3
C.两个实验均表现了NH 是碱性气体
3
D.两个实验均表现了NH 是还原性气体
3
答案 C
解析 实验一是氨的喷泉实验,证明氨极易溶于水,形成的氨水为弱碱性溶液,酚酞溶液变
红色,证明氨是碱性气体。实验二中浓氨水挥发出的氨分子和浓盐酸挥发出的氯化氢分子结
合生成氯化铵固体小颗粒,证明浓氨水易挥发,氨遇到氯化氢发生反应生成氯化铵,证明氨
是碱性气体。
6.科学家从化肥厂生产的(NH )SO 中检出化学式为NH(SO ) 的物质,该物质的晶体中含
4 2 4 4 4 4 2
有SO和NH两种离子,当NH遇到碱性溶液时,会生成N 分子。下列说法正确的是( )
4 4 4
A.14N、N 与N 互为同位素
4 2
B.NH(SO ) 的电离方程式为NH(SO )NH+2SO
4 4 4 2 4 4 4 2 4
C.NH(SO ) 不能与草木灰、KPO 等化肥混合施用
4 4 4 2 3 4
D.NH(SO ) 中只含共价键,不含离子键
4 4 4 2
答案 C
解析 同位素是指同种元素的不同原子的互称,N 与 N 为两种单质,故 A 错误;
4 2
NH(SO ) 的晶体中含有SO和NH,可知该物质为离子化合物,含离子键,完全电离,电
4 4 4 2 4
离方程式为NH(SO )===NH+2SO,故B、D错误;草木灰、KPO 等化肥显碱性,根据
4 4 4 2 4 3 4
题给信息NH遇到碱性溶液时,会生成N 分子判断,混用会使肥效降低,故C正确。
4 4
7.下列制备NH 并制取氨水的装置正确且能达到实验目的的是( )
3
答案 D
解析 A项,固体加热,试管口应略向下倾斜,错误;B项,NH 被酸性干燥剂PO 吸收且
3 2 5
气流方向不对,错误;C项,氨气的密度小于空气,应短进长出,错误。
8.下列实验能达到相应实验目的的是( )A.用甲制备氢氧化铁胶体
B.用乙验证非金属性:Cl>C>Si
C.用丙装置制备干燥的氨气
D.用丁装置吸收HCl,并防止倒吸
答案 C
解析 制备氢氧化铁胶体的方法是把饱和的氯化铁溶液逐滴滴入沸水中,故 A错误;浓氨
水与CaO混合可制备氨气,碱石灰干燥氨气,则图中装置可制备干燥的氨气,故C正确;
苯的密度比水的密度小,不能隔绝气体与水,丁装置不能防止倒吸,故D错误。
9.(NH )SO 是一种常见的化肥,某工厂用石膏、NH 、HO和CO 制备(NH )SO 的工艺流
4 2 4 3 2 2 4 2 4
程如下:
下列说法正确的是( )
A.通入NH 和CO 的顺序可以互换
3 2
B.操作2为将滤液加热浓缩、冷却结晶、过滤,可得(NH )SO
4 2 4
C.步骤②中反应的离子方程式为Ca2++2NH +CO+HO===CaCO ↓+2NH
3 2 2 3
D.通入的NH 和CO 均应过量,且工艺流程中CO 可循环利用
3 2 2
答案 B
解析 由于CO 微溶于水,NH 极易溶于水,应先通入足量NH ,使溶液呈碱性,然后再通
2 3 3
入适量CO ,通入NH 和CO 的顺序不可以互换,故A错误;步骤②中反应的离子方程式
2 3 2
为CaSO +2NH +CO +HO===CaCO +2NH+SO,故C错误;反应过程中二氧化碳参与
4 3 2 2 3
反应生成硫酸铵和碳酸钙,碳酸钙分解生成二氧化碳,工艺流程中产生的CO 可循环利用,
2
但应通适量二氧化碳,否则碳酸钙溶解,故D错误。
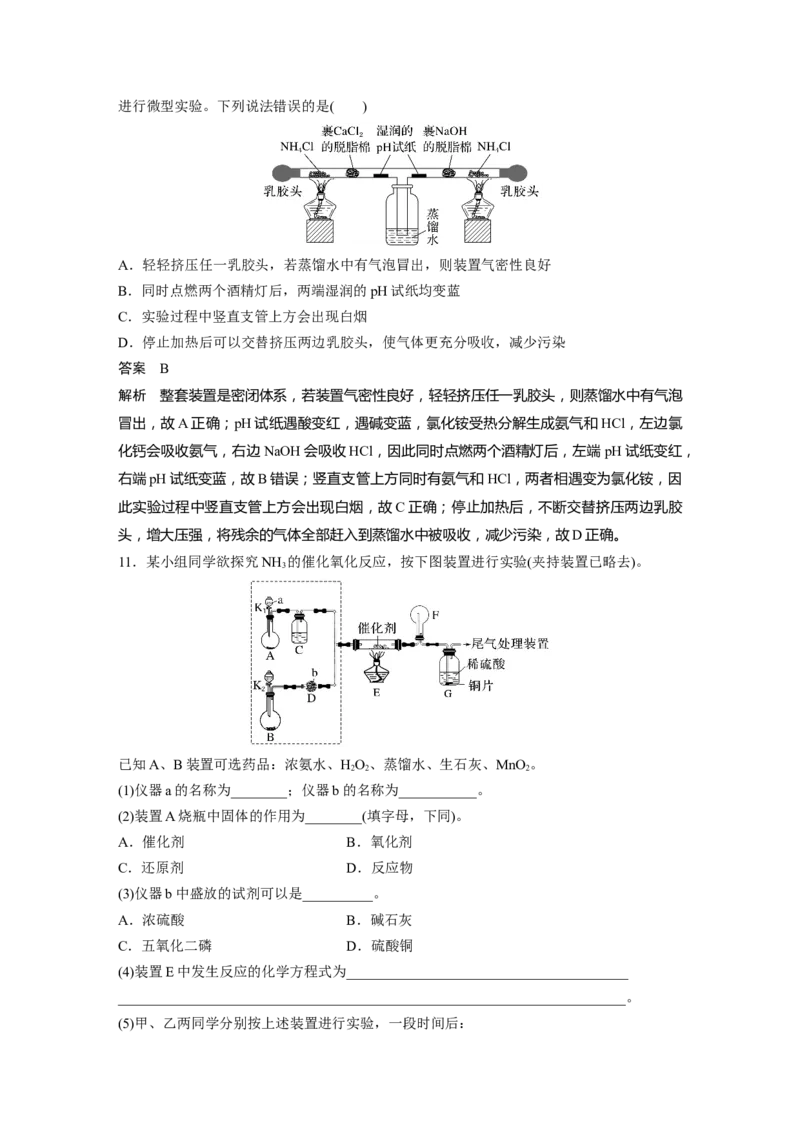
10.(2022·青岛模拟)为探究氨及铵盐性质,将NH Cl晶体装入如图所示T形三通管两端,
4进行微型实验。下列说法错误的是( )
A.轻轻挤压任一乳胶头,若蒸馏水中有气泡冒出,则装置气密性良好
B.同时点燃两个酒精灯后,两端湿润的pH试纸均变蓝
C.实验过程中竖直支管上方会出现白烟
D.停止加热后可以交替挤压两边乳胶头,使气体更充分吸收,减少污染
答案 B
解析 整套装置是密闭体系,若装置气密性良好,轻轻挤压任一乳胶头,则蒸馏水中有气泡
冒出,故A正确;pH试纸遇酸变红,遇碱变蓝,氯化铵受热分解生成氨气和HCl,左边氯
化钙会吸收氨气,右边NaOH会吸收HCl,因此同时点燃两个酒精灯后,左端pH试纸变红,
右端pH试纸变蓝,故B错误;竖直支管上方同时有氨气和HCl,两者相遇变为氯化铵,因
此实验过程中竖直支管上方会出现白烟,故C正确;停止加热后,不断交替挤压两边乳胶
头,增大压强,将残余的气体全部赶入到蒸馏水中被吸收,减少污染,故D正确。
11.某小组同学欲探究NH 的催化氧化反应,按下图装置进行实验(夹持装置已略去)。
3
已知A、B装置可选药品:浓氨水、HO、蒸馏水、生石灰、MnO 。
2 2 2
(1)仪器a的名称为________;仪器b的名称为___________。
(2)装置A烧瓶中固体的作用为________(填字母,下同)。
A.催化剂 B.氧化剂
C.还原剂 D.反应物
(3)仪器b中盛放的试剂可以是__________。
A.浓硫酸 B.碱石灰
C.五氧化二磷 D.硫酸铜
(4)装置E中发生反应的化学方程式为________________________________________
________________________________________________________________________。
(5)甲、乙两同学分别按上述装置进行实验,一段时间后:①甲观察到装置F中只有白烟生成,白烟的成分是______(写化学式)。
②乙观察到装置F中有红棕色气体,装置G中溶液变成蓝色。用离子方程式解释装置G中
溶液变成蓝色的原因: ____________________________________________________。
(6)为帮助甲实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。
你的改进措施是_________________________________________________________
________________________________________________________________________。
答案 (1)分液漏斗 球形干燥管 (2)A (3)B
(4)4NH +5O=====4NO+6HO
3 2 2
(5)①NH NO ②3Cu+8H++2NO===3Cu2++2NO↑+4HO
4 3 2
(6)调节K 增加装置A中产生氧气的量或调节K 减少装置B中产生氨气的量或在E、F间增
1 2
加浓硫酸的洗气装置
解析 (5)①白烟是固体小颗粒,是NH 和HNO(NO、O 、HO共同反应生成)反应生成的
3 3 2 2
NH NO 固体。②反应生成的NO与O 反应生成红棕色的NO ,Cu与稀硫酸不反应,G中溶
4 3 2 2
液变蓝说明Cu被氧化为Cu2+,原因是通入装置G中的NO 和HO反应生成HNO 和NO,
2 2 3
HNO 与Cu反应的离子方程式为3Cu+8H++2NO===3Cu2++2NO↑+4HO。(6)甲的实验
3 2
中只观察到白烟,是因为NH 未被完全催化氧化;要保证NH 充分被氧化,则O 需过量,
3 3 2
所以需增加O 的量或减少NH 的量;可调节K 增加装置A中的产气量或调节K 减少装置B
2 3 1 2
中的产气量,使NH 充分被氧化;也可以在E、F间增加浓硫酸的洗气装置,吸收未反应的
3
氨气。
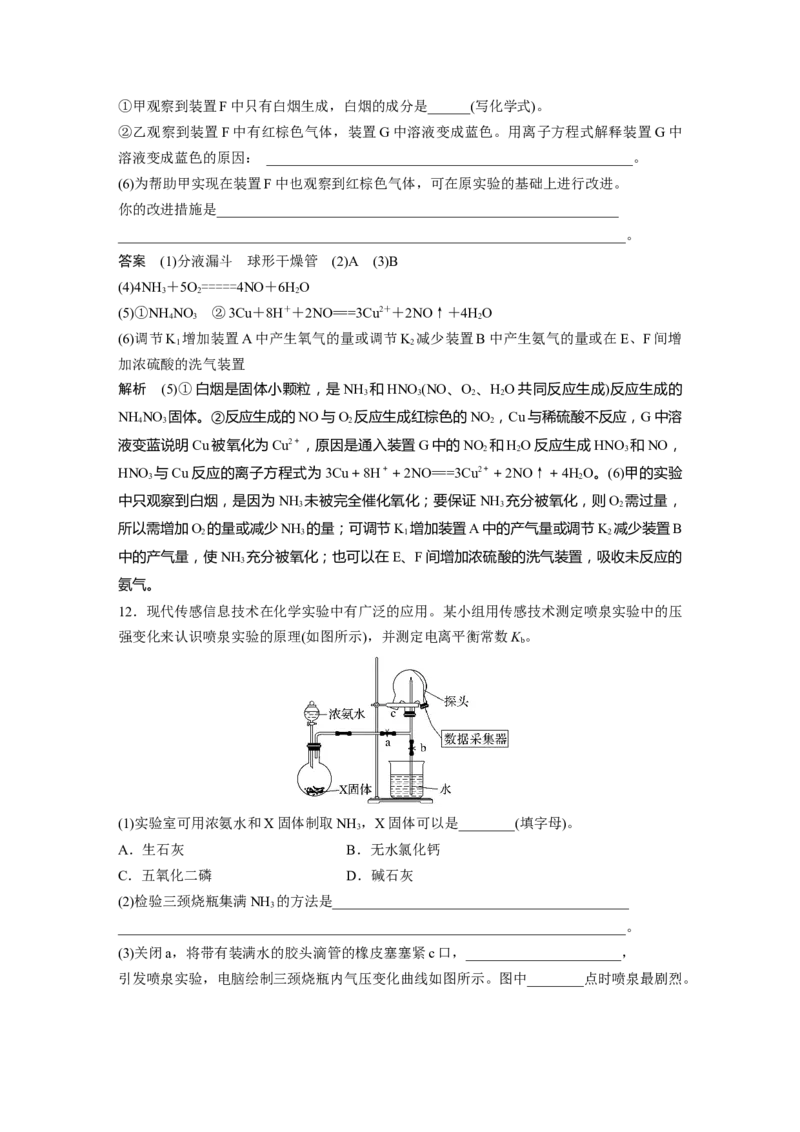
12.现代传感信息技术在化学实验中有广泛的应用。某小组用传感技术测定喷泉实验中的压
强变化来认识喷泉实验的原理(如图所示),并测定电离平衡常数K 。
b
(1)实验室可用浓氨水和X固体制取NH ,X固体可以是________(填字母)。
3
A.生石灰 B.无水氯化钙
C.五氧化二磷 D.碱石灰
(2)检验三颈烧瓶集满NH 的方法是__________________________________________
3
________________________________________________________________________。
(3)关闭a,将带有装满水的胶头滴管的橡皮塞塞紧c口,______________________,
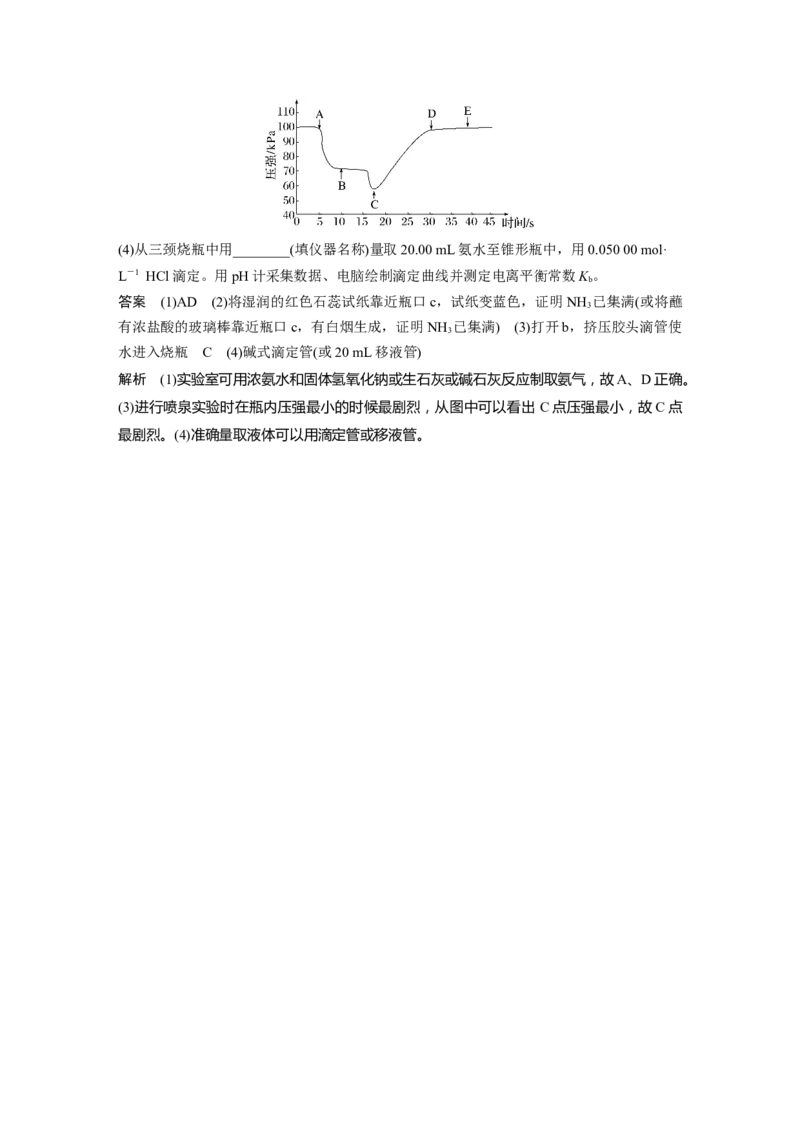
引发喷泉实验,电脑绘制三颈烧瓶内气压变化曲线如图所示。图中________点时喷泉最剧烈。(4)从三颈烧瓶中用________(填仪器名称)量取20.00 mL氨水至锥形瓶中,用0.050 00 mol·
L-1 HCl滴定。用pH计采集数据、电脑绘制滴定曲线并测定电离平衡常数K 。
b
答案 (1)AD (2)将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明NH 已集满(或将蘸
3
有浓盐酸的玻璃棒靠近瓶口c,有白烟生成,证明NH 已集满) (3)打开b,挤压胶头滴管使
3
水进入烧瓶 C (4)碱式滴定管(或20 mL移液管)
解析 (1)实验室可用浓氨水和固体氢氧化钠或生石灰或碱石灰反应制取氨气,故A、D正确。
(3)进行喷泉实验时在瓶内压强最小的时候最剧烈,从图中可以看出 C点压强最小,故C点
最剧烈。(4)准确量取液体可以用滴定管或移液管。