文档内容
课时检测(三十一) 无机化学工艺流程
1.(2024·江西赣州高三质检)钪(Sc)是一种稀土金属,从钛白酸性废水(主要含有Ti4+、Fe2+,还含
有微量Sc3+)中富集钪,并制备氧化钪(Sc O)的工艺流程如图所示[已知:Ti(OH) 、Sc(OH) 均难溶于
2 3 4 3
水]。下列说法错误的是( )
A.酸洗时加入HO 的目的是将Fe2+氧化为Fe3+
2 2
B.实验室进行“操作Ⅰ”需要的玻璃仪器有烧杯、玻璃棒、漏斗
C.“滤渣Ⅰ”的成分是Ti(OH) 、Fe(OH)
4 3
D.草酸钪焙烧时反应的化学方程式:
2Sc (C O)+3O=====2Sc O+12CO
2 2 4 3 2 2 3 2
2.(2024·长沙高三模拟)从废旧铅蓄电池铅膏(主要含PbSO 和PbO 等,还有少量Fe、Al的盐或
4 2
氧化物等)中回收铅的工艺流程如下:
下列说法正确的是( )
A.PbSO 和(NH)CO 溶液反应的离子方程式:Pb2++CO===PbCO ↓
4 4 2 3 3
B.HO 的主要作用是作氧化剂,氧化Fe2+
2 2
C.对于BF离子,其中心原子的杂化方式为sp2
D.电解时,阳极、阴极材料可分别用石墨、铅
3.(2023·山东等级考·改编)一种制备Cu O的工艺路线如图所示,反应Ⅱ所得溶液pH在3~4之
2
间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。常温下,HSO 的电离平衡常数K =
2 3 a1
1.3×10-2,K =6.3×10-8。下列说法不正确的是( )
a2
A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.低温真空蒸发主要目的是防止Na SO 被氧化
2 3
C.溶液Y可循环用于反应Ⅱ所在操作单元中吸收气体ⅠD.若Cu O产量不变,参与反应Ⅲ的X与CuSO 物质的量之比增大时,需补加NaOH的量减少
2 4
4.(2023·潍坊高三模拟)锰及其化合物用途广泛,以菱锰矿(主要成分为MnCO ,还含有铁、镍、钴
3
的碳酸盐以及SiO 杂质)为原料生产金属锰和高品位MnCO 的工艺流程如图所示:
2 3
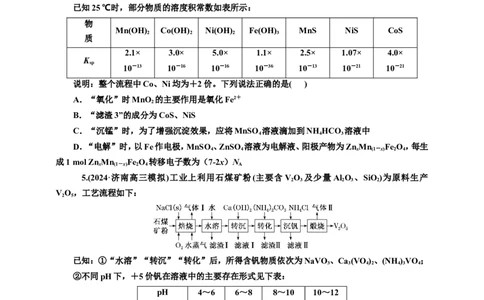
已知25 ℃时,部分物质的溶度积常数如表所示:
物
Mn(OH) Co(OH) Ni(OH) Fe(OH) MnS NiS CoS
2 2 2 3
质
2.1× 3.0× 5.0× 1.1× 2.5× 1.07× 4.0×
K
sp
10-13 10-16 10-16 10-36 10-13 10-21 10-21
说明:整个流程中Co、Ni均为+2价。下列说法正确的是( )
A.“氧化”时MnO 的主要作用是氧化Fe2+
2
B.“滤渣3”的成分为CoS、NiS
C.“沉锰”时,为了增强沉淀效果,应将MnSO 溶液滴加到NH HCO 溶液中
4 4 3
D.“电解”时,以Fe作电极,MnSO 、ZnSO 溶液为电解液、阳极产物为ZnMn FeO,每生
4 4 x (1-x) 2 4
成1 mol Zn Mn FeO 转移电子数为(7-2x)N
x (1-x) 2 4 A
5.(2024·济南高三模拟)工业上利用石煤矿粉(主要含VO 及少量Al O 、SiO )为原料生产
2 3 2 3 2
VO,工艺流程如下:
2 5
已知:①“水溶”“转沉”“转化”后,所得含钒物质依次为NaVO、Ca (VO)、(NH)VO;
3 3 4 2 4 3 4
②不同pH下,+5价钒在溶液中的主要存在形式见下表:
pH 4~6 6~8 8~10 10~12
主要离子 VO VO VO VO
2
③25 ℃时,K (NHVO)=1.6×10-3。
sp 4 3
回答下列问题:
(1)“焙烧”时,VO 发生反应的化学方程式为__________________________________
2 3
________________________________________________________________________。
(2)滤液Ⅰ的成分为________________(填化学式);先“转沉”后“转化”的目的是
________________________________________________________________________。
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入________操作单元中循环使用。
(4)“ 沉 钒 ” 中 析 出 NH VO 晶 体 时 , 需 要 加 入 过 量 NH Cl , 其 原 因 是
4 3 4
①________________________________________________________________________,②________________________________________________________________________;
25 ℃时,测得“转化”后,滤液中c(VO)=0.2 mol·L-1,为使“沉钒”时,钒元素的沉降率达到
96%,应调节溶液中c(NH)至少_______mol·L-1 。
(5)“煅烧”时,NH VO 制得产品VO。但反应体系中,若不及时分离气体Ⅱ,部分VO 会转化成
4 3 2 5 2 5
VO , 反 应 中 氧 化 剂 与 还 原 剂 物 质 的 量 之 比 为 3∶ 2 , 该 反 应 的 化 学 方 程 式 为
2 4
________________________________________________________________________
________________________________________________________________________。
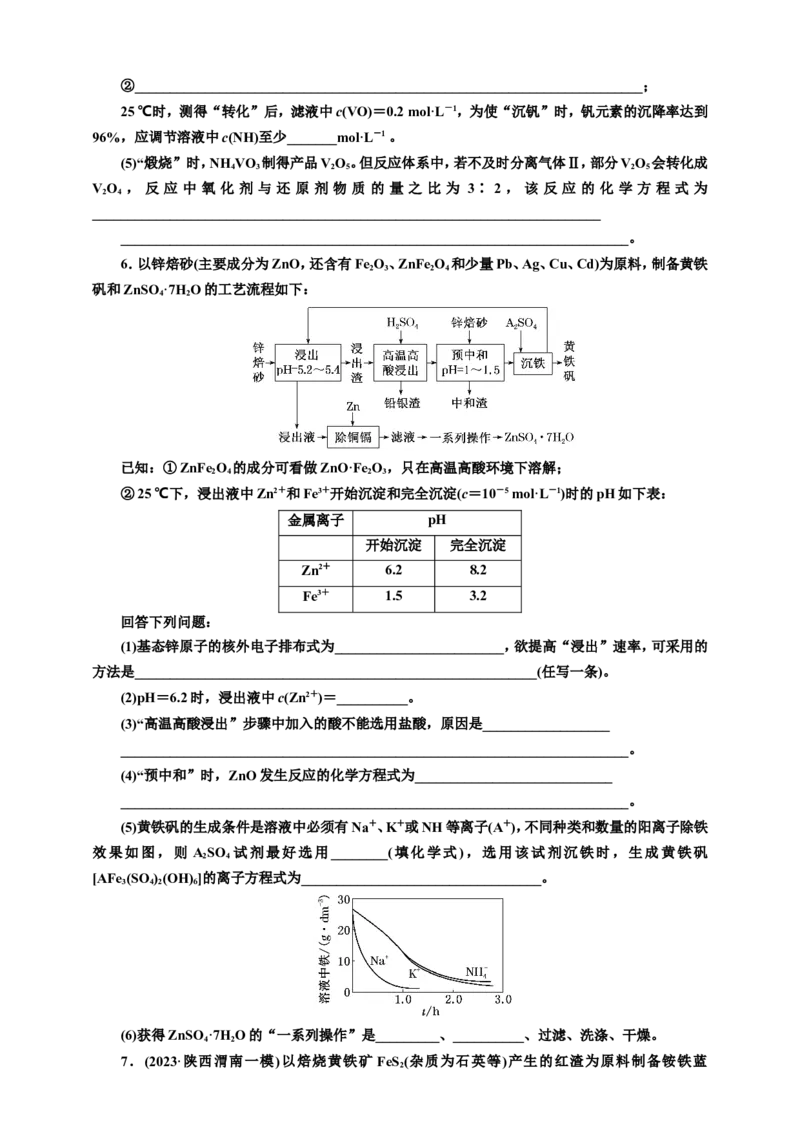
6.以锌焙砂(主要成分为ZnO,还含有FeO、ZnFe O 和少量Pb、Ag、Cu、Cd)为原料,制备黄铁
2 3 2 4
矾和ZnSO ·7HO的工艺流程如下:
4 2
已知:①ZnFe O 的成分可看做ZnO·Fe O,只在高温高酸环境下溶解;
2 4 2 3
②25 ℃下,浸出液中Zn2+和Fe3+开始沉淀和完全沉淀(c=10-5 mol·L-1)时的pH如下表:
金属离子 pH
开始沉淀 完全沉淀
Zn2+ 6.2 8.2
Fe3+ 1.5 3.2
回答下列问题:
(1)基态锌原子的核外电子排布式为________________________,欲提高“浸出”速率,可采用的
方法是_________________________________________________________(任写一条)。
(2)pH=6.2时,浸出液中c(Zn2+)=__________。
(3)“高温高酸浸出”步骤中加入的酸不能选用盐酸,原因是__________________
________________________________________________________________________。
(4)“预中和”时,ZnO发生反应的化学方程式为____________________________
________________________________________________________________________。
(5)黄铁矾的生成条件是溶液中必须有Na+、K+或NH等离子(A+),不同种类和数量的阳离子除铁
效果如图,则 ASO 试剂最好选用________(填化学式),选用该试剂沉铁时,生成黄铁矾
2 4
[AFe (SO )(OH) ]的离子方程式为__________________________________。
3 4 2 6
(6)获得ZnSO ·7HO的“一系列操作”是_________、__________、过滤、洗涤、干燥。
4 2
7.(2023·陕西渭南一模)以焙烧黄铁矿 FeS (杂质为石英等)产生的红渣为原料制备铵铁蓝
2Fe(NH)Fe(CN) 颜料,工艺流程如下:
4 6
回答下列问题:
(1)红渣的主要成分为____________,滤渣①的主要成分为____________。(填化学式)
(2)黄铁矿研细的目的是______________________________________________
________________________________________________________________________。
(3)还原工序中,不生成S单质的反应的化学方程式为_______________________。
(4)工序①的名称为__________________________,所得母液循环使用。
(5)沉铁工序产生的白色沉淀Fe(NH)Fe(CN) 中Fe的化合价为__________,氧化工序发生反应
4 2 6
的离子方程式为_________________________________________________
________________________________________________________________________。
(6)若用还原工序得到的滤液制备FeO·xHO和(NH)SO ,所加试剂为________和
2 3 2 4 2 4
__________(填化学式,不引入杂质)。
课时检测(三十一)
1.C 从钛白酸性废水(主要含有Ti4+、Fe2+,还含有微量Sc3+)中富集钪,酸洗时加入HO 的目的
2 2
是将Fe2+氧化为Fe3+,加入氢氧化钠溶液进行反萃取,过滤得到“滤渣Ⅰ”的主要成分是Ti(OH) 、
4
Fe(OH) 、Sc(OH) ,然后加入10%盐酸调pH溶解Sc(OH) 。转化为含Sc3+的溶液,再加入草酸溶液得
3 3 3
到草酸钪,草酸钪与氧气焙烧时反应生成Sc O 和CO ,酸洗时加入HO 的目的是将Fe2+氧化为Fe3
2 3 2 2 2
+,A正确;由流程可知,“操作Ⅰ”是过滤,过滤操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,B正确;
“滤渣Ⅰ”的主要成分是Ti(OH) 、Fe(OH) 、Sc(OH) ,C错误;草酸钪与氧气焙烧时反应生成Sc O 和
4 3 3 2 3
CO ,反应的化学方程式:2Sc (C O)+3O=====2Sc O+12CO ,D正确。
2 2 2 4 3 2 2 3 2
2.D PbSO 与Na CO 溶液反应生成更难溶的PbCO ,转化后生成的碳酸铅可由酸浸进入溶液
4 2 3 3
中,转化反应的离子方程式:PbSO (s)+CO(aq)===PbCO (s)+SO(aq),A错误;第一步“溶浸”中
4 3
PbO 中Pb元素的化合价降低,PbO 作氧化剂,HO 作还原剂,B错误;对于BF,其中心原子的价层
2 2 2 2
电子对数为4,杂化方式为sp3,C错误;电解四氟合硼酸铅溶液时,石墨是电解池的阳极,铅是阴极,铅
离子在阴极得到电子发生还原反应生成铅,D正确。
3.A 反应Ⅱ所得溶液pH在3~4之间,则反应Ⅱ为SO 和Na CO 溶液反应生成NaHSO 和
2 2 3 3
CO ,为非氧化还原反应,A错误;反应Ⅱ得到NaHSO 溶液,调pH=11时NaHSO 转化为Na SO ,故
2 3 3 2 3
低温真空蒸发主要目的是防止Na SO 被氧化,B正确;溶液Y含少量Na SO ,可循环用于反应Ⅱ所在
2 3 2 3
操作单元中吸收SO 气体生成NaHSO ,C正确;化合物X为Na SO ,当Na SO 少量时,反应Ⅲ为
2 3 2 3 2 3
2CuSO +Na SO +2HO===Cu O↓+Na SO +2HSO ,当 Na SO 过量时,反应Ⅲ为 2CuSO +
4 2 3 2 2 2 4 2 4 2 3 4
3Na SO ===Cu O↓+3Na SO +2SO ↑,生成的SO 气体会逸出,故当增大时,需补加NaOH的量减少,
2 3 2 2 4 2 2D正确。
4.A “溶浸”时,碳酸盐转变为可溶的硫酸盐,加入MnO “氧化”是为了将Fe2+转化为Fe3+;
2
溶液中Fe2+不易沉淀,转化为Fe3+易沉淀除去,A项正确。“除杂”后的滤液中有Co2+和Ni2+,则
MnS将它们转化为CoS和NiS除去;滤渣3中含有MnS、CoS和NiS,B项错误。NH HCO 溶液呈碱
4 3
性,Mn2+易发生水解而损失,C项错误。ZnMn FeO 中Zn、Mn化合价均为+2价,根据物质化合
x (1-x) 2 4
价代数和为0计算,Fe化合价为+3,即每生成1 mol Zn Mn FeO 转移6 mol电子,D项错误。
x (1-x) 2 4
5.解析:石煤矿粉(主要含VO 及少量Al O、SiO ),加入O、HO和NaCl固体,将VO 氧化成
2 3 2 3 2 2 2 2 3
NaVO,生成的气体为HCl,加水溶解,滤渣Ⅰ为Al O、SiO ,滤液为NaVO 水溶液,加入Ca(OH) 将
3 2 3 2 3 2
NaVO 转化为沉淀Ca (VO),可以富集钒元素,再加入(NH)CO 除去Ca2+,最后加入过量NH Cl,
3 3 4 2 4 2 3 4
可以调节pH,将VO转化为VO,也可以促进NH VO 尽可能析出完全,煅烧NH VO 生成VO 。
4 3 4 3 2 5
(1)“焙烧”时,VO 被氧化生成 NaVO ,发生反应的化学方程式为 VO +O +2NaCl+
2 3 3 2 3 2
HO=====2NaVO +2HCl。(2)在 NaVO 溶液中加入 Ca(OH) 形成沉淀,滤液Ⅰ的主要成分为
2 3 3 2
NaOH;先“转沉”后“转化”的目的是富集钒元素。(3)“转化”时,滤渣Ⅱ为CaCO ,经高温煅烧生
3
成CaO再水浸后生成Ca(OH) ,可以导入“转沉”中循环利用。(4)“沉钒”中析出NH VO 晶体时,加
2 4 3
入过量NH Cl是为了调节pH,将VO转化为VO,还可以利用同离子效应,促进NH VO 尽可能析出
4 4 3
完全;K (NHVO)=1.6×10-3,溶液中的c(VO)=0.2 mol·L-1×(1-0.96)=8×10-3 mol·L-1,c(NH)==
sp 4 3
=0.2 mol·L-1。(5)根据题目信息,“煅烧”NH VO 制得产品VO 时,VO 与分解产物NH 反应的化
4 3 2 5 2 5 3
学方程式为3VO+2NH =====3VO+N+3HO。
2 5 3 2 4 2 2
答案:(1)V O+O+2NaCl+HO=====2NaVO+2HCl
2 3 2 2 3
(2)NaOH 富集钒元素 (3)转沉
(4)①调节pH,将VO转化为VO
②利用同离子效应,促进NH VO 尽可能析出完全 0.2
4 3
(5)3V O+2NH =====3VO+N+3HO
2 5 3 2 4 2 2
6.解析:以锌焙砂(主要成分为ZnO,还含有FeO、ZnFe O 和少量Pb、Ag、Cu、Cd)为原料,调节
2 3 2 4
pH=5.2~5.4进行浸出,浸出液加锌除铜镉,所得滤液经一系列操作(蒸发浓缩、冷却结晶、过滤、洗涤、
干燥)得到ZnSO ·7HO;浸出渣加入硫酸在高温高酸条件下浸出铅银渣,浸出液加入锌焙砂预中和除
4 2
去中和渣,滤液加入硫酸钠沉铁,得到黄铁矾。(1)Zn原子基态核外电子排布式为1s22s22p63s23p63d104s2
或[Ar]3d104s2;酸浸时一般要将锌焙砂粉碎,其目的是提高酸浸效率,为达到这一目的,可以采用的方
法是粉碎、搅拌、升温、适当增大酸的浓度等。(2)pH=8.2时,c(OH-)=10-5.8 mol·L-1,根据K [Zn(OH)]
sp 2
=c(Zn2+)·c2(OH-)=10-5×(10-5.8)2=10-16.6;pH=6.2时,c(OH-)=10-7.8 mol·L-1,根据K [Zn(OH) ]
sp 2
=
c(Zn2+)·c2(OH-)=c(Zn2+)×(10-7.8)2=10-16.6,可知浸出液中c(Zn2+)=0.1 mol·L-1。(3)ZnFe O 具有强
2 4
氧化性,“高温高酸浸出”步骤中加入的酸若为盐酸,会被氧化生成氯气引起污染。(4)“预中和”时,
ZnO 与高温高酸浸出液中的硫酸反应生成硫酸锌和水,发生反应的化学方程式为 ZnO+
HSO ===ZnSO +HO。(5)黄铁矾的生成条件是溶液中必须有Na+、K+或NH等离子(A+),由不同种
2 4 4 2
类和数量的阳离子除铁效果图可知,选用Na SO 时用时短,除铁效果也好,故试剂最好选用Na SO ,
2 4 2 4
选用该试剂沉铁时,生成黄铁矾[AFe (SO )(OH) ]的离子方程式为 Na++3Fe3++2SO+6OH-
3 4 2 6
===NaFe(SO )(OH) ↓。(6)由溶液中得到晶体,获得ZnSO ·7HO的“一系列操作”是蒸发浓缩、冷却
3 4 2 6 4 2
结晶、过滤、洗涤、干燥。答案:(1)1s22s22p63s23p63d104s2 粉碎、搅拌、升温、适当增大酸的浓度等(任写一条)
(2)0.1 mol·L-1
(3)ZnFe O 具有强氧化性,“高温高酸浸出”步骤中加入的酸若为盐酸,会被氧化生成氯气引起
2 4
污染
(4)ZnO+HSO ===ZnSO +HO
2 4 4 2
(5)Na SO Na++3Fe3++2SO+6OH-===NaFe(SO )(OH) ↓
2 4 3 4 2 6
(6)蒸发浓缩 冷却结晶
7.解析:已知黄铁矿高温煅烧生成FeO,反应原理为4FeS +11O=====2FeO+8SO ,故产生
2 3 2 2 2 3 2
的红渣主要成分为FeO 和SiO ,将红渣粉碎后加入足量的50%的HSO 溶液加热充分酸浸,反应原
2 3 2 2 4
理为FeO+3HSO ===Fe (SO )+3HO,过滤出滤渣①,主要成分为SiO ,向滤液中加入黄铁矿进行
2 3 2 4 2 4 3 2 2
还原,将Fe3+还原为Fe2+,由(3)小问可知不生成S沉淀,则硫元素被氧化为SO,反应原理为14Fe3++
FeS +8HO===15Fe2++2SO+16H+,然后进行工序①为蒸发浓缩、冷却结晶,得到FeSO 晶体和母
2 2 4
液(主要含有 FeSO 溶液和 HSO ,可以循环利用),加水溶解 FeSO 晶体,向所得溶液中加入
4 2 4 4
(NH)SO 、K[Fe(CN) ]并用HSO 调节溶液的pH为3,进行沉铁过程,反应原理为Fe2++2NH+
4 2 4 4 6 2 4
[Fe(CN) ]4-===Fe(NH )Fe(CN) ↓,然后过滤出沉淀,洗涤后加入HSO 和NaClO 进行氧化步骤,反
6 4 2 6 2 4 3
应原理为6Fe(NH)Fe(CN) +ClO+6H+===6Fe(NH )Fe(CN) +3HO+Cl-+6NH,过滤、洗涤干燥
4 2 6 4 6 2
即制得Fe(NH)Fe(CN) 。(6)还原工序所得的滤液中主要含有FeSO 溶液和HSO ,向滤液中先加入一
4 6 4 2 4
定量的HO 溶液将Fe2+完全氧化为Fe3+,再向氧化后的溶液中加入氨水至不再产生沉淀为止,过滤
2 2
洗涤,对沉淀进行灼烧,即可制得 FeO·xHO 和(NH)SO ,故所需要加入的试剂为 HO 和
2 3 2 4 2 4 2 2
NH ·HO。
3 2
答案:(1)Fe O 和SiO SiO
2 3 2 2
(2)增大固液接触面积,加快反应速率,提高黄铁矿的利用率
(3)7Fe (SO )+FeS +8HO===15FeSO +8HSO
2 4 3 2 2 4 2 4
(4)蒸发浓缩、冷却结晶、过滤洗涤 (5)+2
6Fe(NH)Fe(CN) +ClO+6H+===6Fe(NH )Fe(CN) +3HO+Cl-+6NH (6)H O NH ·HO
4 2 6 4 6 2 2 2 3 2