文档内容
课时检测(三十六) 分子结构与性质的基本知能评价
1.(2023·浙江6月选考)下列化学用语表示正确的是( )
A.HS分子的球棍模型:
2
B.AlCl 的价层电子对互斥模型:
3
C.KI的电子式:
D.CH CH(CH CH ) 的名称:3甲基戊烷
3 2 3 2
2.
某课题组发现水团簇最少需要21个水分子才能实现溶剂化,即1个水分子周围至少需要20个水
分子才能将其“溶解”(“溶解”时,水团簇须形成四面体)。下列叙述正确的是( )
A.(H O) 中水分子之间的作用力主要是氢键
2 21
B.(H O) 和(H O) 互为同系物
2 21 2 23
C.加热(H O) 变为(H O) 还破坏了极性键
2 23 2 19
D.(H O) 晶体属于共价晶体
2 21
3.徐光宪在《分子共和国》一书中介绍了许多明星分子,如HO、CO 、BF 、CH COOH等。下列
2 2 2 3 3
说法正确的是( )
A.HO 分子中H—O—O键的键角为109°28′
2 2
B.CO 分子中的C为sp杂化
2
C.BF 分子中的B为sp3杂化
3
D.1 mol CH COOH分子中含有1 mol π键和6 mol σ键
3
4.用价层电子对互斥模型(VSEPR)可以预测许多分子或离子的空间结构,有时也能用来推测键角
大小,下列判断正确的是( )
A.SO 、CS 、HI都是直线形分子
2 2
B.BF 键角为120°,SnBr 键角大于120°
3 2
C.COCl 、BF 、SO 都是平面三角形分子
2 3 3
D.PCl 、NH 、PCl 都是三角锥形分子
3 3 5
5.(2023·重庆等级考)NCl 和SiCl 均可发生水解反应,其中NCl 的水解机理示意图如下:
3 4 3下列说法正确的是( )
A.NCl 和SiCl 均为极性分子
3 4
B.NCl 和NH 中的N均为sp2杂化
3 3
C.NCl 和SiCl 的水解反应机理相同
3 4
D.NHCl 和NH 均能与HO形成氢键
2 3 2
6.(2023·北京等级考)下列事实不能通过比较氟元素和氯元素的电负性进行解释的是( )
A.F—F键的键能小于Cl—Cl键的键能
B.三氟乙酸的K 大于三氯乙酸的K
a a
C.氟化氢分子的极性强于氯化氢分子的极性
D.气态氟化氢中存在(HF) ,而气态氯化氢中是HCl分子
2
7.(2023·全国新课标卷)一种可吸附甲醇的材料,其化学式为[C(NH )][B(OCH )]Cl,部分晶体
2 3 4 3 4 3
结构如图所示,其中[C(NH )]+为平面结构。
2 3
下列说法正确的是( )
A.该晶体中存在N—H…O氢键
B.基态原子的第一电离能:C”“<” 或 “ = ” ) 。 比 较 ClO 与 Cl O 中 Cl—O 键 的 键 长 并 说 明 原 因 :
2 2
________________________________________________________________________
________________________________________________________________________ 。
(3)(2022·全国乙卷·节选)①一氯乙烯(C HCl)分子中,C的一个________杂化轨道与Cl的3p 轨
2 3 x
道形成C—Cl________键,并且Cl的3p 轨道与C的2p 轨道形成3中心、4电子的大π键(Π)。
z z
②一氯乙烷(C HCl)、一氯乙烯(C HCl)、一氯乙炔(C HCl)分子中,C—Cl 键长的顺序是
2 5 2 3 2
____________________________________________,理由:(ⅰ)C的杂化轨道中s成分越多,形成的C
—Cl键越强;(ⅱ)_______________________________________________
________________________________________________________________________。
(4)(2022·湖南等级考·节选)①富马酸亚铁(FeC HO)是一种补铁剂。富马酸分子的结构模型如图所示。
4 2 4
富马酸分子中σ键与π键的数目比为________。
②科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H,将N3-转化
2
为NH,反应过程如图所示:
产物中 N 的杂化轨道类型为________________;与 NH 互为等电子体的一种分子为
__________(填化学式)。
13.氯吡苯脲是一种常用的膨大剂,其结构简式为 ,它是经国家批准使用的植物
生长调节剂。
(1)氯元素基态原子核外电子的未成对电子数为________。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为_______,羰基碳原子的杂化轨道类型为________。
(3)查文献可知,可用2氯4氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲:
反应过程中,每生成1 mol氯吡苯脲,断裂______个σ键,断裂________个π键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有HO、NH 、CO 等。
2 3 2
请用共价键知识解释HO分子比NH 分子稳定的原因:___________________________。
2 3
14.[Ni(IMI) ](NO) 等过渡金属咪唑类配合物用途非常广泛。回答下列问题:
6 3 2
(1)基态原子Ni价层电子的电子排布图(轨道表示式)为____________________,占据最高能层的
电子云轮廓图为__________形。
(2)Ni 与 Ca 位于同一周期且最外层电子数相同,镍的熔点和沸点均比钙高,这是因为
________________________________________________________________________
________________________________________________________________________。
(3)咪唑(IMI)的结构简式为 ,可以HCHO、 及(NH)SO 等为原料合成。
4 2 4
①咪唑中碳原子的杂化方式为____________。
② 分子中σ键与π键的数目之比为_____________________________。
③分子中的大π键可用符号Π表示,其中m代表参与形成大π键的原子数,n代表参与形成大π
键的电子数(如苯分子中的大π键可表示为Π),则 中形成大π键的电子数为______。课时检测(三十六)
1.D HS分子是V形结构,故A错误;AlCl 中心原子Al的价层电子对数为3+×(3-1×3)=3,
2 3
其价层电子对互斥模型为平面三角形,故B错误;KI是离子化合物,其电子式为 ,故C
错误;CH CH(CH CH ) 的结构简式可写为 ,其名称为3甲基戊烷,故D正确。
3 2 3 2
2.A 水分子中,氧电负性较强,能形成氢键,(H O) 中水分子之间的作用力主要是氢键,A正确;
2 21
同系物是指结构相似、分子组成相差若干个“CH ”原子团的有机化合物,(H O) 和(H O) 不互为同
2 2 21 2 23
系物,B错误;加热(H O) 变为(H O) 只破坏了氢键,氢键不是化学键,C错误;(H O) 晶体属于分
2 23 2 19 2 21
子晶体,D错误。
3.B HO 分子中H—O—O的键角受O上孤电子对的影响,小于109°28′,A错误;CO 分子中
2 2 2
C形成2个σ键,没有孤电子对,采取sp杂化,B正确;BF 分子中B形成3个σ键,没有孤电子对,采
3
取sp2杂化,C错误;1 mol CH COOH分子中含有1 mol π键和7 mol σ键,D错误。
3
4.C SO 分子中含有孤电子对,不是直线形分子,是V形分子,A错误;SnBr 中有两个成键电子
2 2
对,一个孤电子对,孤电子对会产生斥力,所以键角小于120°,B错误;PCl 是三角双锥形分子,D错误。
5
5.D NCl 的中心原子N的价层电子对数为3+=4,有1个孤电子对,故NCl 的空间结构为三角
3 3
锥形,分子中正、负电荷中心不重合,为极性分子,SiCl 的中心原子Si的价层电子对数为4+=4,无孤
4
电子对,故SiCl 的空间结构为正四面体形,分子中正、负电荷中心重合,为非极性分子,A错误;NCl
4 3
和NH 的中心原子N的价层电子对数均为4,故N均为sp3杂化,B错误;由NCl 的水解机理示意图可
3 3
知,NCl 水解时HO中的H与NCl 中N上的孤电子对结合,O与Cl结合,而SiCl 中Si无孤电子对,
3 2 3 4
故SiCl 的水解反应机理与NCl 不相同,C错误;NHCl 和NH 分子中均存在N—H键,均能与HO形
4 3 2 3 2
成氢键,D正确。
6.A F的原子半径小,电子云密度大,两个原子间的斥力较强,F—F键不稳定,因此F—F键的
键能小于Cl—Cl键的键能,与电负性无关,A符合题意;氟的电负性大于氯的电负性,F—C键的极性
大于Cl—C键的极性,使FC—的极性大于Cl C—的极性,导致三氟乙酸的羧基中的羟基极性更大,
3 3
更容易电离出氢离子,酸性更强,B不符合题意;氟的电负性大于氯的电负性,F—H键的极性大于Cl
—H键的极性,导致HF分子的极性强于HCl,C不符合题意;氟的电负性大于氯的电负性,与氟原子
相连的氢原子可以与另外的氟原子形成分子间氢键,因此气态氟化氢中存在(HF) ,D不符合题意。
2
7.A 从结构图可以看出,该晶体中存在N—H…O氢键,A正确;N的价层电子排布式为
2s22p3,2p能级处于半满稳定状态,其第一电离能大于O,B错误;根据B(1s22s22p1)、C(1s22s22p2)、
O(1s22s22p4)、N(1s22s22p3)的电子排布式可知,其未成对电子数分别为1、2、2、3,C错误;该晶体中B、O
的杂化类型均为sp3,[C(NH )]+为平面结构,则其中N的杂化类型为sp2,D错误。
2 3
8.B CH与HO+中C与O的价层电子对数都是4,且都含有1个孤电子对,均为三角锥形结构,
3
A项正确;CH、—CH 、CH中的中心原子C的价层电子对数分别是3、4、4,根据价层电子对互斥模型
3
知,C的杂化类型分别是sp2、sp3、sp3,B项错误;CH中的碳原子采取sp2杂化,所有原子均共面,C项
正确;CH与OH-形成的化合物是CH OH,属于共价化合物,不含离子键,D项正确。
3
9.C 氰气性质与卤素相似,能和氢氧化钠溶液发生反应,故A错误;同一周期元素中,原子半径
随着原子序数的增大而减小,原子半径越大其键长越长,碳原子半径大于氮原子,所以氰分子中C≡N
的键长小于C≡C的键长,故B错误;该分子的结构式为N≡C—C≡N,该分子中含有3个σ键、4个π键,故D错误。
10.C 反应物中,碳原子最外层的四个电子中有3个用于形成σ键,有1个参与形成大π键,没
有孤电子对,碳原子的杂化方式为sp2,氮原子最外层的五个电子中有2个用于形成σ键,有1个参与
形成大π键,孤电子对数为1,氮原子的杂化方式为sp2,氧原子最外层的6个电子中有2个用于形成σ
键,孤电子对数为2,氧原子的杂化方式为sp3,A错误;(CHCH )AlCl与AlCl 都是分子晶体,
3 2 2 3
(CHCH )AlCl比AlCl 的相对分子质量小,因此(CHCH )AlCl晶体中的范德华力较小,熔点较低,B
3 2 2 3 3 2 2
错误;产物中Al形成了5个共价键,其中铝原子与氮原子通过配位键相结合,氮原子提供孤对电子,
铝原子提供空轨道,C正确;产物属于共价化合物,只含有共价键,D错误。
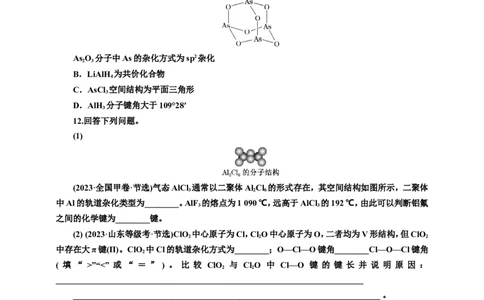
11.D 由题图可知,As形成了3个As—O共价键,As上还有一个孤电子对,As的杂化轨道数目
为4,所以As的杂化方式为sp3杂化,A错误;LiAlH 为离子化合物,阳离子为Li+,阴离子为AlH,B
4
错误;AsCl 中有3个σ键,孤电子对数为×(5-3×1)=1,As为sp3杂化,含有一个孤电子对,所以空间
3
结构为三角锥形,C错误;AlH 中有3个σ键,无孤电子对,空间结构为平面三角形,所以键角大于
3
109°28′,D正确。
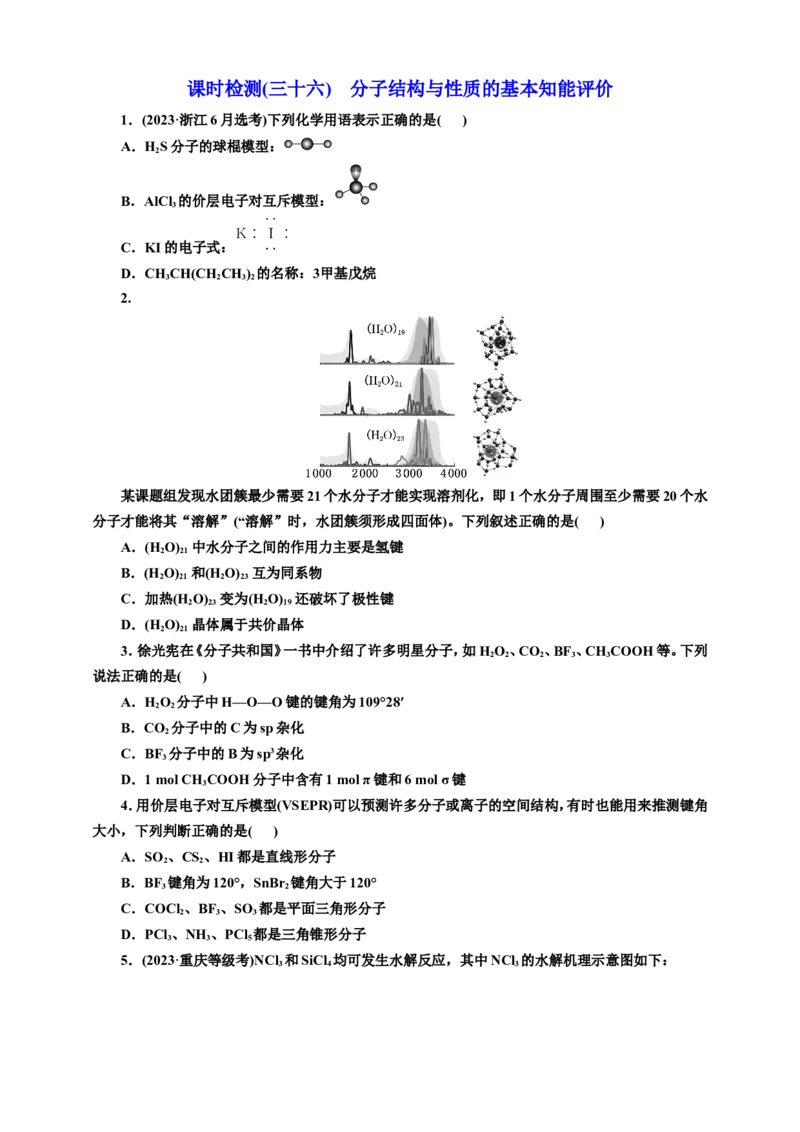
12.解析:(1)根据AlCl 形成的二聚体结构可知,每个Al和4个Cl成键,杂化轨道类型为sp3杂化。
3
AlF 的熔点远高于AlCl ,则AlF 为离子晶体,铝氟之间形成的是离子键。(2)ClO 为V形结构,且存在
3 3 3 2
3原子、5电子的大π键,则Cl的杂化类型为sp2,Cl有1个孤电子对,Cl O中O存在2个孤电子对,孤
2
电子对与成键电子对间的斥力大于成键电子对与成键电子对间的斥力,故Cl O中Cl—O—Cl键角小
2
于ClO 中O—Cl—O键角。(3)①杂化轨道形成共价键时只形成σ键。②C的杂化轨道中,s轨道成分
2
越多,形成的C—Cl键越强,C—Cl键的键长越短,一氯乙烷中C采取sp3杂化,一氯乙烯中C采取sp2
杂化,一氯乙炔中C采取sp杂化,sp杂化时p轨道成分少,sp3杂化时p轨道成分多,因此三种物质中
C—Cl键键长顺序为一氯乙烷>一氯乙烯>一氯乙炔,同时Cl参与形成的大π键越多,形成的C—Cl
键的键长越短,一氯乙烯中Cl的3p轨道与C的2p轨道形成3中心、4电子的大π键,一氯乙炔中Cl
的3p轨道与C的2p轨道形成2个3中心、4电子的大π键,因此三种物质中C—Cl键键长顺序为一
氯乙烷>一氯乙烯>一氯乙炔。(4)①由球棍模型可知,富马酸的结构简式为HOOCCH===CHCOOH,
则分子中σ键和π键的数目比为11∶3。②由结构简式可知,产物中氮形成4个共价键,原子的杂化方
式为sp3杂化。
答案:(1)sp3 离子 (2)sp2 > 键长:ClO 一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,形成的C—Cl键
的键长越短 (4)①11∶3
②sp3 HO
2
13.解析:(2)根据氯吡苯脲的结构简式可知,有2个氮原子均形成3个单键,孤电子对数为1,属于
sp3杂化,还有1个氮原子是sp2杂化;羰基碳原子形成2个单键和1个双键,为sp2杂化。(3)由于σ键比
π键更稳定,根据化学方程式可以看出,断裂的化学键为异氰酸苯酯分子中的N===C中的π键和2氯-
4氨基吡啶分子中的N—H。(4)O、N属于同周期元素,O的原子半径小于N,H—O键的键能大于H—
N键的键能,所以HO分子比NH 分子稳定。
2 3
答案:(1)1 (2)sp2、sp3 sp2 (3)N N
A A
(4)H—O键的键能大于H—N键的键能
14.解析:(1)基态原子Ni价层电子排布式为3d84s2,其电子排布图(轨道表示式)为,占据最高能层的是4s能级,电子云轮廓图为球形。(3)①分子中碳原子均形成双
键,所以碳原子的杂化方式为sp2杂化。②单键都是σ键,双键中含有1个σ键和1个π键,则 分
子中σ键与π键的数目之比为5∶2。
③ INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\3\\25YLCXHXⅡ4-66.TIF" \*
MERGEFORMATINET 中碳原子和形成双键的氮原子各有1个电子、形成单键的氮原子有2
个电子参与形成大π键,则形成大π键的电子数为6。
答案:(1) 球
(2)Ni的原子半径比Ca小且价电子数比Ca多,故镍的金属键比钙的强 (3)①sp2杂化 ②5∶2
③6