文档内容
课时检测(六十二) 水溶液中的新型图像
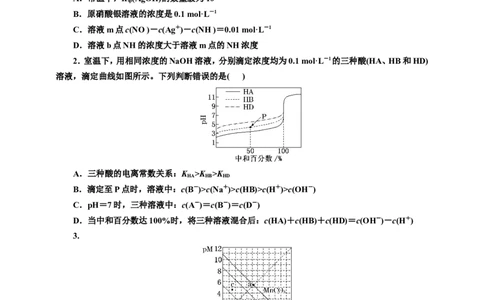
1.(2024·洛阳模拟)常温下,向10 mL一定浓度的硝酸银溶液中,逐滴加入0.1 mol·L-1的氨水,反
应过程中-lg c(Ag+)或-lg c([(Ag(NH )]+ )与加入氨水体积的关系如图所示。下列说法错误的是(
3 2
)
A.常温下,K (AgOH)的数量级为10-8
sp
B.原硝酸银溶液的浓度是0.1 mol·L-1
C.溶液m点c(NO )-c(Ag+)-c(NH )=0.01 mol·L-1
D.溶液b点NH的浓度大于溶液m点的NH浓度
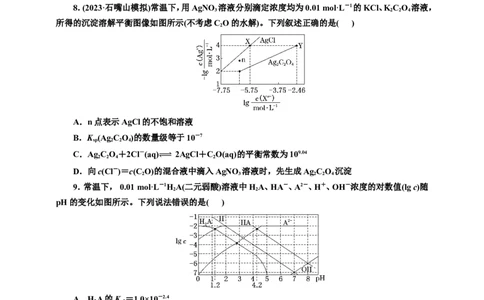
2.室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1 mol·L-1的三种酸(HA、HB和HD)
溶液,滴定曲线如图所示。下列判断错误的是( )
A.三种酸的电离常数关系:K >K >K
HA HB HD
B.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
3.
一定温度下,三种碳酸盐MCO (M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示。已知:pM
3
=-lg c(M2+),p(CO)=-lg c(CO)。
下列说法正确的是( )
A.MgCO 、CaCO 、MnCO 的K 依次增大
3 3 3 sp
B.a点可表示MnCO 的饱和溶液,且c(Mn2+)>c(CO)
3
C.b点可表示CaCO 的饱和溶液,且c(Ca2+)d点
D.三甲胺[N(CH )]的电离常数为10-4.2
3 3
7.(2023·福建等级考)25 ℃时,某二元酸(H A)的K =10-3.04、K =10-4.37。1.0 mol·L-1NaHA 溶液
2 a1 a2
稀释过程中,δ(H A)、δ(HA-)、δ(A2-)与pc(Na+)的关系如图所示。已知pc(Na+)=-lg c(Na+),HA-的
2
分布系数δ(HA-)=。下列说法错误的是( )A.曲线n为δ(HA-)的变化曲线
B.a点:pH=4.37
C.b点:2c(H A)+c(HA-)=c(Na+)
2
D.c点:c(Na+)+c(H+)=3c(HA-)+c(OH-)
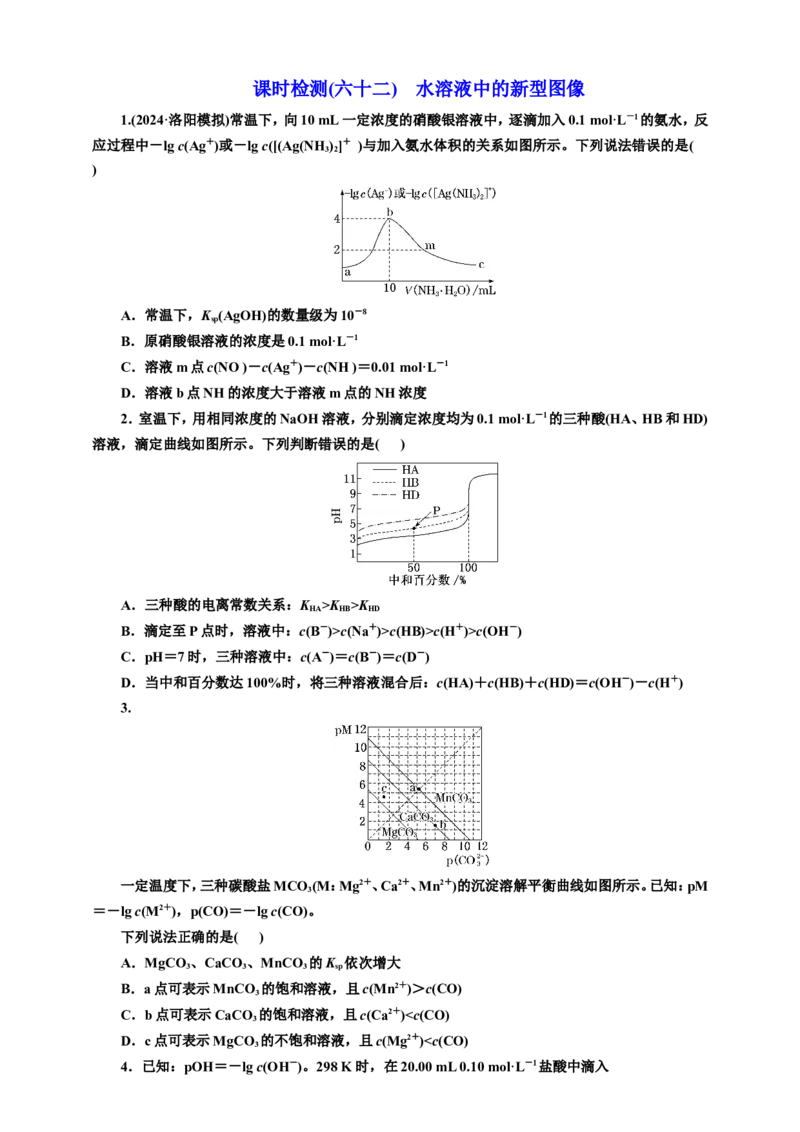
8.(2023·石嘴山模拟)常温下,用AgNO 溶液分别滴定浓度均为0.01 mol·L-1的KCl、KCO 溶液,
3 2 2 4
所得的沉淀溶解平衡图像如图所示(不考虑CO的水解)。下列叙述正确的是( )
2
A.n点表示AgCl的不饱和溶液
B.K (Ag CO)的数量级等于10-7
sp 2 2 4
C.Ag CO+2Cl-(aq) 2AgCl+CO(aq)的平衡常数为109.04
2 2 4 2
D.向c(Cl-)=c(C 2 O)的 ⥫ 混 ⥬ 合液中滴入AgNO 3 溶液时,先生成Ag 2 C 2 O 4 沉淀
9.常温下, 0.01 mol·L-1HA(二元弱酸)溶液中HA、HA-、A2-、H+、OH-浓度的对数值(lg c)随
2 2
pH 的变化如图所示。下列说法错误的是( )
A.HA 的K =1.0×10-2.4
2 a1
B.溶液 pH=3 时,=10-1.2
C.等浓度 NaHA 与Na A 的混合溶液中c(A2-)>c(HA-)
2
D.0.01 mol·L-1 Na A 溶液的pH 约为 8
2
10.(2024·湖南衡阳模拟)常温下,向某浓度HA溶液中缓慢加入NaOH(s),保持溶液体积和温度
2
不变,测得pH与-lg c(H A)、-lg c(A2-)、-lg 变化如图所示。下列说法正确的是( )
2A.a到b的滴定过程水的电离程度逐渐减小
B.常温下,HA电离平衡常数K 为10-0.8
2 a1
C.a点溶液中c(A2-)>c(HA-)>c(H+)>c(OH-)
D.NaHA溶液中c(Na+)>c(HA-)>c(H A)>c(A2-)
2
11.(2024·烟台模拟)常温下,用0.5 mol·L-1NaHCO 溶液滴定25.00 mL 0.25 mol·L-1CaCl 溶液,
3 2
消耗NaHCO 溶液的体积与混合液pH关系如图所示。滴定过程中有白色沉淀生成,但整个过程未见
3
气泡产生。已知:碳酸K =4.5×10-7,K =4.7×10-11;K (CaCO )=3.4×10-9。下列说法正确的是( )
a1 a2 sp 3
A.ab段pH升高的主要原因:HCO+Ca2+===CaCO ↓+H+
3
B.bc段溶液不可能出现白色沉淀
C.b点:c(H CO )2c(CO)+c(HCO)
课时检测(六十二)
1.C 向10 mL一定浓度的硝酸银溶液中,逐滴加入0.1 mol·L-1的氨水,首先发生反应:Ag++
NH ·HO===AgOH↓+NH,继而发生AgOH+2NH ·HO===Ag(NH )+2HO+OH-;b点-lg c(Ag+
3 2 3 2 3 2
)达到最大值,可认为此时Ag+与NH ·HO恰好完全反应。b点溶液溶质为NH NO ,Ag+完全沉淀,存
3 2 4 3
在沉淀溶解平衡AgOH(s) Ag+(aq)+OH-(aq),所以可以近似地认为c(Ag+)=c(OH-),此时-lg
c(Ag+)=4,则c(Ag+)=c(O⥫H⥬-)=1×10-4mol,K (AgOH)=c(Ag+)·c(OH-)=1×10-8,A正确;b点完全
sp
反应,此时加入的氨水体积为10 mL,氨水的浓度为0.1 mol·L-1,原硝酸银溶液体积也为10 mL,根据
方程式Ag++NH ·HO===AgOH↓+NH可知,硝酸银溶液的浓度为0.1 mol·L-1,B正确;m点溶液存
3 2
在电荷守恒c(OH-)+c(NO)=c(Ag+)+c[Ag(NH )]+c(NH)+c(H+),此时加入了过量的氨水,溶液应
3
呈碱性,则有:c(NO)-c(Ag+)-c(NH)=c[Ag(NH )]+c(H+)-c(OH-)=10-2+c(H+)-c(OH-)<10-
3
2mol·L-1,C错误;b点溶液溶质为NH NO ,b到m过程发生反应AgOH+2NH ·HO===Ag(NH )+
4 3 3 2 3
2HO+OH-,随着氨水的加入,并没有引入铵根离子,并且碱性增强铵根离子的水解受到促进,则铵
2根离子的浓度减小,即b点铵根离子的浓度大于溶液m点铵根离子的浓度,D正确。
2.C A项,根据图像知,在未滴加NaOH溶液时,0.1 mol·L-1的三种酸(HA、HB和HD)溶液的
pH均大于1,说明三种酸均为弱酸,且HA的pH最小、酸性最强,HD的pH最大、酸性最弱,因酸性
越强,电离常数越大,故K >K >K ,正确; B项,滴定至P点时,溶液中未反应的HB与生成的
HA HB HD
NaB 的浓度相等,且溶液呈酸性,说明 HB 的电离程度大于 B-的水解程度,故 c(B-)>c(Na
+)>c(HB)>c(H+)>c(OH-),正确;C项,pH=7时,三种离子的浓度分别等于c(Na+),然而三种溶液中
阴离子水解程度不同,加入的NaOH的体积不同,故三种阴离子的浓度也不同,错误;D项,根据质子
守恒即可得出,三种溶液混合后溶液的质子守恒关系:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+),正确。
3.D 当p(CO)=0,即c(CO)为1 mol·L-1时,三种碳酸盐MgCO 、CaCO 、MnCO 的pM依次增
3 3 3
大,即对应的c(Mg2+)、c(Ca2+)、c(Mn2+)依次减小,可知MgCO 、CaCO 、MnCO 的K 依次减小,A选
3 3 3 sp
项错误;曲线上的a点为MnCO 的饱和溶液,a点的纵横坐标数值相同,即pM=p(CO),c(Mn2+)=
3
c(CO),B选项错误;而曲线上b点的纵坐标数值小于横坐标数值,即pM<p(CO),c(Ca2+)>c(CO),C
选项错误;c点为MgCO 直线右上方的点,即该点表示MgCO 的不饱和溶液,该点的纵坐标数值大于
3 3
横坐标数值,即pM>p(CO),c(Mg2+)<c(CO),D选项正确。
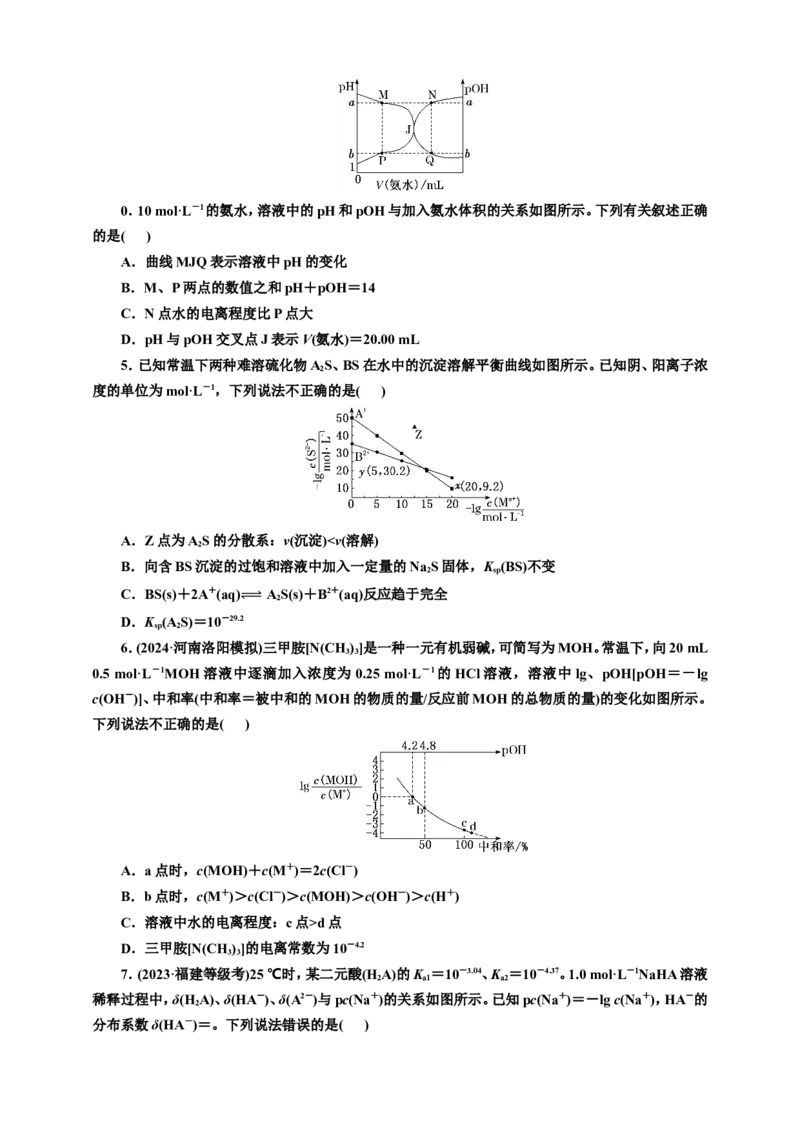
4.B 把碱溶液滴入酸溶液中,溶液的pH逐渐增大,故曲线PJN表示溶液pH的变化,而曲线
MJQ表示溶液pOH的变化,A错误;298 K时,水的离子积K =1.0×10-14,M、P两点为滴定过程中相
w
同时刻的溶液,故pH+pOH=-lg c(H+)-lg c(OH-)=-lg[c(H+)·c(OH-)]=-lgK =14,B正确;N点
w
溶液的pH与M点溶液的pOH相等,故N、M两点水的电离程度相同,而M、P两点为滴定过程中相
同时刻的溶液,故N、P两点水的电离程度相同,C错误;J点pH=pOH=7,故氨水过量,即J点表示
V(氨水)>20.00 mL,错误。
5.D Z点在曲线的上方,Qd点,故C正确;根据a点,=1时c(OH-)=10
-4.2,三甲胺[N(CH )]的电离常数 为10-4.2,故D正确。
3 3
7.B 1.0 mol·L-1NaHA溶液稀释过程中,随着水的加入,因存在电离平衡HA-⥫⥬ H++A2-和
水解平衡HA-+HOOH-+HA,HA-的分布系数先保持不变后减小,曲线n为δ(HA-)的变化曲
2 2
线,随pc(Na+)的增大,c(Na+)减小,δ(A2-)增大明显,故曲线m为δ(A2-)的变化曲线,则曲线p为
δ(H A)的变化曲线,A正确;a点, pc(Na+)=1.0,则c(Na+)=0.1 mol·L-1,δ(HA-)=0.70,δ(H A)=δ(A2
2 2
-)=0.15,K ==10-4.37,c(H+)=×10-4.37,pH≠4.37,B错误;b点,δ(HA-)=0.70,δ(H A)=δ(A2-)=
a2 2
0.15,即c(H A)=c(A2-),根据物料守恒,有c(A2-)+c(H A)+c(HA-)=c(Na+),故2c(H A)+c(HA-)=
2 2 2
c(Na+),C正确;c点:δ(HA-)=δ(A2-),故c(A2-)=c(HA-),根据电荷守恒,有c(Na+)+c(H+)=2c(A2-)
+c(HA-)+c(OH-),故c(Na+)+c(H+)=3c(HA-)+c(OH-),D正确。
8.C 由题图可知,n点AgCl的浓度熵Q大于其溶度积K ,则n点表示AgCl的过饱和溶液,会
sp析出AgCl沉淀,A错误;由题图可知,当c(Ag+)=1.0×10-4mol·L-1时,c(C O)=1.0×10-2.46mol·L-1,则
2
溶度积K (Ag CO)=c2(Ag+)·c(C O)=(1.0×10-4)2×1.0×10-2.46=1.0×10-10.46,B错误;Ag CO(s)+2Cl
sp 2 2 4 2 2 2 4
-(aq) 2AgCl(s)+CO(aq)的平衡常数K=====109.04,C正确;由题图可知,当溶液中c(Cl-)=
2
c(C O)时,AgCl饱和溶液中c(Ag+)小于Ag CO 饱和溶液中c(Ag+),则向c(Cl-)=c(C O)的混合液中
2 ⥫⥬ 2 2 4 2
滴入AgNO 溶液时,先生成AgCl沉淀,D错误。
3
9.A 根据pH=1.2的点得到c(H A)=c(HA-),因此HA的K =c(H+)=1.0×10-1.2,故A错误;
2 2 a1
根据pH=4.2的点得到c(A2-)=c(HA-),因此HA的K =c(H+)=1.0×10-4.2,溶液 pH=3 时,===
2 a2
10-1.2,故B正确;HA的K =1.0×10-1.2,K =1.0×10-4.2,得到K ===1×10-9.8,说明NaHA电离大
2 a1 a2 h1
于Na A的水解,等浓度 NaHA 与Na A 的混合溶液中,c(HA-)<c(A2-),故C正确;根据B选项得到
2 2
K =1.0×10-4.2,因此0.01 mol·L-1 Na A 溶液的K ====,解得c(OH-)=1×10-5.9mol·L-1,pOH=
a2 2 h1
5.9,则pH=14-5.9=8.1,即约为8,故D正确。
10.B 向某浓度 HA溶液中缓慢加入 NaOH 溶液时,由于二者发生反应,所以 HA 逐渐减少,
2
-lg c(H A)会逐渐增大,所以题图中呈上升趋势的为-lg c(H A)与pH变化关系,标①;HAH++
2 2 2
HA-,HA-H++A2-,A2-会逐渐增大,-lg c(A2-)会逐渐减小,但是不会等于 0,所以呈下降趋势
且与横坐标无交点的为-lg c(A2-)与pH变化关系,标②,另一条则是-lg与pH的变化图,标③。a到
b的滴定过程中,-lg c(A2-)逐渐减小,则c(A2-)浓度逐渐增大,促进水的电离,A错误;K =, K =,
a1 a2
K ·K =④,当pH=3.05 时,lg c(A2-)与-lgc(H A)相等,c(A2-)=c(H A),K ·K =(10-3.05)2=10-6.1,又
a1 a2 2 2 a1 a2
由题图中③可知,pH=5.3时,-lg=0,即c(A2-)=c(HA-),即K =10-5.3,所以K ==10-0.8,故B正
a2 a1
确;a点溶液中c(A2-)=c(H A),a点时K ==,===102.25,则c(HA-)>c(A2-),故C错误;NaHA溶
2 a1
液中,HA-既存在电离又存在水解,K =10-5.3,HA-的水解常数K ===10-13.2,所以HA-的水解程
a2 h
度小于HA-的电离程度,所以c(H A)K ,则HCO的水
2 2 3 h a2
解程度大于电离程度,故c(H CO )>c(CO),C错误;c点pH=7.2,溶液显碱性,故c(OH-)>c(H+),根据
2 3
电荷守恒可知2c(Ca2+)+c(Na+)+c(H+)=c(OH-)+2c(CO)+c(HCO)+c(Cl-),由碳酸氢钠和氯化钙
的物质的量可知,c(Na+)=c(Cl-),则有2c(Ca2+)>2c(CO)+c(HCO),D正确。