文档内容
铁及其化合物作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 1-7,15,19-21,23,25-26 题为三星,8-12,14,16-18,24,27 为四星,
13,22 为五星
1.《新修本草》是我国古代中药学著作之一,记载药物 844 种,其中有关于“青
矾”的描述为:“本来绿色,新出窟未见风者,正如瑠璃…烧之赤色…”据此推测,
“青矾”的主要成分为( ) ☆☆☆
A.CuSO •5H O B.FeSO •7H O
4 2 4 2
C.KAl(SO ) •12H O D.Fe (SO ) •9H O
4 2 2 2 4 3 2
【解答】
“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑠璃…烧之赤色…”,青矾是
绿色,经煅烧后,分解成粒度非常细而活性又很强的 Fe O 超细粉末为红色,
2 3
A 为蓝色晶体,
B 为 FeSO •7H O 是绿色晶体,
4 2
C 为 KAl(SO ) •12H O 是无色晶体,
4 2 2
D 为 Fe (SO ) •9H O 为黄色晶体,
2 4 3 2
所以判断“青矾”的主要成分为 FeSO •7H O,
4 2
故选 B.
2.下列有关铁及其化合物的说法中正确的是( ) ☆☆☆
A.赤铁矿的主要成分是 Fe O
3 4
B.铁与水蒸气在高温下的反应产物为 Fe O 和 H
2 3 2
C.除去 FeCl 溶液中的 FeCl 杂质可以向溶液中加入铁粉,然后过滤
2 3
第 1页(共 15页)D.Fe3 与 KSCN 溶液产生红色沉淀
+
【解答】
A、赤铁矿的主要成分是 Fe O ,故 A 错误;
2 3
B、铁与水蒸气在高温下的反应产物为 Fe O 和 H ,故 B 错误;
3 4 2
C、铁粉把 FeCl 还原成 FeCl ,从而除去 FeCl ,故 C 正确;
3 2 3
D、Fe3 与 KSCN 产生血红色溶液,不是沉淀,故 D 错误.
+
故选 C.
3.下列关于铁及其化合物的叙述正确的是( ) ☆☆☆
①氧化亚铁在空气中加热可以生成四氧化三铁
②在人体内的血红蛋白中含有铁元素
③不能通过化合反应制得 FeCl 和 Fe(OH)
2 3
④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧
⑤赤铁矿的主要成分是 Fe O
3 4
A.②③④ B.①②④ C.②④⑤ D.①②③
【解答】
①氧化亚铁中亚铁离子不稳定,在空气中加热能够转化成四氧化三铁,故①正确;
②在人体内的血红蛋白中含有铁元素,铁在人体内的主要功能是以血红蛋白(含
低价铁)的形式运输氧,故②正确;
③氯化铁与铁粉反应生成 FeCl 的反应为化合反应,氢氧化亚铁与氧气、水反应
2
生成 F e(OH) 的反应为化合反应,可以通过化合反应制取 FeCl 和 Fe(OH) ,
3 2 3
故③错误;
④铁能在氧气中剧烈燃烧,铁与水蒸气在高温条件下反应生成 Fe O 和氢气,方
3 4
程式为 3Fe+4H O(g) Fe O +4H ,该反应不满足燃烧的条件,所以不属
2 3 4 2
于燃烧,故④正确;
⑤氧化铁为红棕色粉末,赤铁矿的主要成分是氧化铁,而 Fe O 为黑色粉末,不
3 4
是赤铁矿主要成分,故⑤错误;
第 2页(共 15页)故选 B.
4.为了防止 FeSO 被氧化而变质,实验室在配制 FeSO 溶液时,常在溶液中加
4 4
入少量的( ) ☆☆☆
A.铜粉 B.铁粉 C.锌粉 D.Fe (SO )
2 4
【解答】
FeSO 中 Fe 为+2 价,所以极易被氧化为+3 价,加入铁粉后,会与+3 价的铁反应
4
使之成为亚铁离子后,融入到 FeSO 溶液中,这样便有效地减少 FeSO 的损失,
4 4
故选:B.
5.为了使 FeSO 氧化成 Fe (SO ) 而又不引入杂质,应向悬浊液中加入( )
4 2 4 3
☆☆☆
A.Cl B.HNO C.H O D.Na O
2 3 2 2 2 2
【解答】
将 FeSO 氧化为 Fe (SO ) ,根据不能够引进新的杂质:用氯气引入氯离子杂
4 2 4 3
质,用 HNO 引入硝酸根离子,用 Na O 引入钠离子,需用 H O ,反应为
3 2 2 2 2
H SO +H O +2FeSO =Fe (SO ) +2H O
2 4 2 2 4 2 4 3 2
故选 C.
6.某溶液中可能存在 Mg2 、Fe2 、Fe3 ,加入 NaOH 溶液,开始有白色絮状沉
+ + +
淀生成,白色沉淀迅速变成灰绿色,最后变成红褐色,下列结论正确的是( )
☆☆☆
A.一定有 Fe2 ,一定没有 Mg2 、Fe3
+ +
+
B.一定有 Fe3 ,一定没有 Mg2 、Fe2
+ +
+
C.一定有 Fe3 ,可能有 Fe2 ,一定没有 Mg2
+ +
+
D.一定有 Fe2 ,可能有 Mg2 ,一定没有 Fe3
+ +
+第 3页(共 15页)【解答】
加入 NaOH 溶液,开始时有白色絮状沉淀,后迅速变为灰绿色,最后变为红褐色,
该变化为亚铁离子与氢氧根离子反应的现象,据此判断一定存在亚铁离子,氢氧
化铁为红褐色,颜色比白色深,若有铁离子存在,不会看到溶液中白色沉淀,所
以一定不存在铁离子;镁离子与氢氧根离子反应生成白色的氢氧化镁沉淀,所以
不能确定是否有镁离子
故选:D.
7.把一块生锈的铁片投入盛有稀硫酸溶液的烧杯里,待铁片完全溶解后,往烧
杯里滴加氢氧化钠溶液至过量,然后过滤,并充分灼烧不溶物,则最终留下的固
体是( ) ☆☆☆
A.Na O B.Fe O 和 Fe C.Fe O D.Fe O 和 NaOH
2 2 3 2 3 2 3
【解答】
生锈的铁片含有铁和氧化铁,投入盛有稀硫酸溶液的烧杯里,铁与硫酸反应生成
硫酸亚铁,氧化铁与硫酸反应生成硫酸铁,往烧杯里滴加氢氧化钠溶液至过量,
生成氢氧化亚铁、氢氧化铁,氢氧化亚铁不稳定,被氧化生成氢氧化铁,灼烧氢
氧化铁生成氧化铁,所以最终得到的产物为氧化铁。
故选:C.
8.准确称取某种铁的氧化物 2.88g,用足量的 CO 进行还原,将生成的 CO 全部
2
用足量的澄清石灰水吸收,得到沉淀 4g,则这种铁的氧化物为( )
☆☆☆☆
A.Fe O B.Fe O C.FeO D.以上都不是
3 4 2 3
【解答】
4g 沉淀 CaCO 的物质的量为 0.04mol,则 CO、CO 的物质的量也为 0.04mol,增
3 2
加的氧元素为 0.04mol,质量为 0.04mol×16g • mol﹣1=0.64g,铁的氧化物中氧元
第 4页(共 15页)素质量为 0.64g,铁元素质量为 2.88g﹣0.64g=2.24g,铁的氧化物中铁元素与氧元
素物质的量之比为 : =1:1,则铁的化学式为 FeO
故选:C.
9.下列叙述正确的是( ) ☆☆☆☆
A.向 FeSO 溶液中加入 NaOH 溶液,充分振荡后,可以制得 Fe(OH)
4 2
B.Al O 能和 NaOH 溶液反应,得到 NaAlO
2 3 2
C.某溶液焰色反应的火焰呈黄色,则该溶液中不含钾离子
D.某溶液中加入 BaCl 溶液有白色沉淀产生,再加盐酸,沉淀不消失,则该溶
2
液中一定有 SO 2
4 ﹣
【解答】
A、向 FeSO 溶液中加入 NaOH 溶液,先生成白色沉淀,白色沉淀迅速变成灰绿
4
色,最终会变成红褐色,所以无法获得 Fe(OH) ,故 A 错误;
2
B、氧化铝为两性氧化物,所以 Al O 能和 NaOH 溶液反应生成 NaAlO 和水,
2 3 2
反应的化学方程式为:Al O +2NaOH=2NaAlO +H O,故 B 正确;
2 3 2 2
C、观察钾离子的焰色反应的火焰颜色时,需要通过蓝色的钴玻璃观察,否则无
法可得紫色,所以某溶液焰色反应的火焰呈黄色,溶液中一定含有钠离子,但是
无法确定溶液中是否含钾离子,故 C 错误;
D、某溶液中加入 BaCl 溶液有白色沉淀产生,白色沉淀可能为氯化银,不一定
2
为硫酸钡沉淀,所以不能确定该溶液中是否有 SO 2﹣,故 D 错误;
4
故选 B.
10.制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为
2FeCl +Cu=2FeCl +CuCl 向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应
3 2 2
结束后,在烧杯中下列结果不可能出现的是( ) ☆☆☆☆
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
【解答】
第 5页(共 15页)A.Fe 的还原性大于 Cu,所以加入 Fe、Cu 时 Fe 先参加反应,当 Fe 完全反应后、
Cu 才反应,则烧杯中有 Cu 无 Fe,故 A 不选;
B.Fe 的还原性大于 Cu,所以加入 Fe、Cu 时 Fe 先参加反应,当 Fe 完全反应后、
Cu 才反应,因此有 Fe 剩余说明 Cu 没有反应,故 Cu 有剩余,所以不可能出现
有 Fe 而无 Cu 现象,故 B 可选;
C.如果铁完全将铁离子还原还剩余,则 Cu 就不参加反应,所以烧杯中还剩 Fe、
Cu,故 C 不选;
D.如果铁离子的量足够大,Fe、Cu 完全反应后铁离子还剩余,则烧杯中 Cu、
Fe 都不存在,故 D 不选;
故选 B.
11.FeCl 、CuCl 的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判
3 2
断不正确的是( ) ☆☆☆☆
A.加入 KSCN 溶液一定不变红色 B.溶液中一定含 Cu2
+
C.溶液中一定含 Fe2 D.剩余固体中一定含铜
+
【解答】
①当固体为铁、铜时,溶液中的 Fe3+、Cu2+全部参加反应生成 Fe2+和 Cu,反应
的反应方程式为:2FeCl +Fe=3FeCl 、CuCl +Fe=Cu+FeCl ,所以溶液中一定没
3 2 2 2
有 Fe3+、Cu2+,一定含有 Fe2+;
②当固体为铜时,溶液中一定没有 Fe3+,Cu2+恰好全部参加反应或部分反应生成
Fe2+和 Cu,
所以溶液中一定没有 Fe3+,可能含有 Cu2+,一定含有 Fe2+;
A、溶液中一定不含 Fe3 ,所以加入 KSCN 溶液不变红色,故 A 正确;
+
B、通过以上分析知,溶液中可能含有 Cu2 ,故 B 错误;
+
C、通过以上分析知,溶液中一定含有 Fe2 ,故 C 正确;
+
D、通过以上分析知,剩余固体中一定含 Cu,故 D 正确;
故选 B.
第 6页(共 15页)12.在 FeCl 、CuCl 混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,
3 2
下列说法中正确的是( ) ☆☆☆☆
A.若滤出的固体只有铜,则溶液中一定含有的阳离子是 Fe2 ,一定不含 Cu2
+
+
B.若滤出的固体只有铜,则溶液中一定含有的阳离子是 Fe2 ,可能含有 Cu2 和
+ +
Fe3
+
C.若滤出的固体只有铜,则溶液中一定含有的阳离子是 Fe3 和 Fe2 ,一定不含
+ +
Cu2
+
D.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是 Fe2 ,一定不含
+
Cu2 和 Fe3
+
+
【解答】
在 FeCl 、CuCl 混合溶液中,加入一定量的铁屑,反应先后顺序是:2FeCl +Fe
3 2 3
═3FeCl ,CuCl +Fe═FeCl +Cu.
2 2 2
A、若滤出的固体只有铜,则溶液中一定含有的阳离子是 Fe2 ,也可能含 Cu2 ,
+ +
故 A 错误;
B、若滤出的固体只有铜,则溶液中一定含有的阳离子是 Fe2 ,也可能含 Cu2 ,
+ +
一定不含 Fe3 ,故 B 错误;
+
C、若滤出的固体只有铜,则溶液中一定含有的阳离子是 Fe2 ,也可能含 Cu2 ,
+ +
一定不含 Fe3 ,故 C 错误;
+
D、若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是 Fe2 ,一定不含
+
Cu2 和 Fe3 ,故 D 正确;
+ +
故选 D.
13.在 FeCl 、CuCl 、FeCl 的混合溶液中,Fe3 、Cu2 、Fe2 的物质的量浓度之
3 2 2 + + +
比为:4:2:1,现加入适量的铁粉,使溶液中的三种离子的物质的量浓度之比
为:1:3:9,则投入的铁粉与原溶液中 Cu2 的物质的量之比为( )
+
☆☆☆☆☆
A.5:4 B.4:5 C.3:5 D.5:6第 7页(共 15页)【解答】
依据加入适量的铁粉,使溶液中的三种离子的物质的量浓度之比为:1:3:9,
结合原溶液中 Fe3 、Cu2 、Fe2 的物质的量浓度之比为:4:2:1,可知铜离子未
+ + +
参加反应,反应后的铜离子为 2 时,剩余的三价铁离子根据比值可知为 ,参加
反应的三价铁离子为 4﹣ = ,根据反应 2Fe3 +Fe=3Fe2 可知反应的铁为 ,
+ +
所以投入的铁和溶液中的铜离子物质的量之比为 :2=5:6
故选 D.
14.在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束,所剩余的固
体滤出后能被磁铁吸引,则反应后溶液存在较多的阳离子是( ) ☆☆☆☆
A.Cu2 B.Fe3 C.Fe2 D.H
+ + +
+
【解答】
充分反应后,所剩余的固体滤出后能被磁铁吸引,则铁粉有剩余,因为三价铁离
子会和铁单质生成二价铁离子,所以一定没有三价铁离子,B 错误,
铜离子会和单质铁发生置换反应二价铁离子和单质铜,盐酸中的氢离子会和铁单
质发生置换反应生成氢气和二价铁离子,所以溶液中一定不含有铜离子、氢离子,
A、D 错误,所以一定存在的是 Fe2 ;
+
故选:C.
15.要证明某溶液中不含 Fe3 而可能含有 Fe2 .进行如下实验操作时最佳顺序为
+ +
( ) ☆☆☆
①加入适量氯水 ②加入足量 KMnO 溶液 ③加入少量 KSCN 溶液
4
A.①③ B.③② C.③① D.①②③
【解答】
先根据 Fe3 的特征反应,加入硫氰酸钾溶液判断溶液不含 Fe3 ;然后加入氧化剂
+ +
氯水,如果含有 Fe2 ,Fe2 被氧化剂氧化成 Fe3 溶液变成红色,以此证明 Fe2 的存
+ + + +
第 8页(共 15页)在,注意高锰酸钾溶液为紫红色,不反应溶液也可以变红,所以不能选用高锰酸
钾氧化二价铁离子。
故选:C.
16.把一定量铁粉放入氯化铁溶液中,完全反应后,得到溶液中 Fe2 和 Fe3 的浓
+ +
度恰好相等.则已反应的 Fe3 和未反应的 Fe3 的物质的量之比为( )
+ +
☆☆☆☆
A.1:1 B.1:2 C.2:3 D.3:2
【解答】
设已反应的 Fe3 的物质的量为 2mol,则:
+
Fe+2Fe3 =3Fe2
+
+
2mol 3mol
溶液中 Fe2 的物质的量为 3mol,溶液中的 Fe3 和 Fe2 浓度相等,所以未反应的 Fe3
+ + +
+
的物质的量为 3mol,则已反应的 Fe3 和未反应的 Fe3 的物质的量之比为
+ +
2mol:3mol=2:3,
故选 C.
17.关于反应过程中的先后顺序,下列评价正确的是( ) ☆☆☆☆
A.向浓度都为 0.1mol/L 的 FeCl 和 CuCl 加入铁粉,溶质 CuCl 首先与铁粉反
3 2 2
应
B.向过量的 Ba(OH) 溶液中滴加少量的 KAl(SO ) 溶液,开始没有白色沉
2 4 2
淀生成
C.向浓度都为 0.1mol/L Na CO 和 NaOH 溶液通入 CO 气体,NaOH 首先反应
2 3 2
D.向浓度都为 0.1mol/L 的 FeCl 溶液中,加入质量相同、颗粒大小相同的铁和
3
铜,铜单质首先参加反应
【解答】第 9页(共 15页)A、三价铁的氧化性强于铜离子,还原剂铁先是和氧化性强的离子反应铁离子反
应,故 A 错误;
B、钡离子和硫酸根离子反应生成白色沉淀硫酸钡,所以开始有白色沉淀生成,
故 B 错误;
C、碳酸钠和氢氧化钠均可以和二氧化碳反应,但是氢氧化钠的碱性强于碳酸钠,
所以 NaOH 先和二氧化碳发生反应,故 C 正确;
D、一种氧化剂与多种还原剂反应,还原性强的铁首先反应,故 D 错误;
故选 C.
18.在 500 毫升 1mol/L FeCl 溶液中加入铁粉,完全反应后,除去多余的铁粉,
3
加入足量的 NaOH 溶液,搅拌充分反应,所得沉淀的物质的量是( )
☆☆☆☆
A.0.5mol B.1mol C.0.75mol D.不能确定
【解答】
500 毫升 1mol/L FeCl 溶液中,Fe3 的物质的量是 0.5L×1mol/L=0.5mol,根据反
3 +
应,设生成的亚铁离子物质的量为 n,则
2Fe3 +Fe=3Fe2
+
+
2 3
0.5mol n
解得 n=0.75mol,根据氯化亚铁和氢氧化钠的反应:
FeCl +2NaOH=Fe(OH) ↓+2NaCl,所以 0.75mol 的氯化亚铁和氢氧化钠的反应
2 2
生成沉淀 0.75mol,Fe(OH) 会迅速被氧化,
2
即 4Fe(OH) +2H O+O =4Fe(OH) ,所以 0.75mol 的 Fe(OH) 会生成 0.75mol
2 2 2 3 2
的 Fe(OH)
3
故选 C.
第 10页(共 15页)19.向某晶体的水溶液中加入 Fe2 的溶液后,无明显变化,当滴加几滴氯水后混
+
合液出现红色,那么由此得出的下列结论,错误的是( ) ☆☆☆
A.该晶体中一定含有 SCN﹣ B.Fe3
+
的氧化性比氯气的氧化性强
C.Fe2
+
被 Cl
2
氧化为 Fe3
+
D.Fe3
+
与 SCN﹣能形成红色的物质
【解答】
A、只有三价铁遇 SCN﹣才能形成红色的化合物,所以晶体中一定含有 SCN﹣,
故 A 正确;
B、二价铁能被氯气氧化为正三价,氯气是氧化剂,三价铁是氧化产物,氧化剂
的氧化性强于氧化产物的氧化性,即 Fe3 的氧化性比 Cl 的氧化性弱,故 B 错误;
+ 2
C、氯气具有氧化性,Fe2 被 Cl 氧化为 Fe3 ,故 C 正确;
+ 2 +
D、只有三价铁遇 SCN﹣能形成红色的化合物,Fe2
+
与 SCN﹣不能,故 D 正确.
故选 B.
20.为了检验某 FeCl 溶液是否变质,可向溶液中加入( ) ☆☆☆
2
A.NaOH B.铁片 C.KSCN 溶液 D.石蕊溶液
【解答】
A、FeCl 和 NaOH 溶液生成灰绿色沉淀氢氧化亚铁,氢氧化亚铁不稳定,能迅
2
速被氧化成红褐色沉淀氧氢化铁,所以不能检验是否变质,故 A 错误;
B、铁片与氯化亚铁不反应,故 B 错误;
C、如果 FeCl
2
溶液变质,变质后的物质是 FeCl
3
,Fe3
+
能和 SCN﹣生成络合物,
使溶液呈现血红色现象明显,这一反应是 Fe3 的特征反应,所以用 KSCN 溶液,
+
故 C 正确;
D、无论氯化亚铁是否变质,都是强酸弱碱盐,溶液都呈酸性,所以用石蕊溶液
无法检验,故 D 错误;
故选 C.
21.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可使用的试剂是( )
第 11页(共 15页)☆☆☆
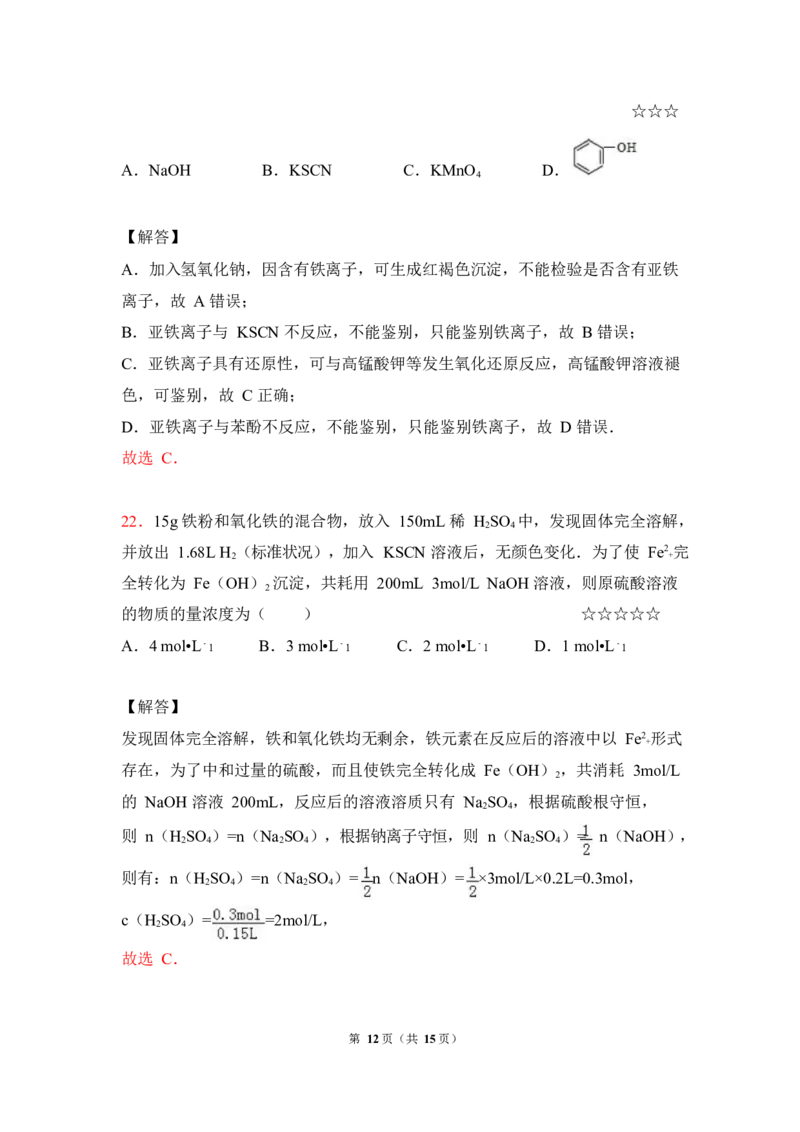
A.NaOH B.KSCN C.KMnO D.
4
【解答】
A.加入氢氧化钠,因含有铁离子,可生成红褐色沉淀,不能检验是否含有亚铁
离子,故 A 错误;
B.亚铁离子与 KSCN 不反应,不能鉴别,只能鉴别铁离子,故 B 错误;
C.亚铁离子具有还原性,可与高锰酸钾等发生氧化还原反应,高锰酸钾溶液褪
色,可鉴别,故 C 正确;
D.亚铁离子与苯酚不反应,不能鉴别,只能鉴别铁离子,故 D 错误.
故选 C.
22.15g 铁粉和氧化铁的混合物,放入 150mL 稀 H SO 中,发现固体完全溶解,
2 4
并放出 1.68L H (标准状况),加入 KSCN 溶液后,无颜色变化.为了使 Fe2 完
2 +
全转化为 Fe(OH) 沉淀,共耗用 200mL 3mol/L NaOH 溶液,则原硫酸溶液
2
的物质的量浓度为( ) ☆☆☆☆☆
A.4 mol•L﹣1 B.3 mol•L﹣1 C.2 mol•L﹣1 D.1 mol•L﹣1
【解答】
发现固体完全溶解,铁和氧化铁均无剩余,铁元素在反应后的溶液中以 Fe2 形式
+
存在,为了中和过量的硫酸,而且使铁完全转化成 Fe(OH) ,共消耗 3mol/L
2
的 NaOH 溶液 200mL,反应后的溶液溶质只有 Na SO ,根据硫酸根守恒,
2 4
则 n(H SO )=n(Na SO ),根据钠离子守恒,则 n(Na SO )= n(NaOH),
2 4 2 4 2 4
则有:n(H SO )=n(Na SO )= n(NaOH)= ×3mol/L×0.2L=0.3mol,
2 4 2 4
c(H SO )= =2mol/L,
2 4
故选 C.
第 12页(共 15页)23.下列方法能用来验证 Fe3 的是( ) ☆☆☆
+
①溶液呈浅绿色 ②与碱反应生成红褐色沉淀 ③Fe3+既具有氧化性,又具有还
原性
④Fe3+的水溶液滴入 KSCN 试液后,立即出现红色
A.①② B.②③ C.③④ D.②④
【解答】
①溶液呈浅绿色,是亚铁离子溶液的颜色,故①错误;
②与碱反应生成红褐色沉淀,红褐色沉淀为氢氧化铁,证明溶液中一定存在铁离
子,故②正确;
③Fe3+一般具有氧化性,不具有还原性,而亚铁离子既具有氧化性,又具有还原
性,故③错误;
④Fe3+的水溶液滴入 KSCN 试液后,立即出现红色,这是检验铁离子的常用方法,
故④正确;
故选 D.
24.下列各组物质中,X 是主体物质,Y 是少量杂质,Z 是要除去杂质而加入的
试剂,其中正确的组别是( ) ☆☆☆☆
X Y Z
A FeCl 溶液 FeCl KSCN 溶液
2 3
B Fe 粉 A1 粉 NaOH 溶液
C Fe (SO ) 溶液 FeSO C1
2 4 3 4 2
D FeCl 溶液 CuCl Zn 粉
2 2
【解答】
A.KSCN 溶液与氯化亚铁不反应,与氯化铁发生络合反应,不能除去杂质,故
A 错误;
B.铝与氢氧化钠溶液发生反应生成偏铝酸钠溶液,铁与氢氧化钠溶液不反应,
过滤可以除去铝,故 B 正确;
第 13页(共 15页)C.硫酸亚铁与氯气反应生成氯化铁,引人杂质氯离子,故 C 错误;
D.锌与氯化铜反应生成氯化锌和铜,除去杂质铜离子,引入锌离子,故 D 错误;
故选:B.
25.若在一支试管中加入 2mL 的 X 溶液,然后再加入足量的氯水,再滴加几滴
KSCN 溶液,观察到溶液呈血红色,则 X 溶液中( ) ☆☆☆
A.一定含有 Fe3 B.一定不含 Fe3
+
+
C.可能含有 Fe2 D.一定含有 Fe2
+
+
【解答】
由于氯水能将 Fe2 氧化为 Fe3 ,故先加入足量的氯水后,再滴入 KSCN 溶液,观
+ +
察到溶液呈血红色,则说明此时溶液中含 Fe3 ,而此时存在的 Fe3 可能是原溶液
+ +
本来就有的,也可能是原溶液中的 Fe2 被氧化生成的,故原溶液中可能含 Fe3 ,
+ +
也可能含 Fe2 ,
+
故选 C.
26.不能证明某溶液中含有 Fe2 的是( ) ☆☆☆
+
A.该溶液呈浅绿色
B.该溶液中加入 NaOH 溶液,生成白色沉淀并迅速变成灰绿色,最后变为红褐
色
C.向该溶液中加入氯水,再滴入几滴 KSCN 溶液,呈红色
D.向该溶液中滴入几滴 KSCN 溶液,不变色,再加入氯水,呈红色
【解答】
A、Fe2 的溶液呈浅绿色,故当溶液呈浅绿色时,说明含 Fe2 ,故 A 错误;
+ +
B、滴加 NaOH 溶液,利用先产生白色沉淀,后变灰绿,最后变为红褐色,说明
原溶液含有 Fe2 ,Fe3 和氢氧化钠溶液反应立即生成氢氧化铁沉淀,所以只能观
+ +
察到红褐色沉淀,所以该实验能证明某溶液只含有 Fe2 而不含 Fe3 ,故 B 正确;
+ +第 14页(共 15页)C、先滴加氯水,若原溶液含 Fe3 ,滴加 KSCN 溶液后也显红色,无法证明原溶
+
液是否含有 Fe2 ,故 C 错误;
+
D、向溶液中滴加 KSCN 溶液,不显红色,说明原溶液不含有 Fe3 ,再加入氯水,
+
溶液变红,则说明滴入氯水后溶液中含 Fe3 ,则说明原溶液中含 Fe2 ,是滴入的
+ +
氯水将 Fe2 氧化为 Fe3 ,故 D 正确.
+ +
故选:C.
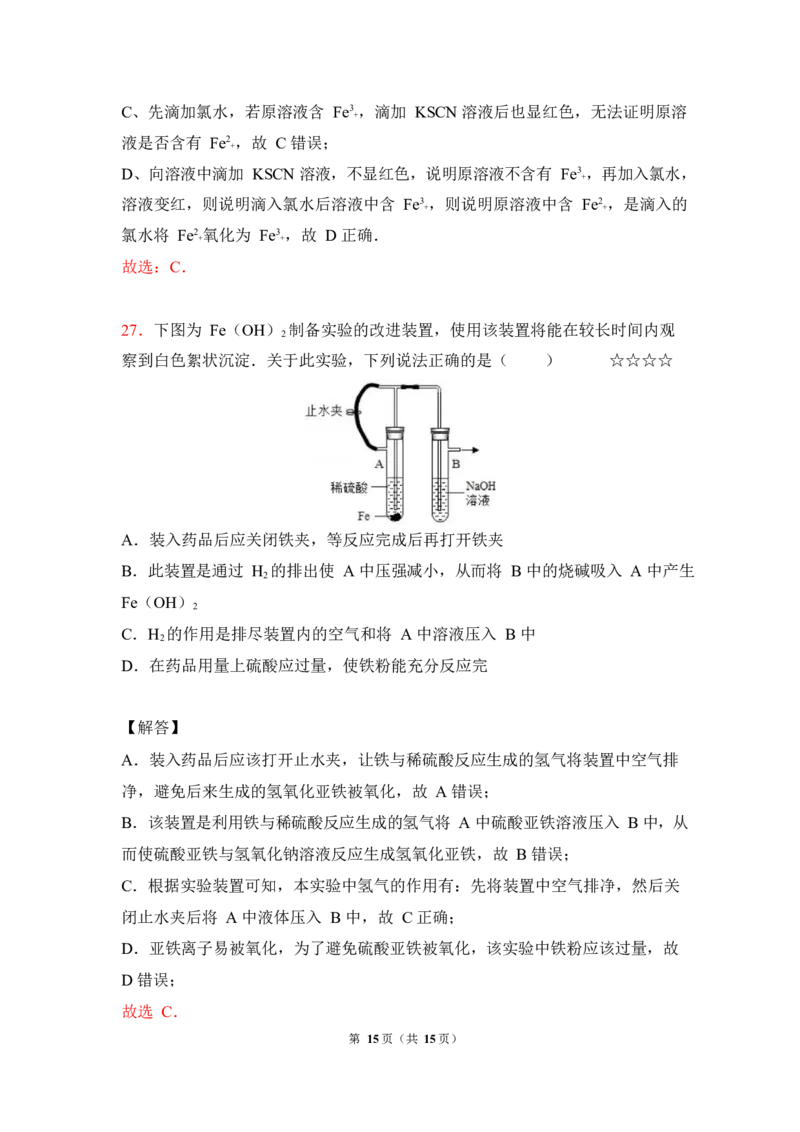
27.下图为 Fe(OH) 制备实验的改进装置,使用该装置将能在较长时间内观
2
察到白色絮状沉淀.关于此实验,下列说法正确的是( ) ☆☆☆☆
A.装入药品后应关闭铁夹,等反应完成后再打开铁夹
B.此装置是通过 H 的排出使 A 中压强减小,从而将 B 中的烧碱吸入 A 中产生
2
Fe(OH)
2
C.H 的作用是排尽装置内的空气和将 A 中溶液压入 B 中
2
D.在药品用量上硫酸应过量,使铁粉能充分反应完
【解答】
A.装入药品后应该打开止水夹,让铁与稀硫酸反应生成的氢气将装置中空气排
净,避免后来生成的氢氧化亚铁被氧化,故 A 错误;
B.该装置是利用铁与稀硫酸反应生成的氢气将 A 中硫酸亚铁溶液压入 B 中,从
而使硫酸亚铁与氢氧化钠溶液反应生成氢氧化亚铁,故 B 错误;
C.根据实验装置可知,本实验中氢气的作用有:先将装置中空气排净,然后关
闭止水夹后将 A 中液体压入 B 中,故 C 正确;
D.亚铁离子易被氧化,为了避免硫酸亚铁被氧化,该实验中铁粉应该过量,故
D 错误;
故选 C.
第 15页(共 15页)