文档内容
一、选择题
1.只改变一个影响化学平衡的因素,平衡常数K与化学平衡移动的关系叙述不正确的
是( )
A.K不变,平衡可能移动
B.平衡向右移动时,K不一定变化
C.K有变化,平衡一定移动
D.相同条件下,同一个反应的方程式的化学计量数增大2倍,K也增大2倍
解析:选D。因改变压强或浓度引起化学平衡移动时,K不变,A项和B项均正确;K只与
温度有关,K发生了变化,说明体系的温度改变,则平衡一定移动,C项正确;相同条件下,同
一个反应的方程式的化学计量数增大2倍,化学平衡常数应为K2,D项错误。
2.下列说法不正确的是( )
A.焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应是放热反应
B.在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大
C.一个反应能否自发进行取决于该反应是放热还是吸热
D.一个反应能否自发进行,与焓变和熵变的共同影响有关
解析:选C。一个反应能否自发进行应由该反应的熵变和焓变共同判断,C项错误。
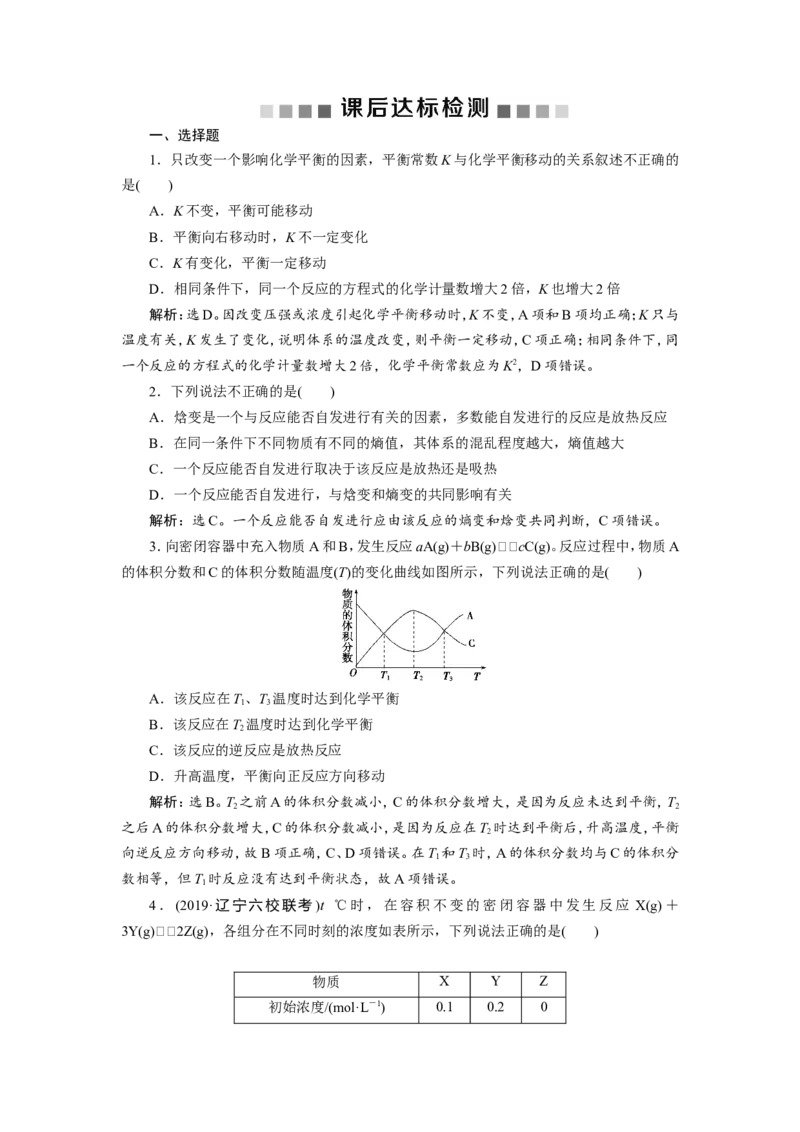
3.向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)cC(g)。反应过程中,物质A
的体积分数和C的体积分数随温度(T)的变化曲线如图所示,下列说法正确的是( )
A.该反应在T、T 温度时达到化学平衡
1 3
B.该反应在T 温度时达到化学平衡
2
C.该反应的逆反应是放热反应
D.升高温度,平衡向正反应方向移动
解析:选B。T 之前A的体积分数减小,C的体积分数增大,是因为反应未达到平衡,T
2 2
之后A的体积分数增大,C的体积分数减小,是因为反应在T 时达到平衡后,升高温度,平衡
2
向逆反应方向移动,故B项正确,C、D项错误。在T 和T 时,A的体积分数均与C的体积分
1 3
数相等,但T 时反应没有达到平衡状态,故A项错误。
1
4.(2019·辽宁六校联考)t ℃时,在容积不变的密闭容器中发生反应 X(g)+
3Y(g)2Z(g),各组分在不同时刻的浓度如表所示,下列说法正确的是( )
物质 X Y Z
初始浓度/(mol·L-1) 0.1 0.2 02 min时浓度/(mol·L-1) 0.08 a b
平衡浓度/(mol·L-1) 0.05 0.05 0.1
A. 平衡时,X的转化率为20%
B.t ℃时,该反应的平衡常数为40
C.平衡后,增大体系压强,
v正
增大,
v逆
减小,平衡向正反应方向移动
D.前2 min内,用Y的变化量表示的平均反应速率 v(Y)=0.03 mol·L-1·min-1
解析:选D。平衡时,X的转化率=×100%=50%,A项错误;t ℃时该反应的平衡常数K
==1 600,B项错误;该反应是气体分子数减小的反应,平衡后,增大体系压强,
v正
、
v逆
均增
大,平衡向正反应方向移动,C项错误;前2 min内,用Y的变化量表示的平均反应率 v(Y)=
3v(X) = 3× = 0.03 mol·
L-1·min-1,D项正确。
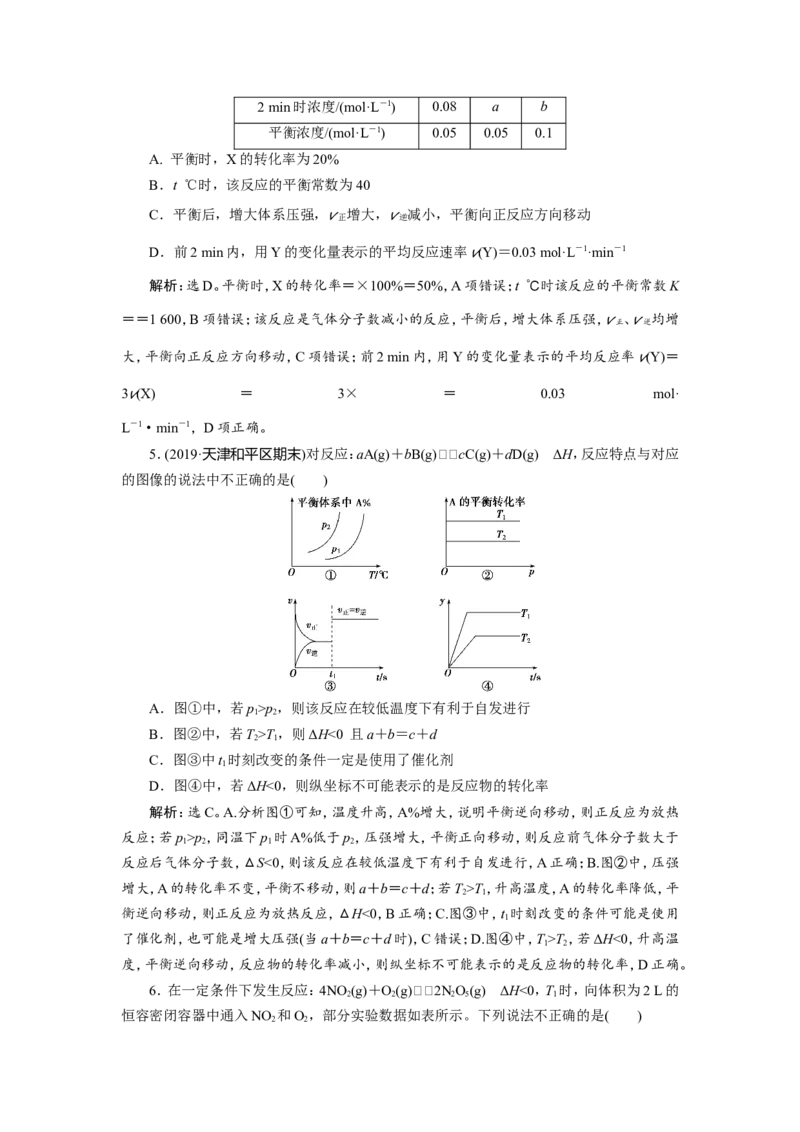
5.(2019·天津和平区期末)对反应:aA(g)+bB(g)cC(g)+dD(g) ΔH,反应特点与对应
的图像的说法中不正确的是( )
A.图①中,若p>p,则该反应在较低温度下有利于自发进行
1 2
B.图②中,若T>T,则ΔH<0 且a+b=c+d
2 1
C.图③中t 时刻改变的条件一定是使用了催化剂
1
D.图④中,若ΔH<0,则纵坐标不可能表示的是反应物的转化率
解析:选C。A.分析图①可知,温度升高,A%增大,说明平衡逆向移动,则正反应为放热
反应;若p>p,同温下p 时A%低于p,压强增大,平衡正向移动,则反应前气体分子数大于
1 2 1 2
反应后气体分子数,ΔS<0,则该反应在较低温度下有利于自发进行,A正确;B.图②中,压强
增大,A的转化率不变,平衡不移动,则a+b=c+d;若T>T,升高温度,A的转化率降低,平
2 1
衡逆向移动,则正反应为放热反应,ΔH<0,B正确;C.图③中,t 时刻改变的条件可能是使用
1
了催化剂,也可能是增大压强(当a+b=c+d时),C错误;D.图④中,T>T,若ΔH<0,升高温
1 2
度,平衡逆向移动,反应物的转化率减小,则纵坐标不可能表示的是反应物的转化率,D正确。
6.在一定条件下发生反应:4NO (g)+O(g)2NO(g) ΔH<0,T 时,向体积为2 L的
2 2 2 5 1
恒容密闭容器中通入NO 和O,部分实验数据如表所示。下列说法不正确的是( )
2 2时间/s 0 5 10 15
c(NO )/(mol·L-1) 4.00 2.52 2.00 c
2 3
c(O )/(mol·L-1) 1.00 c c 0.50
2 1 2
A. 0~5 s内NO 的平均反应速率为0.148 mol·L-1·s-1
2 5
B.其他条件不变,将容器体积压缩一半,则重新达到平衡时c(N O)<2.00 mol·L-1
2 5
C.设T 时平衡常数为K ,T 时平衡常数为K ,若TK
1 1 2 2 1 2 1 2
D.T 时平衡常数为0.125,平衡时NO 和O 的转化率均为50%
1 2 2
解析:选B。0~5 s内, v(N
2
O
5
)= v(NO
2
)=×=0.148 mol·
L-1·s-1,A项正确;根据反应物转化的物质的量之比等于化学计量数之比,可得c=0.63,c
1 2
=0.50,c=2.00,由此可知10 s时达到平衡,平衡时c(N O)=1.00 mol·L-1,将容器体积压缩
3 2 5
一半,此时c(N O)=2.00 mol·L-1,随后平衡正向移动,c(N O)>2.00 mol·L-1,B项错误;对
2 5 2 5
于放热反应,温度越高,平衡常数越小,C项正确;达到平衡时c(NO )=2.00 mol·
2
L-1,c(O )=0.50 mol·L-1,c(N O)=1.00 mol·L-1,K==0.125,平衡时NO 的转化率为
2 2 5 2
×100%=50%,O 的转化率为×100%=50%,D项正确。
2
7.(2019·烟台自主练习)已知NO和O 经反应①和反应②转化为NO ,其能量变化随反
2 2
应过程如图所示。
①2NO(g)NO(g) ΔH,平衡常数K
2 2 1 1
②NO(g)+O(g)2NO (g) ΔH,平衡常数K
2 2 2 2 2 2
下列说法中不正确的是( )
A.ΔH<0,ΔH<0
1 2
B.2NO(g)+O(g)2NO (g)的平衡常数K=K /K
2 2 1 2
C.2NO(g)+O(g)2NO (g)的ΔH=ΔH+ΔH
2 2 1 2
D.反应②的速率大小决定2NO(g)+O(g)2NO (g)的反应速率
2 2
解析:选B。由题图可知,反应①和反应②的反应物总能量均高于生成物总能量,所以
ΔH<0,ΔH<0,A项正确;反应①+反应②得2NO(g)+O(g)2NO (g),所以K=K ·K ,
1 2 2 2 1 2
B项错误;反应①+反应②得2NO(g)+O(g)2NO (g),所以ΔH=ΔH+ΔH,C项正确;反
2 2 1 2
应速率主要取决于慢反应的反应速率,反应②的活化能大于反应①,所以反应②的反应速率
小于反应①,故反应②的速率大小决定2NO(g)+O(g)2NO (g)的反应速率,D项正确。
2 2
8.(2019·衡水中学高三期末)在容积均为1 L的三个密闭
容器中,分别放入镍粉并充入1 mol CO,控制在不同温度下发生反应:Ni(s)+4CO(g)Ni(CO) (g),当反应进行到5 min时,测得Ni(CO) 的体积分数与
4 4
温度的关系如图所示。下列说法正确的是( )
A.正反应为吸热反应,平衡常数:K(T)>K(T)
1 2
B.反应进行到5 min时,b容器中 v正 (CO)= v逆 (CO)
C.达到平衡时,a、b、c中CO的转化率为b>a>c
D.减压或升温可将b中的平衡状态转变成c中的平衡状态
解析:选D。温度越低,反应速率越慢,再结合a、b、c三容器中Ni(CO) 的体积分数可知,
4
a容器中反应未达到平衡,b→c的变化则说明随温度升高,化学平衡逆向移动,则正反应为放
热反应,A错误;反应进行到5 min时,b容器未必达到平衡状态,则b容器中
v正
(CO)不一定
等于
v逆
(CO),B错误;其他条件相同时,随温度升高,平衡逆向移动,K减小,CO转化率减小,
故达到平衡时,CO的转化率为a>b>c,C错误;结合A项分析知,升温可使b中的平衡状态转
变为c中的平衡状态,减压平衡逆向移动,导致Ni(CO) 浓度变小,即可使b中的平衡状态转
4
变为c中的平衡状态,D正确。
9.(热点题)在一恒容的密闭容器中充入0.1 mol·L-1 CO、0.1 mol·L-1CH,在一定条件
2 4
下发生反应:CH(g)+CO(g)2CO(g)+2H(g),测得CH 平衡时转化率与温度、压强关系
4 2 2 4
如图。下列有关说法不正确的是( )
A.上述反应的ΔH>0
B.压强:p>p>p>p
4 3 2 1
C.1 100 ℃时该反应平衡常数为1.64
D.压强为p 4 时,在Y点: v正 0,A项正确;该反应为气体分子数增加的反应,压强越大,CH 的平衡转化率越小,
4
故p>p>p>p,B项正确;1 100 ℃时,甲烷的平衡转化率为80.00%,故平衡时各物质的浓度
4 3 2 1
分别为c(CH)=0.02 mol·L-1,c(CO)=0.02 mol·L-1,c(CO)=0.16 mol·L-1,c(H )=0.16
4 2 2
mol·L-1,即平衡常数K=≈1.64,C项正确;压强为p 时,Y点反应未达到平衡,需增大CH
4 4
的转化率才能达到平衡,此时 v正 >v逆 ,D项错误。
10.(2019·遂宁诊断)固定容积为2 L的密闭容器中发生反应xA(g)+yB(g)zC(g),图1
表示T ℃时容器中各物质的量随时间变化的关系,图2表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是( )
A.该反应可表示为2A(g)+B(g)C(g) ΔH<0
B.T ℃时该反应的平衡常数K=6.25
C.当容器中气体密度不再变化时,该反应达到平衡状态
D.T ℃,在第6 min时再向体系中充入0.4 mol C,再次达到平衡时C的体积分数大于
0.25
解析:选D。A项,由图2知,升高温度,平衡常数逐渐增大,该反应为吸热反应,ΔH>0,
错误;B项,根据图1知0~5 min内,A、B、C变化的物质的量分别为0.4 mol、0.2 mol、0.2
mol,该反应可表示为2A(g)+B(g)C(g),反应达到平衡时A、B、C的平衡浓度分别为0.2
mol·L-1、0.1 mol·L-1、0.1 mol·L-1,故T ℃时该反应的平衡常数K==25,错误;C项,根据质
量守恒定律知,容器内气体的质量保持不变,容器的容积保持不变,故容器内气体的密度为
恒量,不能作为平衡标志,错误;D项,根据图1知T ℃时反应达平衡后C的体积分数为
0.25,在第6 min时再向体系中充入0.4 mol C,相当于加压,平衡正向移动,再次达到平衡时,
C的体积分数大于0.25,正确。
二、非选择题
11.将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试
样体积忽略不计),在恒定温度下使其达到分解平衡:NH COONH(s)2NH (g)+CO(g)。实
2 4 3 2
验测得不同温度下的平衡数据列于下表:
温度/℃ 15.0 20.0 25.0 30.0 35.0
平衡总压强/kPa 5.7 8.3 12.0 17.1 24.0
平衡气体总浓度/
2.4 3.4 4.8 6.8 9.4
(×10-3 mol·L-1)
(1)该反应的焓变ΔH________0,熵变ΔS________0(填“>”“<”或“=”)。
(2)可以判断该分解反应已经达到化学平衡的是________(填字母)。
A.2v正 (NH 3 )= v逆 (CO 2 )
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中NH 的体积分数不变
3
(3)根据表中数据计算,在25.0 ℃时,反应2NH (g)+CO(g)NH COONH(s)的平衡常
3 2 2 4
数K=________。
(4)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25 ℃下达到平衡
状态。若在恒温下压缩容器体积,氨基甲酸铵固体的质量________(填“增大”“减小”或“不变”)。
解析:(1)分析表中数据可知,升高温度,平衡气体总浓度增大,说明平衡正向移动,该反
应为吸热反应,则有ΔH>0;该反应是气体体积增大的反应,则有ΔS>0。
(2)达到平衡时,正、逆反应速率相等,则有 v正 (NH 3 )=2v逆 (CO 2 ),A项不符合题意;因为
反应前后气体分子数不相等,未达到平衡前压强一直在变,所以总压强不变时,说明反应达
到平衡,B项符合题意;反应未达到平衡前,气体质量一直在变,而容器容积不变,根据ρ=可
知,混合气体的密度也在变,所以混合气体的密度不变时,说明反应达到平衡,C项符合题意;
反应产物中NH 和CO 的物质的量之比始终为2∶1,密闭容器中NH 的体积分数始终不变,
3 2 3
D项不符合题意。
(3)由表中数据可知,在25.0 ℃时,平衡气体的总浓度为4.8×10-3 mol·L-1,则有c(NH )
3
=3.2×10-3 mol·L-1,c(CO)=1.6×10-3 mol·L-1,反应2NH (g)+CO(g)NH COONH(s)
2 3 2 2 4
的平衡常数K=≈6.1×107。
(4)在恒温条件下压缩容器体积,平衡逆向移动,氨基甲酸铵固体的质量增大。
答案:(1)> > (2)BC (3)6.1×107 (4)增大
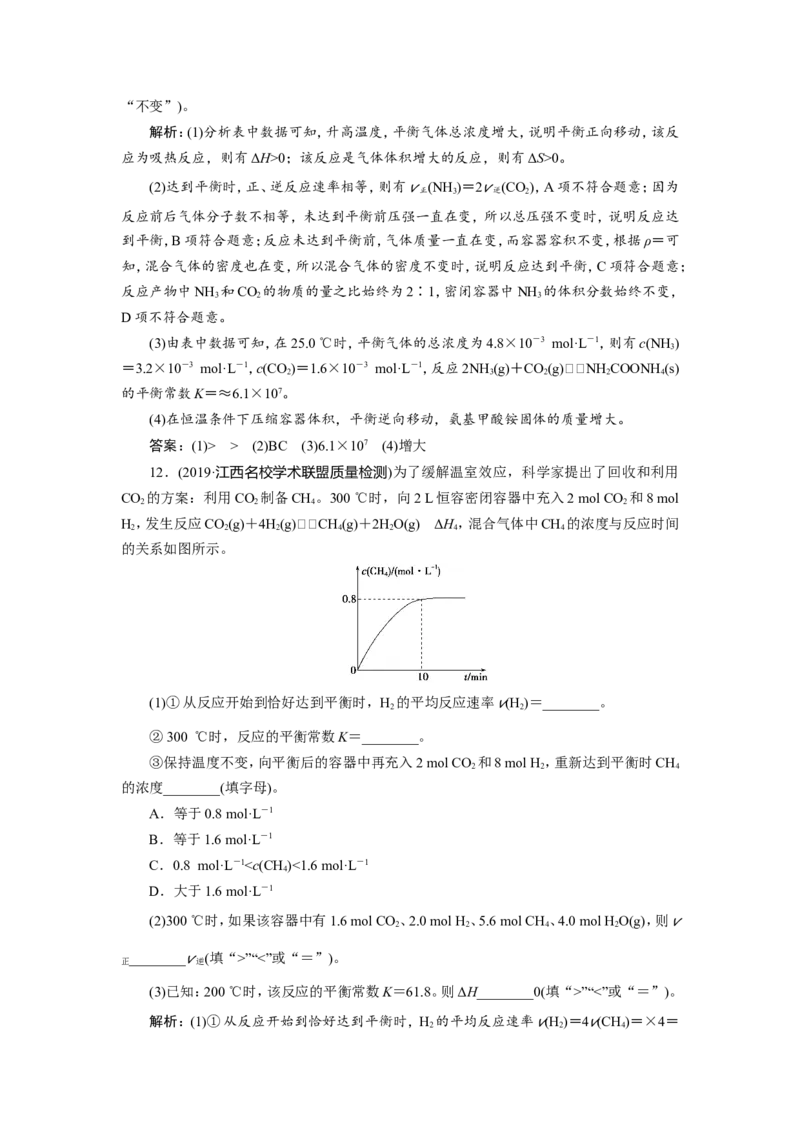
12.(2019·江西名校学术联盟质量检测)为了缓解温室效应,科学家提出了回收和利用
CO 的方案:利用CO 制备CH 。300 ℃时,向2 L恒容密闭容器中充入2 mol CO 和8 mol
2 2 4 2
H,发生反应CO(g)+4H(g)CH(g)+2HO(g) ΔH,混合气体中CH 的浓度与反应时间
2 2 2 4 2 4 4
的关系如图所示。
(1)①从反应开始到恰好达到平衡时,H
2
的平均反应速率 v(H
2
)=________。
②300 ℃时,反应的平衡常数K=________。
③保持温度不变,向平衡后的容器中再充入2 mol CO 和8 mol H ,重新达到平衡时CH
2 2 4
的浓度________(填字母)。
A.等于0.8 mol·L-1
B.等于1.6 mol·L-1
C.0.8 mol·L-1”“<”或“=”)。
(3)已知:200 ℃时,该反应的平衡常数K=61.8。则ΔH________0(填“>”“<”或“=”)。
解析:(1)①从反应开始到恰好达到平衡时,H
2
的平均反应速率 v(H
2
)=4v(CH
4
)=×4=0.32 mol·L-1·min-1。
② CO(g)+4H(g)CH(g)+2HO(g)
2 2 4 2
1 4 0 0
0.8 3.2 0.8 1.6
0.2 0.8 0.8 1.6
300 ℃时,反应的平衡常数K==25。
③保持温度不变,向平衡后的容器中再充入2 mol CO 和8 mol H ,相当于增大压强,平
2 2
衡正向移动,则重新达到平衡时CH 的浓度大于1.6 mol·L-1。
4
(2)Q c ==14v逆 。
(3)200 ℃时,该反应的平衡常数K=61.8,说明升高温度,平衡常数减小,平衡逆向移动,
正反应为放热反应,则ΔH<0。
答案:(1)①0.32 mol·L-1·min-1 ②25 ③D
(2)> (3)<
13.(2019·辽宁五校协作体联考)“绿水青山就是金山银山”。近年来,绿色发展、生态保
护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少
氮的氧化物在大气中的排放是环境保护的重要内容之一。请回答下列问题:
(1)已知:N(g)+O(g)===2NO(g) ΔH=+180.5 kJ·mol-1
2 2 1
C(s)+O(g)===CO (g) ΔH=-393.5 kJ·mol-1
2 2 2
2C(s)+O(g)===2CO(g) ΔH=-221 kJ·mol-1
2 3
若 某 反 应 的 平 衡 常 数 表 达 式 为 K = , 则 此 反 应 的 热 化 学 方 程 式 为
________________________________。
(2)N O 在一定条件下可发生分解反应:2NO(g)4NO (g)+O(g),某温度下向恒容密
2 5 2 5 2 2
闭容器中加入一定量NO,测得NO 浓度随时间的变化如下表:
2 5 2 5
t/min 0 1 2 3 4 5
c(N O)/
2 5
1.00 0.71 0.50 0.35 0.25 0.17
(mol·L-1)
①反应开始时体系压强为p,第2 min时体系压强为p,则p∶p=________。2~5 min
0 1 1 0
内用NO 表示的该反应的平均反应速率为________________。
2
②一定温度下,在恒容密闭容器中充入一定量NO 进行该反应,能判断反应已达到化学
2 5
平衡状态的是________________(填字母)。
a.NO 和O 的浓度比保持不变
2 2
b.容器中压强不再变化
c.2v正 (NO 2 )= v逆 (N 2 O 5 )
d.气体的密度保持不变
(3)K 是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用
p平衡分压代替。已知反应:NO
2
(g)+CO(g)NO(g)+CO
2
(g),该反应中正反应速率
v正
=k
正 ·p(NO 2 )·p(CO),逆反应速率 v逆 =k 逆 ·p(NO)·p(CO 2 ),其中k 正 、k 逆 为速率常数,则K p 为
________________(用k 、k 表示)。
正 逆
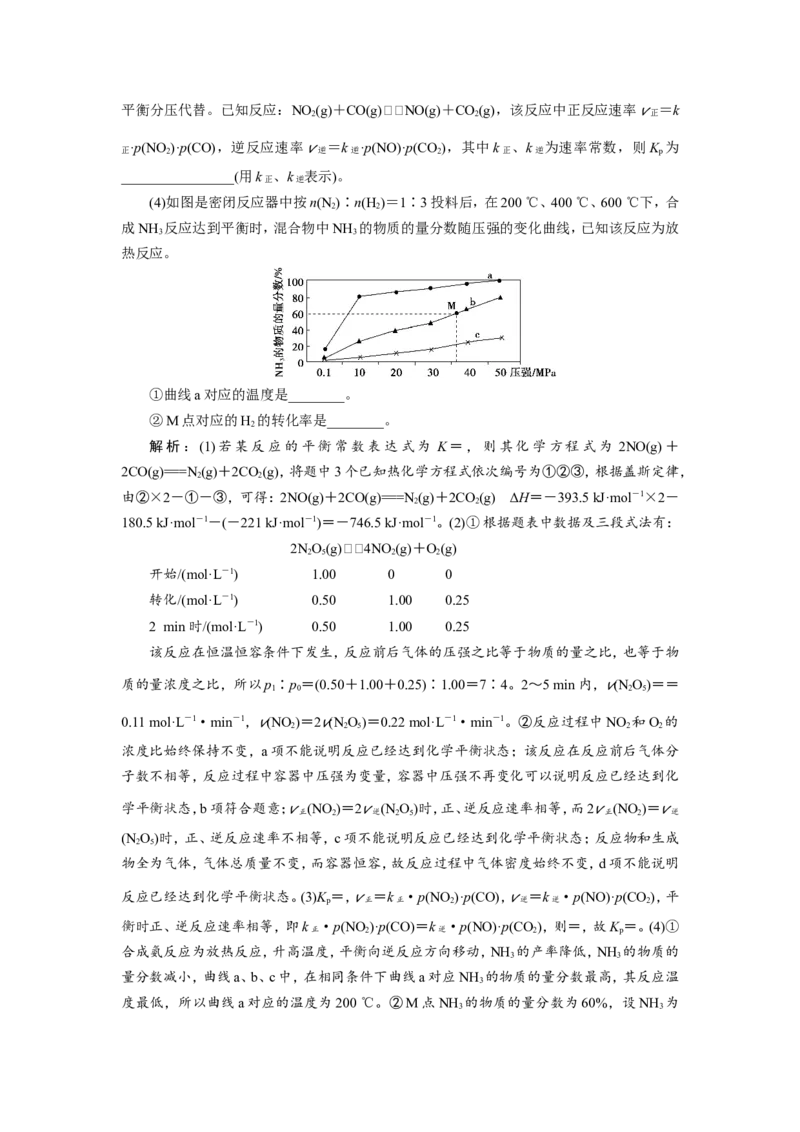
(4)如图是密闭反应器中按n(N )∶n(H )=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合
2 2
成NH 反应达到平衡时,混合物中NH 的物质的量分数随压强的变化曲线,已知该反应为放
3 3
热反应。
①曲线a对应的温度是________。
②M点对应的H 的转化率是________。
2
解析:(1)若某反应的平衡常数表达式为 K=,则其化学方程式为 2NO(g)+
2CO(g)===N (g)+2CO(g),将题中3个已知热化学方程式依次编号为①②③,根据盖斯定律,
2 2
由②×2-①-③,可得:2NO(g)+2CO(g)===N (g)+2CO(g) ΔH=-393.5 kJ·mol-1×2-
2 2
180.5 kJ·mol-1-(-221 kJ·mol-1)=-746.5 kJ·mol-1。(2)①根据题表中数据及三段式法有:
2NO(g)4NO (g)+O(g)
2 5 2 2
开始/(mol·L-1) 1.00 0 0
转化/(mol·L-1) 0.50 1.00 0.25
2 min时/(mol·L-1) 0.50 1.00 0.25
该反应在恒温恒容条件下发生,反应前后气体的压强之比等于物质的量之比,也等于物
质的量浓度之比,所以p
1
∶p
0
=(0.50+1.00+0.25)∶1.00=7∶4。2~5 min内, v(N
2
O
5
)==
0.11 mol·L-1·min-1, v(NO
2
)=2v(N
2
O
5
)=0.22 mol·L-1·min-1。②反应过程中NO
2
和O
2
的
浓度比始终保持不变,a项不能说明反应已经达到化学平衡状态;该反应在反应前后气体分
子数不相等,反应过程中容器中压强为变量,容器中压强不再变化可以说明反应已经达到化
学平衡状态,b项符合题意; v正 (NO 2 )=2v逆 (N 2 O 5 )时,正、逆反应速率相等,而2v正 (NO 2 )= v逆
(N O)时,正、逆反应速率不相等,c项不能说明反应已经达到化学平衡状态;反应物和生成
2 5
物全为气体,气体总质量不变,而容器恒容,故反应过程中气体密度始终不变,d项不能说明
反应已经达到化学平衡状态。(3)K
p
=,
v正
=k
正
·p(NO
2
)·p(CO),
v逆
=k
逆
·p(NO)·p(CO
2
),平
衡时正、逆反应速率相等,即k ·p(NO )·p(CO)=k ·p(NO)·p(CO),则=,故K =。(4)①
正 2 逆 2 p
合成氨反应为放热反应,升高温度,平衡向逆反应方向移动,NH 的产率降低,NH 的物质的
3 3
量分数减小,曲线a、b、c中,在相同条件下曲线a对应NH 的物质的量分数最高,其反应温
3
度最低,所以曲线a对应的温度为200 ℃。②M点NH 的物质的量分数为60%,设NH 为
3 30.6a mol,则N、H 共为0.4a mol,因为反应器中按n(N )∶n(H )=1∶3投料,故M点时H
2 2 2 2 2
为0.3a mol,结合N(g)+3H(g)2NH (g)可知,转化的H 的物质的量为0.9a mol,所以M
2 2 3 2
点对应H 的转化率=×100%=75%。
2
答案:(1)2NO(g)+2CO(g)===N (g)+2CO(g) ΔH=-746.5 kJ·mol-1
2 2
(2)①7∶4(或1.75∶1) 0.22 mol·L-1·min-1 ②b
(3)
(4)①200 ℃ ②75%