文档内容
第三篇 化学反应与能量
专项 24 金属的腐蚀与防护
金属腐蚀,是金属和周围介质接触时由于发生化学和电化学作用而引起的破坏作用。金属腐蚀是自发
的普遍存在的现象,金属被腐蚀后,在外形、色泽以及机械性能方面都将发生变化。造成设备破坏、管道
泄漏、产品污染,酿成燃烧或爆炸等恶性事故以及资源和能源的严重浪费,遭受巨大的经济损失。金属腐
蚀是一个亟待解决的问题,每年由于金属的腐蚀所引起的损失是巨大的。在新高考中逐渐出现相关的题型,
要理解化学腐蚀与电化学腐蚀,联系生产、生活中的金属腐蚀现象,会分析和区别化学腐蚀和电化学腐蚀,
了解一般防腐蚀方法。
1.(2022•广东选择性考试)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁
片放入酸化的3%NaCl溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是( )
A.加入AgNO 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
3
C.加入KSCN溶液无红色出现 D.加入K[Fe(CN) ]溶液无蓝色沉淀生成
3 6
【答案】D
【解析】镀层有破损的镀锌铁片被腐蚀,则将其放入到酸化的3%NaCl溶液中,会构成原电池,由于
锌比铁活泼,作原电池的负极,而铁片作正极,溶液中破损的位置会变大,铁也会继续和酸化的氯化钠溶
液反应产生氢气,溶液中会有亚铁离子生成。A项,氯化钠溶液中始终存在氯离子,所以加入硝酸银溶液
后,不管铁片是否被腐蚀,均会出现白色沉淀,故A不符合题意;B项,淀粉碘化钾溶液可检测氧化性物
质,但不论铁片是否被腐蚀,均无氧化性物质可碘化钾发生反应,故B不符合题意;C项,KSCN溶液可
检测铁离子的存在,上述现象中不会出现铁离子,所以无论铁片是否被腐蚀,加入KSCN溶液后,均无红
色出现,故C不符合题意;D项,K[Fe(CN) ]是用于检测Fe2+的试剂,若铁片没有被腐蚀,则溶液中不会
3 6
生成亚铁离子,则加入K[Fe(CN) ]溶液就不会出现蓝色沉淀,故D符合题意。故选D。
3 6
2.(2020•江苏卷)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情境
中,下列有关说法正确的是( )A.阴极的电极反应式为
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
【答案】C
【解析】A项,阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A错误;B项,
阳极金属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性比Fe的
活动性强,故B错误;C项,金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电
子,自身金属不再失电子从而被保护,故C正确;D项,海水中的离子浓度大于河水中的离子浓度,离子
浓度越大,溶液的导电性越强,因此钢铁设施在海水中的腐蚀速率比在河水中快,故D错误;故选C。
3.(2019•江苏卷)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化
学腐蚀实验。下列有关该实验的说法正确的是( )
A.铁被氧化的电极反应式为Fe−3e−=Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
【答案】C
【解析】A.该装置中发生吸氧腐蚀,Fe作负极,Fe失电子生成亚铁离子,电极反应式为 Fe﹣2e﹣
═Fe2+,故A错误;B.铁腐蚀过程发生电化学反应,部分化学能转化为电能,放热,所以还存在化学能转
化为热能的变化,故B错误;C.Fe、C和电解质溶液构成原电池,Fe易失电子被腐蚀,加速Fe的腐蚀,故C正确;D.弱酸性或中性条件下铁腐蚀吸氧腐蚀,水代替NaCl溶液,溶液仍然呈中性,Fe发生吸氧
腐蚀,故D错误;故选C。
1.金属的腐蚀
(1)吸氧腐蚀:钢铁表面吸附的水膜酸性很弱或呈中性时,氧气参加电极反应,发生吸氧腐蚀。
(2)析氢腐蚀:金属表面的电解质溶液酸性较强,腐蚀过程中不断有H 放出。
2
2.判断金属腐蚀快慢的方法
(1)在同一电解质溶液中,金属腐蚀由快到慢的顺序为:电解原理引起的腐蚀>原电池原理引起的腐蚀>
化学腐蚀>应用原电池原理有防护措施的腐蚀>应用电解原理有防护措施的腐蚀,或电解池阳极>原电池负
极>化学腐蚀>原电池正极>电解池阴极。
(2)同一种金属在不同介质中腐蚀由快到慢的顺序为:强电解质溶液中的腐蚀>弱电解质溶液中的腐蚀>
非电解质溶液中的腐蚀。
(3)对于活泼性不同的两种金属,活泼性差别越大,氧化还原反应速率越快,活泼金属腐蚀越快。
(4)对于同一电解质溶液,电解质溶液浓度越大,金属腐蚀越快(除钝化外)。
(5)纯度越高的金属,腐蚀的速率越慢(纯金属几乎不被腐蚀)。
(6)不纯的金属或合金,在潮湿的空气中腐蚀速率远大于在干燥、隔绝空气条件下的腐蚀速率。
3.电化学防护法
电化学防护 牺牲阳极的阴极保护法 外加电流的阴极保护法
依据 原电池原理 电解池原理
形成原电池时,被保护金属作正极 将被保护金属与另一附加电极作为电
(阴极),不反应受到保护;活泼金属 解池的两个极,使被保护金属作阴
原理
作负极(阳极),发生反应受到腐蚀。 极,在外加直流电的作用下使阴极得
阳极要定期予以更换 到保护
应用 一些钢铁设备如锅炉内壁、船体外壳 土壤、海水及河水中的金属设备等等装上镁合金或锌块
实例示意图
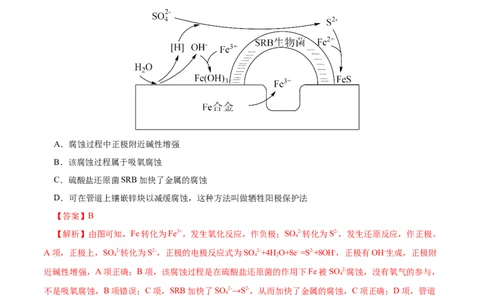
1.(2023届·山东省日照市校际联考)深埋在潮湿土壤中的铁管道,在硫酸盐还原菌的作用下能被SO 2-腐
4
蚀,原理如图所示。下列说法错误的是( )
A.腐蚀过程中正极附近碱性增强
B.该腐蚀过程属于吸氧腐蚀
C.硫酸盐还原菌SRB加快了金属的腐蚀
D.可在管道上镶嵌锌块以减缓腐蚀,这种方法叫做牺牲阳极保护法
【答案】B
【解析】由图可知,Fe转化为Fe3+,发生氧化反应,作负极;SO 2-转化为S2-,发生还原反应,作正极。
4
A项,正极上,SO 2-转化为S2-,正极的电极反应式为SO 2-+4H O+8e- =S2-+8OH-,正极有OH-生成,正极附
4 4 2
近碱性增强,A项正确;B项,该腐蚀过程是在硫酸盐还原菌的作用下Fe被SO 2-腐蚀,没有氧气的参与,
4
不是吸氧腐蚀,B项错误;C项,SRB加快了SO 2-→S2-,从而加快了金属的腐蚀,C项正确;D项,管道
4
上镶嵌更为活泼的锌块以减缓腐蚀,属于牺牲阳极的阴极保护法,D项正确;故选B。
2.(2022·河南省豫南名校联考《本草纲目》中载有一药物,名“铜青[Cu OH) CO]”。铜青则是铜器
2( 2 3
上绿色者,淘洗用之。时珍曰:近时人以醋制铜生绿,取收晒干货之。下列有关说法正确的是( )
A.铜在空气中主要发生析氢腐蚀
B.铜在O、CO、HO存在时易发生电化学腐蚀
2 2 2
C.用硝酸清洗铜器可以除去铜绿,保护铜器
D.每生成111g Cu (OH) CO,转移1mol电子
2 2 3【答案】B
【解析】A项,铜在空气中被腐蚀的化学方程式为2Cu+O +CO +H O=Cu OH) CO,则铜在空气中主
2 2 2 2( 2 3
要发生吸氧腐蚀,A错误;B项,铜在空气中被腐蚀的化学方程式为2Cu+O +CO +H O=Cu (OH) CO,铜
2 2 2 2 2 3
在O、CO、HO存在时易发生电化学腐蚀,B正确;C项,铜可以和硝酸反应,用硝酸清洗铜器可以除
2 2 2
去铜绿,但也会破坏铜器,C错误;D项,由化学方程式2Cu+O +CO +H O=Cu (OH) CO 可知,每生成
2 2 2 2 2 3
1mol Cu (OH) CO,转移4mol电子,则生成111g Cu (OH) CO(物质的量为0.5mol)时,转移2mol电子,D
2 2 3 2 2 3
错误;故选B。
3.(2022·山东省烟台二中等校期中)实验室利用如下装置模拟探究铝制品表面出现白斑的腐蚀现象。
下列说法正确的是( )
A.活性炭上发生氧化反应
B.电子从活性炭经电流表流向铝箔
C.NaCl既是离子导体又是电极反应物
D.总反应为4Al +3O + 6H O =4Al( OH) ,生成的Al(OH) 进一步脱水形成白斑
2 2 3 3
【答案】D
【解析】该装置为原电池,铝易失电子发生氧化反应而作负极,碳作正极,发生吸氧腐蚀,电子从负
极流向正极,阴离子向负极移动。A项,碳作正极,正极上氧气得电子生成氢氧根离子,则正极的反应为
2HO+O+4e-═4OH-,发生还原反应,故A错误;B项,铝易失电子做负极,碳作正极,电子从负极流向正
2 2
极,则电子从铝箔经电流表流向活性炭,故B错误;C项,负极电极反应式为Al-3e-=Al3+,正极反应式
O+2H O+4e-═4OH-,NaCl不是电极反应物,故C错误;D项,负极电极反应式为Al-3e-=Al3+,正极反应
2 2
式O+2H O+4e-═4OH-,总反应方程式为:4Al+3O +6H O═4Al(OH) ,生成的Al(OH) 分解生成Al O,则
2 2 2 2 3 3 2 3
白斑的主要成分可能是Al O,故D正确;故选D。
2 3
4.(2022·河南省豫北名校调研考试)用压强传感器探究生铁分别在pH=2.0、4.0和6.0的酸性溶液中发
生电化学腐蚀,得到反应体系气体压强与时间的关系如图。有关叙述错误的是( )A.负极的电极反应式均为:Fe-2e-=Fe2+
B.pH=2.0时,生铁主要发生析氢腐蚀
C.pH>4.0时,生铁主要发生吸氧腐蚀
D.一般情况下,化学腐蚀比电化学腐蚀普遍的多
【答案】D
【解析】生铁是由铁和C组成的合金,易发生电化学腐蚀,其中铁作负极,电极反应为:Fe-2e-
=Fe2+,C作正极,电极反应随溶液pH的变化而不同,强酸性时为2H++2e-=H ↑,弱酸性或中性、碱性时为
2
2HO+4e-+O =4OH-。A项,负极失电子,负极为铁,电极反应式为:Fe-2e - =Fe2+,A正确;B项,pH=2.0
2 2
时,溶液酸性较强,生铁发生析氢腐蚀,使得气压增大,B正确;C项,pH=4.0时,若只发生吸氧腐蚀,
气压应下降,而图中pH=4.0时,气压几乎不变,说明除了发生吸氧腐蚀,还发生了析氢腐蚀,当pH>4.0
时,气压减小,生铁主要发生吸氧腐蚀,C正确;D项,一般情况下电化学腐蚀比化学腐蚀普遍的多,D
错误;故选D。
5.(2022·广东·信宜市第二中学高二开学考试)金属的腐蚀与防护和生活密切相关,下列有关说法正确的
是( )
A.银首饰表面变黑属于电化学腐蚀
B.图中氧气传感器测得氧气体积分数变小,说明三颈瓶中发生的一定只有吸氧腐蚀
C.图中压强传感器测得压强变小,说明三颈瓶中发生的一定以吸氧腐蚀为主
D.海里在轮船外面连接一块废铜块保护轮船的方法叫牺牲阳极的阴极保护法
【答案】C【解析】A项,银首饰表面变黑是因为银和空气中极少量的硫化氢反应生成黑色的硫化银所致,发生了
化学腐蚀,A错误;B项,图中氧气传感器测得氧气体积分数变小,可能是发生吸氧腐蚀使氧气的量减少,
也可能是发生了析氢腐蚀,使混合气体的体积变大,从而造成氧气体积分数变小,B错误;C项,图中压
强传感器测得压强变小,说明三颈瓶中气体的物质的量减少了,则三颈瓶中主要发生了吸氧腐蚀,C正确;
D项,铜比铁不活泼,轮船外面连接一块废铜块,铁作负极被氧化,无法保护轮船,应该保护轮船锌等活
泼金属,D错误;故选C。
6.(2022·上海市杨浦中学教学质量评估)下列关于金属的腐蚀与防护的叙述不正确的是( )
A.图①马口铁(镀锡铁)即使镀层破损,依然不易生锈
B.图②若将钢闸门与电源的负极相连,可防止钢闸门腐蚀
C.图②若断开电源,钢闸门将发生吸氧腐蚀
D.图③若金属M比铁活泼,可防止钢铁输水管腐蚀
【答案】A
【解析】A项,由于Fe比Sn活泼,图①马口铁(镀锡铁)即使镀层破损,将因为与空气中的CO、HO、
2 2
O 等形成电化学腐蚀,加快铁生锈,A不正确;B项,图②若将钢闸门与电源的负极相连,则钢闸门作阴
2
极,故可防止钢闸门腐蚀,B正确;C项,图②若断开电源,钢闸门中将形成Fe和C两电极,在海水和O
2
作用下形成原电池,电解质溶液呈中性或弱酸性,故将发生吸氧腐蚀,C正确;D项,图③若金属M比铁
活泼,则M作负极,失电子,从而保护了铁,故可防止钢铁输水管腐蚀,D正确;故选A。
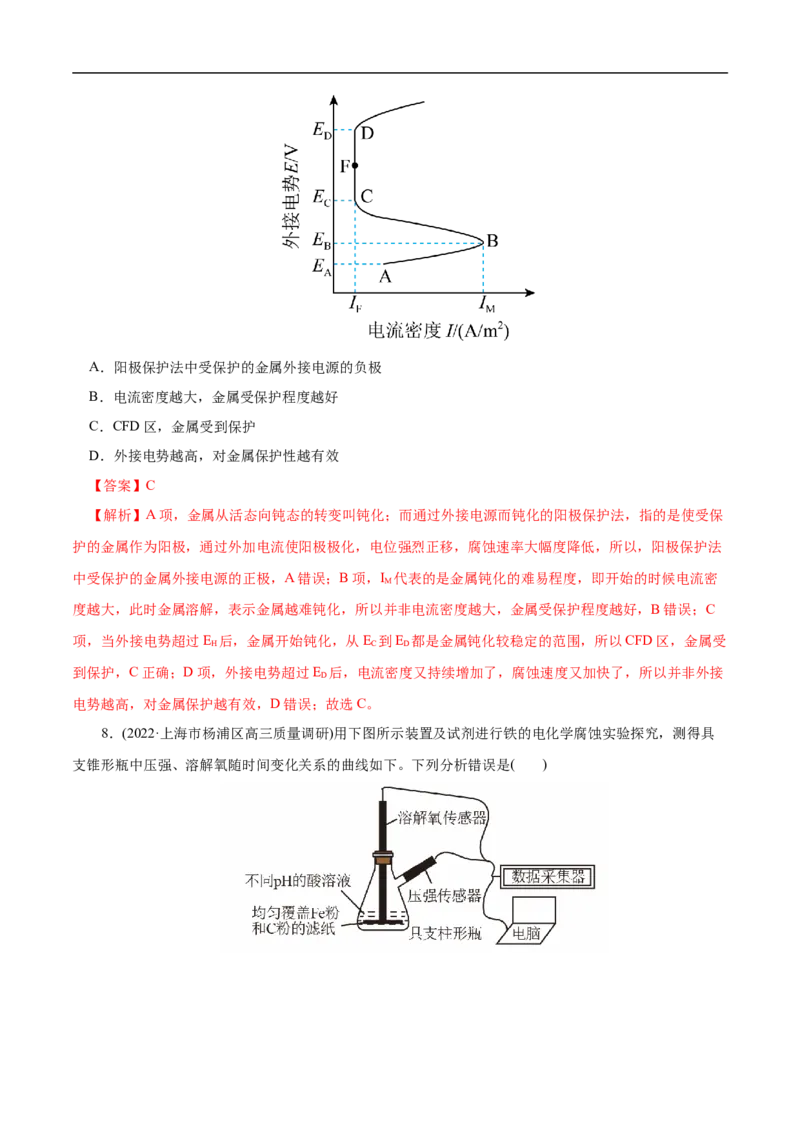
7.含可钝化金属的工业管道或反应器,由于会被内部溶液腐蚀,通过外接电源而钝化,称之为阳极保
护法。下图是某金属外接电势与电流密度的变化关系,有关说法正确的是( )A.阳极保护法中受保护的金属外接电源的负极
B.电流密度越大,金属受保护程度越好
C.CFD区,金属受到保护
D.外接电势越高,对金属保护性越有效
【答案】C
【解析】A项,金属从活态向钝态的转变叫钝化;而通过外接电源而钝化的阳极保护法,指的是使受保
护的金属作为阳极,通过外加电流使阳极极化,电位强烈正移,腐蚀速率大幅度降低,所以,阳极保护法
中受保护的金属外接电源的正极,A错误;B项,I 代表的是金属钝化的难易程度,即开始的时候电流密
M
度越大,此时金属溶解,表示金属越难钝化,所以并非电流密度越大,金属受保护程度越好,B错误;C
项,当外接电势超过E 后,金属开始钝化,从E 到E 都是金属钝化较稳定的范围,所以CFD区,金属受
H C D
到保护,C正确;D项,外接电势超过E 后,电流密度又持续增加了,腐蚀速度又加快了,所以并非外接
D
电势越高,对金属保护越有效,D错误;故选C。
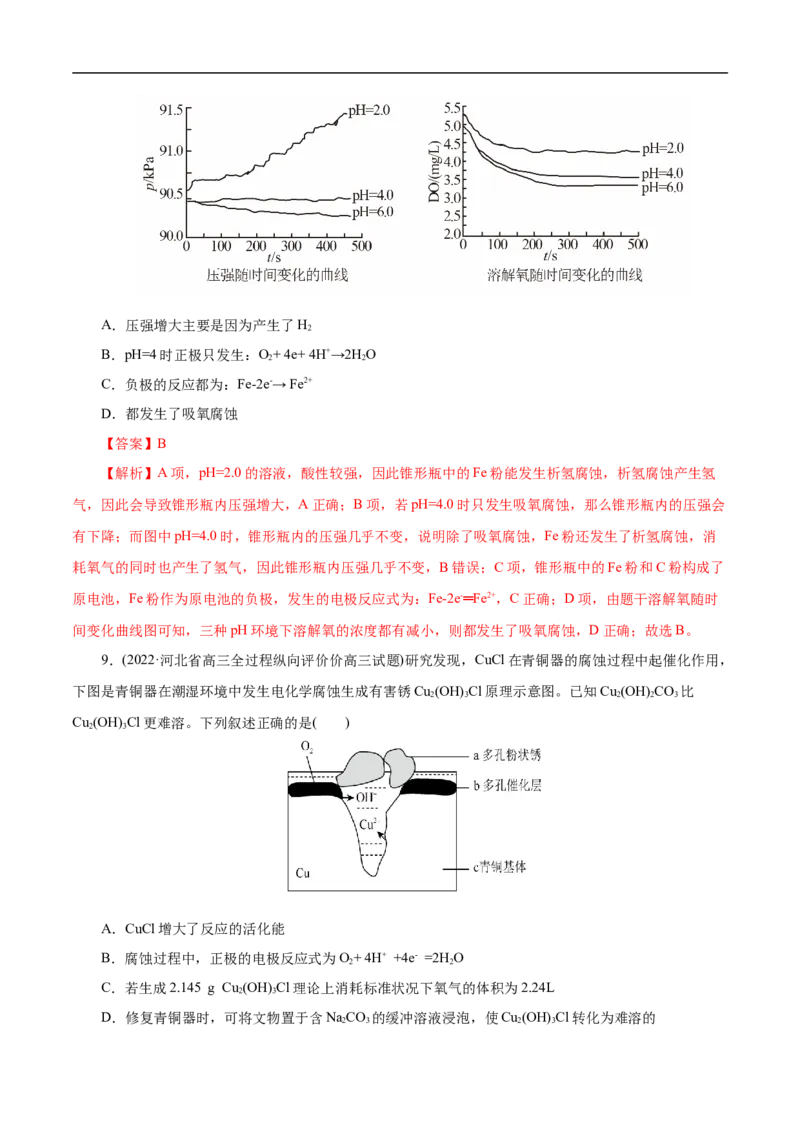
8.(2022·上海市杨浦区高三质量调研)用下图所示装置及试剂进行铁的电化学腐蚀实验探究,测得具
支锥形瓶中压强、溶解氧随时间变化关系的曲线如下。下列分析错误是( )A.压强增大主要是因为产生了H
2
B.pH=4时正极只发生:O+ 4e+ 4H+→2HO
2 2
C.负极的反应都为:Fe-2e-→ Fe2+
D.都发生了吸氧腐蚀
【答案】B
【解析】A项,pH=2.0的溶液,酸性较强,因此锥形瓶中的Fe粉能发生析氢腐蚀,析氢腐蚀产生氢
气,因此会导致锥形瓶内压强增大,A正确;B项,若pH=4.0时只发生吸氧腐蚀,那么锥形瓶内的压强会
有下降;而图中pH=4.0时,锥形瓶内的压强几乎不变,说明除了吸氧腐蚀,Fe粉还发生了析氢腐蚀,消
耗氧气的同时也产生了氢气,因此锥形瓶内压强几乎不变,B错误;C项,锥形瓶中的Fe粉和C粉构成了
原电池,Fe粉作为原电池的负极,发生的电极反应式为:Fe-2e-═Fe2+,C正确;D项,由题干溶解氧随时
间变化曲线图可知,三种pH环境下溶解氧的浓度都有减小,则都发生了吸氧腐蚀,D正确;故选B。
9.(2022·河北省高三全过程纵向评价价高三试题)研究发现,CuCl在青铜器的腐蚀过程中起催化作用,
下图是青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu (OH) Cl原理示意图。已知Cu (OH) CO 比
2 3 2 2 3
Cu (OH) Cl更难溶。下列叙述正确的是( )
2 3
A.CuCl增大了反应的活化能
B.腐蚀过程中,正极的电极反应式为O+ 4H+ +4e- =2H O
2 2
C.若生成2.145 g Cu (OH) Cl理论上消耗标准状况下氧气的体积为2.24L
2 3
D.修复青铜器时,可将文物置于含NaCO 的缓冲溶液浸泡,使Cu (OH) Cl转化为难溶的
2 3 2 3Cu (OH) CO
2 2 3
【答案】D
【解析】A项,催化剂降低了反应的活化能,增大活化分子百分数,A错误;B项,由图像可知CuCl
在青铜器的腐蚀属于吸氧腐蚀,故正极为氧气得电子,碱性环境下,其电极方程式为O+ 2H O+4e- =
2 2
4OH-,B错误;C项,生成2.145 g Cu (OH) Cl,物质的量 ,则转移电子物质的
2 3
量 , 氧气转移电子 ,则生成氧气为 ,标况下体积为
,C错误;D项,Cu (OH) Cl到Cu (OH) CO 难溶电解质的溶解平衡,
2 3 2 2 3
向更难溶的物质转化能更好的保护好文物,D正确。故选D。
10.(2022·黑龙江省哈师大附中高三模拟预测)厌氧性硫酸盐还原菌(SRB)是导致金属微生物腐蚀最为
普遍的菌种,腐蚀过程如图所示。下列说法正确的是( )
A.正极的电极反应式为8H++8e- = 8H·(吸附)、SO 2-+8H·(吸附) S2-+4H O
4 2
B.正极区溶液的pH变小
C.生成1molFeS,转移6mol电子
D.若引入新细菌,一定会加速金属的腐蚀
【答案】A
【解析】A项,根据示意图可知,正极上发生了2个电极反应,分别为8H++8e- = 8H·(吸附) (吸附)、
SO 2-+8H·(吸附) S2-+4H O,故A正确;B项,正极区消耗氢离子,所以溶液的pH变大,而
4 2不是减小,故B错误;C项,由A可知:生成1 molFeS,转移8mol电子,故C错误;D项,若引入新的
菌种,不一定能参与电极反应,故不一定会加速金属的腐蚀,故D错误;故选A。
11.(2022·福建省福州三中高三模拟)利用物质由高浓度向低浓度自发扩散的能量可制成浓差电池。在
海水中的不锈钢制品,缝隙处氧浓度比海水低,易形成浓差电池而发生缝隙腐蚀。缝隙处腐蚀机理如图所
示。下列说法不正确的是( )
A.金属缝隙内表面为负极,外自由表面为正极
B.缝隙内溶液pH增大,加快了缝隙内腐蚀速率
C.为了维持电中性,海水中大量Cl-进入縫隙
D.正极的电极反应为O+2H O+4e-=4OH-
2 2
【答案】B
【解析】A项,根据氧气得电子发生还原反应生成氢氧根离子,所以金属缝隙外自由表面为正极,金
属缝隙内表面为负极,A正确;B项,金属缝隙外自由表面为正极,生成氢氧根离子,缝隙外溶液pH增大,
加快了缝隙内腐蚀速率,B错误;C项,阴离子由正极向负极移动,所以大量Cl-进入缝隙维持电中性,C
正确;D项,正极为氧气得电子发生还原反应生成氢氧根离子,电极反应为O+2H O+4e-═4OH-,D正确;
2 2
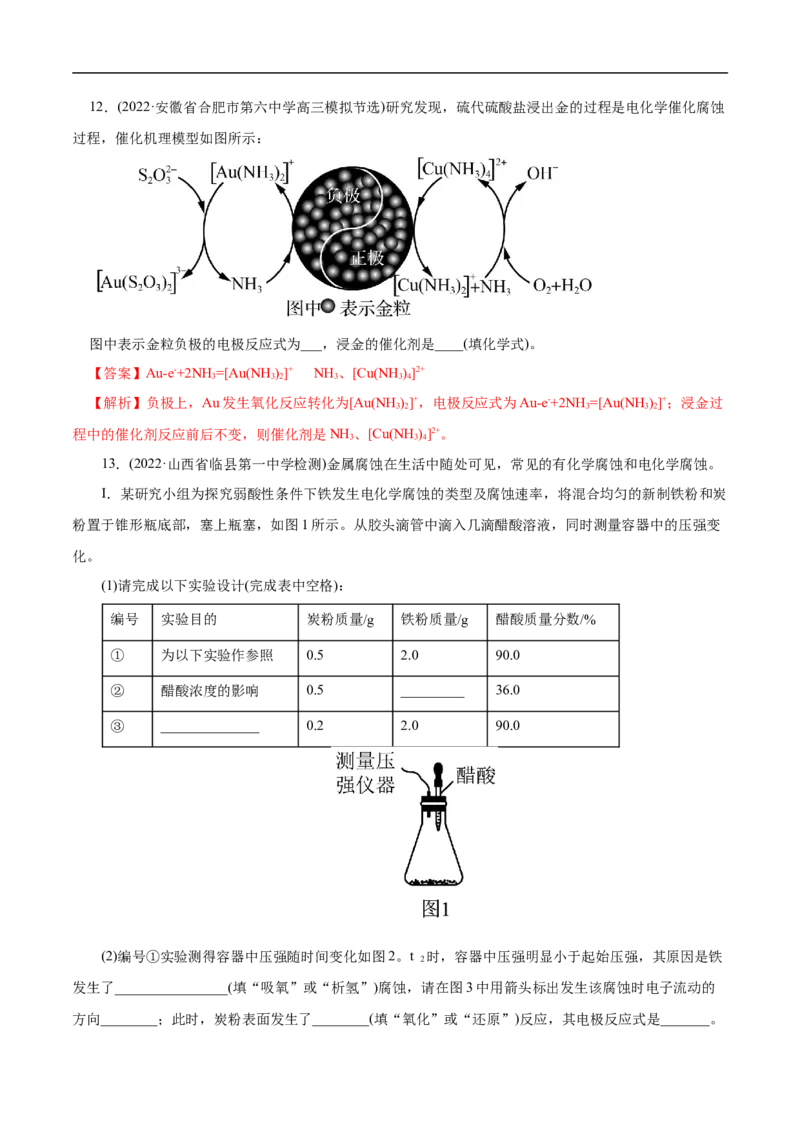
故选B。12.(2022·安徽省合肥市第六中学高三模拟节选)研究发现,硫代硫酸盐浸出金的过程是电化学催化腐蚀
过程,催化机理模型如图所示:
图中表示金粒负极的电极反应式为___,浸金的催化剂是____(填化学式)。
【答案】Au-e-+2NH=[Au(NH )]+ NH 、[Cu(NH )]2+
3 3 2 3 3 4
【解析】负极上,Au发生氧化反应转化为[Au(NH)]+,电极反应式为Au-e-+2NH=[Au(NH )]+;浸金过
3 2 3 3 2
程中的催化剂反应前后不变,则催化剂是NH 、[Cu(NH )]2+。
3 3 4
13.(2022·山西省临县第一中学检测)金属腐蚀在生活中随处可见,常见的有化学腐蚀和电化学腐蚀。
I.某研究小组为探究弱酸性条件下铁发生电化学腐蚀的类型及腐蚀速率,将混合均匀的新制铁粉和炭
粉置于锥形瓶底部,塞上瓶塞,如图1所示。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变
化。
(1)请完成以下实验设计(完成表中空格):
编号 实验目的 炭粉质量/g 铁粉质量/g 醋酸质量分数/%
① 为以下实验作参照 0.5 2.0 90.0
② 醋酸浓度的影响 0.5 _________ 36.0
③ ______________ 0.2 2.0 90.0
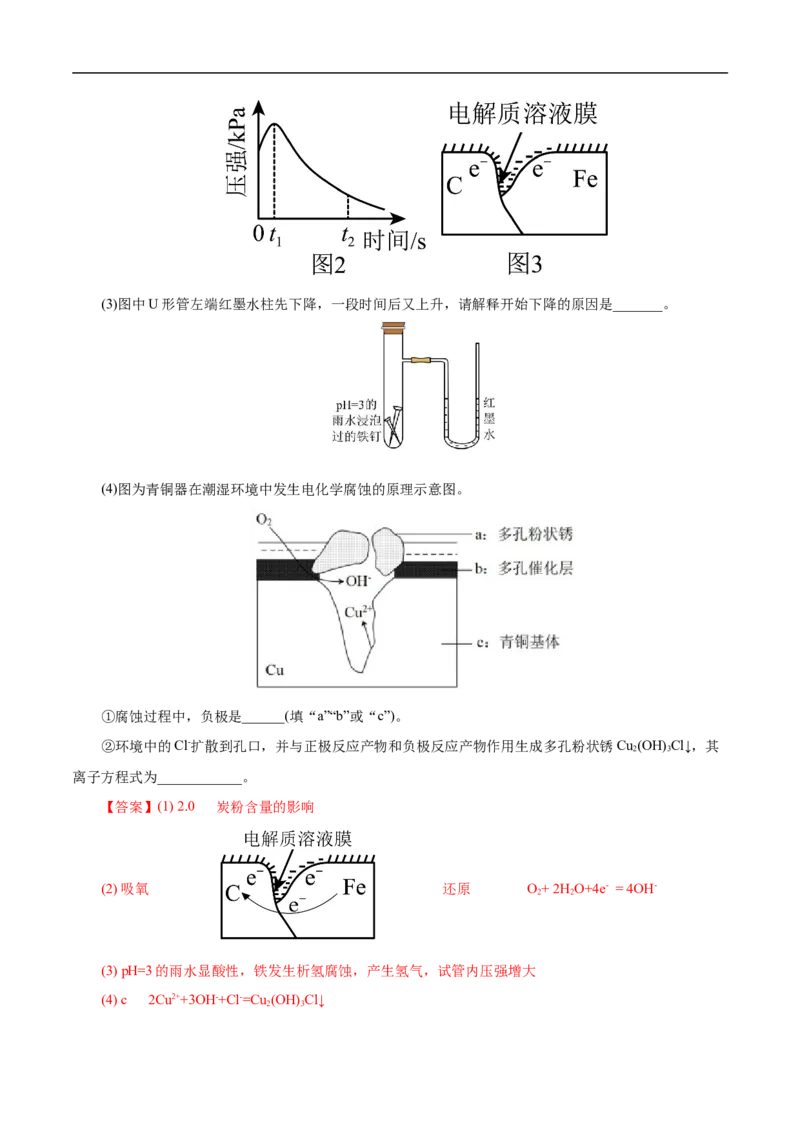
(2)编号①实验测得容器中压强随时间变化如图2。t 时,容器中压强明显小于起始压强,其原因是铁
2
发生了________________(填“吸氧”或“析氢”)腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动的
方向________;此时,炭粉表面发生了________(填“氧化”或“还原”)反应,其电极反应式是_______。(3)图中U形管左端红墨水柱先下降,一段时间后又上升,请解释开始下降的原因是_______。
(4)图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
①腐蚀过程中,负极是______(填“a”“b”或“c”)。
②环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu (OH) Cl↓,其
2 3
离子方程式为____________。
【答案】(1) 2.0 炭粉含量的影响
(2) 吸氧 还原 O+ 2H O+4e- = 4OH-
2 2
(3) pH=3的雨水显酸性,铁发生析氢腐蚀,产生氢气,试管内压强增大
(4) c 2Cu2++3OH-+Cl-=Cu (OH) Cl↓
2 3【解析】(1)探究弱酸条件下铁发生电化学腐蚀的类型及腐蚀速率,如图所示。②探究醋酸浓度的影响,
故铁粉质量不变,为2.0g;③炭粉质量变化,可知探究炭粉含量的影响;(2)t 时,容器中压强明显小于起
2
始压强,说明锥形瓶中气体体积减小,说明发生了吸氧腐蚀,碳为正极,铁为负极,电子转移的方向为
,碳电极氧气得到电子发生还原反应,电极反应式为O+ 2H O+4e- = 4OH-;(3) pH=3
2 2
的雨水显酸性,铁发生析氢腐蚀,产生氢气,试管内压强增大,故U形管左端红墨水柱下降。(4)①根据图
知,O 得电子生成OH-,Cu失电子生成Cu2+,发生吸氧腐蚀,则Cu作负极,即c是负极。②Cl-扩散到孔
2
口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu (OH) Cl,负极上生成Cu2+、正极上生成
2 3
OH-,所以该离子反应为2Cu2++3OH-+Cl-=Cu (OH) Cl↓。
2 3