文档内容
第五篇 水溶液中的离子反应与平衡
专项 34 K 图象
sp
图像是高考试题的形象化语言,化学图像题是一种利用数学中的二维图像来描述化学问题的题型,它
体现了数学方法在解决化学问题中的应用。它考查范围广。近几年沉淀溶解平衡图像这种数形结合的试题
频频出现,成了高考的热点题型。以此考查沉淀溶解平衡原理,分析图像中离子浓度的关系、K 的计算等。
sp
主要的沉淀溶解平衡图像如下:
1.双曲线型
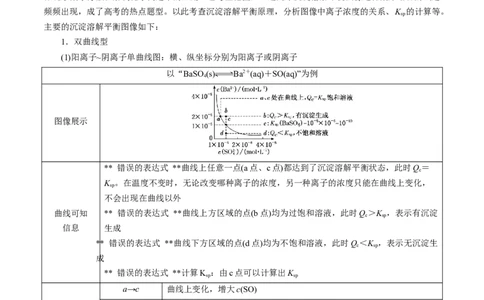
(1)阳离子~阴离子单曲线图:横、纵坐标分别为阳离子或阴离子
以“BaSO(s) Ba2+(aq)+SO(aq)”为例
4
图像展示
** 错误的表达式 **曲线上任意一点(a点、c点)都达到了沉淀溶解平衡状态,此时Q=
c
K 。在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变化,
sp
不会出现在曲线以外
曲线可知 ** 错误的表达式 **曲线上方区域的点(b点)均为过饱和溶液,此时Q>K ,表示有沉淀
c sp
信息 生成
** 错误的表达式 **曲线下方区域的点(d点)均为不饱和溶液,此时Q<K ,表示无沉淀生
c sp
成
** 错误的表达式 **计算K :由c点可以计算出K
sp sp
a→c 曲线上变化,增大c(SO)
b→c 加入1×10-5 mol·L-1 Na SO 溶液(加水不可以)
2 4
点的变化
d→c 加入BaCl 固体(忽略溶液的体积变化)
2
c→a 曲线上变化,增大c(Ba2+)
溶液蒸发时,离子浓度的变化 原溶液不饱和时,离子浓度都增大;原溶液饱和时,离子浓度都不变
溶度积常数只是温度的函数,与溶液中溶质的离子浓度无关,在同一曲线上的点,溶度积常数相同
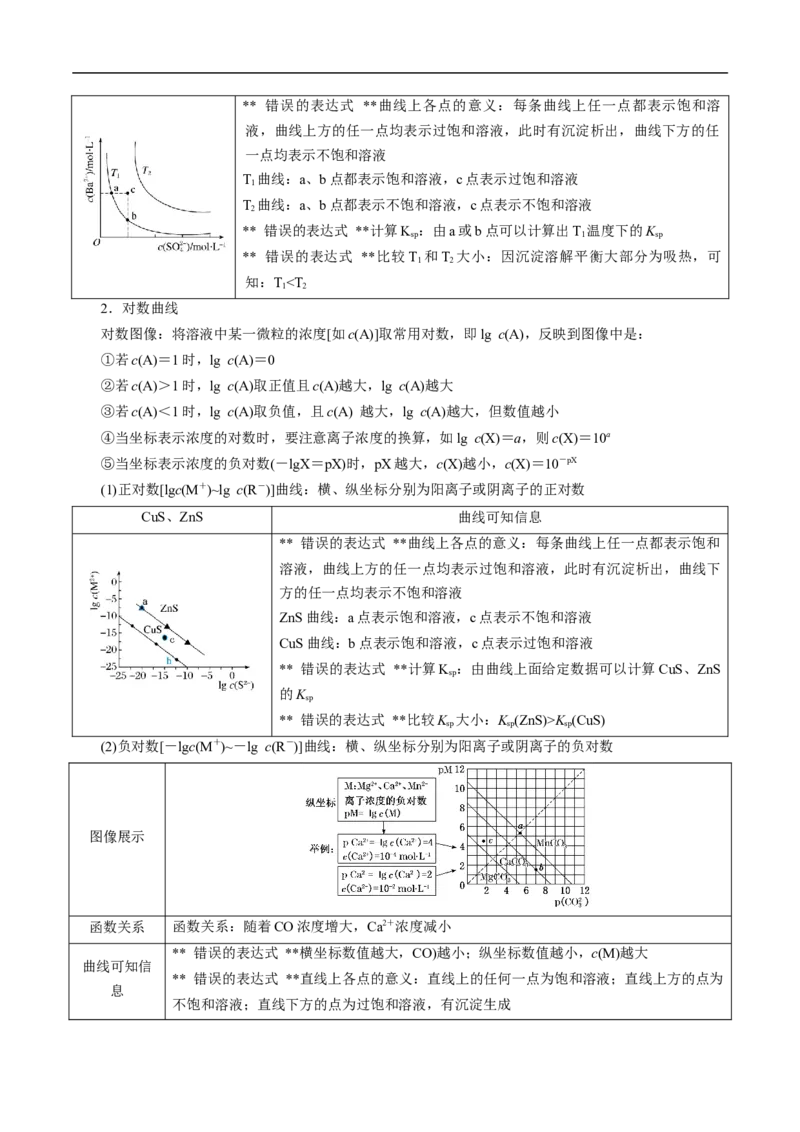
(2)阴阳离子浓度~温度双曲线图:横、纵坐标分别为阳离子或阴离子,两条曲线为不同温度
BaSO 曲线可知信息
4** 错误的表达式 **曲线上各点的意义:每条曲线上任一点都表示饱和溶
液,曲线上方的任一点均表示过饱和溶液,此时有沉淀析出,曲线下方的任
一点均表示不饱和溶液
T 曲线:a、b点都表示饱和溶液,c点表示过饱和溶液
1
T 曲线:a、b点都表示不饱和溶液,c点表示不饱和溶液
2
** 错误的表达式 **计算K :由a或b点可以计算出T 温度下的K
sp 1 sp
** 错误的表达式 **比较T 和T 大小:因沉淀溶解平衡大部分为吸热,可
1 2
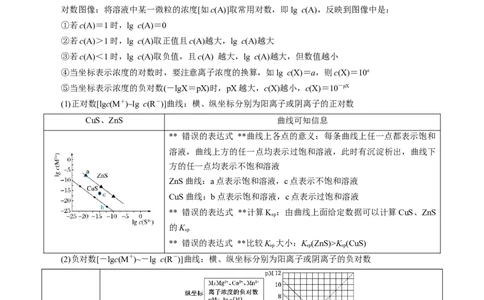
知:TK (CuS)
sp sp sp
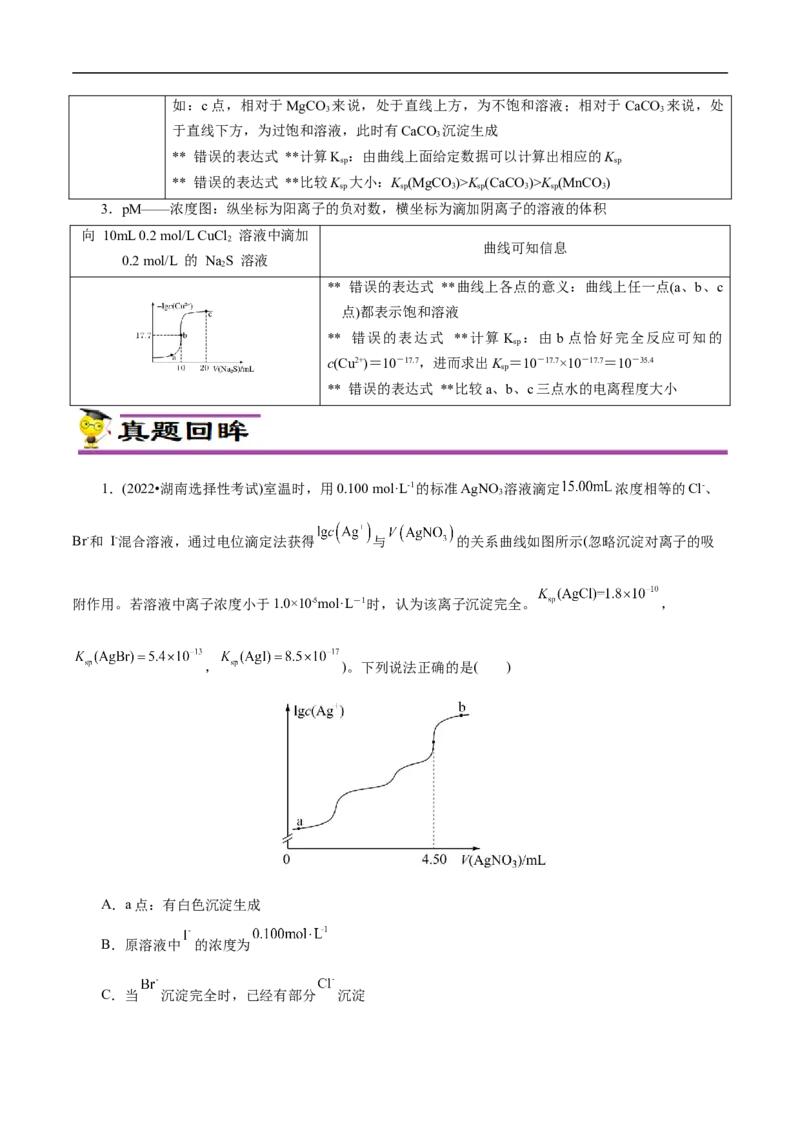
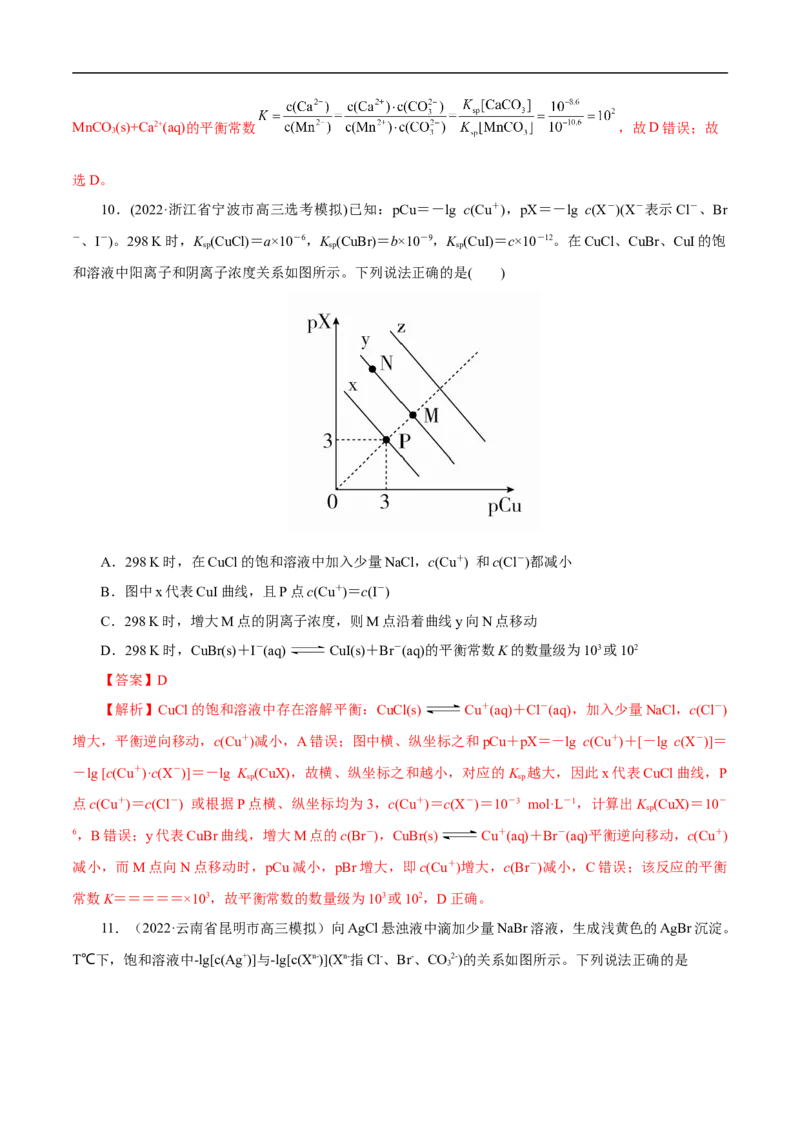
(2)负对数[-lgc(M+)~-lg c(R-)]曲线:横、纵坐标分别为阳离子或阴离子的负对数
图像展示
函数关系 函数关系:随着CO浓度增大,Ca2+浓度减小
** 错误的表达式 **横坐标数值越大,CO)越小;纵坐标数值越小,c(M)越大
曲线可知信
** 错误的表达式 **直线上各点的意义:直线上的任何一点为饱和溶液;直线上方的点为
息
不饱和溶液;直线下方的点为过饱和溶液,有沉淀生成如:c点,相对于MgCO 来说,处于直线上方,为不饱和溶液;相对于CaCO 来说,处
3 3
于直线下方,为过饱和溶液,此时有CaCO 沉淀生成
3
** 错误的表达式 **计算K :由曲线上面给定数据可以计算出相应的K
sp sp
** 错误的表达式 **比较K 大小:K (MgCO )>K (CaCO )>K (MnCO )
sp sp 3 sp 3 sp 3
3.pM——浓度图:纵坐标为阳离子的负对数,横坐标为滴加阴离子的溶液的体积
向 10mL 0.2 mol/L CuCl 溶液中滴加
2
曲线可知信息
0.2 mol/L 的 NaS 溶液
2
** 错误的表达式 **曲线上各点的意义:曲线上任一点(a、b、c
点)都表示饱和溶液
** 错误的表达式 **计算 K :由 b 点恰好完全反应可知的
sp
c(Cu2+)=10-17.7,进而求出K =10-17.7×10-17.7=10-35.4
sp
** 错误的表达式 **比较a、b、c三点水的电离程度大小
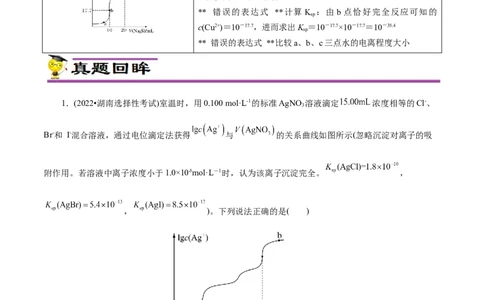
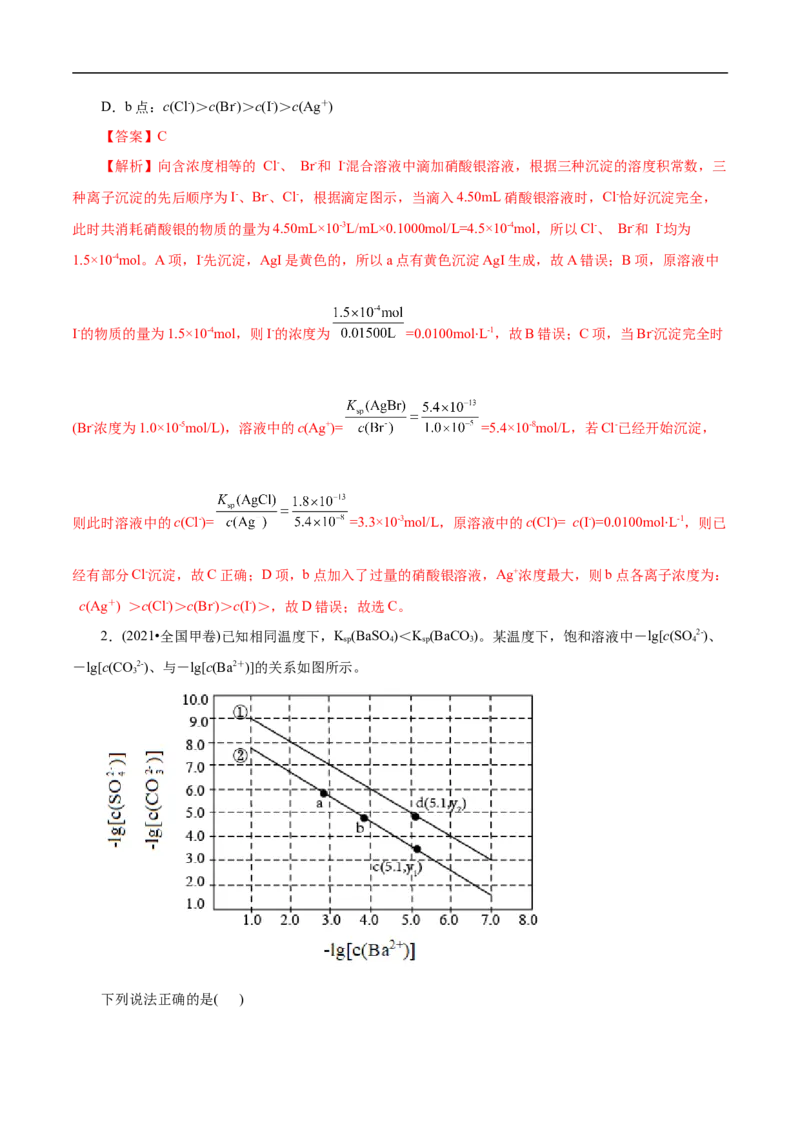
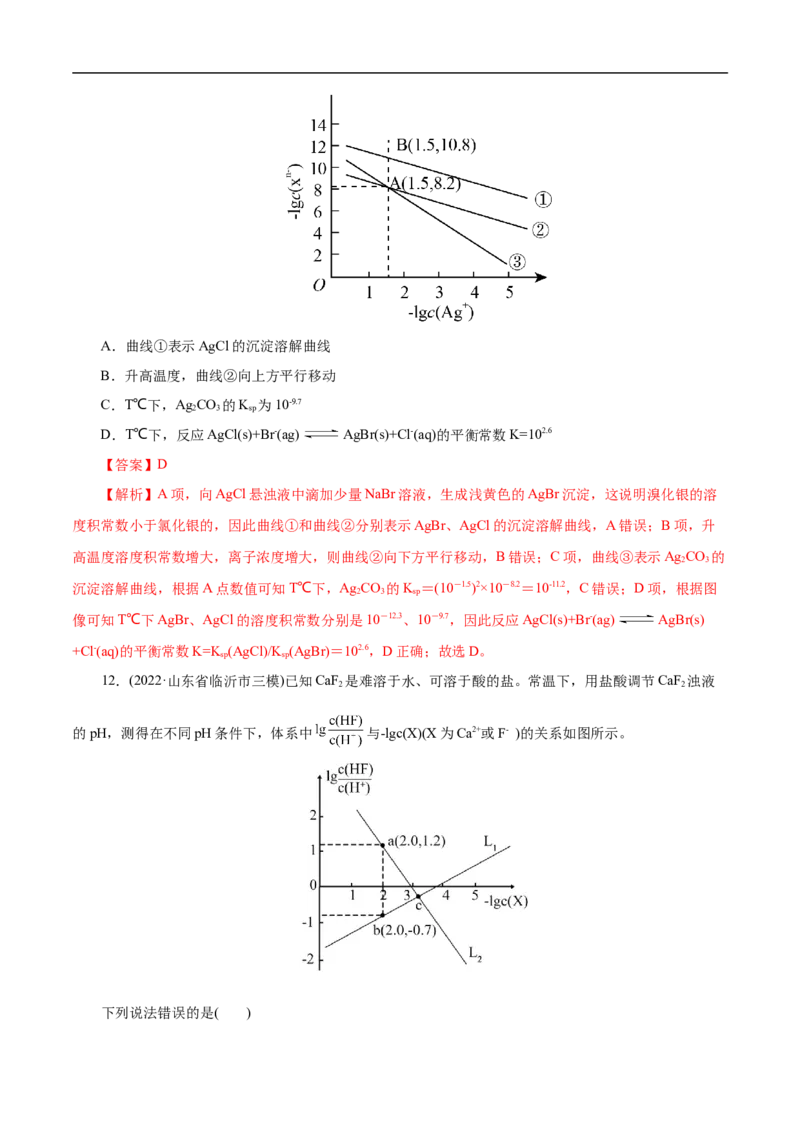
1.(2022•湖南选择性考试)室温时,用0.100 mol·L-1的标准AgNO 溶液滴定 浓度相等的Cl-、
3
Br-和 I-混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸
附作用。若溶液中离子浓度小于1.0×10-5mol·L-1时,认为该离子沉淀完全。 ,
, )。下列说法正确的是( )
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀D.b点:c(Cl-)>c(Br-)>c(I-)>c(Ag+)
【答案】C
【解析】向含浓度相等的 Cl-、 Br-和 I-混合溶液中滴加硝酸银溶液,根据三种沉淀的溶度积常数,三
种离子沉淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50mL硝酸银溶液时,Cl-恰好沉淀完全,
此时共消耗硝酸银的物质的量为4.50mL×10-3L/mL×0.1000mol/L=4.5×10-4mol,所以Cl-、 Br-和 I-均为
1.5×10-4mol。A项,I-先沉淀,AgI是黄色的,所以a点有黄色沉淀AgI生成,故A错误;B项,原溶液中
I-的物质的量为1.5×10-4mol,则I-的浓度为 =0.0100molL-1,故B错误;C项,当Br-沉淀完全时
⋅
(Br-浓度为1.0×10-5mol/L),溶液中的c(Ag+)= =5.4×10-8mol/L,若Cl-已经开始沉淀,
则此时溶液中的c(Cl-)= =3.3×10-3mol/L,原溶液中的c(Cl-)= c(I-)=0.0100molL-1,则已
⋅
经有部分Cl-沉淀,故C正确;D项,b点加入了过量的硝酸银溶液,Ag+浓度最大,则b点各离子浓度为:
c(Ag+) >c(Cl-)>c(Br-)>c(I-)>,故D错误;故选C。
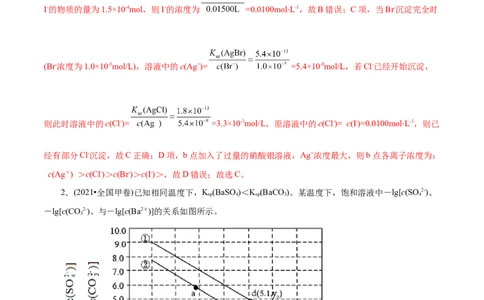
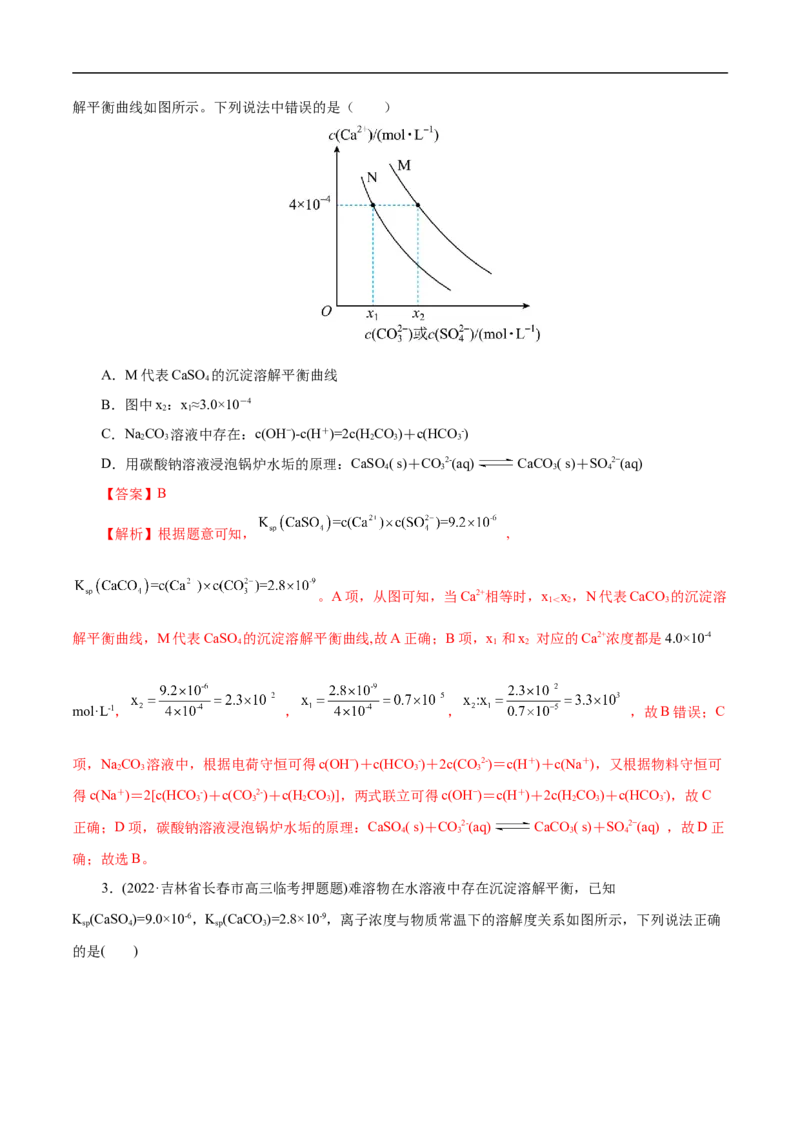
2.(2021•全国甲卷)已知相同温度下,K (BaSO)<K (BaCO)。某温度下,饱和溶液中-lg[c(SO 2-)、
sp 4 sp 3 4
-lg[c(CO2-)、与-lg[c(Ba2+)]的关系如图所示。
3
下列说法正确的是( )A.曲线①代表BaCO 的沉淀溶解曲线
3
B.该温度下BaSO 的K (BaSO)值为1.0×10-10
4 sp 4
C.加适量BaCl 固体可使溶液由a点变到b点
2
D.c(Ba2+)=10-5.1时两溶液中
【答案】B
【解析】因BaCO 、BaSO 均为难溶物,饱和溶液中-lg[c(Ba2+)]+{-lg[c(SO 2-)]}=-lg[c(Ba2
3 4 4
+)×c(SO 2-)]=-lg[K (BaSO)],同理可知溶液中-lg[c(Ba2+)]+{-lg[c(CO2-)]}=-lg[K (BaCO)],因
4 sp 4 3 sp 3
K (BaSO)< K (BaCO),则-lg[K (BaCO)]<-lg[K (BaSO)],由此可知曲线①为-lg[c(Ba2+)]与-
sp 4 sp 3 sp 3 sp 4
lg[c(SO 2-)]的关系,曲线②为-lg[c(Ba2+)]与-lg[c(CO2-)]的关系。A项,由题可知,曲线上的点均为饱和
4 3
溶液中微粒浓度关系,由上述分析可知,曲线①为BaSO 的沉淀溶解曲线,故A错误;B项,曲线①为
4
BaSO 溶液中-lg[c(Ba2+)]与-lg[c(SO 2-)]的关系,由图可知,当溶液中-lg[c(Ba2+)]=3时,-lg[c(SO 2-)=
4 4 4
7,则-lg[K (BaSO)]=7+3=10,因此K (BaSO)=1.0×10-10,故B正确;C项,向饱和BaSO 溶液中加
sp 4 sp 4 4
入适量BaCl 固体后,溶液中c(Ba2+)增大,根据温度不变则K (BaSO)不变可知,溶液中c(SO 2-)将减小,
2 sp 4 4
因此a点将沿曲线①向左上方移动,故C错误;D项,由图可知,当溶液中c(Ba2+)=10-5.1时,两溶液中
= = ,故D错误;故选B。
3.(2021•全国乙卷)HA是一元弱酸,难溶盐MA的饱和溶液中c(M+)随c(H+)而变化,M+不发生水解。
实验发现, 时c2(M+)-c(H+)为线性关系,如下图中实线所示。下列叙述错误的是( )
A.溶液pH=4时,c(M+)<3.0×10-4mol·L-1
B.MA的溶度积度积K (MA)=5.0×10-8
sp
C.溶液pH=7时,c(M+)+c(H+) =c(A-)+c(OH―)
D.HA的电离常数K (HA)≈2.0×10-4
a1
【答案】C
【解析】A项,由图可知pH=4,即c(H+)=10×10-5mol/L时,c2(M+)=7.5×10-8mol2/L2,c(M+)=
mol/L<3.0×10-4mol/L,A正确;B项,由图可知,c(H+)=0时,可看作溶液中
有较大浓度的OH-,此时A-的水解极大地被抑制,溶液中c(M+)=c(A-),则K (MA)= c(M+)×c(A-)= c2(M
sp
+)=5.0×10-8,B正确;C.设调pH所用的酸为HX,则结合电荷守恒可知c(M+)+c(H+) =c(A-)+c(OH―)+
n
nc(Xn-),题给等式右边缺阴离子部分nc(Xn-),C错误;D项, 当c(HA)= c(A-)时,
由物料守恒知c(A-)+ c(HA)=c(M+),则 , ,
则c2(M+)=5.0×10-8,对应图得此时溶液中c(H+) =2.0×10-4mol/L,
,D正确;故选C。1.沉淀溶解平衡图像题解题策略
(1)沉淀溶解平衡曲线类似于溶解度曲线,曲线上任意一点都表示饱和溶液,曲线上方的任意一点均表
示过饱和溶液,此时有沉淀析出,曲线下方的任意一点均表示不饱和溶液。
(2)从图像中找到数据,根据K 公式计算得出K 的值。
sp sp
(3)比较溶液的Q与K 的大小,判断溶液中有无沉淀析出。
sp
(4)涉及Q的计算时,所代入的离子浓度一定是混合溶液中的离子浓度,因此计算离子浓度时,所代入
的溶液体积也必须是混合溶液的体积。
2.分析沉淀溶解平衡图像的三步骤
3.沉淀溶解平衡图像题解题模板
第一步:明确图像中横、纵坐标的含义
横、纵坐标通常是难溶物溶解后电离出的离子浓度或其对数或其负对数。
第二步:理解图像中线上点、线外点的含义
曲线上任意一点都达到了沉淀溶解平衡状态,此时Q=K 。在温度不变时,无论改变哪种离子的浓度,
c sp
另一种离子的浓度只能在曲线上变化,不会出现在曲线外。
当横、纵坐标为离子浓度或其对数时,则:
曲线上方区域的点均为过饱和溶液,此时Q>K 。
c sp
曲线下方区域的点均为不饱和溶液,此时Qd,a>e
1
D.降低温度a点可移动至c点
【答案】C
【解析】K (CaSO)=9.0×10-6则饱和CaSO 溶液中 。
sp 4 4
K (CaCO)=2.8×10-9,则 。计算得知c(SO 2-)>c(CO2-),则
sp 3 4 3
L2为CaSO,L1为CaCO 。A项,L 为CaSO,L 为CaCO ,A项错误;B项,c、c 分别为饱和溶液中
4 3 2 4 1 3 1 2
的离子浓度,则c 的数量级为10-5而c=3×10-3,B项错误;C项,a→d点溶液中Ca2+增加而CO2-减少,说
1 2 3
明向该溶液中加入了Ca2+溶解平衡CaCO (s) Ca2+(sq)+ CO 2-(aq)逆向,所有CaCO 溶解度降低。所有
3 3 3
溶解度a>d。a→e点溶液中CO2-增加而Ca2+减少,说明向该溶液中加入了CO2-溶解平衡CaCO (s)
3 3 3
Ca2+(sq)+ CO 2-(aq)逆向,所有CaCO 溶解度降低。所有溶解度a>e。C项正确;D项,降低温度,CaCO 溶
3 3 3
解平衡逆向,饱和溶液中离子浓度降低,a不会移向c点,D项错误;故选C。
4.(2022·福建省福州第一中学模拟预测)天然溶洞的形成与水体中含碳物种的浓度有密切关系。已知
K (CaCO)=10-8.7,某溶洞水体中lgc(X)(X为HCO -、CO2-或Ca2+)与pH变化的关系如下图所示。下列说法
sp 3 3 3
错误的是( )A.曲线②代表CO2- B.K (H CO)的数量级为10-11
3 a2 2 3
C.a=-4.35,b=-2.75 D.pH=10.3时,c(Ca2+)=10-7.6 mol·L-1
【答案】C
【解析】根据图象可知:横坐标代表pH,随着pH增大,溶液碱性增强,c(HCO -)、c(CO2-)增大,先
3 3
生成HCO -,再生成CO2-,所以曲线①代表HCO -,曲线②代表CO2-,因为碳酸钙是难溶物,因此随着
3 3 3 3
c(CO2-)增大,溶液中c(Ca2+ )减小,推出曲线③代表Ca2+。A项,曲线②代表CO2-,A正确;B项,电离
3 3
平衡常数只受温度的影响,曲线①和②的交点代表c(HCO -)=c(CO2-),即K =
3 3 a2
,故K (H CO)的数量级为10-11,B正确;C项,曲线②和③的交点,代表
a2 2 3
c(CO2-)=c(Ca2+),根据K (CaCO)=c(CO2-)·c(Ca2+)=10-8.7,则c(CO2-)=
3 sp 3 3 3
,即a=-4.35;根据电离平衡常数K = ,c(
a2
)= ,即b=-2.65,C错误;D项,当pH=10.3时,c(CO2-)=10-
3
1.1 mol/L,根据K (CaCO)= c(CO2-)·c(Ca2+),c(Ca2+)= ,D正确;故选C。
sp 3 3
5.(2022·安徽省名校高三毕业班考前定位测试)已知相同温度下,K [ Cu(OH) ]