文档内容
专题 02 化学计量与化学计算
2020年高考真题
1.【2020新课标Ⅲ】N 是阿伏加德罗常数的值。下列说法正确的是
A
A.22.4 L(标准状况)氮气中含有7N 个中子
A
B.1 mol重水比1 mol水多N 个质子
A
C.12 g石墨烯和12 g金刚石均含有N 个碳原子
A
D.1 L 1 mol·L−1 NaCl溶液含有28N 个电子
A
2.【2020年7月浙江选考】N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.
4MnO−+5HCHO+12H+=4Mn2++5CO ↑+11H O
,
1mol[4MnO−+5HCHO]
完全反应转移的电子数为
4 2 2 4
20N
A
B.用电解粗铜的方法精炼铜,当电路中通过的电子数为N 时,阳极应有32gCu转化为Cu2+
A
C.常温下, 的 溶液中,水电离出的 数为
pH=9 CH COONa H+ 10−5N
3 A
D.1L浓度为0.100mol⋅L−1的Na CO 溶液中,阴离子数为0.100N
2 3 A
2020届高考模拟试题
3.(2020届安徽省江淮十校联考)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.52g苯乙烯含碳碳双键数目为2N
A
B.1L0.5mol·L-1醋酸钠溶液中阴阳离子总数目小于N
A
C.标准状况下,22.4L一氯甲烷含共用电子对数为4N
A
D.有铁粉参加的反应若生成3molFe2+,则转移电子数一定为6N
A
4.(2020届东北三省四市联合模拟)已知N 为阿伏加德罗常数的值。下列说法正确的是
A
A.1L0.1mol/L的NaCO 溶液中含阴离子总数为0.1N
2 3 A
B.7.8gNa O 与过量CO 反应时,转移的电子数为0.2N
2 2 2 A
C.2gH18O与D16O的混合物中所含的中子数和电子数均为N
2 2 A
D.足量乙烷与22.4L(标准状况)Cl 发生取代反应,形成C-Cl键的数目为2N
2 A
5.(2020届湖北省七市州教科研协作5月高三联合)N 是阿伏加德罗常数的值,下列说法正确的是
A
A.若1molFeCl 跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为N
3 A
B.将一定量的Cl 通入FeBr 溶液中,当有1molBr-转化为Br 时,转移的电子数为N
2 2 2 AC.44.0g环氧乙烷中含有6.0N 个极性键
A
D.1molCaO 晶体中含离子总数为3N
2 A
6.(2020届河北唐山市高三第一次模拟)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.将4.6g 钠用铝箔包裹并刺小孔,与足量水充分反应生成H 分子数为0.1 N
2 A
B.标准状况下,22.4L 已烷中含有的共价键的数目为19N
A
C.标准状况下,11.2L 12C18O中含有的中子数为8N
A
D.标准状况下,7.1 gCl 通入足量石灰水中反应转移的电子数为0.2N
2 A
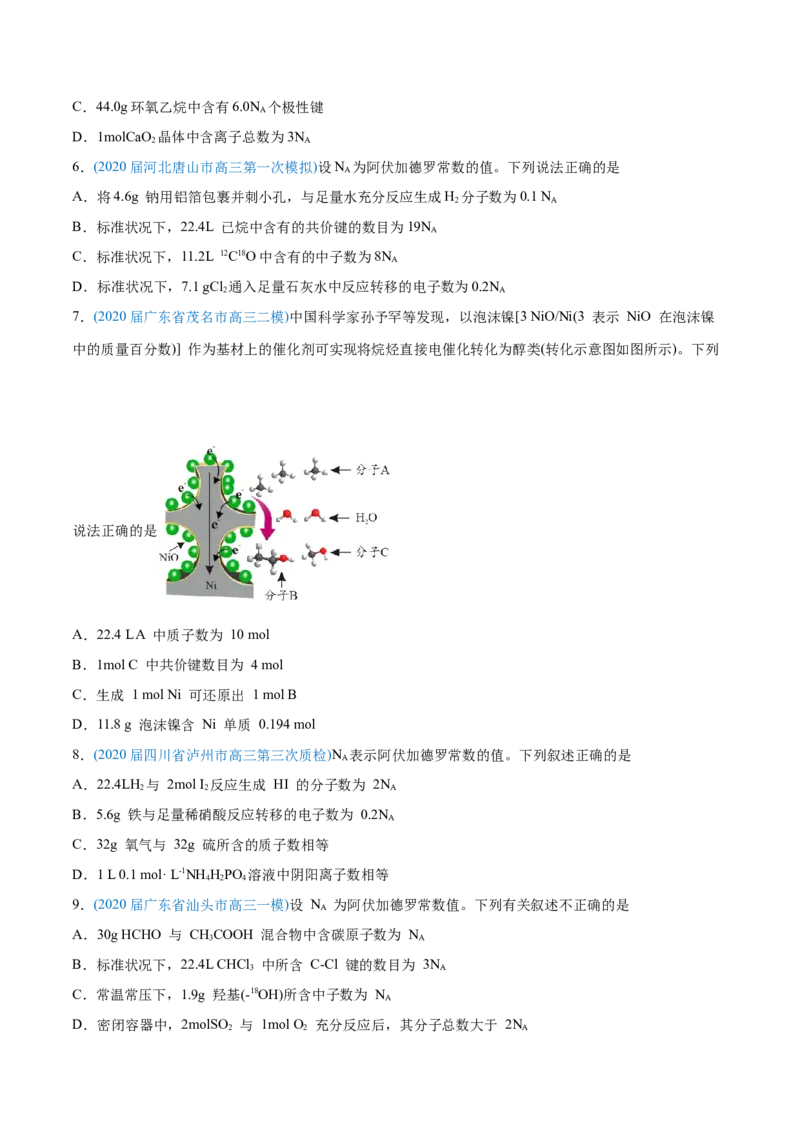
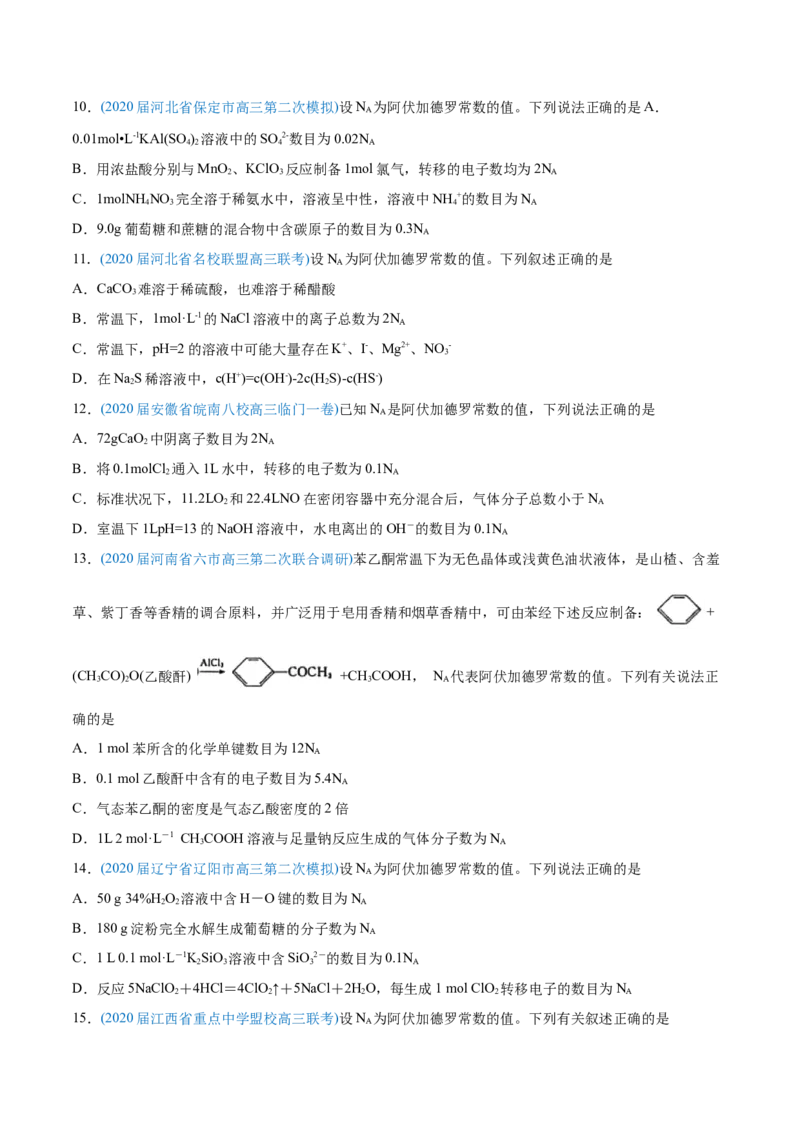
7.(2020届广东省茂名市高三二模)中国科学家孙予罕等发现,以泡沫镍[3 NiO/Ni(3 表示 NiO 在泡沫镍
中的质量百分数)] 作为基材上的催化剂可实现将烷烃直接电催化转化为醇类(转化示意图如图所示)。下列
说法正确的是
A.22.4 L A 中质子数为 10 mol
B.1mol C 中共价键数目为 4 mol
C.生成 1 mol Ni 可还原出 1 mol B
D.11.8 g 泡沫镍含 Ni 单质 0.194 mol
8.(2020届四川省泸州市高三第三次质检)N 表示阿伏加德罗常数的值。下列叙述正确的是
A
A.22.4LH 与 2mol I 反应生成 HI 的分子数为 2N
2 2 A
B.5.6g 铁与足量稀硝酸反应转移的电子数为 0.2N
A
C.32g 氧气与 32g 硫所含的质子数相等
D.1 L 0.1 mol· L-1NH HPO 溶液中阴阳离子数相等
4 2 4
9.(2020届广东省汕头市高三一模)设 N 为阿伏加德罗常数值。下列有关叙述不正确的是
A
A.30g HCHO 与 CHCOOH 混合物中含碳原子数为 N
3 A
B.标准状况下,22.4L CHCl 中所含 C-Cl 键的数目为 3N
3 A
C.常温常压下,1.9g 羟基(-18OH)所含中子数为 N
A
D.密闭容器中,2molSO 与 1mol O 充分反应后,其分子总数大于 2N
2 2 A10.(2020届河北省保定市高三第二次模拟)设N 为阿伏加德罗常数的值。下列说法正确的是A.
A
0.01mol•L-1KAl(SO ) 溶液中的SO 2-数目为0.02N
4 2 4 A
B.用浓盐酸分别与MnO 、KClO 反应制备1mol氯气,转移的电子数均为2N
2 3 A
C.1molNH NO 完全溶于稀氨水中,溶液呈中性,溶液中NH +的数目为N
4 3 4 A
D.9.0g葡萄糖和蔗糖的混合物中含碳原子的数目为0.3N
A
11.(2020届河北省名校联盟高三联考)设N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.CaCO 难溶于稀硫酸,也难溶于稀醋酸
3
B.常温下,1mol·L-1的NaCl溶液中的离子总数为2N
A
C.常温下,pH=2的溶液中可能大量存在K+、I-、Mg2+、NO -
3
D.在NaS稀溶液中,c(H+)=c(OH-)-2c(HS)-c(HS-)
2 2
12.(2020届安徽省皖南八校高三临门一卷)已知N 是阿伏加德罗常数的值,下列说法正确的是
A
A.72gCaO 中阴离子数目为2N
2 A
B.将0.1molCl 通入1L水中,转移的电子数为0.1N
2 A
C.标准状况下,11.2LO 和22.4LNO在密闭容器中充分混合后,气体分子总数小于N
2 A
D.室温下1LpH=13的NaOH溶液中,水电离出的OH-的数目为0.1N
A
13.(2020届河南省六市高三第二次联合调研)苯乙酮常温下为无色晶体或浅黄色油状液体,是山楂、含羞
草、紫丁香等香精的调合原料,并广泛用于皂用香精和烟草香精中,可由苯经下述反应制备: +
(CHCO) O(乙酸酐) +CH COOH, N 代表阿伏加德罗常数的值。下列有关说法正
3 2 3 A
确的是
A.1 mol苯所含的化学单键数目为12N
A
B.0.1 mol乙酸酐中含有的电子数目为5.4N
A
C.气态苯乙酮的密度是气态乙酸密度的2倍
D.1L 2 mol·L-1 CHCOOH溶液与足量钠反应生成的气体分子数为N
3 A
14.(2020届辽宁省辽阳市高三第二次模拟)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.50 g 34%H O 溶液中含H-O键的数目为N
2 2 A
B.180 g淀粉完全水解生成葡萄糖的分子数为N
A
C.1 L 0.1 mol·L-1KSiO 溶液中含SiO2-的数目为0.1N
2 3 3 A
D.反应5NaClO+4HCl=4ClO ↑+5NaCl+2HO,每生成1 mol ClO 转移电子的数目为N
2 2 2 2 A
15.(2020届江西省重点中学盟校高三联考)设N 为阿伏加德罗常数的值。下列有关叙述正确的是
AA.用浓盐酸分别和MnO 、KClO 反应制备1 mol氯气,转移的电子数均为2N
2 3 A
B.0.1 mol·L-1 NaF溶液中所含F-的数目小于0.1N
A
C.用1 L 1 mol·L-1 FeCl 溶液充分反应制备氢氧化铁胶体,该体系中含氢氧化铁胶体粒子数目为1N
3 A
D.标准状况下,4.48 L CO 和NO的混合气体中含有的电子数为4.4N
2 2 A
16.(2020届宁夏三校高三联考)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.20gH18O和DO的混合物中含有中子10N
2 2 A
B.密闭容器中2molNO与1molO 充分反应,产物的分子数为2N
2 A
C.1L0.1mol·L-1的NaCO 溶液中HCO -和CO2-离子数之和为0.1N
2 3 3 3 A
D.pH=1的硫酸溶液,含有氢离子数目为2N
A
17.(2020届陕西省咸阳市高三模拟)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.1.8 g NH+含有的电子数为N
4 A
B.1 L 1 mol·L-1的NaAlO 水溶液中含有的氧原子数为2N
2 A
C.标况下,22.4 L NO与11.2 L O 充分反应后,生成物的分子总数为N
2 A
D.50 mL 18 mol·L-1的浓硫酸与足量的铜片共热,生成SO 的分子数为0.45N
2 A
18.(2020届福建省厦门市高三质检)N 表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用千冶
A
金染料、皮革等工业。硫化钠的一种制备方法是NaSO +2C NaS+2CO↑。下列有关说法正确的是
2 4 2 2
A.12g石墨晶体中含有碳碳键的数目为3N
A
B.1L0.1mol•L-1NaS溶液中含阴离子的数目小于0.lN
2 A
C.生成1mol氧化产物时转移电子数为4N
A
D.常温常压下,11.2LCO 中含质子的数目为11N
2 A