文档内容
专题 03 铁 金属材料
1.下列化合物中,通常用来做红色颜料、俗称“铁红”的是( )
A.FeO B.Fe O C.Fe O D.Fe O
2 3 3 4 5 7
2.下列物质不属于合金的是( )
A.青铜器 B.不锈钢 C.合金钢 D.金刚石
3.在生活、生产中,目前用量最大,用途最广的合金是( )
A.钛合金 B.铜 C.钢 D.硬铝
4.下列铝合金的性质与其用于国产C919飞机外壳无关的是( )
A.导电性 B.密度小 C.抗腐蚀性强 D.硬度大
5.不锈钢由于其抗腐蚀性好,在生产和生活中有许多用途,不锈钢属于( )
A.单质 B.化合物 C.混合物 D.氧化物
6.将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是( )
A.硫酸 B.氯水 C.硫酸锌 D.氯化铜
7.在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸
引,则反应后溶液中存在较多的阳离子是( )
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
8.某物质溶于盐酸,滴加KSCN溶液后颜色没有变化,再加入氯水后溶液呈血红色,这种物质是(
)
A.FeCl B.FeCl C.Fe O D.Fe(OH)
3 2 2 3 3
9.要证明某溶液中不含Fe3+而可能含有Fe2+进行如下实验操作时,最佳顺序为( )
①加入足量氯水 ②加入足量酸性KMnO 溶液 ③加入少量NH SCN溶液
4 4
A.①③ B.③② C.③① D.①②③
10.下列各组物质相互反应后,再向得到的溶液中滴入KSCN溶液,溶液变成红色的是 ( )
A.新制氯水和FeCl 溶液 B.铁屑和CuCl 溶液
2 2
C.铁屑和过量稀硫酸 D.过量铁屑和FeCl 溶液
3
11.下列实验只能制备氢氧化铁沉淀的是( )
A.将氧化铁和水直接加热 B.将水蒸气通过炽热铁粉
C.氧化铁先用盐酸溶解再加烧碱溶液 D.饱和氯化铁溶液逐滴滴入沸水中
12.证明某溶液中只含有Fe2+而不含有Fe3+的实验方法是( )
A.先滴加氯水,再滴加KSCN溶液后显红色
B.先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C.先滴加KSCN溶液,不显红色,再滴加KMnO 溶液后显红色
4
D.只需滴加KSCN溶液13.在氯化铁、氯化铜和盐酸混合溶液中加人铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸引,
则反应后溶液中存在较多的阳离子是( )
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
14.向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴加几滴新制氯水后,混合液变成血红色,
则下列结论错误的是( )
A.该晶体中一定含有SCN- B.氧化性:Fe3+>Cl
2
C.Fe2+与SCN-不能形成红色物质 D.Fe2+被氯水氧化为Fe3+
15.铁及其化合物是中学化学中的一类重要物质,下列关于铁元素的叙述中正确的是 ( )
A.2Fe3++Fe==3Fe2+,说明氧化性:Fe3+>Fe2+
B.25 ℃,pH=0的溶液中,Al3+、NH +、NO -、Fe2+可以大量共存
4 3
C.5.6 g铁与足量的氯气反应失去电子为0.2 mol
D.硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H O+4H+==Fe3++4H O
2 2 2
16.下列关于元素及其化合物的说法不正确的是( )
A.Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应
B.Al、Cl 均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同
2
C.在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO 固体,铜粉会溶解
3
D.金属单质Na、Mg、Fe在一定条件下与水反应都生成H 和相应的碱
2
17.某学生设计了如图的方法对X盐进行鉴定:
由此分析,下列结论中正确的是( )
A.X中一定有Fe3+ B.Z中一定有Fe3+
C.Y为AgI沉淀 D.X一定为FeBr 溶液
2
18.易拉罐的主要成分为铝合金,其中以铝铁合金和铝镁合金最为常见。现取几小块易拉罐碎片进行
下列实验,其中实验方案与现象、结论正确的是( )
序号 实验方案 现象、结论
A 加入盐酸 产生无色气体,含铝、铁、镁三种元素
B 加入NaOH溶液 有无色气体产生,含有镁、铝两种元素
加入盐酸后,所得溶液中再加入少
C 产生白色沉淀,含有镁元素
量NaOH溶液
用盐酸溶解并放置一会后,加入
D 溶液呈血红色,含有铁元素
KSCN溶液
19.下列有关物质性质与用途具有对应关系的是( )
A.NaHCO 受热易分解,可用于制胃酸中和剂
3B.铁比铜金属性强,FeCl 腐蚀Cu刻制印刷电路板
3
C.SiO 熔点高硬度大,可用于制光导纤维
2
D.铝热反应能放出大量的热,常用作焊接钢轨
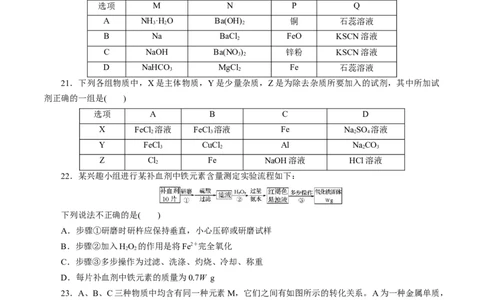
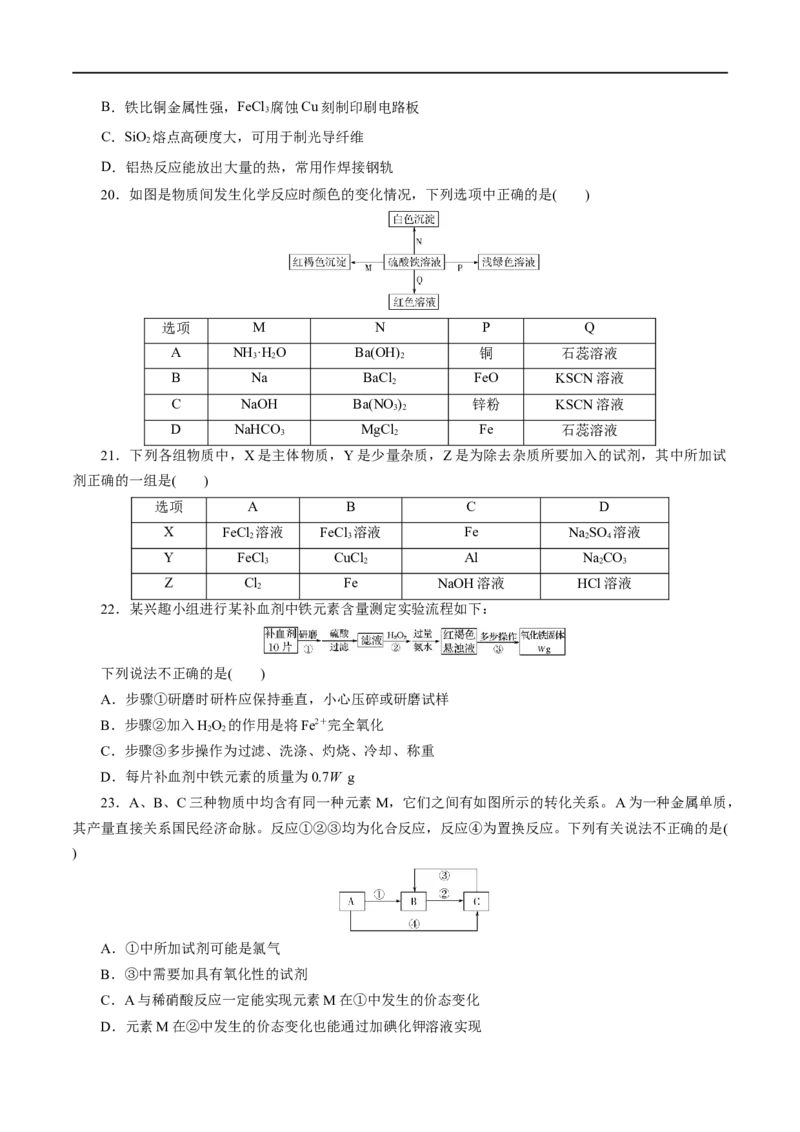
20.如图是物质间发生化学反应时颜色的变化情况,下列选项中正确的是( )
选项 M N P Q
A NH ·H O Ba(OH) 铜 石蕊溶液
3 2 2
B Na BaCl FeO KSCN溶液
2
C NaOH Ba(NO ) 锌粉 KSCN溶液
3 2
D NaHCO MgCl Fe 石蕊溶液
3 2
21.下列各组物质中,X是主体物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试
剂正确的一组是( )
选项 A B C D
X FeCl 溶液 FeCl 溶液 Fe NaSO 溶液
2 3 2 4
Y FeCl CuCl Al NaCO
3 2 2 3
Z Cl Fe NaOH溶液 HCl溶液
2
22.某兴趣小组进行某补血剂中铁元素含量测定实验流程如下:
下列说法不正确的是( )
A.步骤①研磨时研杵应保持垂直,小心压碎或研磨试样
B.步骤②加入HO 的作用是将Fe2+完全氧化
2 2
C.步骤③多步操作为过滤、洗涤、灼烧、冷却、称重
D.每片补血剂中铁元素的质量为0.7W g
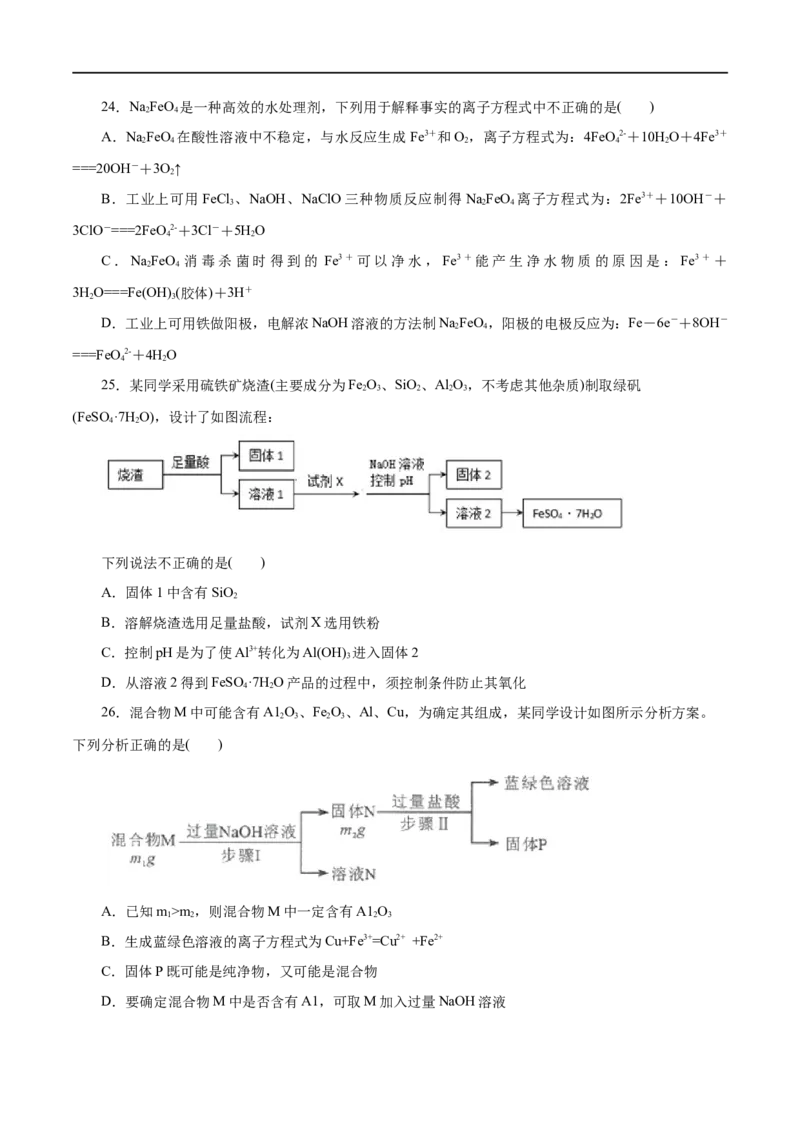
23.A、B、C三种物质中均含有同一种元素M,它们之间有如图所示的转化关系。A为一种金属单质,
其产量直接关系国民经济命脉。反应①②③均为化合反应,反应④为置换反应。下列有关说法不正确的是(
)
A.①中所加试剂可能是氯气
B.③中需要加具有氧化性的试剂
C.A与稀硝酸反应一定能实现元素M在①中发生的价态变化
D.元素M在②中发生的价态变化也能通过加碘化钾溶液实现24.NaFeO 是一种高效的水处理剂,下列用于解释事实的离子方程式中不正确的是( )
2 4
A.NaFeO 在酸性溶液中不稳定,与水反应生成Fe3+和O ,离子方程式为:4FeO2-+10HO+4Fe3+
2 4 2 4 2
===20OH-+3O↑
2
B.工业上可用FeCl 、NaOH、NaClO三种物质反应制得NaFeO 离子方程式为:2Fe3++10OH-+
3 2 4
3ClO-===2FeO2-+3Cl-+5HO
4 2
C.NaFeO 消毒杀菌时得到的 Fe3+可以净水,Fe3+能产生净水物质的原因是:Fe3++
2 4
3HO===Fe(OH) (胶体)+3H+
2 3
D.工业上可用铁做阳极,电解浓NaOH溶液的方法制NaFeO,阳极的电极反应为:Fe-6e-+8OH-
2 4
===FeO2-+4HO
4 2
25.某同学采用硫铁矿烧渣(主要成分为Fe O、SiO、Al O,不考虑其他杂质)制取绿矾
2 3 2 2 3
(FeSO ·7H O),设计了如图流程:
4 2
下列说法不正确的是( )
A.固体1中含有SiO
2
B.溶解烧渣选用足量盐酸,试剂X选用铁粉
C.控制pH是为了使Al3+转化为Al(OH) 进入固体2
3
D.从溶液2得到FeSO ·7H O产品的过程中,须控制条件防止其氧化
4 2
26.混合物M中可能含有A1 O、Fe O、Al、Cu,为确定其组成,某同学设计如图所示分析方案。
2 3 2 3
下列分析正确的是( )
A.已知m>m,则混合物M中一定含有A1 O
1 2 2 3
B.生成蓝绿色溶液的离子方程式为Cu+Fe3+=Cu2+ +Fe2+
C.固体P既可能是纯净物,又可能是混合物
D.要确定混合物M中是否含有A1,可取M加入过量NaOH溶液27.某兴趣小组将过量Cu与FeCl 溶液充分及应,静置后取上层清液于试管中,将KSCN溶液滴加到
3
清液中,观察到瞬间产生白色沉淀,局部出现红色;振荡试管,红色又迅速褪去。已知:
①CuCl +Cu=2CuCl↓(白色)——该反应速率很慢
2
②2CuCl +4KSCN=2CuSCN↓(白色)+(SCN) +4KCl——该反应速率很快
2 2
③(SCN) 是拟卤素,化学性质和氯气相似
2
下列说法正确的是( )
A.用KSCN溶液检验Fe3+时,Cu2+的存在不会对检验产生干扰
B.局部出现红色主要是因为溶液中的Fe2+被空气中的O 氧化成Fe3+,Fe3+与KSCN反应生成Fe(SCN)
2 3
C.白色沉淀是CuCl,是溶液中CuCl 与Cu反应生成的
2
D.红色迅速褪去的原因是振荡试管时Cu2+与SCN-发生反应,从而使Fe3++3SCN- Fe(SCN) 平衡逆移
3
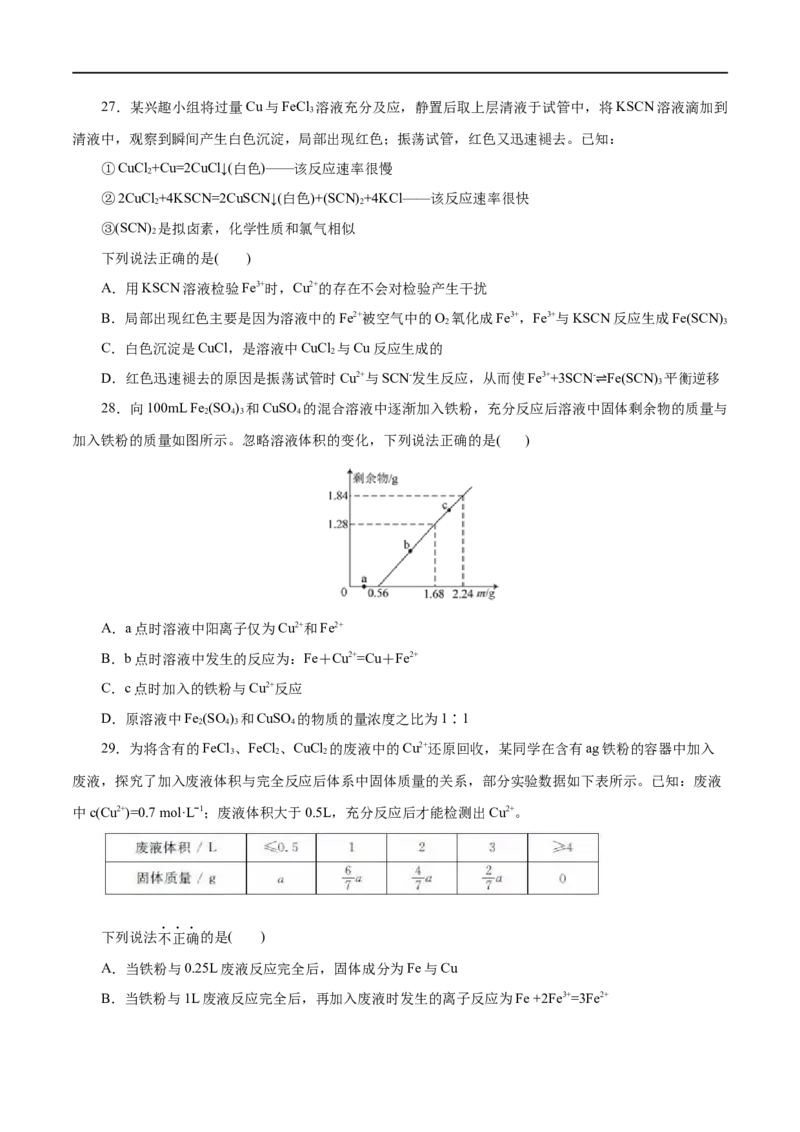
28.向100mL Fe (SO ) 和CuSO 的混合溶液中逐渐加入铁粉,充分反应后溶液中⇌固体剩余物的质量与
2 4 3 4
加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法正确的是( )
A.a点时溶液中阳离子仅为Cu2+和Fe2+
B.b点时溶液中发生的反应为:Fe+Cu2+=Cu+Fe2+
C.c点时加入的铁粉与Cu2+反应
D.原溶液中Fe (SO ) 和CuSO 的物质的量浓度之比为1∶1
2 4 3 4
29.为将含有的FeCl 、FeCl 、CuCl 的废液中的Cu2+还原回收,某同学在含有ag铁粉的容器中加入
3 2 2
废液,探究了加入废液体积与完全反应后体系中固体质量的关系,部分实验数据如下表所示。已知:废液
中c(Cu2+)=0.7 mol·Lˉ1;废液体积大于0.5L,充分反应后才能检测出Cu2+。
下列说法不正确的是( )
A.当铁粉与0.25L废液反应完全后,固体成分为Fe与Cu
B.当铁粉与1L废液反应完全后,再加入废液时发生的离子反应为Fe +2Fe3+=3Fe2+C.废液中c(Fe3+)=0.2 mol·Lˉ1
D.要将1L废液中的Cu2+全部还原,则至少需要铁粉44.8g