文档内容
专题 04 氧化还原反应及其应用
1.(2022·云南省玉溪市第一次教学质量检测模拟)2022年10月16日,国家药监局网站公布2026年起将
全面禁止生产含汞体温计。《本草纲目》记载:“水银乃至阴之毒物,因火煅丹砂而出,加以盐、(明)矾
而为轻粉,加以硫磺升而为银朱”。下列说法错误的是( )
A.短时间内吸入大量汞蒸气,会汞中毒
B.“火煅丹砂”是氧化还原反应
C.明矾的化学式是KAl(SO )·12H O,是混合物
4 2 2
D.水银温度计打碎后,洒出的汞可以用硫磺处理
2.(2022·湖北省荆州市第一次质量检查)下列颜色变化未涉及氧化还原反应的是( )
A.向 溶液中滴入 溶液,溶液由橙色变黄色
B.浓 在光照一段时间后溶液变黄色
C.向 溶液中先滴加 溶液,再滴加氯水,溶液变为红色
D.淡黄色 固体露置于空气中逐渐变为白色
3.(2022·湖南省郴州市第一次质检模拟)工业上用发烟HClO 把潮湿的CrCl 氧化为棕色的烟
4 3
[CrO (ClO )]来除去Cr(III),HClO 中部分氯元素转化为最低价态。下列说法错误的
2 4 2 4
A.HClO 属于强酸,该反应也生成了另一种强酸
4
B.CrO(ClO ) 中Cr元素显+6价
2 4 2
C.该反应每生成1 mol氧化产物,便有0.375 mol HClO 被还原.
4
D.该反应的离子方程式为19 +8Cr3+=8CrO(ClO )+3Cl-
2 4 2
4.(2022·河北省张家口市第一次质量检测)C和CuO在高温下反应生成Cu、Cu O、CO、CO。现将1 g
2 2
碳粉跟8 g CuO混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收
集残余的气体,测得溶液增加的质量为1.1 g,残余气体在标准状况下的体积为560 mL。下列说法不正确
的是
A.反应后硬质试管中碳粉有剩余
B.反应后生成Cu O为0.025 mol
2
C.该氧化还原反应共转移电子0.2 mol
D.反应后硬质试管中剩余的固体混合物的总质量为7.2 g
5.(2022·黑龙江省哈尔滨市第六中学模拟)某同学用KSCN溶液和FeCl 溶液探究Fe2+的还原性时出现异
2
常现象,实验如下:
① ② ③溶液变红,大约10秒左
右红色褪去,有气体生成
溶液变红且不褪色,有气体 溶液变红且不褪色,滴加盐
(经检验为O)。取褪色
2
生成(经检验为O),经检 酸和BaCl 溶液,无白色沉
2 2
后溶液,滴加盐酸和
验有丁达尔效应。 淀,经检验无丁达尔效应。
BaCl 溶液,产生白色沉
2
淀
下列说法错误的是( )
A.②中红色溶液中含有Fe(OH) 胶体
3
B.实验②中发生的氧化还原反应只有两种
C.对比①②③,可以判定酸性条件下HO 可以氧化SCN-
2 2
D.③中发生的氧化还原反应为:4Fe2++O +4H+=4Fe3++2H O
2 2
6.(2022·宁夏回族自治区固原市第一中学模拟)自然界中时刻存在着氮的转化。实现氮气按照一定方向
转化一直是科学领域研究的重要课题,如图为N 分子在催化剂的作用下发生的一系列转化示意图。下列叙
2
述正确的是
A.N→NH ,NH →NO均属于氮的固定
2 3 3
B.在催化剂b作用下,O 发生了氧化反应
2
C.使用催化剂a、b均可以提高单位时间内生成物的产量
D.催化剂a、b表面均发生了极性共价键的断裂
1.(2022·河北省“五个一名校联盟”第一次诊断)向重铬酸盐酸性溶液中加入乙醚和HO,水层发生反
2 2
应: (已知CrO 的结构为 ),乙醚层发生反应:CrO+(C H)O=
5 5 2 5 2
CrO·O(C H) 反应上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
5 2 5 2.
( )
A.由水层反应可知,氧化性:B.乙醚在检验过程中可用乙醇代替
C.CrO·O(C H) 中不存在非极性键
5 2 5 2
D.水相变为绿色的离子反应为4CrO+12H+=4Cr3++6HO+7O↑
5 2 2
2.(2022·上海市奉贤区模拟)在某酸性溶液中,天然气脱硫原理如图所示。下列说法正确的是( )
A.为了增强氧化性,溶液的酸化可以使用硝酸
B.CH 是反应的催化剂
4
C.过程②使溶液酸性增强
D.过程①与过程②转移电子的物质的量之比为1﹕1
3.(2022·河北衡水深州市中学模拟)为实现随处可上网,中国发射了“中星16号”卫星。NH ClO 是其运
4 4
载火箭的固体燃料,发生反应为2NH ClO =N ↑+Cl↑+2O ↑+4H O↑,下列有 关该反应的说法正确的是(
4 4 2 2 2 2
)
A.上述条件下,氧化性:O>NHClO
2 4 4
B.该反应中,还原产物与氧化产物的物质的量之比为1:3
C.产生6.4 gO 时,反应转移的电子物质的量为0.8 mol
2
D.0.5 mol NH ClO 分解产生气体的体积为44.8 L
4 4
4.(2022·福建省莆田市高三毕业班第一次教学质量检测)已知: 、锌和稀硫酸反应会生成 、
硫酸锌和水。现将 含 的试样和锌、稀硫酸混合恰好完全反应,将生成的 缓慢通过热玻
璃管中, 完全分解冷却后得到 固体。下列有关说法错误的是( )
A.试样中 的质量分数为
B.参与反应的锌失去电子的物质的量为
C.分解产生的氢气在标准状况下体积为
D.若硫酸的物质的量浓度为 ,则消耗稀硫酸的体积为
5.(2022·重庆市育才中学高三期中)让天更蓝、山更绿、水更清,化学在行动。利用Cu-ZSM-5分子筛催化
剂,NH 可脱除燃煤烟气中的NO和NO ,生成两种无毒物质,反应历程如图,下列说法错误的是( )
3 2A.过程Ⅰ、Ⅱ发生的是非氧化还原反应
B.过程Ⅲ中X为N,它既是氧化产物,又是还原产物
2
C.过程Ⅳ中,每生成0.1molH+,转移的电子数为0.15N
A
D.上述历程的总反应为2NH +NO+NO 2N+3H O
3 2 2 2
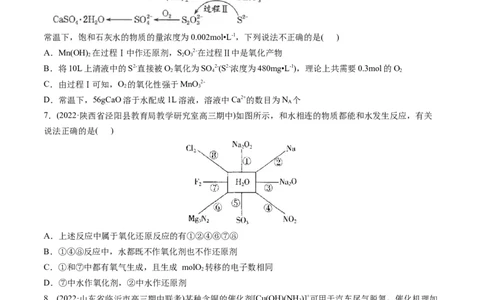
6.(2022·江西省赣州市十六县市十七校高三期中联考)工业上除去电石渣浆(含CaO)上清液中的S2-,并制取
石膏(CaSO•2H O)的常用流程如图:
4 2
常温下,饱和石灰水的物质的量浓度为0.002mol•L-1,下列说法不正确的是( )
A.Mn(OH) 在过程Ⅰ中作还原剂,SO2-在过程Ⅱ中是氧化产物
2 2 3
B.将10L上清液中的S2-直接被O 氧化为SO 2-(S2-浓度为480mg•L-1),理论上共需要0.3mol的O
2 4 2
C.由过程Ⅰ可知,O 的氧化性强于MnO 2-
2 3
D.常温下,56gCaO溶于水配成1L溶液,溶液中Ca2+的数目为N 个
A
7.(2022·陕西省泾阳县教育局教学研究室高三期中)如图所示,和水相连的物质都能和水发生反应,有关
说法正确的是( )
A.上述反应中属于氧化还原反应的有①②④⑥⑦⑧
B.①④⑧反应中,水都既不作氧化剂也不作还原剂
C.①和⑦中都有氧气生成,且生成 molO 转移的电子数相同
2
D.⑦中水作氧化剂,②中水作还原剂
8.(2022·山东省临沂市高三期中联考)某种含铜的催化剂[Cu(OH)(NH )]+可用于汽车尾气脱氮,催化机理如
3
图所示。下列说法正确的是( )A.每一步骤只存在铜和氮元素之间的电子转移
B.该催化循环中Cu的成键数目没有发生变化
C.反应过程中存在非极性键的断裂和形成
D.总反应的化学方程式为4NH +2NO+2O 3N 6HO
3 2 2+ 2
9.(2022·山东省青岛市4区市教学研究室高三联考)党十九大报告中首次将树立和践行“绿水青山就是金山
银山”的理念写入党代会报告,治理污染减少排放具有十分重要的意义。回答下列问题:
(1)下面是消除NO 排放的三个案例:
x
①利用纯碱溶液可以吸收硝酸厂废气中的NO和NO [n(NO):n(NO )=1:1],该过程中发生反应的化学方
2 2
程式为___________。
②三元催化可以将汽车尾气中的CO和NO 进行净化处理,该过程中发生反应的化学方程式为
x
___________。
③利用尿素消除NO 污染的转化反应为Ⅰ.NO+O→NO ,Ⅱ.NO +CO(NH )→无污染气体。尿素中C元
x 2 2 2 3 2
素的化合价___________,反应Ⅱ的化学方程式为___________。
(2)为测定热电厂排放气中SO 的含量,进行了如下实验:标准状况下,将排放气匀速通入100mL0.5mol/L
2
酸性KMnO 溶液中。若排放气的流速为 ,经过bmin溶液恰好褪色,则该排放气中SO 的含量为
4 2
___________g/L。
(3)通过如下流程可实现SO 和NO综合处理并获得保险粉(NaSO)和硝铵。
2 2 2 4
①装置Ⅲ中生成Ce4+与SO2-的物质的量之比为___________。
2 4
②装置Ⅳ中溶液含有a mol·Lˉ1NO -和b mol·Lˉ1NO -,欲将cL该溶液完全转化为硝铵,需要通入O 与NH
2 3 2 3
的体积比为___________(同温同压下)。
10.(2022·上海市第二中学高一月考)实验室可通过置换反应完成卤素单质活泼性比较的实验。某实验小组
设计了装置如图,回答下列问题:(1)已知:常温下KClO 与浓盐酸反应可制取氯气,反应如下。配平该化学方程式,标出电子转移的方向和
3
数目。
反应①___________KClO +___________HCl(浓)=___________KCl + ___________Cl ↑+
3 2
___________HO___________
2
该反应中氧化剂为___________,被还原的元素是___________。
(2)该装置中,吸有KI淀粉溶液的棉球颜色变为___________。吸有NaBr溶液的棉球中发生反应的离子方
程式为___________。
(3)由反应现象能否得出活泼性Br >I 的结论?回答并说明理由___________。
2 2
(4)实验室还可通过以下反应制取氯气:
反应② 2KMnO +16HCl=2KCl + 2MnCl +5Cl ↑+ 8H O;
4 2 2 2
反应③ MnO +4HCl(浓) MnCl +Cl ↑+ 2H O;
2 2 2 2
若要制得相同质量的氯气,反应②和③中电子转移的数目之比为___________。
(5)通过反应①~③,比较反应中氧化剂的氧化性强弱___________,(用“>”、“<”或“=”连接)说明判
断依据:___________。
(6)通过反应①~③,可以知道HCl的还原性强弱与___________、___________等因素有关。