文档内容
专题 39 化学综合实验
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 物质制备型综合实验
考点二 实验设计与评价综合实验
考点一 物质制备型综合实验
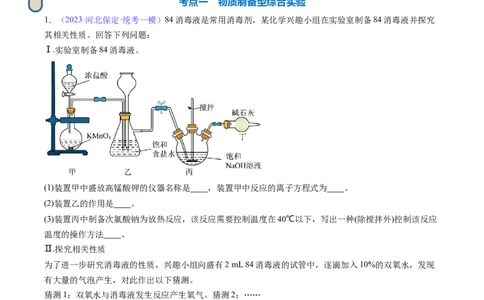
1.(2023·河北保定·统考一模)84消毒液是常用消毒剂,某化学兴趣小组在实验室制备84消毒液并探究
其相关性质。回答下列问题:
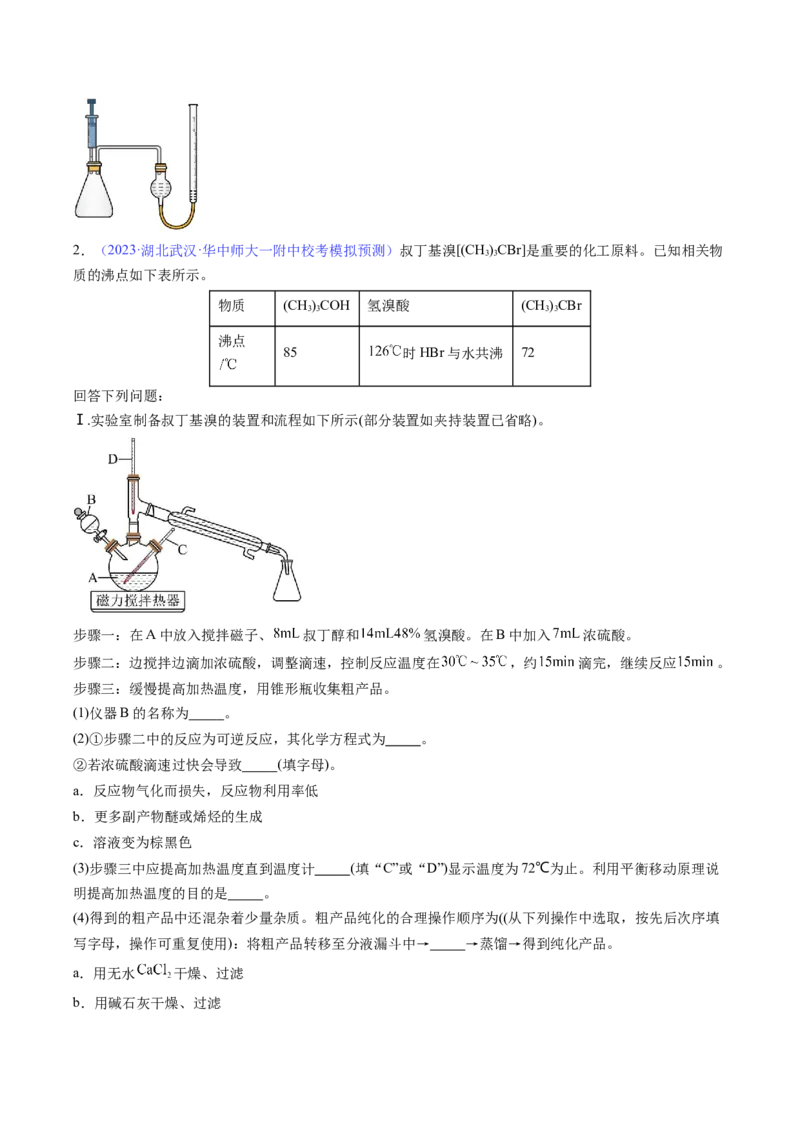
Ⅰ.实验室制备84消毒液。
(1)装置甲中盛放高锰酸钾的仪器名称是 ,装置甲中反应的离子方程式为 。
(2)装置乙的作用是 。
(3)装置丙中制备次氯酸钠为放热反应,该反应需要控制温度在40℃以下,写出一种(除搅拌外)控制该反应
温度的操作方法 。
Ⅱ.探究相关性质
为了进一步研究消毒液的性质,兴趣小组向盛有2 mL 84消毒液的试管中,逐滴加入10%的双氧水,发现
有大量的气泡产生,对此作出以下猜测。
猜测1:双氧水与消毒液发生反应产生氧气。猜测2:……
(4)猜测1中反应的化学方程式为 。猜测2可能为 。
(5)为了验证猜想,某探究小组设计用如图装置进行实验,所选药品有:10%的双氧水、一定浓度的84消毒
液、二氧化锰等。该小组通过实验得出猜测1正确,请依据此装置和所给的药品推测该探究小组的实验设
计是 。
1
原创精品资源学科网独家享有版权,侵权必究!2.(2023·湖北武汉·华中师大一附中校考模拟预测)叔丁基溴[(CH )CBr]是重要的化工原料。已知相关物
3 3
质的沸点如下表所示。
物质 (CH)COH 氢溴酸 (CH)CBr
3 3 3 3
沸点
85 时HBr与水共沸 72
回答下列问题:
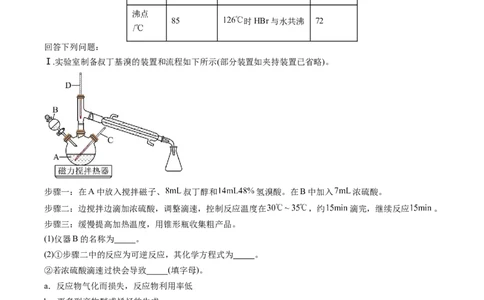
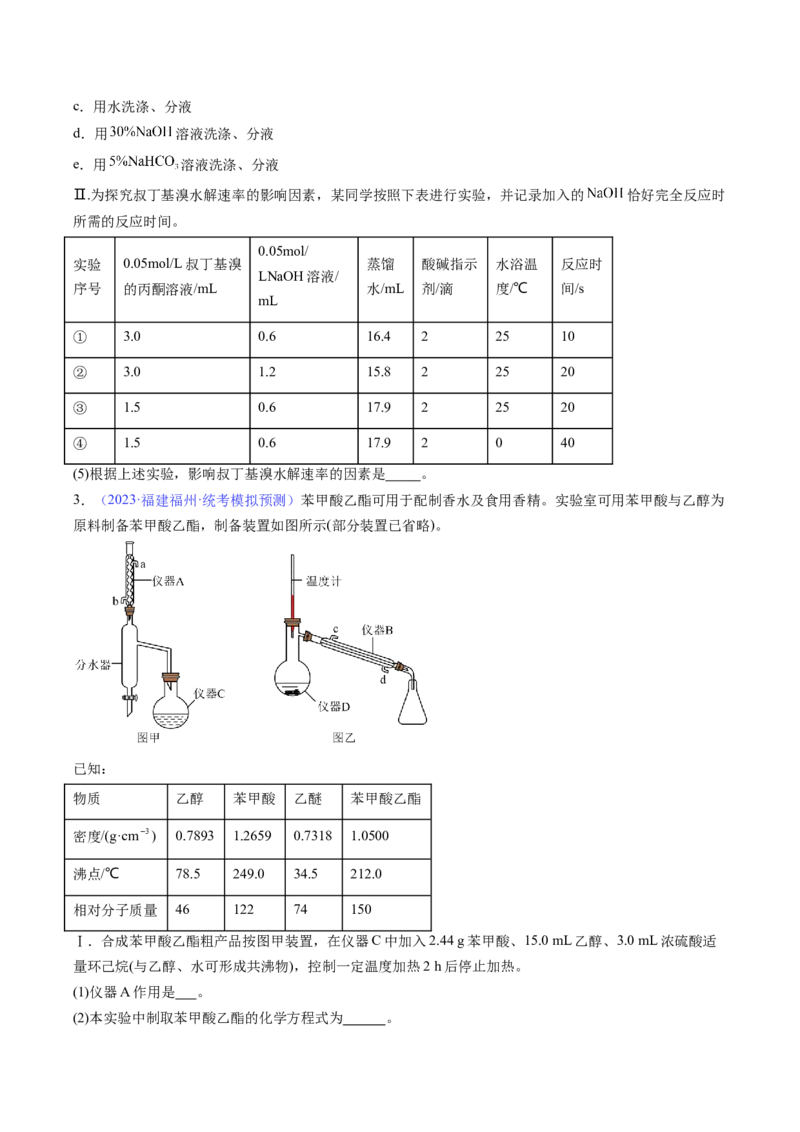
Ⅰ.实验室制备叔丁基溴的装置和流程如下所示(部分装置如夹持装置已省略)。
步骤一:在A中放入搅拌磁子、 叔丁醇和 氢溴酸。在B中加入 浓硫酸。
步骤二:边搅拌边滴加浓硫酸,调整滴速,控制反应温度在 ,约 滴完,继续反应 。
步骤三:缓慢提高加热温度,用锥形瓶收集粗产品。
(1)仪器B的名称为 。
(2)①步骤二中的反应为可逆反应,其化学方程式为 。
②若浓硫酸滴速过快会导致 (填字母)。
a.反应物气化而损失,反应物利用率低
b.更多副产物醚或烯烃的生成
c.溶液变为棕黑色
(3)步骤三中应提高加热温度直到温度计 (填“C”或“D”)显示温度为72℃为止。利用平衡移动原理说
明提高加热温度的目的是 。
(4)得到的粗产品中还混杂着少量杂质。粗产品纯化的合理操作顺序为((从下列操作中选取,按先后次序填
写字母,操作可重复使用):将粗产品转移至分液漏斗中→ →蒸馏→得到纯化产品。
a.用无水 干燥、过滤
b.用碱石灰干燥、过滤c.用水洗涤、分液
d.用 溶液洗涤、分液
e.用 溶液洗涤、分液
Ⅱ.为探究叔丁基溴水解速率的影响因素,某同学按照下表进行实验,并记录加入的 恰好完全反应时
所需的反应时间。
0.05mol/
实验 0.05mol/L叔丁基溴 蒸馏 酸碱指示 水浴温 反应时
LNaOH溶液/
序号 的丙酮溶液/mL 水/mL 剂/滴 度/℃ 间/s
mL
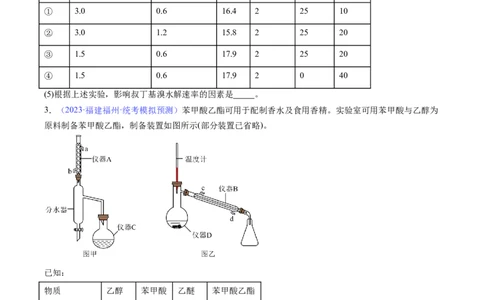
① 3.0 0.6 16.4 2 25 10
② 3.0 1.2 15.8 2 25 20
③ 1.5 0.6 17.9 2 25 20
④ 1.5 0.6 17.9 2 0 40
(5)根据上述实验,影响叔丁基溴水解速率的因素是 。
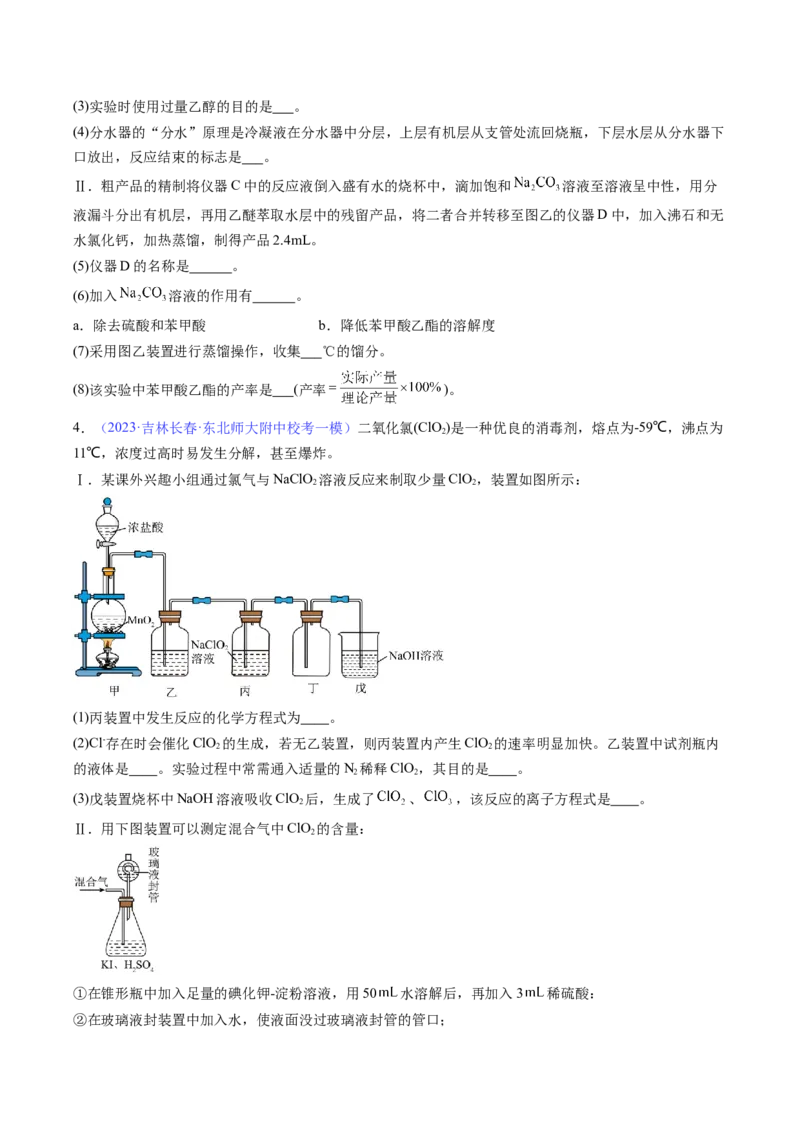
3.(2023·福建福州·统考模拟预测)苯甲酸乙酯可用于配制香水及食用香精。实验室可用苯甲酸与乙醇为
原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。
已知:
物质 乙醇 苯甲酸 乙醚 苯甲酸乙酯
密度/(g·cm ) 0.7893 1.2659 0.7318 1.0500
沸点/℃ 78.5 249.0 34.5 212.0
相对分子质量 46 122 74 150
Ⅰ.合成苯甲酸乙酯粗产品按图甲装置,在仪器C中加入2.44 g苯甲酸、15.0 mL乙醇、3.0 mL浓硫酸适
量环己烷(与乙醇、水可形成共沸物),控制一定温度加热2 h后停止加热。
(1)仪器A作用是 。
(2)本实验中制取苯甲酸乙酯的化学方程式为 。(3)实验时使用过量乙醇的目的是 。
(4)分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下
口放出,反应结束的标志是 。
Ⅱ.粗产品的精制将仪器C中的反应液倒入盛有水的烧杯中,滴加饱和 溶液至溶液呈中性,用分
液漏斗分出有机层,再用乙醚萃取水层中的残留产品,将二者合并转移至图乙的仪器D中,加入沸石和无
水氯化钙,加热蒸馏,制得产品2.4mL。
(5)仪器D的名称是 。
(6)加入 溶液的作用有 。
a.除去硫酸和苯甲酸 b.降低苯甲酸乙酯的溶解度
(7)采用图乙装置进行蒸馏操作,收集 ℃的馏分。
(8)该实验中苯甲酸乙酯的产率是 (产率 )。
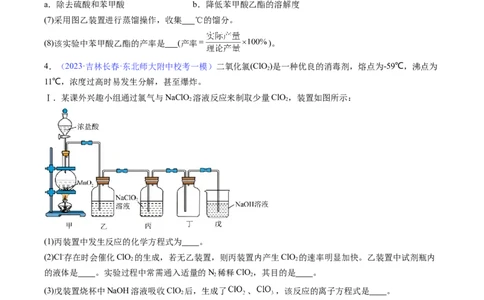
4.(2023·吉林长春·东北师大附中校考一模)二氧化氯(ClO )是一种优良的消毒剂,熔点为-59℃,沸点为
2
11℃,浓度过高时易发生分解,甚至爆炸。
Ⅰ.某课外兴趣小组通过氯气与NaClO 溶液反应来制取少量ClO ,装置如图所示:
2 2
(1)丙装置中发生反应的化学方程式为 。
(2)Cl-存在时会催化ClO 的生成,若无乙装置,则丙装置内产生ClO 的速率明显加快。乙装置中试剂瓶内
2 2
的液体是 。实验过程中常需通入适量的N 稀释ClO ,其目的是 。
2 2
(3)戊装置烧杯中NaOH溶液吸收ClO 后,生成了 、 ,该反应的离子方程式是 。
2
Ⅱ.用下图装置可以测定混合气中ClO 的含量:
2
①在锥形瓶中加入足量的碘化钾-淀粉溶液,用50 水溶解后,再加入3 稀硫酸:
②在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;③将一定量的混合气体通入锥形瓶中吸收;
④将玻璃液封装置中的水倒入锥形瓶中:
⑤用0.1000 硫代硫酸钠标准溶液滴定锥形瓶中的溶液( ),指示剂显示终点
时共用去20.00 硫代硫酸钠溶液。在此过程中:
(4)玻璃液封装置的作用是 , 。
(5)滴定至终点的现象是 。
(6)测得混合气中ClO 的质量为 g。
2
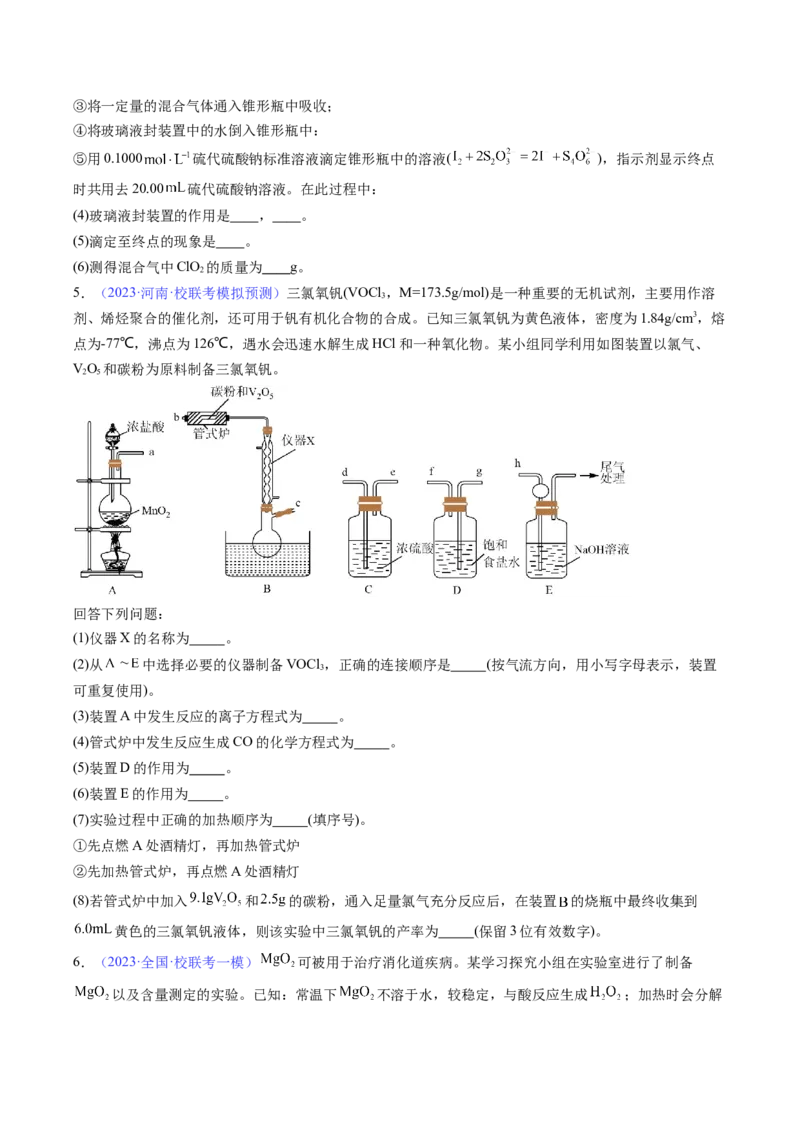
5.(2023·河南·校联考模拟预测)三氯氧钒(VOCl ,M=173.5g/mol)是一种重要的无机试剂,主要用作溶
3
剂、烯烃聚合的催化剂,还可用于钒有机化合物的合成。已知三氯氧钒为黄色液体,密度为1.84g/cm3,熔
点为-77℃,沸点为126℃,遇水会迅速水解生成HCl和一种氧化物。某小组同学利用如图装置以氯气、
VO 和碳粉为原料制备三氯氧钒。
2 5
回答下列问题:
(1)仪器X的名称为 。
(2)从 中选择必要的仪器制备VOCl ,正确的连接顺序是 (按气流方向,用小写字母表示,装置
3
可重复使用)。
(3)装置A中发生反应的离子方程式为 。
(4)管式炉中发生反应生成CO的化学方程式为 。
(5)装置D的作用为 。
(6)装置E的作用为 。
(7)实验过程中正确的加热顺序为 (填序号)。
①先点燃A处酒精灯,再加热管式炉
②先加热管式炉,再点燃A处酒精灯
(8)若管式炉中加入 和 的碳粉,通入足量氯气充分反应后,在装置 的烧瓶中最终收集到
黄色的三氯氧钒液体,则该实验中三氯氧钒的产率为 (保留3位有效数字)。
6.(2023·全国·校联考一模) 可被用于治疗消化道疾病。某学习探究小组在实验室进行了制备
以及含量测定的实验。已知:常温下 不溶于水,较稳定,与酸反应生成 ;加热时会分解生成 和 。
请回答下列问题:
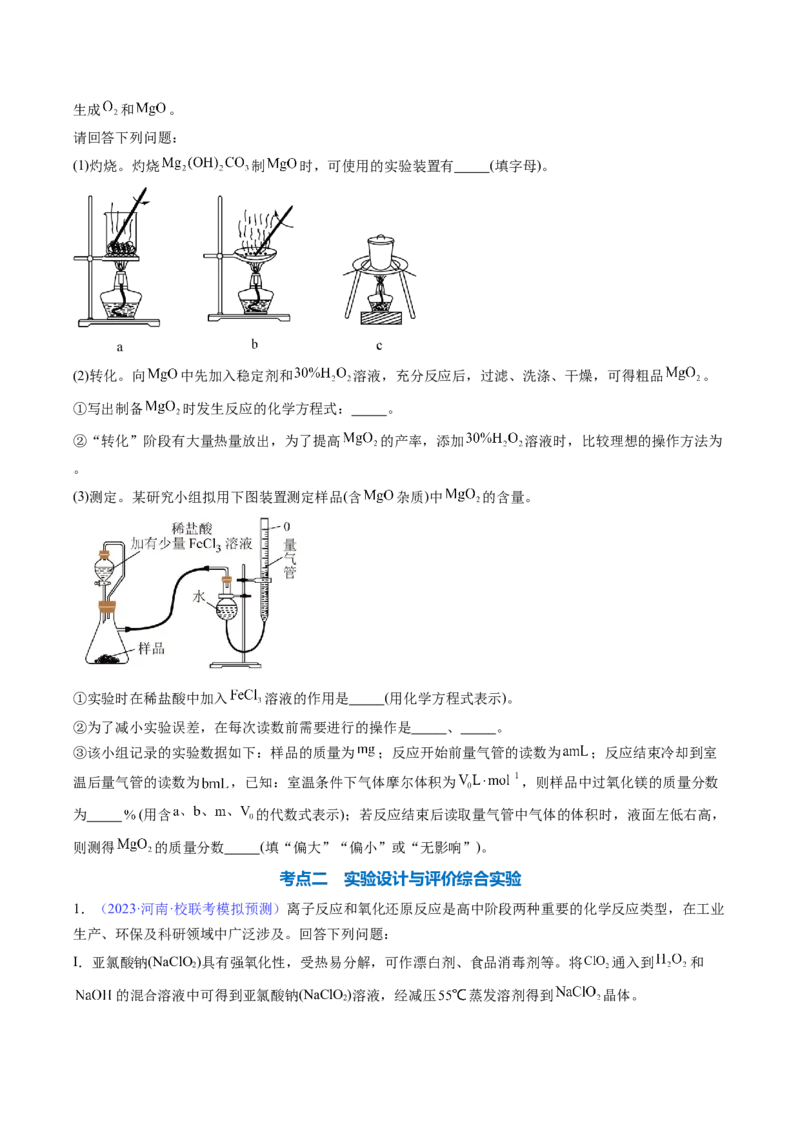
(1)灼烧。灼烧 制 时,可使用的实验装置有 (填字母)。
(2)转化。向 中先加入稳定剂和 溶液,充分反应后,过滤、洗涤、干燥,可得粗品 。
①写出制备 时发生反应的化学方程式: 。
②“转化”阶段有大量热量放出,为了提高 的产率,添加 溶液时,比较理想的操作方法为
。
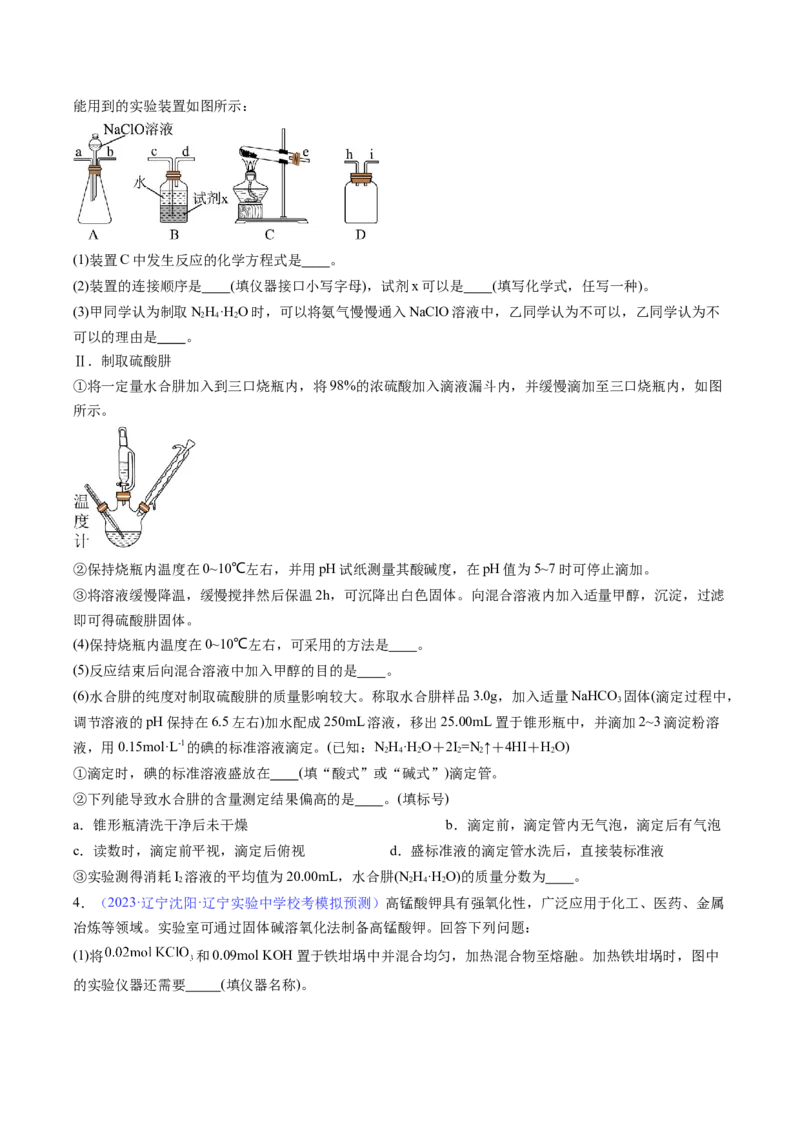
(3)测定。某研究小组拟用下图装置测定样品(含 杂质)中 的含量。
①实验时在稀盐酸中加入 溶液的作用是 (用化学方程式表示)。
②为了减小实验误差,在每次读数前需要进行的操作是 、 。
③该小组记录的实验数据如下:样品的质量为 ;反应开始前量气管的读数为 ;反应结束冷却到室
温后量气管的读数为 ,已知:室温条件下气体摩尔体积为 ,则样品中过氧化镁的质量分数
为 (用含 的代数式表示);若反应结束后读取量气管中气体的体积时,液面左低右高,
则测得 的质量分数 (填“偏大”“偏小”或“无影响”)。
考点二 实验设计与评价综合实验
1.(2023·河南·校联考模拟预测)离子反应和氧化还原反应是高中阶段两种重要的化学反应类型,在工业
生产、环保及科研领域中广泛涉及。回答下列问题:
I.亚氯酸钠(NaClO)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。将 通入到 和
2
的混合溶液中可得到亚氯酸钠(NaClO)溶液,经减压 蒸发溶剂得到 晶体。
2(1)写出上述生成 的化学方程式:
(2)上述反应中 作 (填“氧化剂”或“还原剂”), 属于二元弱酸,写出 的第一步电离
方程式: 。
(3)减压 蒸发而不直接常压蒸发的原因为 。
II.硫代硫酸钠(Na SO)俗称大苏打,易溶于水,溶于水后呈碱性,遇酸不稳定, 与硫酸的反应常
2 2 3
用于定性分析影响化学反应速率的因素; 在“碘量法”氧化还原滴定中常作标准试剂,用于定量
测量碘的含量。
(4)写出 与硫酸反应的离子方程式: 。
(5)利用“碘量法”测定芒硝( ,含 杂质)中 的质量分数。称取 样品,置于碘量瓶
中,移取 溶液(含 )置于其中,并加入乙酸溶液,密闭并置于暗处充分反应 ,
有单质硫析出,以淀粉为指示剂,过量的 用 溶液滴定,测定消耗 溶液的体
积为VmL。已知: 。
①“密闭并置于暗处充分反应 ”过程中采用密闭的目的是 。
②滴定终点的现象为 。
③样品中 的质量分数为 (写出表达式)。
2.(2023·四川成都·石室中学校考模拟预测)硫酸亚铁铵[(NH )Fe(SO )•6H O]俗称莫尔盐,是一种常见
4 2 4 2 2
的补血剂,石室中学2023届的同学们分小组制取了莫尔盐晶体并对其热分解产物进行了探究。
I.莫尔盐晶体的制备
(1)用如图1的装置制备FeSO 。
4
①废铁屑需要先进行碱煮,目的是 。
②加入的废铁屑需过量,除废铁屑不纯外,主要原因是 。
③用离子方程式解释C中所盛试剂的作用: 。
(2)反应结束后趁热过滤,向滤液中加入HSO 调节pH在1~2,迅速加入一定质量的(NH )SO 固体,在
2 4 4 2 4
70~80℃条件下溶解后,趁热倒入50mL乙醇中,析出莫尔盐晶体。乙醇的作用为 。
II.莫尔盐晶体热分解产物探究
查阅文献得知:莫尔盐隔绝空气加热至500℃时可完全分解,产物复杂。
[提出猜想](3)莫尔盐晶体受热分解,同学们认为分解产物可能有以下几种情况:
A.FeO、NH 、SO 、HO
3 3 2
B.FeO、NH 、SO 、HO
3 2 2
C.Fe O、NH 、SO 、HO
2 3 3 3 2
D.FeO、N、SO 、HO
2 2 2
E.Fe O、NH 、SO 、SO 、HO
2 3 3 3 2 2
F.Fe O、NH 、SO 、SO 、N、HO
2 3 3 3 2 2 2
经认真分析,通过推理即可确定猜想 (填序号)不成立。
[实验探究]
(4)甲组同学设计如图2的实验装置,观察到A中固体逐渐变为红棕色,B中白色固体变蓝,D中酚酞溶液
变红色,由此可知莫尔盐分解的产物中有HO、 (填化学式)。进一步实验证实A中充分反应后的固体
2
残留物中不含FeO,操作方法及实验现象:取少量A中固体残留物于试管中, 。
(5)乙组选用甲组实验中的装置A和图3所示的装置进行实验,验证了莫尔盐分解的产物中还有SO 、SO
2 3
和N。
2
①乙组同学的实验装置中,依次连接的合理顺序(用装置的字母表示)为A、E、 。(各装置中试剂均足
量)
②实验中,准确称量莫尔盐7.8400g,加热充分反应后,测得装置A中固体残留物的质量为1.6000g,装置
F中生成白色沉淀的质量为5.8250g。写出该条件下莫尔盐受热分解的化学方程式: 。(已
M[(NH)Fe(SO )•6H O]=392g•mol-1,分解产物被充分吸收,不考虑其损失)
4 2 4 2 2
3.(2023·广西柳州·柳州高级中学校联考模拟预测)硫酸肼(N H·H SO )又名硫酸联氨,无色或白色棱形
2 4 2 4
结晶或粉末。易溶于热水,微溶于冷水,不溶于醇。某实验小组用水合肼制取硫酸肼。
Ⅰ.水合肼的制取
NH·H O(水合肼)为无色透明油状发烟液体,具有强还原性。原理为NaClO+2NH =N H·H O+NaCl,可
2 4 2 3 2 4 2能用到的实验装置如图所示:
(1)装置C中发生反应的化学方程式是 。
(2)装置的连接顺序是 (填仪器接口小写字母),试剂x可以是 (填写化学式,任写一种)。
(3)甲同学认为制取NH·H O时,可以将氨气慢慢通入NaClO溶液中,乙同学认为不可以,乙同学认为不
2 4 2
可以的理由是 。
Ⅱ.制取硫酸肼
①将一定量水合肼加入到三口烧瓶内,将98%的浓硫酸加入滴液漏斗内,并缓慢滴加至三口烧瓶内,如图
所示。
②保持烧瓶内温度在0~10℃左右,并用pH试纸测量其酸碱度,在pH值为5~7时可停止滴加。
③将溶液缓慢降温,缓慢搅拌然后保温2h,可沉降出白色固体。向混合溶液内加入适量甲醇,沉淀,过滤
即可得硫酸肼固体。
(4)保持烧瓶内温度在0~10℃左右,可采用的方法是 。
(5)反应结束后向混合溶液中加入甲醇的目的是 。
(6)水合肼的纯度对制取硫酸肼的质量影响较大。称取水合肼样品3.0g,加入适量NaHCO 固体(滴定过程中,
3
调节溶液的pH保持在6.5左右)加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶
液,用0.15mol·L-1的碘的标准溶液滴定。(已知:NH·H O+2I=N ↑+4HI+HO)
2 4 2 2 2 2
①滴定时,碘的标准溶液盛放在 (填“酸式”或“碱式”)滴定管。
②下列能导致水合肼的含量测定结果偏高的是 。(填标号)
a.锥形瓶清洗干净后未干燥 b.滴定前,滴定管内无气泡,滴定后有气泡
c.读数时,滴定前平视,滴定后俯视 d.盛标准液的滴定管水洗后,直接装标准液
③实验测得消耗I 溶液的平均值为20.00mL,水合肼(N H·H O)的质量分数为 。
2 2 4 2
4.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)高锰酸钾具有强氧化性,广泛应用于化工、医药、金属
冶炼等领域。实验室可通过固体碱溶氧化法制备高锰酸钾。回答下列问题:
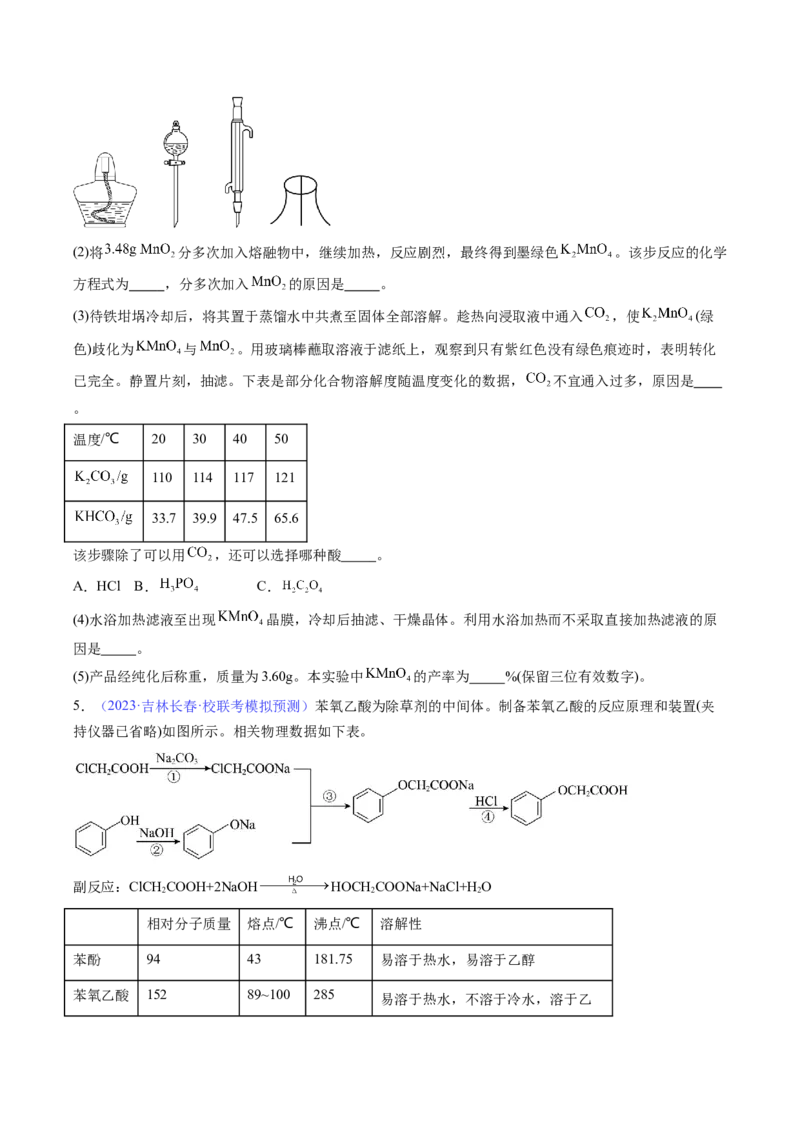
(1)将 和0.09mol KOH置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,图中
的实验仪器还需要 (填仪器名称)。(2)将 分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色 。该步反应的化学
方程式为 ,分多次加入 的原因是 。
(3)待铁坩埚冷却后,将其置于蒸馏水中共煮至固体全部溶解。趁热向浸取液中通入 ,使 (绿
色)歧化为 与 。用玻璃棒蘸取溶液于滤纸上,观察到只有紫红色没有绿色痕迹时,表明转化
已完全。静置片刻,抽滤。下表是部分化合物溶解度随温度变化的数据, 不宜通入过多,原因是
。
温度/℃ 20 30 40 50
110 114 117 121
33.7 39.9 47.5 65.6
该步骤除了可以用 ,还可以选择哪种酸 。
A.HCl B. C.
(4)水浴加热滤液至出现 晶膜,冷却后抽滤、干燥晶体。利用水浴加热而不采取直接加热滤液的原
因是 。
(5)产品经纯化后称重,质量为3.60g。本实验中 的产率为 %(保留三位有效数字)。
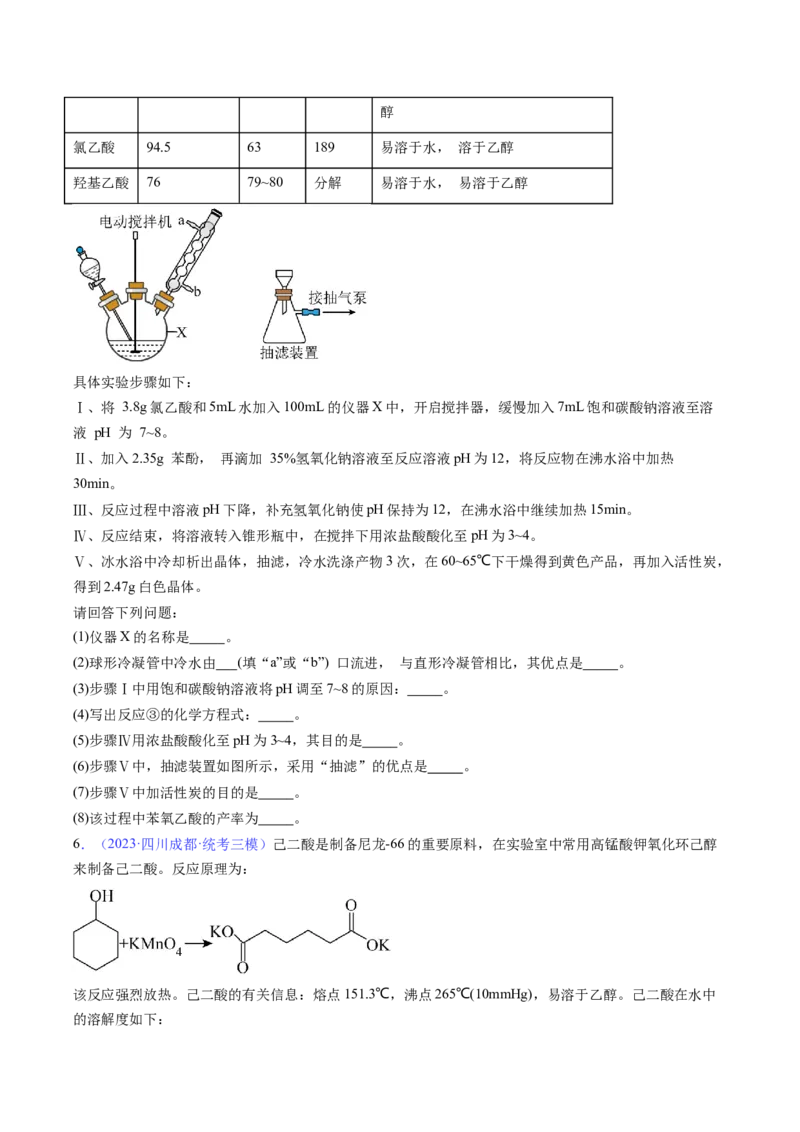
5.(2023·吉林长春·校联考模拟预测)苯氧乙酸为除草剂的中间体。制备苯氧乙酸的反应原理和装置(夹
持仪器已省略)如图所示。相关物理数据如下表。
副反应:ClCH COOH+2NaOH HOCH COONa+NaCl+H O
2 2 2
相对分子质量 熔点/℃ 沸点/℃ 溶解性
苯酚 94 43 181.75 易溶于热水,易溶于乙醇
苯氧乙酸 152 89~100 285 易溶于热水,不溶于冷水,溶于乙醇
氯乙酸 94.5 63 189 易溶于水, 溶于乙醇
羟基乙酸 76 79~80 分解 易溶于水, 易溶于乙醇
具体实验步骤如下:
Ⅰ、将 3.8g氯乙酸和5mL水加入100mL的仪器X中,开启搅拌器,缓慢加入7mL饱和碳酸钠溶液至溶
液 pH 为 7~8。
Ⅱ、加入2.35g 苯酚, 再滴加 35%氢氧化钠溶液至反应溶液pH为12,将反应物在沸水浴中加热
30min。
Ⅲ、反应过程中溶液pH下降,补充氢氧化钠使pH保持为12,在沸水浴中继续加热15min。
Ⅳ、反应结束,将溶液转入锥形瓶中,在搅拌下用浓盐酸酸化至pH为3~4。
Ⅴ、冰水浴中冷却析出晶体,抽滤,冷水洗涤产物3次,在60~65℃下干燥得到黄色产品,再加入活性炭,
得到2.47g白色晶体。
请回答下列问题:
(1)仪器X的名称是 。
(2)球形冷凝管中冷水由 (填“a”或“b”) 口流进, 与直形冷凝管相比,其优点是 。
(3)步骤Ⅰ中用饱和碳酸钠溶液将pH调至7~8的原因: 。
(4)写出反应③的化学方程式: 。
(5)步骤Ⅳ用浓盐酸酸化至pH为3~4,其目的是 。
(6)步骤Ⅴ中,抽滤装置如图所示,采用“抽滤”的优点是 。
(7)步骤Ⅴ中加活性炭的目的是 。
(8)该过程中苯氧乙酸的产率为 。
6.(2023·四川成都·统考三模)己二酸是制备尼龙-66的重要原料,在实验室中常用高锰酸钾氧化环己醇
来制备己二酸。反应原理为:
该反应强烈放热。己二酸的有关信息:熔点151.3℃,沸点265℃(10mmHg),易溶于乙醇。己二酸在水中
的溶解度如下:温度/℃ 15 34 50 70 87 100
溶解度/(g/100gH O) 1.44 3.08 8.46 34 94 100
2
回答下列问题:
(1)高锰酸钾与环己醇反应的还原产物是一种黑色固体,其化学式是 ;向KMnO 溶液中滴加环己醇时,
4
一段时间才有明显现象,初期速率较慢的原因可能是 (写一条);反应中期应小心维持反应液温度在
45℃左右,宜选择的仪器有 。
①冰水浴 ②温度计 ③球形冷凝管 ④恒压滴液漏斗
(2)加入全部环己醇后,再用沸水浴加热5分钟,用玻璃棒蘸取1滴反应混合物于滤纸上,若滤纸上出现
现象,说明KMnO 有剩余,可再加入少量NaHSO 固体处理。
4 3
(3)趁热抽滤并用热水洗涤滤渣三次,合并滤液和洗涤液。合并的目的是 。
(4)合并液用浓盐酸酸化至pH为1~2,然后加热浓缩, ,减压过滤,冰水洗涤,称量。用冰水洗涤的
目的是 。
(5)可用NaOH标准溶液滴定产品测定其纯度。测定时,为了使己二酸固体在水中全部溶解,可采取的措施
有 、 。