文档内容
表格型实验方案的评价
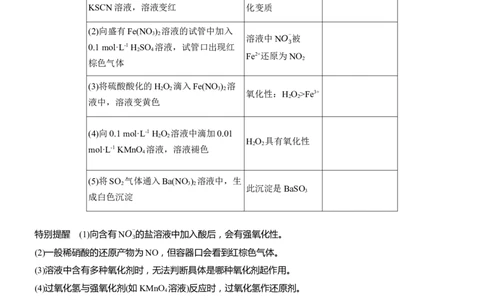
1.氧化性、还原性强弱探究
判断(填
实验操作及现象 实验结论
“√”或“×”)
(1)将Fe(NO ) 样品溶于稀硫酸,滴加 Fe(NO ) 晶体已氧
3 2 3 2
KSCN溶液,溶液变红 化变质
(2)向盛有Fe(NO ) 溶液的试管中加入
3 2 溶液中NO-
被
3
0.1 mol·L-1 H SO 溶液,试管口出现红
2 4
Fe2+还原为NO
2
棕色气体
(3)将硫酸酸化的H O 滴入Fe(NO ) 溶
2 2 3 2
氧化性:H O >Fe3+
2 2
液中,溶液变黄色
(4)向0.1 mol·L-1 H O 溶液中滴加0.01
2 2
H O 具有氧化性
2 2
mol·L-1 KMnO 溶液,溶液褪色
4
(5)将SO 气体通入Ba(NO ) 溶液中,生
2 3 2
此沉淀是BaSO
3
成白色沉淀
特别提醒
(1)向含有NO-
的盐溶液中加入酸后,会有强氧化性。
3
(2)一般稀硝酸的还原产物为NO,但容器口会看到红棕色气体。
(3)溶液中含有多种氧化剂时,无法判断具体是哪种氧化剂起作用。
(4)过氧化氢与强氧化剂(如KMnO 溶液)反应时,过氧化氢作还原剂。
4
2.电解质强弱探究
判断(填
探究方案 探究目的
“√”或“×”)
(1)室温下,用pH计测量醋酸溶液、盐酸
CH COOH是弱电解质
3
的pH,比较溶液pH大小
(2)室温下,用pH试纸测得CH COONa HNO 2 电离出H+的能力比
3
溶液的pH约为9,NaNO 溶液的pH约 CH 3 COOH强
2为8
特别提醒 应比较同温度、同浓度、同类型的电解质。
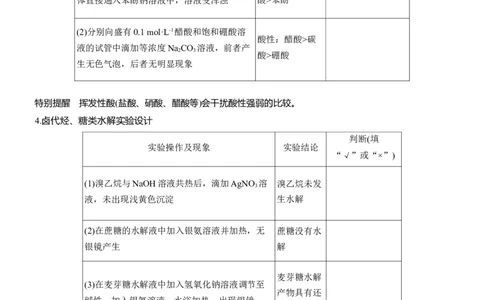
3.通过现象判断酸性强弱
判断(填
实验操作及现象 实验结论
“√”或“×”)
(1)向Na CO 溶液中加入冰醋酸,将产生的气 酸性:醋酸>碳
2 3
体直接通入苯酚钠溶液中,溶液变浑浊 酸>苯酚
(2)分别向盛有0.1 mol·L-1醋酸和饱和硼酸溶
酸性:醋酸>碳
液的试管中滴加等浓度Na CO 溶液,前者产
2 3
酸>硼酸
生无色气泡,后者无明显现象
特别提醒 挥发性酸(盐酸、硝酸、醋酸等)会干扰酸性强弱的比较。
4.卤代烃、糖类水解实验设计
判断(填
实验操作及现象 实验结论
“√”或“×”)
(1)溴乙烷与NaOH溶液共热后,滴加AgNO 溶 溴乙烷未发
3
液,未出现浅黄色沉淀 生水解
(2)在蔗糖的水解液中加入银氨溶液并加热,无 蔗糖没有水
银镜产生 解
麦芽糖水解
(3)在麦芽糖水解液中加入氢氧化钠溶液调节至
产物具有还
碱性,加入银氨溶液,水浴加热,出现银镜
原性
特别提醒 ①水解液要先中和,后加检验试剂。②麦芽糖水解时,由于麦芽糖自身具有还原性,故无法根
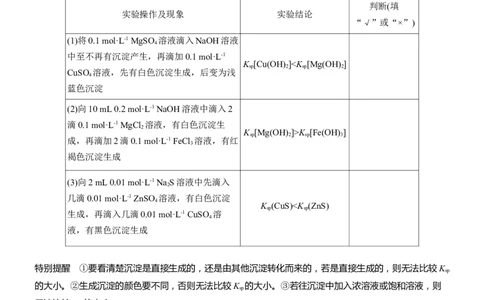
据是否有银镜(或砖红色沉淀)产生来判断麦芽糖是否水解。5.有关K 的判断
sp
判断(填
实验操作及现象 实验结论
“√”或“×”)
(1)将0.1 mol·L-1 MgSO 溶液滴入NaOH溶液
4
中至不再有沉淀产生,再滴加0.1 mol·L-1
K [Cu(OH) ]K [Fe(OH) ]
sp 2 sp 3
成,再滴加2滴0.1 mol·L-1 FeCl 溶液,有红
3
褐色沉淀生成
(3)向2 mL 0.01 mol·L-1 Na S溶液中先滴入
2
几滴0.01 mol·L-1 ZnSO 溶液,有白色沉淀
4
K (CuS)