文档内容
专题九 定量分析及方案设计类实验专题突破
【考情分析】
定量实验是将化学实验与化学计量有机的结合在一起测定物质化学组成与含量
的探究性实验,探究类实验主要探究物质分解的产物和物质的性质;设计并完成
实验报告包括补充实验步骤或实验步骤的排序、选择试剂和现象的描述等。都是
近几年高考命题的常考题型。如2018·课标全国Ⅱ28,2018·课标全国Ⅲ26,2017.
全国卷Ⅱ28等,此类题设计实验目的性、实用性强,能给予学生较大的创造空间
更能激发学生的学习兴趣,培养学生严谨求实的科学态度。
考点指导1 定量分析型综合实验
1.定量实验数据的测定方法
(1)沉淀法
先将某种成分转化为沉淀,然后称量纯净、干燥的沉淀的质量,再进行相关计算。
(2)测气体体积法
对于产生气体的反应,可以通过测定气体体积的方法测定样品纯度。
①常见测量气体体积的实验装置
②量气时应注意的问题
a.量气时应保持装置处于室温状态。
b.读数时要特别注意消除“压强差”,保持液面相平还要注意视线与液面最低处
相平。如上图(Ⅰ)(Ⅳ)应使左侧和右侧的液面高度保持相平。(3)测气体质量法
将生成的气体通入足量的吸收剂中,通过称量实验前后吸收剂的质量,求得所吸
收气体的质量,然后进行相关计算。
(4)滴定法
即利用滴定操作原理,通过酸碱中和滴定、沉淀滴定和氧化还原反应滴定等获得
相应数据后再进行相关计算。
2.定量实验数据处理
如何用好、选好数据,是解决化学定量实验题的关键所在。解决化学定量实验题
的一般方法为比较数据、转变物质、分析利弊、确定方案。
(1)对数据进行比较是解决问题的突破口,注意比较数据的交点与重合区。
(2)转变物质则是实现实验目标的重要途径,在一些物质提纯与制备的问题中,往
往会提供一些物质沉淀的pH范围、物质的沸点、密度、溶解性等呈现物质物理性
质的数据。
(3)在实际生产、生活中,除了涉及是否能够通过相应反应来实现实验目标外,还
涉及经济效益的问题,在原理、环保等没有大的差异时,选择廉价原料完成相应
的实验成为首选。
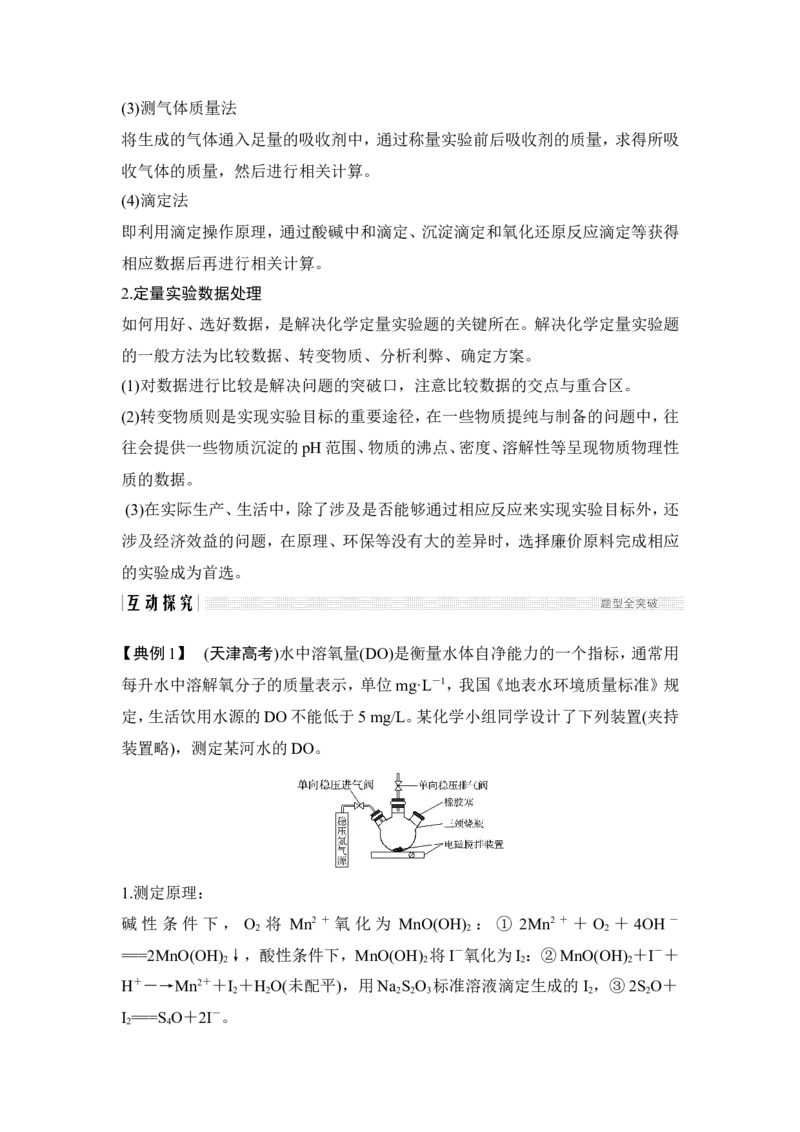
【典例1】 (天津高考)水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用
每升水中溶解氧分子的质量表示,单位mg·L-1,我国《地表水环境质量标准》规
定,生活饮用水源的DO不能低于5 mg/L。某化学小组同学设计了下列装置(夹持
装置略),测定某河水的DO。
1.测定原理:
碱 性 条 件 下 , O 将 Mn2 + 氧 化 为 MnO(OH) : ① 2Mn2 + + O + 4OH -
2 2 2
===2MnO(OH) ↓,酸性条件下,MnO(OH) 将I-氧化为I :②MnO(OH) +I-+
2 2 2 2
H+―→Mn2++I +H O(未配平),用Na S O 标准溶液滴定生成的I ,③2S O+
2 2 2 2 3 2 2
I ===S O+2I-。
2 42.测定步骤:
a.安装装置,检验气密性,充N 排尽空气后,停止充N 。
2 2
b.向烧瓶中加入200 mL水样。
c.向烧瓶中依次迅速加入1 mL MnSO 无氧溶液(过量)2 mL碱性KI无氧溶液(过
4
量),开启搅拌器,至反应①完全。
d.搅拌并向烧瓶中加入2 mLH SO 无氧溶液,至反应②完全,溶液为中性或弱酸
2 4
性。
e.从烧瓶中取出40.00 mL溶液,以淀粉作指示剂,用0.010 00 mol·L-1 Na S O 溶
2 2 3
液进行滴定,记录数据。
f.……
g.处理数据(忽略氧气从水样中的溢出量和加入试剂后水样体积的变化)。
回答下列问题:
(1)配制以上无氧溶液时,除去所用溶剂水中氧的简单操作为________。
(2)在橡胶塞处加入水样及有关试剂应选择的仪器为________。
①滴定管 ②注射器 ③量筒
(3)搅拌的作用是________。
(4)配平反应②的方程式,其化学计量数依次为________。
(5)步骤f为__________________________________________________________。
(6)步骤e中达到滴定终点的标志为________。若某次滴定消耗Na S O 溶液4.50
2 2 3
mL,水样的DO=________mg·L-1(保留一位小数)。作为饮用水源,此次测得DO
是否达标:________(填“是”或“否”)。
(7)步骤d中加入H SO 溶液反应后,若溶液pH过低,滴定时会产生明显的误差,
2 4
写 出 产 生 此 误 差 的 原 因 ( 用 离 子 方 程 式 表 示 , 至 少 写 出 2
个 )__________________________________________________________________
_
_____________________________________________________________________
。
[标准答案] (1)将溶剂水煮沸后冷却 (2)②
(3)使溶液混合均匀,快速完成反应 (4)1,2,4,1,1,3
(5)重复步骤e的操作2~3次(6)溶液蓝色褪去且半分钟内不变色 9.0 是
(7)2H++S O===S↓+SO ↑+H O、
2 2 2
SO +I +2H O===4H++SO+2I-、4H++4I-+O ===2I +2H O(任写其中2个)
2 2 2 2 2 2
[命题分析]
第(1)问考查化学实验的基本操作
气体的溶解度随温度升高而减小,故可将水加热煮沸法除去溶解在水中的O 。
2
第(2)问考查实验仪器的选择
测定步骤中加入的试剂为无氧溶液,且加入的水样要防止空气中氧气的干扰,故
需要隔绝空气,所以选用密封性较好的注射器。
第(3)问考查化学实验基本操作的作用
搅拌使物质混合均匀,加快化学反应的进行。
第(4)问考查氧化还原方程式的配平
MnO(OH) 中Mn的化合价为+4,能将I-氧化成I ,依据氧化还原方程式配平的
2 2
方法配平化学方程式
MnO(OH) +2I-+4H+===Mn2++I +3H O。
2 2 2
第(5)(6)问考查中和滴定的实验操作及滴定终点的判断
中和滴定一般采用重复滴定2~3次来减小滴定误差,用Na S O 溶液进行滴定时
2 2 3
I 的量逐渐减小至消失时为滴定终点,此时的现象是蓝色消失且半分钟内不变色
2
第(6)问考查多步反应方程式的计算
根据题中所给的反应方程式得出关系式:
2Mn2+~O ~2MnO(OH) ~2I ~4Na S O
2 2 2 2 2 3
1 4
n(O ) 0.004 5 L×0.010 00 mol·L-1
2
则n(O )=×0.004 5 L×0.010 00 mol·L-1
2
DO==9.0×10-3 g·L-1=9.0 mg·L-1
高于5 mg·L-1,故此次测得DO达标。
第(7)问考查氧化还原滴定的误差分析
Na S O 在酸性条件下可以发生歧化反应生成S和SO ,且生成的SO 可被I 氧化
2 2 3 2 2 2
另外,酸性较强时I-也可被空气中的O 氧化。
2
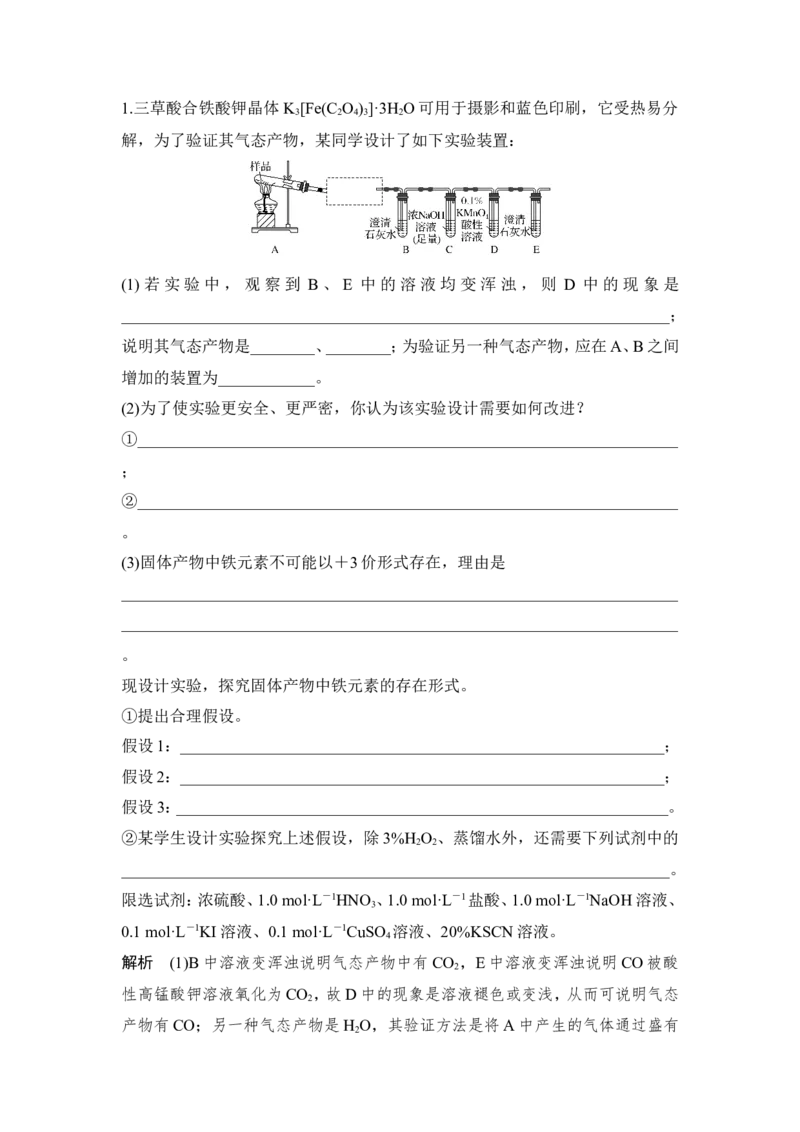
【对点训练】1.三草酸合铁酸钾晶体K [Fe(C O ) ]·3H O可用于摄影和蓝色印刷,它受热易分
3 2 4 3 2
解,为了验证其气态产物,某同学设计了如下实验装置:
(1)若实验中,观察到 B、E 中的溶液均变浑浊,则 D 中的现象是
____________________________________________________________________;
说明其气态产物是________、________;为验证另一种气态产物,应在A、B之间
增加的装置为____________。
(2)为了使实验更安全、更严密,你认为该实验设计需要如何改进?
①___________________________________________________________________
;
②___________________________________________________________________
。
(3)固体产物中铁元素不可能以+3价形式存在,理由是
_____________________________________________________________________
_____________________________________________________________________
。
现设计实验,探究固体产物中铁元素的存在形式。
①提出合理假设。
假设1:____________________________________________________________;
假设2:____________________________________________________________;
假设3:_____________________________________________________________。
②某学生设计实验探究上述假设,除3%H O 、蒸馏水外,还需要下列试剂中的
2 2
____________________________________________________________________。
限选试剂:浓硫酸、1.0 mol·L-1HNO 、1.0 mol·L-1盐酸、1.0 mol·L-1NaOH溶液、
3
0.1 mol·L-1KI溶液、0.1 mol·L-1CuSO 溶液、20%KSCN溶液。
4
解析 (1)B中溶液变浑浊说明气态产物中有CO ,E中溶液变浑浊说明CO被酸
2
性高锰酸钾溶液氧化为CO ,故D中的现象是溶液褪色或变浅,从而可说明气态
2
产物有CO;另一种气态产物是H O,其验证方法是将A中产生的气体通过盛有
2无水CuSO 的干燥管。(2)从安全角度考虑应在B装置前加一个防倒吸装置,从严
4
密性角度考虑,要在C装置后增加一个检验CO 是否除尽的装置。(3)①由于反应
2
过程中有CO生成,能还原三价的铁,故固体产物中无三价铁,其成分可能有三种
情况:Fe、FeO、Fe和FeO。②探究固体产物中铁元素的存在形式;可以将固体产
物放入足量的0.1 mol·L-1的CuSO 溶液中搅拌使其充分反应,然后过滤洗涤沉
4
淀,再加入足量的1.0 mol·L-1的盐酸,若溶液中有不溶的红色物质,则说明固体
产物中含有Fe(发生反应为Fe+CuSO ===FeSO +Cu),向溶液中加入20%KSCN
4 4
溶液,不变红色,然后再向溶液中滴加双氧水,若变红色,则说明固体产物中含有
FeO。
答案 (1)溶液褪色或变浅 CO CO 盛有无水CuSO 的干燥管
2 4
(2)①在B装置之前加一个防倒吸装置 ②在C装置后增加一个检验二氧化碳是
否除尽的装置(或盛有澄清石灰水的试管)
(3)有还原性气体CO生成,能将三价铁还原,故不可能有三价铁存在
①铁元素的存在形式为Fe单质 铁元素的存在形式为FeO 铁元素的存在形式
为Fe与FeO的混合物
②1.0 mol·L-1盐酸、20%KSCN溶液、0.1 mol·L-1CuSO 溶液
4
2.(全国高考)某小组以CoCl ·6H O、NH Cl、H O 、浓氨水为原料,在活性炭催化下,
2 2 4 2 2
合成了橙黄色晶体X。为确定其组成,进行如下实验。
①氨的测定:精确称取 g X,加适量水溶解,注入如图所示的三颈瓶中,然后
w
逐滴加入足量10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V mL
1
c mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c mol·L-1 NaOH标
1 2
准溶液滴定过剩的HCl,到终点时消耗V mL NaOH溶液。
2
②氯的测定:准确称取样品X,配成溶液后用AgNO 标准溶液滴定,K CrO 溶液
3 2 4
为指示剂,至出现淡红色沉淀不再消失为终点(Ag CrO 为砖红色)。
2 4回答下列问题:
(1)装置中安全管的作用原理是____________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用________式滴定管,可使用的指
示剂为________。
(3)样品中氨的质量分数表达式为________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好,测定结果将
________(填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是________________;滴定终点时,
若溶液中 c(Ag+)=2.0×10-5 mol·L-1,c(CrO)为________ mol·L-1。[已知:
K (Ag CrO )=1.12×10-12]
sp 2 4
(6)经测定,样品 X 中钴、氨和氯的物质的量之比为 1∶6∶3,钴的化合价为
________。 制备X的化学方程式为__________________;X的制备过程中温度
不能过高的原因是__________________。
解析 (3)实验①中,从样品液中蒸出的n(NH )=V ×10-3 L×c mol·L-1-V ×
3 1 1 2
10-3 L×c mol·L-1=(c V -c V )×10-3 mol,样品中氨的质量分数为×100%=
2 1 1 2 2
×100%。
(4)若装置气密性不好,有部分NH 逸出,而不能被HCl吸收,则剩余的HCl的物
3
质的量会增多,消耗 NaOH增多,即 c V 的值增大,由(3)中计算式可知测得
2 2
m(NH )变小,NH 的含量偏低。
3 3
(5)滴定氯的过程中,使用棕色滴定管的原因是防止 AgNO 见光分解,根据
3
Ag CrO (s) 2Ag+(aq)+CrO(aq)及K 的表达式得:c(CrO)== mol·L-1=
2 4 sp
2.8×10-3 mol·L-1。
(6)由n(Co)∶n(NH )∶n(Cl)=1∶6∶3,则知X为[Co(NH ) ]Cl ,故Co的化合价
3 3 6 3
为+3价,制备X的过程中温度不能过高的原因是防止H O 分解,NH 逸出。
2 2 3
答案 (1)当压力过大时,安全管中液面上升,使A瓶中压力稳定
(2)碱 酚酞(或甲基橙)
(3)×100%
(4)偏低
(5)防止AgNO 见光分解 2.8×10-3
3
(6)+3 2CoCl +2NH Cl+10NH +H O ===2[Co(NH ) ]Cl +2H O
2 4 3 2 2 3 6 3 2温度过高,H O 分解,氨气逸出
2 2
考点指导2 化学实验方案的设计与评价
1.实验方案设计的基本原则
2.实验方案设计的基本内容
3.实验方案评价的基本原则
(1)可行性原则
①分析实验方案是否科学可行;
②实验操作是否安全合理;
③实验步骤是否简单方便;
④实验效果是否明显。
(2)绿色化学原则
①实验过程中是否造成环境污染;
②原料是否无毒、安全、易得;
③原料利用率是否较高;④反应速率是否较快。
(3)安全性原则
(4)规范性原则
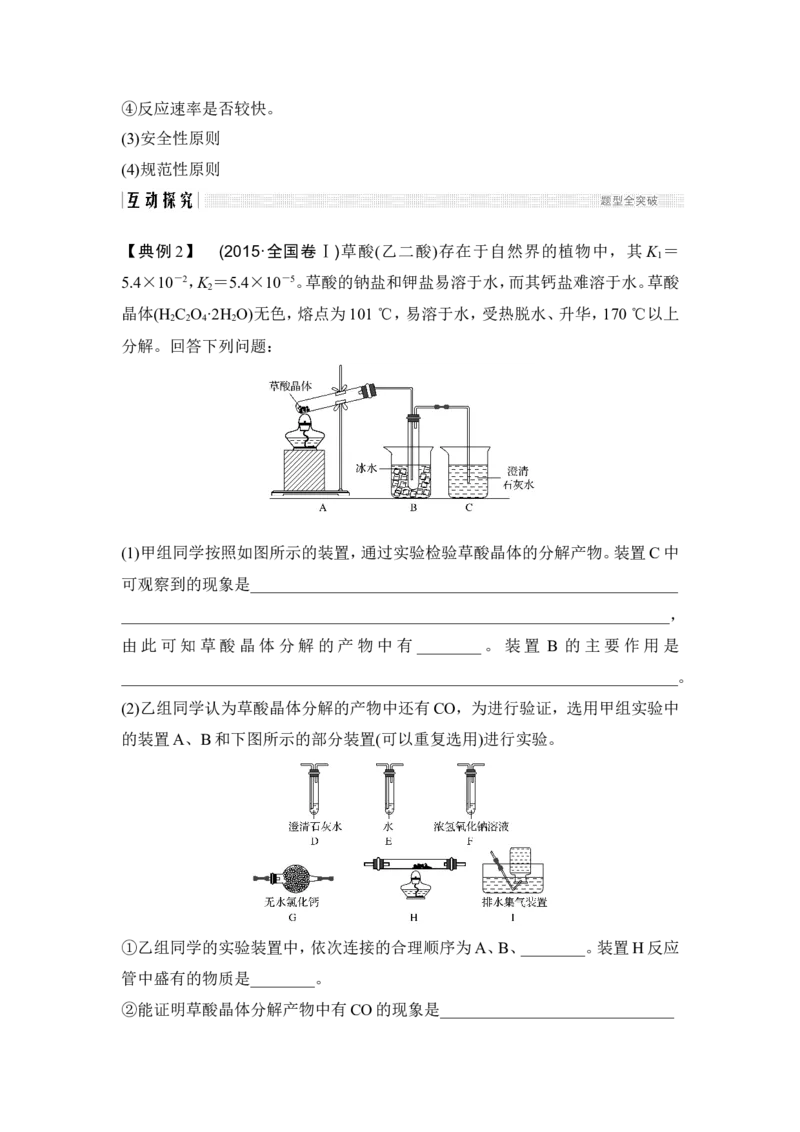
【典例 2】 (2015·全国卷Ⅰ)草酸(乙二酸)存在于自然界的植物中,其 K =
1
5.4×10-2,K =5.4×10-5。草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸
2
晶体(H C O ·2H O)无色,熔点为101 ℃,易溶于水,受热脱水、升华,170 ℃以上
2 2 4 2
分解。回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。装置C中
可观察到的现象是_____________________________________________________
____________________________________________________________________,
由此可知草酸晶体分解的产物中有________。装置 B 的主要作用是
_____________________________________________________________________。
(2)乙组同学认为草酸晶体分解的产物中还有CO,为进行验证,选用甲组实验中
的装置A、B和下图所示的部分装置(可以重复选用)进行实验。
①乙组同学的实验装置中,依次连接的合理顺序为A、B、________。装置H反应
管中盛有的物质是________。
②能证明草酸晶体分解产物中有CO的现象是__________________________________________________________________________________________________
_
_____________________________________________________________________
。
(3)设计实验证明:
①草酸的酸性比碳酸的强______________________________________________。
②草酸为二元酸______________________________________________________。
答案 (1)有气泡逸出,澄清石灰水变浑浊 CO 冷凝(水蒸气、草酸等) ,防止草
2
酸进入装置C反应生成沉淀,干扰CO 的检验
2
(2)①F、D、G、H、D、I CuO(氧化铜)
②前面澄清石灰水无现象,H中黑色粉末变红色,其后的D中澄清石灰水变浑浊
(3)①向盛有少量NaHCO 的试管里滴加草酸溶液,有气泡产生
3
②用NaOH标准溶液滴定草酸,消耗NaOH的物质的量为草酸的2倍
[命题分析]
第(1)问考查CO 的检验方法
2
CO 能使澄清石灰水变浑浊
2
第(1)问考查草酸的物理性质
草酸的熔点为101 ℃,故草酸蒸气遇冷后会冷凝为非气态物质,故装置B的作用
是冷凝。冷凝的目的是防止草酸蒸气对CO 的检验造成干扰。
2
第(2)①问考查实验方案的设计
先分析如何排除CO 对CO检验的干扰:
2
检验CO气体,应先在H装置中进行CO还原CuO的反应,气体进入H装置前需
除去CO中的CO 气体,从H装置中导出的气体需用澄清石灰水检验CO 气体的
2 2
存在。
再设计实验流程:第(2)②考查CO的检验方法
CO还原CuO时,黑色的CuO变成红色的单质Cu,且CO的氧化产物是CO 。
2
故证明草酸晶体分解产物中有CO的现象是H中的黑色粉末变成红色,其后的D
中澄清石灰水变浑浊。
第(3)问考查草酸与碳酸酸性强、二元酸的证明方法
向NaHCO 溶液中加入草酸,若有CO 生成,即可证明草酸的酸性强于碳酸,当1
3 2
mol草酸与NaOH完全中和时,需要消耗2 mol NaOH溶液即可证明草酸为二元
酸。
【对点训练】
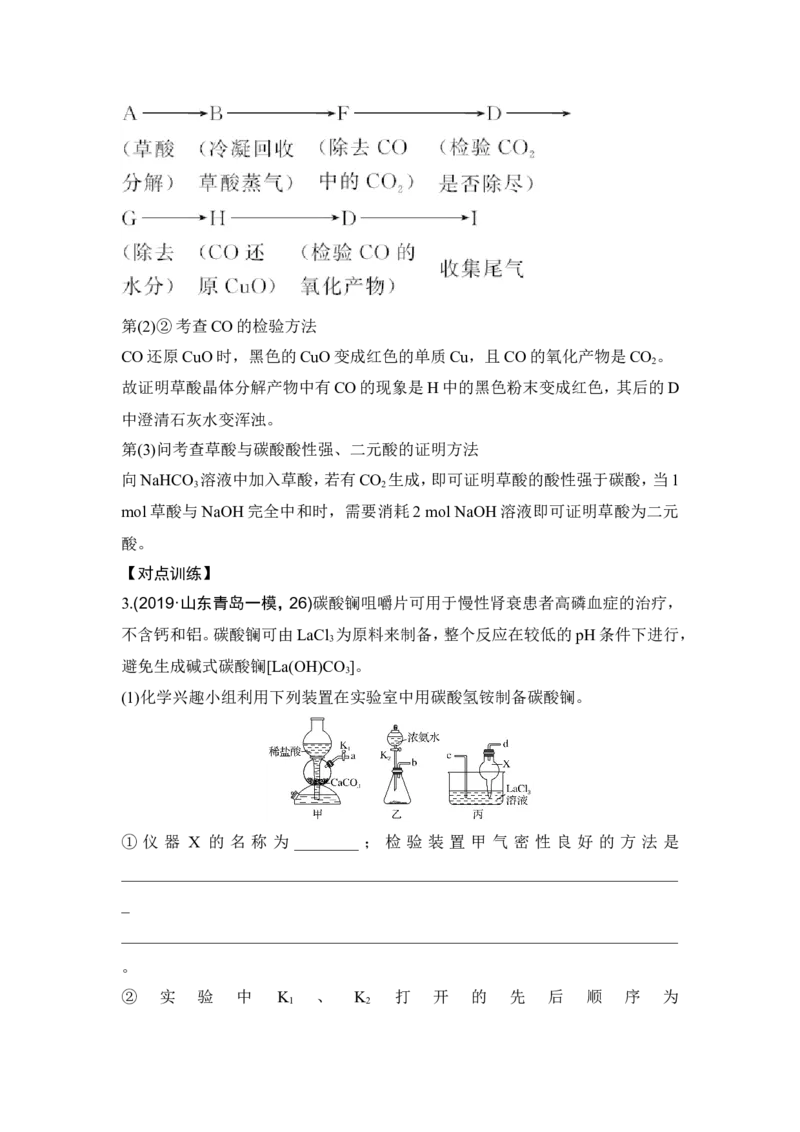
3.(2019·山东青岛一模,26)碳酸镧咀嚼片可用于慢性肾衰患者高磷血症的治疗,
不含钙和铝。碳酸镧可由LaCl 为原料来制备,整个反应在较低的pH条件下进行,
3
避免生成碱式碳酸镧[La(OH)CO ]。
3
(1)化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
① 仪 器 X 的 名 称 为 ________ ; 检 验 装 置 甲 气 密 性 良 好 的 方 法 是
_____________________________________________________________________
_
_____________________________________________________________________
。
② 实 验 中 K 、 K 打 开 的 先 后 顺 序 为
1 2_____________________________________________________________________;
为 保 证 碳 酸 镧 的 纯 度 , 实 验 过 程 中 需 要 注 意 的 问 题 有
____________________________________________________________________。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,过程中会发生两个平行反
应,其离子方程式为___________________________________________________
和__________________________________________________________________。
②选择碳酸氢钠溶液制备碳酸镧的优点是_________________________________
(任写一条)。
(3)碳酸镧(摩尔质量为458 g·mol-1)质量分数的测定:准确称取15.0 g产品试样,
溶于10.0 mL稀盐酸中,加入10 mL NH NH Cl缓冲溶液,加入0.2 g紫脲酸铵混
3 4
合指示剂,用0.5 mol·L-1 EDTA(Na H Y)标准溶液滴定至呈蓝紫色(La3++
2 2
H Y2-===LaY-+2H+),消耗EDTA溶液60.00 mL。则产品中碳酸镧的质量分数
2
=________。
w
解析 (1)①仪器X的名称为球形干燥管;检验装置甲气密性良好的方法是关闭
活塞K ,向球形漏斗中加水至漏斗内外形成液面差,一段时间后,液面差保持不
1
变,说明气密性良好。
②氨气是极易溶于水的气体,先通氨气,在碱性条件下再通入二氧化碳,溶解的
量较大,故实验中先打开K 再打开K ;为保证碳酸镧的纯度,实验过程中需要控
2 1
制氨气(或CO )通入量。
2
(2)① 碳酸氢钠分别与 La3+、H+反应,反应的离子方程式为 2La3++
3HCO===La (CO ) ↓+3H+和H++HCO===CO ↑+H O。
2 3 3 2 2
②选择碳酸氢钠溶液制备碳酸镧的优点是碳酸氢钠碱性相对较弱,可防止生成碱
式碳酸镧[La(OH)CO ]。
3
(3)滴定时消耗EDTA的物质的量为60.00×10-3L×0.5 mol·L-1=0.03 mol,根据
反应 La3++H Y2-===LaY-+2H+可知,La (CO ) 的物质的量为 0.015 mol 即
2 2 3 3
mol,产品中碳酸镧的质量分数 =×100%=45.8%。
w
答案 (1)①球形干燥管 关闭活塞K ,向球形漏斗中加水至漏斗内外形成液面
1差,一段时间后,液面差保持不变,说明气密性良好
②先打开K ,再打开K 控制氨气(或CO )通入量
2 1 2
(2)①2La3++3HCO===La (CO ) ↓+3H+ H++HCO===CO ↑+H O
2 3 3 2 2
②碳酸氢钠碱性相对较弱,可防止生成碱式碳酸镧
(3)45.8%
4.(2018·课标全国Ⅰ,26)醋酸亚铬[(CH COO) Cr·2H O]为砖红色晶体,难溶于冷
3 2 2
水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中
利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可
制得醋酸亚铬。实验装置如图所示。回答下列问题:
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是
_____________________________________________________________________
。
仪器a的名称是________。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开
K 、K ,关闭K 。
1 2 3
①c 中 溶 液 由 绿 色 逐 渐 变 为 亮 蓝 色 , 该 反 应 的 离 子 方 程 式 为
_____________________________________________________________________。
② 同 时 c 中 有 气 体 产 生 , 该 气 体 的 作 用 是
_____________________________________________________________________
_____________________________________________________________________
。
(3) 打 开 K , 关 闭 K 和 K 。 c 中 亮 蓝 色 溶 液 流 入 d , 其 原 因 是
3 1 2
____________________________________________________________________;
d中析出砖红色沉淀。为使沉淀充分析出并分离,需采用的操作是________、
________、洗涤、干燥。
(4)指出装置d可能存在的缺点_____________________________________________________________________________________________________________。
解析 (1)审题时抓住醋酸亚铬“在气体分析中用作氧气吸收剂”,这暗示醋酸亚
铬具有强还原性,易被氧气氧化,故该实验中使用的蒸馏水必须去除溶解氧。
(2)①依题意可知,c中溶液由绿色逐渐变为亮蓝色,主要是由于锌与铬离子反应
生成亚铬离子和锌离子,即Zn+2Cr3+===Zn2++2Cr2+。②c中产生的气体为氢
气,该气体主要用于排尽装置内的空气,避免O 氧化Cr2+。(3)c中有氢气产生,打
2
开K ,关闭K 和K 后,c中压强大于外界压强,从而将c中溶液压入醋酸钠溶液
3 1 2
中。析出并分离产品的操作是冷却、过滤、洗涤、干燥。(4)观察d装置,可发现其与
空气相通,这会导致生成的醋酸亚铬被O 氧化。
2
答案 (1)去除水中溶解氧 分液漏斗
(2)①Zn+2Cr3+===Zn2++2Cr2+
②排除c中空气
(3)c中产生H 使压强大于大气压 (冰浴)冷却 过滤
2
(4)敞开体系,可能使醋酸亚铬与空气接触
【课堂小结】
定量型实验题的解题模板