文档内容
2025新教材化学高考第一轮
专题十七 实验方案的设计和评价
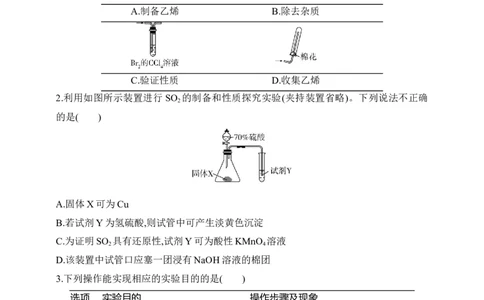
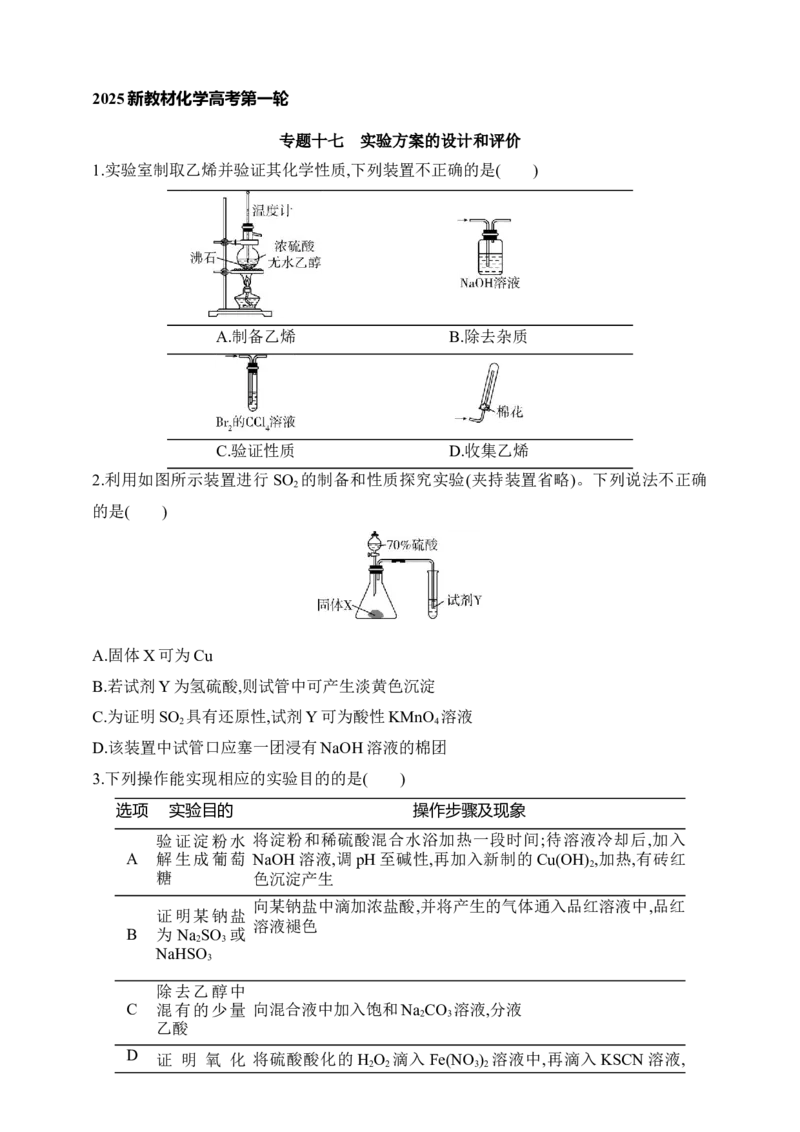
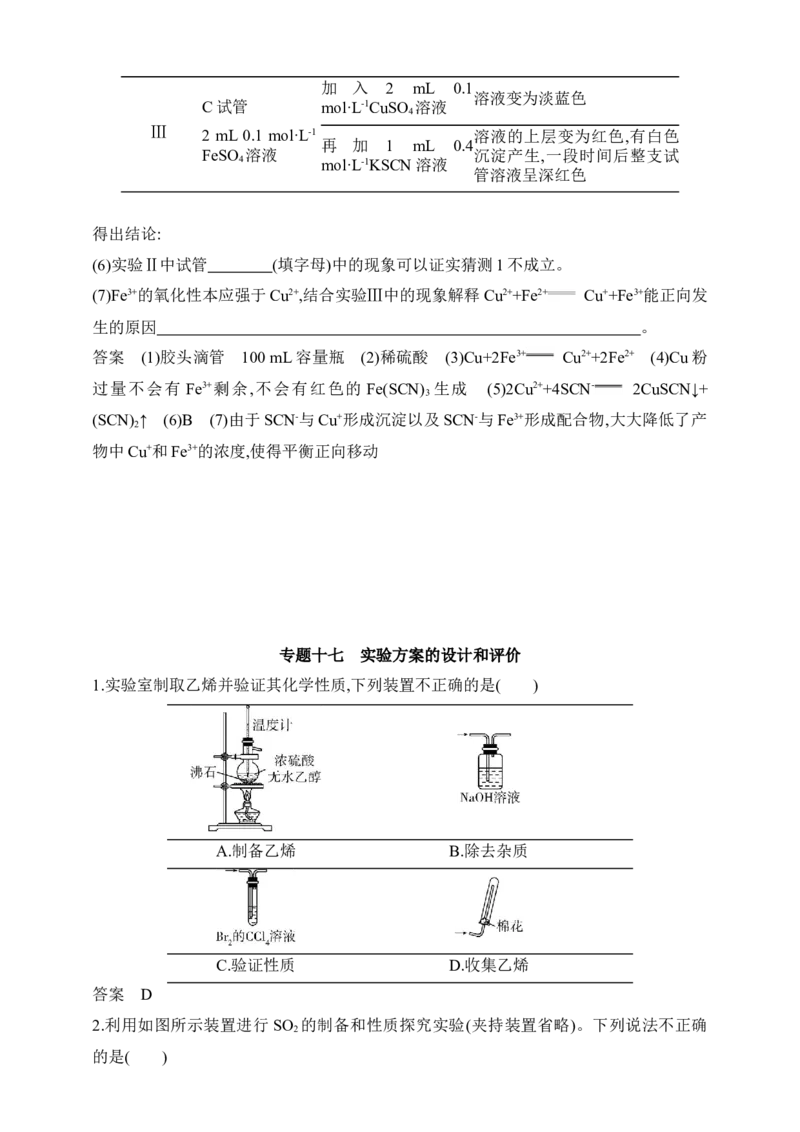
1.实验室制取乙烯并验证其化学性质,下列装置不正确的是( )
A.制备乙烯 B.除去杂质
C.验证性质 D.收集乙烯
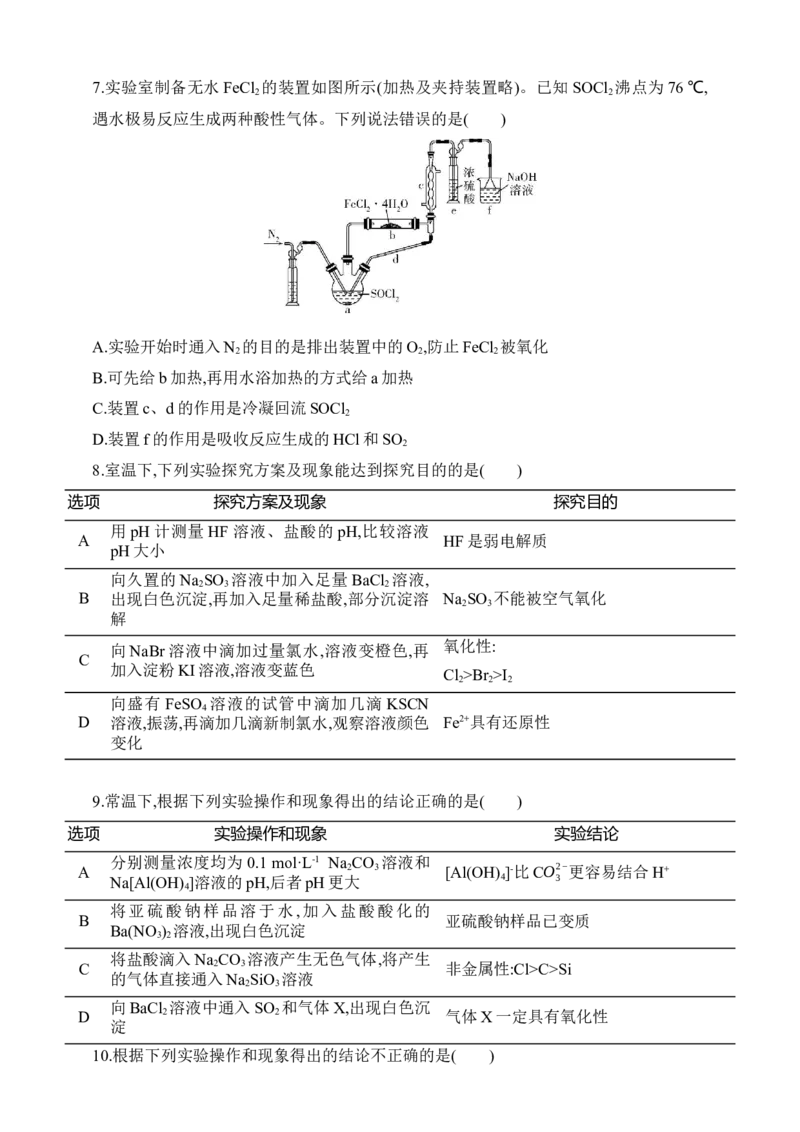
2.利用如图所示装置进行 SO 的制备和性质探究实验(夹持装置省略)。下列说法不正确
2
的是( )
A.固体X可为Cu
B.若试剂Y为氢硫酸,则试管中可产生淡黄色沉淀
C.为证明SO 具有还原性,试剂Y可为酸性KMnO 溶液
2 4
D.该装置中试管口应塞一团浸有NaOH溶液的棉团
3.下列操作能实现相应的实验目的的是( )
选项 实验目的 操作步骤及现象
验证淀粉水 将淀粉和稀硫酸混合水浴加热一段时间;待溶液冷却后,加入
A 解生成葡萄 NaOH溶液,调pH至碱性,再加入新制的Cu(OH) ,加热,有砖红
2
糖 色沉淀产生
向某钠盐中滴加浓盐酸,并将产生的气体通入品红溶液中,品红
证明某钠盐
溶液褪色
B 为 Na SO 或
2 3
NaHSO
3
除去乙醇中
C 混有的少量 向混合液中加入饱和Na CO 溶液,分液
2 3
乙酸
D 证 明 氧 化 将硫酸酸化的 H O 滴入Fe(NO ) 溶液中,再滴入 KSCN溶液,
2 2 3 2性:H O >Fe3+ 溶液变红
2 2
4.实验探究是化学学习的方法之一。下列实验设计、现象和实验结论都正确的是( )
实验设计 现象 实验结论
加热后坩埚内固体为
在坩埚中加入 16.4 g CaC O ·2H O,称取坩埚中剩余物质质量
A 2 4 2 CaO 和 CaC O 的混合
加热一段时间,在干燥器中冷却 为12.8 g 2 4
物
滴加稀硝酸时无明显现象,
向溶液X中先滴加稀硝酸,然后再滴 溶 液 X 中 含 SO2−或
B 滴加 BaCl 溶液时产生白 4
加BaCl 溶液 2 Ag+
2 色沉淀
分别用蒸馏水、1.0 mol·L-1 AlCl 溶喷洒 AlCl 溶液的纸张老
C 3 3 Cl-能促进纸张的老化
液喷洒甲、乙两张白纸,静置、干燥 化明显
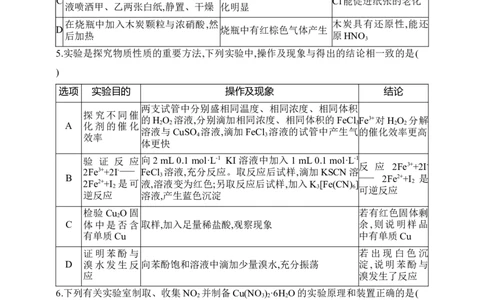
在烧瓶中加入木炭颗粒与浓硝酸,然 木炭具有还原性,能还
D 烧瓶中有红棕色气体产生
后加热 原HNO
3
5.实验是探究物质性质的重要方法,下列实验中,操作及现象与得出的结论相一致的是(
)
选项 实验目的 操作及现象 结论
两支试管中分别盛相同温度、相同浓度、相同体积
探究不同催
的H O 溶液,分别滴加相同浓度、相同体积的FeCl Fe3+对H O 分解
A 化剂的催化 2 2 3 2 2
溶液与CuSO 溶液,滴加FeCl 溶液的试管中产生气的催化效率更高
效率 4 3
体更快
验 证 反 应向2 mL 0.1 mol·L-1 KI溶液中加入1 mL 0.1 mol·L-1
反 应 2Fe3++2I-
2Fe3++2I- FeCl 溶液,充分反应。取反应后试样,滴加KSCN溶
B 3 2Fe2++I 是
2Fe2++I 是可液,溶液变为红色;另取反应后试样,加入K [Fe(CN) ] 2
2 3 6 可逆反应
逆反应 溶液,产生蓝色沉淀
检验Cu O固 若有红色固体剩
2
C 体中是否含取样,加入足量稀盐酸,观察现象 余,则说明样品
有单质Cu 中有单质Cu
证明苯酚与 若出现白色沉
D 溴水发生反向苯酚饱和溶液中滴加少量溴水,充分振荡 淀,说明苯酚与
应 溴发生了反应
6.下列有关实验室制取、收集 NO 并制备Cu(NO ) ·6H O的实验原理和装置正确的是(
2 3 2 2
)
A.用装置甲制取NO B.用装置丁收集NO
2 2
C.用装置丙吸收NO D.用装置乙蒸干溶液获得Cu(NO ) ·6H O
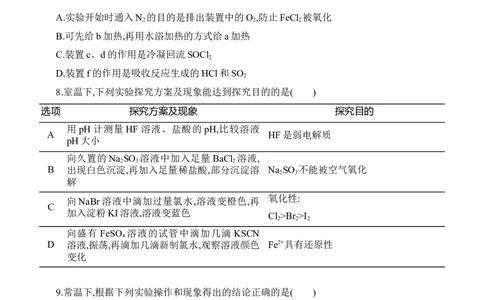
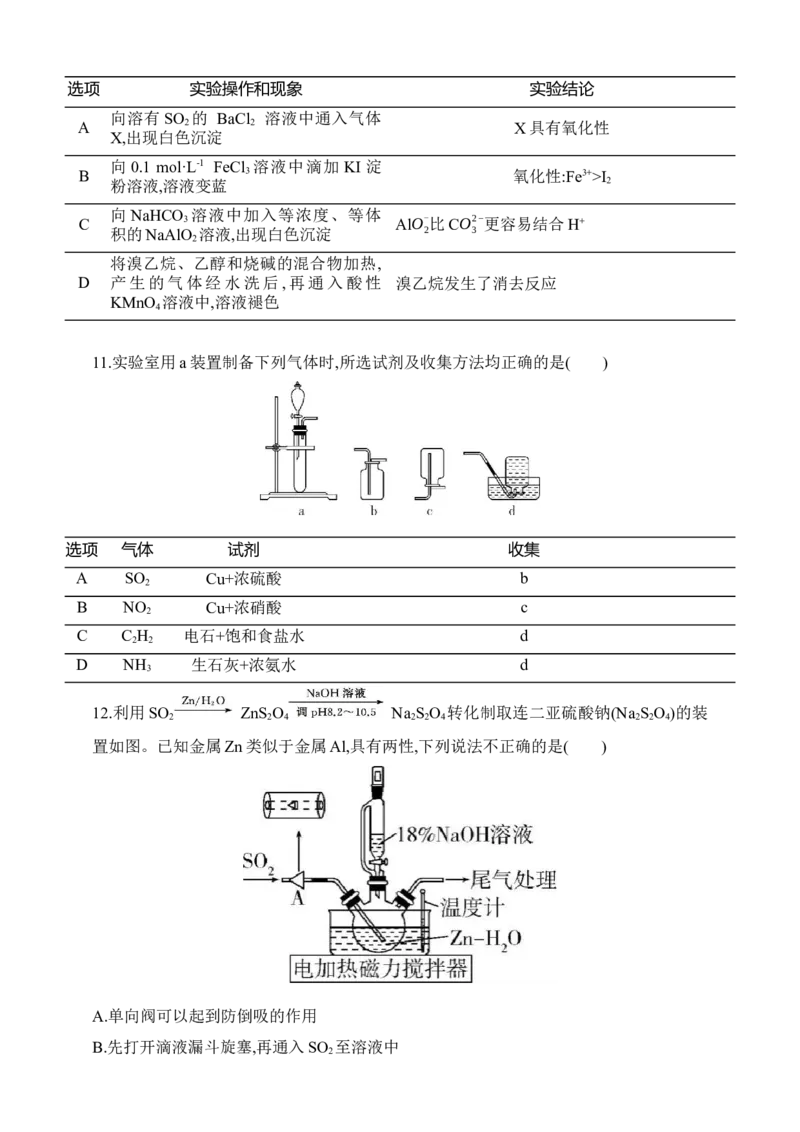
2 3 2 27.实验室制备无水FeCl 的装置如图所示(加热及夹持装置略)。已知SOCl 沸点为76 ℃,
2 2
遇水极易反应生成两种酸性气体。下列说法错误的是( )
A.实验开始时通入N 的目的是排出装置中的O ,防止FeCl 被氧化
2 2 2
B.可先给b加热,再用水浴加热的方式给a加热
C.装置c、d的作用是冷凝回流SOCl
2
D.装置f的作用是吸收反应生成的HCl和SO
2
8.室温下,下列实验探究方案及现象能达到探究目的的是( )
选项 探究方案及现象 探究目的
用pH计测量 HF溶液、盐酸的 pH,比较溶液
A HF是弱电解质
pH大小
向久置的Na SO 溶液中加入足量BaCl 溶液,
2 3 2
B 出现白色沉淀,再加入足量稀盐酸,部分沉淀溶 Na SO 不能被空气氧化
2 3
解
向NaBr溶液中滴加过量氯水,溶液变橙色,再
氧化性:
C
加入淀粉KI溶液,溶液变蓝色
Cl >Br >I
2 2 2
向盛有 FeSO 溶液的试管中滴加几滴 KSCN
4
D 溶液,振荡,再滴加几滴新制氯水,观察溶液颜色 Fe2+具有还原性
变化
9.常温下,根据下列实验操作和现象得出的结论正确的是( )
选项 实验操作和现象 实验结论
分别测量浓度均为 0.1 mol·L-1 Na CO 溶液和
A 2 3 [Al(OH) ]-比CO2−更容易结合H+
Na[Al(OH) ]溶液的pH,后者pH更大 4 3
4
将亚硫酸钠样品溶于水,加入盐酸酸化的
B 亚硫酸钠样品已变质
Ba(NO ) 溶液,出现白色沉淀
3 2
将盐酸滴入Na CO 溶液产生无色气体,将产生
C 2 3 非金属性:Cl>C>Si
的气体直接通入Na SiO 溶液
2 3
向BaCl 溶液中通入SO 和气体X,出现白色沉
D 2 2 气体X一定具有氧化性
淀
10.根据下列实验操作和现象得出的结论不正确的是( )选项 实验操作和现象 实验结论
向溶有 SO 的 BaCl 溶液中通入气体
A 2 2 X具有氧化性
X,出现白色沉淀
向 0.1 mol·L-1 FeCl 溶液中滴加 KI 淀
B 3 氧化性:Fe3+>I
粉溶液,溶液变蓝 2
向 NaHCO 溶液中加入等浓度、等体
C 3 AlO-比CO2−更容易结合H+
积的NaAlO 溶液,出现白色沉淀 2 3
2
将溴乙烷、乙醇和烧碱的混合物加热,
D 产生的气体经水洗后,再通入酸性 溴乙烷发生了消去反应
KMnO 溶液中,溶液褪色
4
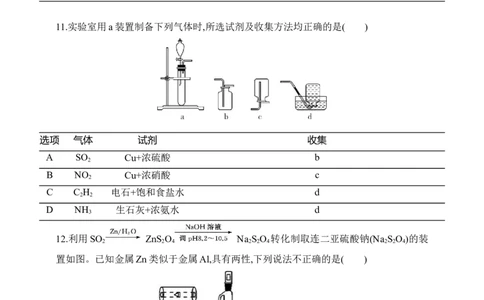
11.实验室用a装置制备下列气体时,所选试剂及收集方法均正确的是( )
选项 气体 试剂 收集
A SO Cu+浓硫酸 b
2
B NO Cu+浓硝酸 c
2
C C H 电石+饱和食盐水 d
2 2
D NH 生石灰+浓氨水 d
3
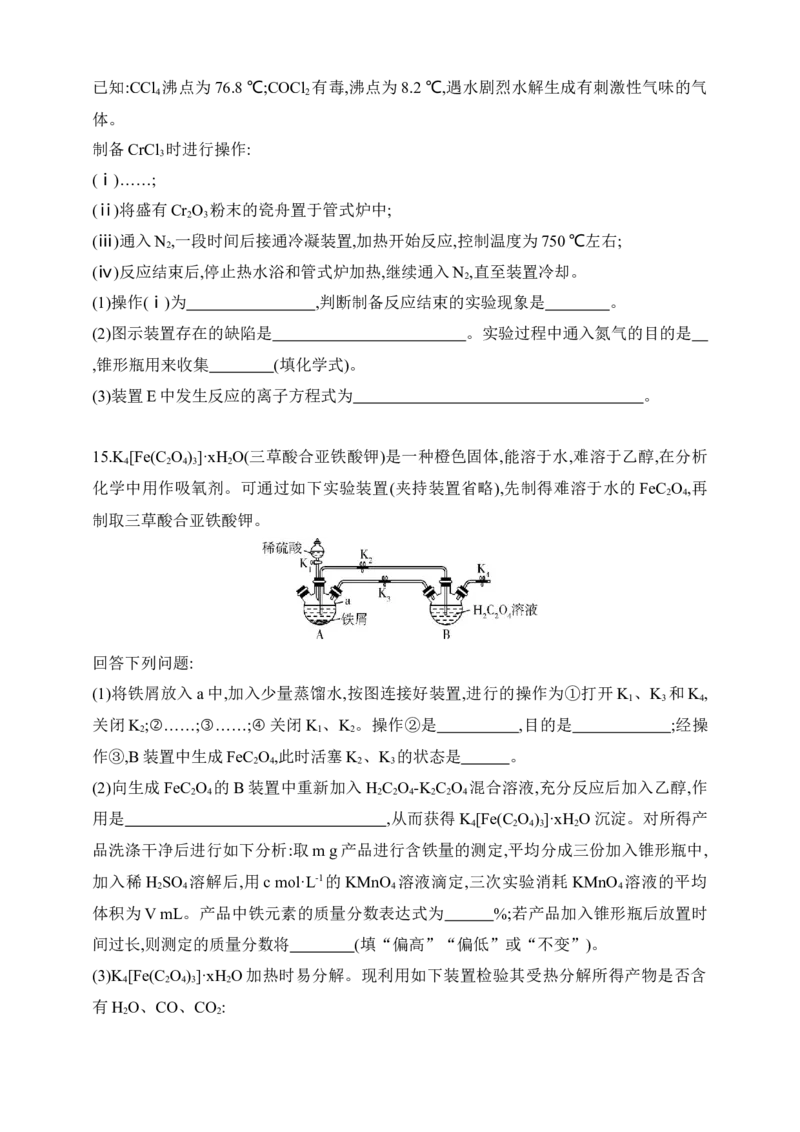
12.利用SO ZnS O Na S O 转化制取连二亚硫酸钠(Na S O )的装
2 2 4 2 2 4 2 2 4
置如图。已知金属Zn类似于金属Al,具有两性,下列说法不正确的是( )
A.单向阀可以起到防倒吸的作用
B.先打开滴液漏斗旋塞,再通入SO 至溶液中
2C.NaOH溶液不宜加入过多的原因是防止产品中混有含锌元素的杂质
D.该实验适合使用NaOH溶液进行尾气处理
13.探究硫及其化合物的性质,下列方案设计、现象和结论中有不正确的是( )
实验方案 现象 结论
产生淡黄色
在过硫化钠
沉淀和臭鸡
A (Na S ) 中 加 发生歧化反应:Na S +2HCl 2NaCl+H S↑+S↓
2 2 蛋气味的气 2 2 2
入稀盐酸
体
已 知
溶液先变为
[Fe(SO ) ]3+
2 6 红棕色,过Fe3+与SO 络合反应速率比氧化还原反应速率快,但氧化还原反应的
B 呈红棕色,将 2
一段时间又平衡常数更大
SO 气体通入
2 变成浅绿色
FeCl 溶液中
3
实验方案 现象 结论
燃着的镁条
插 入 盛 有 剧烈燃烧,
SO 的集气瓶 集气瓶口有
2
中。冷却后, 淡黄色固体
往集气瓶中 附着,集气
C 加入适量稀 瓶底有白色镁能在SO 中燃烧:2Mg+SO 2MgO+S
2 2
盐酸,静置,取 固体生成。
少量上层清 试管中没有
液于试管中, 产生黑色沉
滴 加 少 量 淀
CuSO 溶液
4
将电石与饱
和食盐水反
应产生的气
探究电石与
D 体通入酸性若酸性高锰酸钾溶液褪色,说明电石与水反应生成了乙炔
水的反应
高锰酸钾溶
液,观察现
象
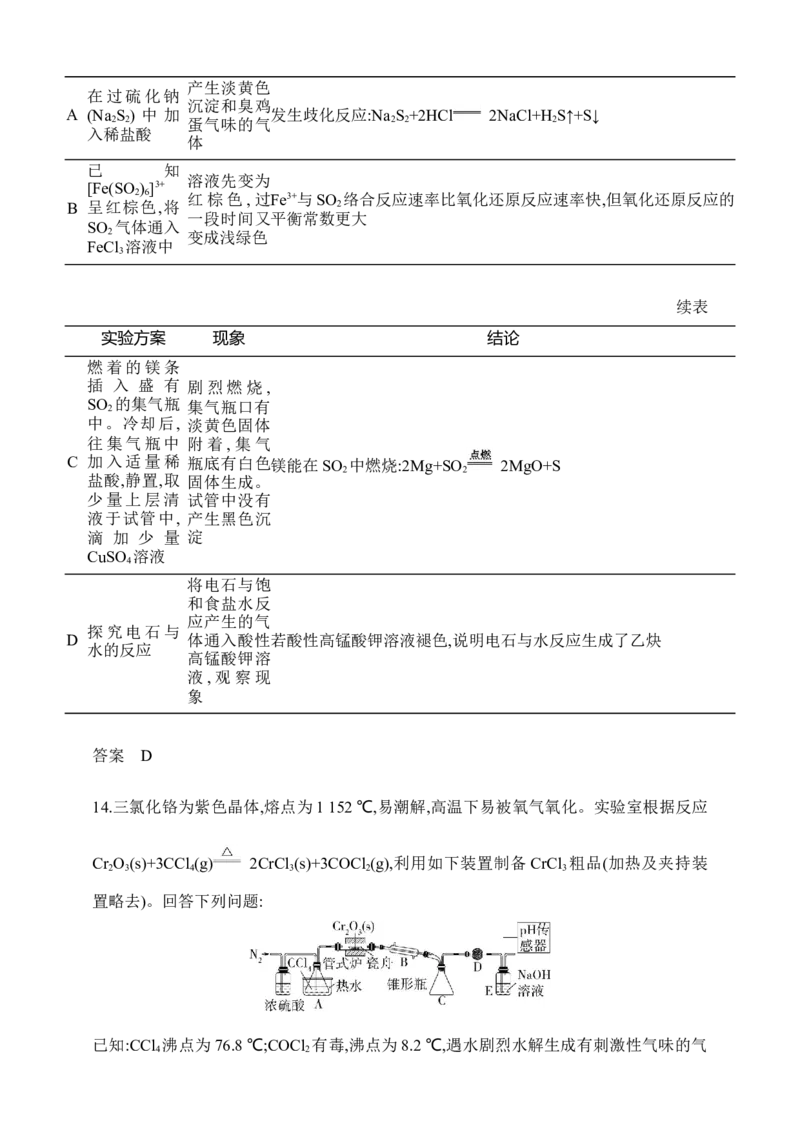
14.三氯化铬为紫色晶体,熔点为1 152 ℃,易潮解,高温下易被氧气氧化。实验室根据反应
Cr O (s)+3CCl (g) 2CrCl (s)+3COCl (g),利用如下装置制备 CrCl 粗品(加热及夹持装
2 3 4 3 2 3
置略去)。回答下列问题:已知:CCl 沸点为76.8 ℃;COCl 有毒,沸点为8.2 ℃,遇水剧烈水解生成有刺激性气味的气
4 2
体。
制备CrCl 时进行操作:
3
(ⅰ)……;
(ⅱ)将盛有Cr O 粉末的瓷舟置于管式炉中;
2 3
(ⅲ)通入N ,一段时间后接通冷凝装置,加热开始反应,控制温度为750 ℃左右;
2
(ⅳ)反应结束后,停止热水浴和管式炉加热,继续通入N ,直至装置冷却。
2
(1)操作(ⅰ)为 ,判断制备反应结束的实验现象是 。
(2)图示装置存在的缺陷是 。实验过程中通入氮气的目的是
,锥形瓶用来收集 (填化学式)。
(3)装置E中发生反应的离子方程式为 。
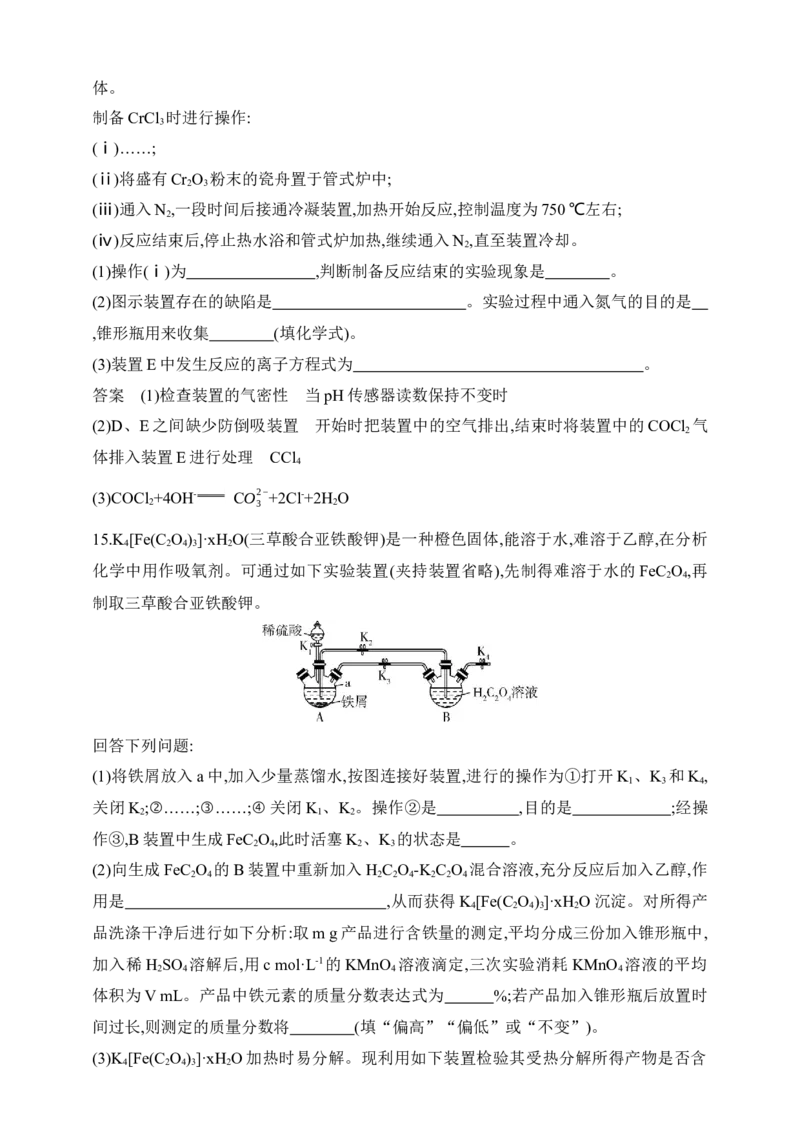
15.K [Fe(C O ) ]·xH O(三草酸合亚铁酸钾)是一种橙色固体,能溶于水,难溶于乙醇,在分析
4 2 4 3 2
化学中用作吸氧剂。可通过如下实验装置(夹持装置省略),先制得难溶于水的 FeC O ,再
2 4
制取三草酸合亚铁酸钾。
回答下列问题:
(1)将铁屑放入a中,加入少量蒸馏水,按图连接好装置,进行的操作为①打开K 、K 和K ,
1 3 4
关闭K ;②……;③……;④关闭K 、K 。操作②是 ,目的是 ;经操
2 1 2
作③,B装置中生成FeC O ,此时活塞K 、K 的状态是 。
2 4 2 3
(2)向生成FeC O 的B装置中重新加入H C O -K C O 混合溶液,充分反应后加入乙醇,作
2 4 2 2 4 2 2 4
用是 ,从而获得K [Fe(C O ) ]·xH O沉淀。对所得产
4 2 4 3 2
品洗涤干净后进行如下分析:取m g产品进行含铁量的测定,平均分成三份加入锥形瓶中,
加入稀H SO 溶解后,用c mol·L-1的KMnO 溶液滴定,三次实验消耗 KMnO 溶液的平均
2 4 4 4
体积为V mL。产品中铁元素的质量分数表达式为 %;若产品加入锥形瓶后放置时
间过长,则测定的质量分数将 (填“偏高”“偏低”或“不变”)。
(3)K [Fe(C O ) ]·xH O加热时易分解。现利用如下装置检验其受热分解所得产物是否含
4 2 4 3 2
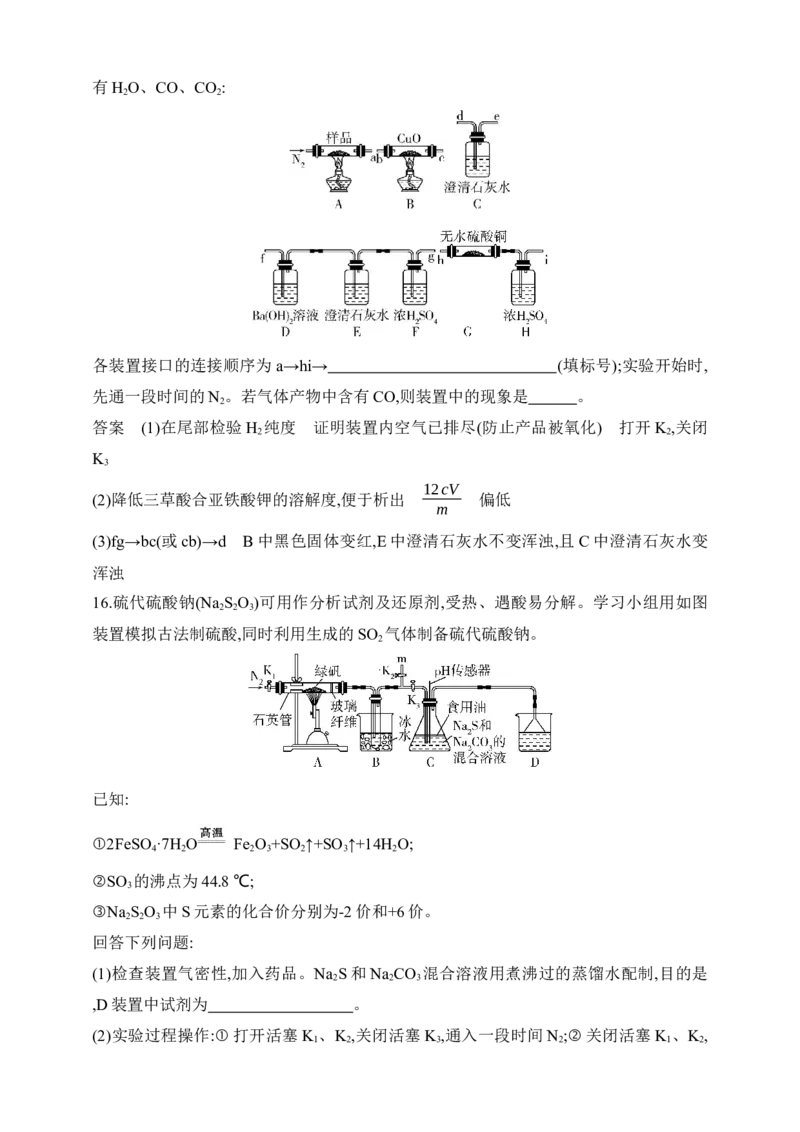
有H O、CO、CO :
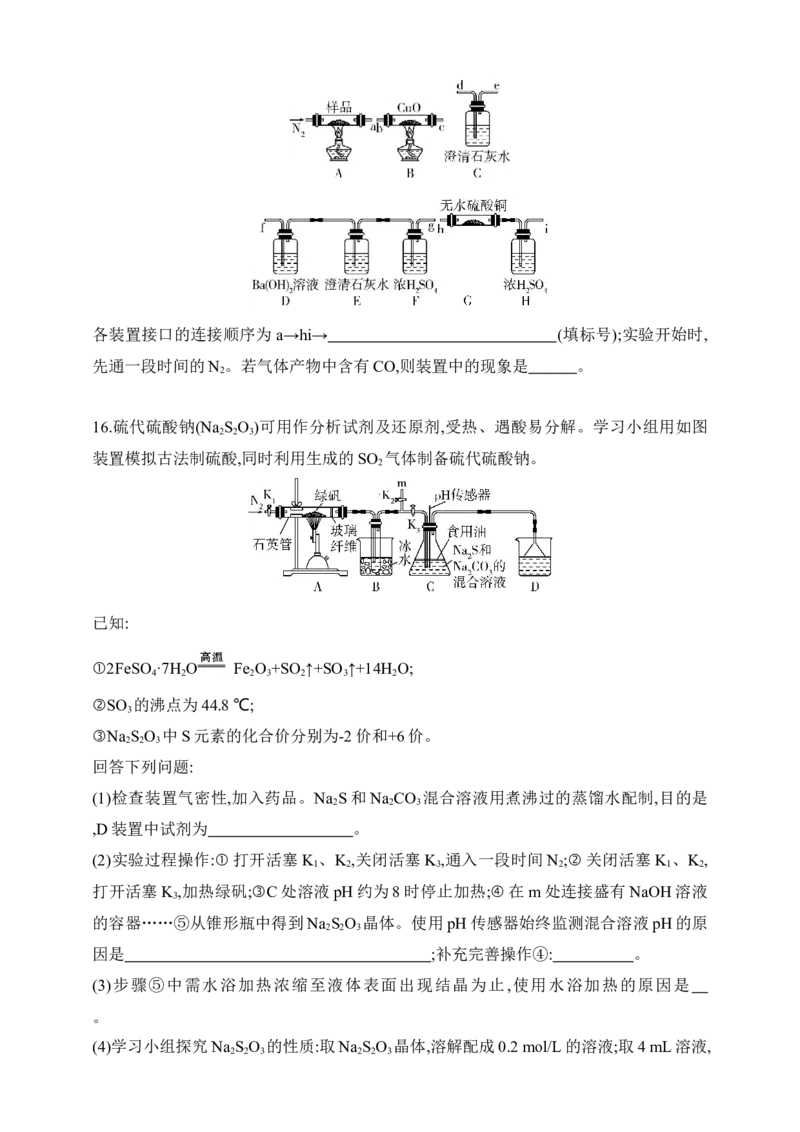
2 2各装置接口的连接顺序为a→hi→ (填标号);实验开始时,
先通一段时间的N 。若气体产物中含有CO,则装置中的现象是 。
2
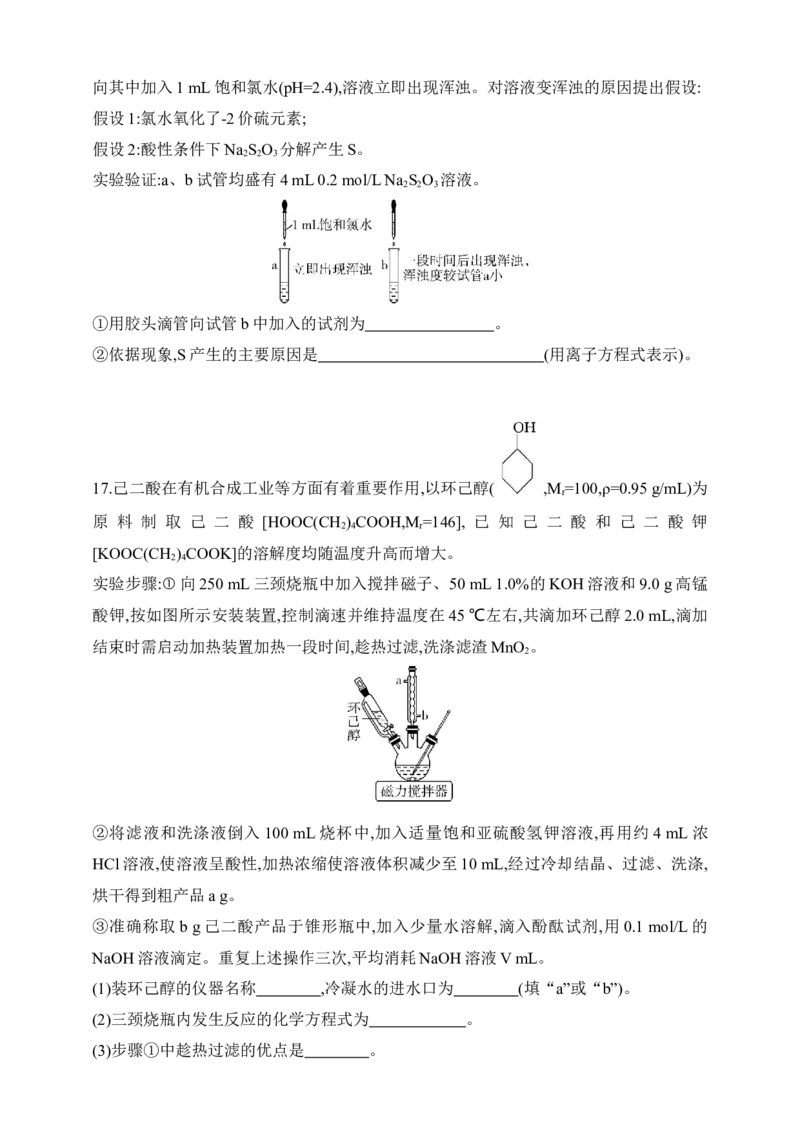
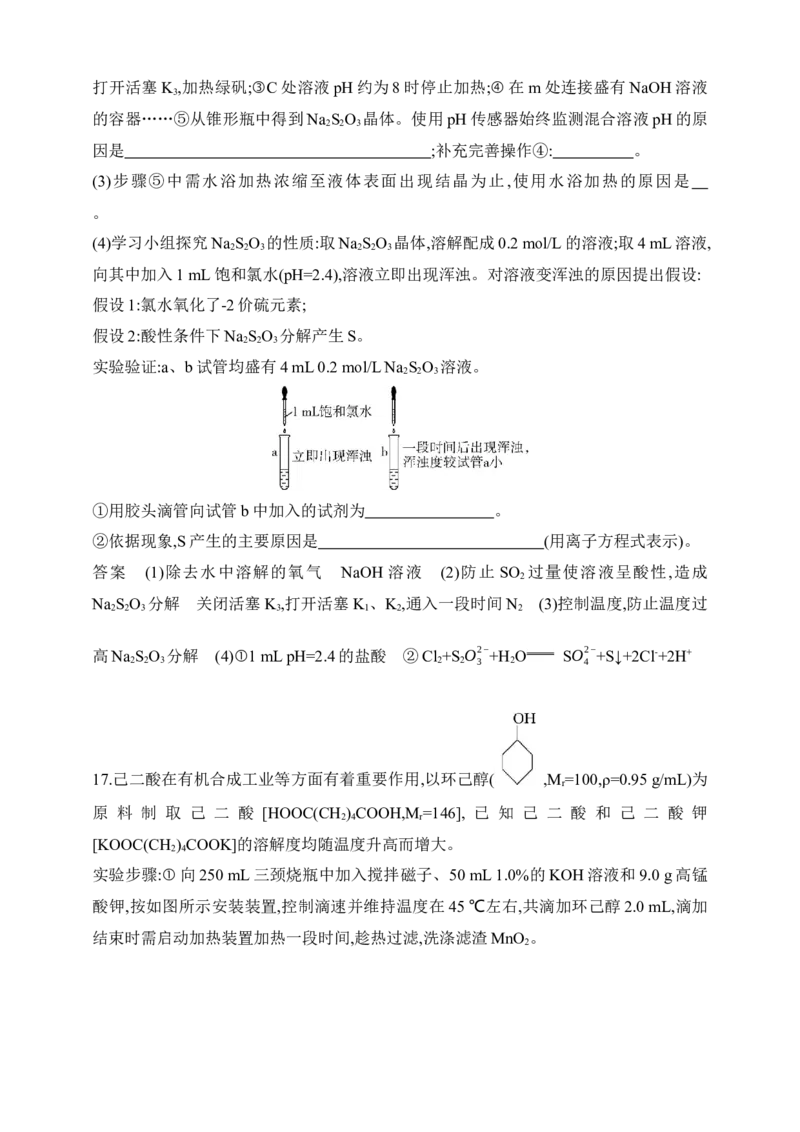
16.硫代硫酸钠(Na S O )可用作分析试剂及还原剂,受热、遇酸易分解。学习小组用如图
2 2 3
装置模拟古法制硫酸,同时利用生成的SO 气体制备硫代硫酸钠。
2
已知:
①2FeSO ·7H O Fe O +SO ↑+SO ↑+14H O;
4 2 2 3 2 3 2
②SO 的沸点为44.8 ℃;
3
③Na S O 中S元素的化合价分别为-2价和+6价。
2 2 3
回答下列问题:
(1)检查装置气密性,加入药品。Na S和Na CO 混合溶液用煮沸过的蒸馏水配制,目的是
2 2 3
,D装置中试剂为 。
(2)实验过程操作:①打开活塞K 、K ,关闭活塞K ,通入一段时间N ;②关闭活塞K 、K ,
1 2 3 2 1 2
打开活塞K ,加热绿矾;③C处溶液pH约为8时停止加热;④在m处连接盛有NaOH溶液
3
的容器……⑤从锥形瓶中得到Na S O 晶体。使用pH传感器始终监测混合溶液pH的原
2 2 3
因是 ;补充完善操作④: 。
(3)步骤⑤中需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是
。
(4)学习小组探究Na S O 的性质:取Na S O 晶体,溶解配成0.2 mol/L的溶液;取4 mL溶液,
2 2 3 2 2 3向其中加入1 mL饱和氯水(pH=2.4),溶液立即出现浑浊。对溶液变浑浊的原因提出假设:
假设1:氯水氧化了-2价硫元素;
假设2:酸性条件下Na S O 分解产生S。
2 2 3
实验验证:a、b试管均盛有4 mL 0.2 mol/L Na S O 溶液。
2 2 3
①用胶头滴管向试管b中加入的试剂为 。
②依据现象,S产生的主要原因是 (用离子方程式表示)。
17.己二酸在有机合成工业等方面有着重要作用,以环己醇( ,M=100,ρ=0.95 g/mL)为
r
原 料 制 取 己 二 酸 [HOOC(CH ) COOH,M=146], 已 知 己 二 酸 和 己 二 酸 钾
2 4 r
[KOOC(CH ) COOK]的溶解度均随温度升高而增大。
2 4
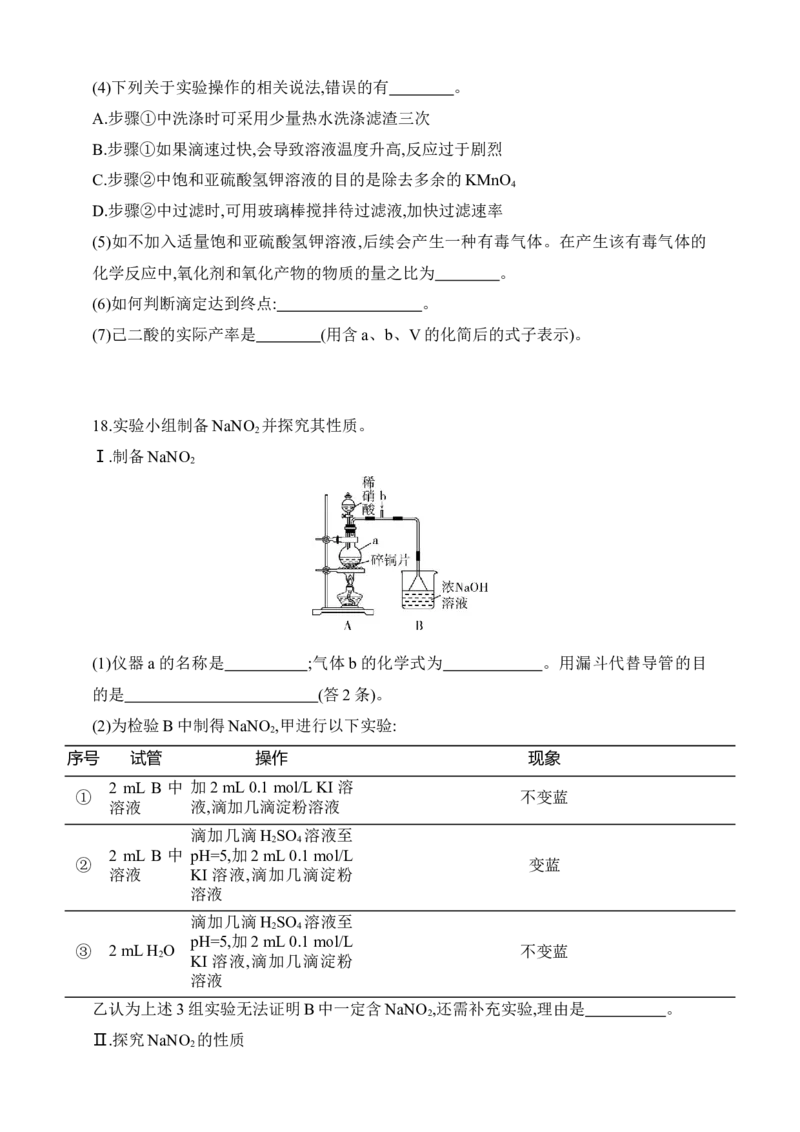
实验步骤:①向250 mL三颈烧瓶中加入搅拌磁子、50 mL 1.0%的KOH溶液和9.0 g高锰
酸钾,按如图所示安装装置,控制滴速并维持温度在45 ℃左右,共滴加环己醇2.0 mL,滴加
结束时需启动加热装置加热一段时间,趁热过滤,洗涤滤渣MnO 。
2
②将滤液和洗涤液倒入100 mL 烧杯中,加入适量饱和亚硫酸氢钾溶液,再用约4 mL 浓
HCl溶液,使溶液呈酸性,加热浓缩使溶液体积减少至10 mL,经过冷却结晶、过滤、洗涤,
烘干得到粗产品a g。
③准确称取b g己二酸产品于锥形瓶中,加入少量水溶解,滴入酚酞试剂,用0.1 mol/L的
NaOH溶液滴定。重复上述操作三次,平均消耗NaOH溶液V mL。
(1)装环己醇的仪器名称 ,冷凝水的进水口为 (填“a”或“b”)。
(2)三颈烧瓶内发生反应的化学方程式为 。
(3)步骤①中趁热过滤的优点是 。(4)下列关于实验操作的相关说法,错误的有 。
A.步骤①中洗涤时可采用少量热水洗涤滤渣三次
B.步骤①如果滴速过快,会导致溶液温度升高,反应过于剧烈
C.步骤②中饱和亚硫酸氢钾溶液的目的是除去多余的KMnO
4
D.步骤②中过滤时,可用玻璃棒搅拌待过滤液,加快过滤速率
(5)如不加入适量饱和亚硫酸氢钾溶液,后续会产生一种有毒气体。在产生该有毒气体的
化学反应中,氧化剂和氧化产物的物质的量之比为 。
(6)如何判断滴定达到终点: 。
(7)己二酸的实际产率是 (用含a、b、V的化简后的式子表示)。
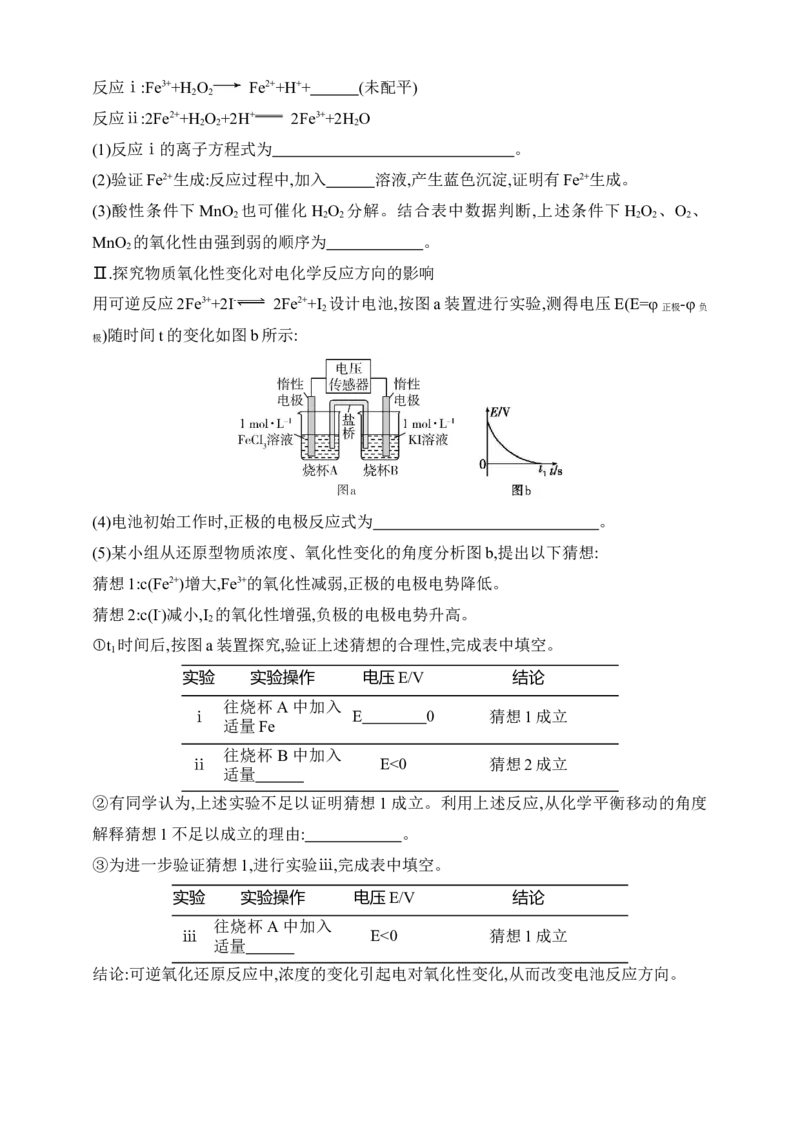
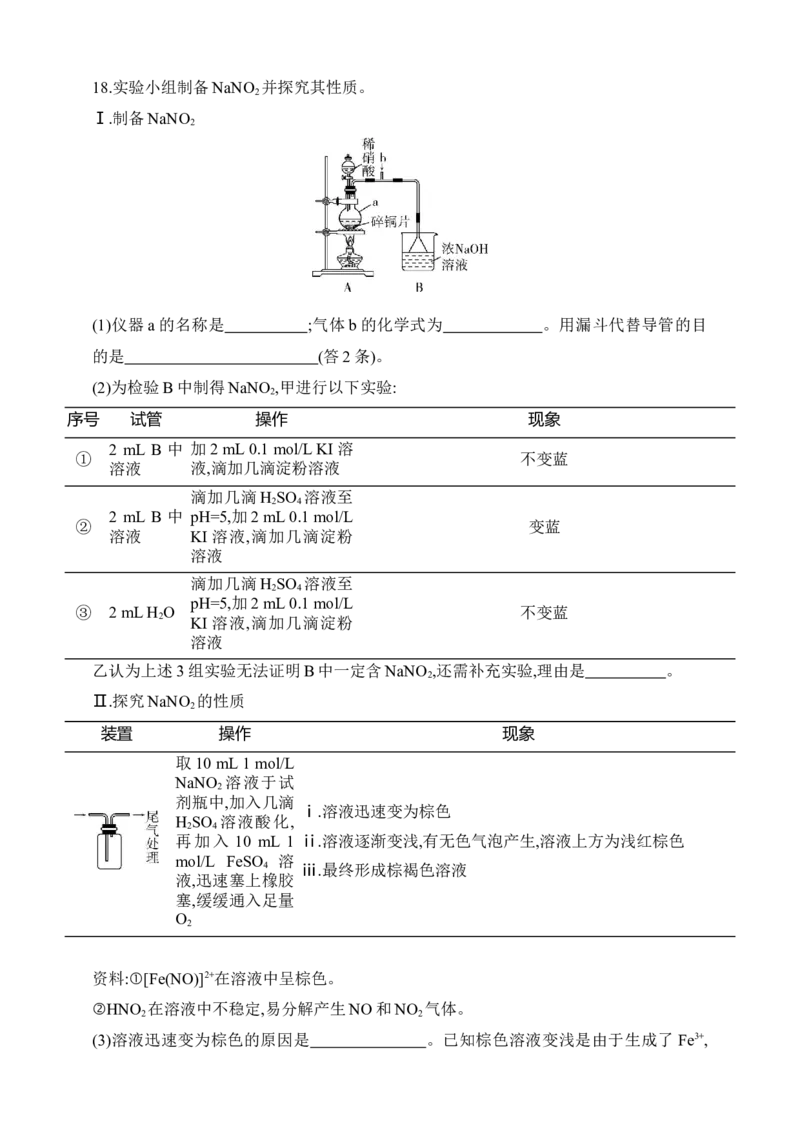
18.实验小组制备NaNO 并探究其性质。
2
Ⅰ.制备NaNO
2
(1)仪器a的名称是 ;气体b的化学式为 。用漏斗代替导管的目
的是 (答2条)。
(2)为检验B中制得NaNO ,甲进行以下实验:
2
序号 试管 操作 现象
2 mL B 中 加2 mL 0.1 mol/L KI溶
① 不变蓝
溶液 液,滴加几滴淀粉溶液
滴加几滴H SO 溶液至
2 4
2 mL B 中 pH=5,加2 mL 0.1 mol/L
② 变蓝
溶液 KI 溶液,滴加几滴淀粉
溶液
滴加几滴H SO 溶液至
2 4
pH=5,加2 mL 0.1 mol/L
③ 2 mL H O 不变蓝
2 KI 溶液,滴加几滴淀粉
溶液
乙认为上述3组实验无法证明B中一定含NaNO ,还需补充实验,理由是 。
2
Ⅱ.探究NaNO 的性质
2装置 操作 现象
取10 mL 1 mol/L
NaNO 溶液于试
2
剂瓶中,加入几滴
ⅰ.溶液迅速变为棕色
H SO 溶液酸化,
2 4
再加入 10 mL 1 ⅱ.溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色
mol/L FeSO 溶
4 ⅲ.最终形成棕褐色溶液
液,迅速塞上橡胶
塞,缓缓通入足量
O
2
资料:①[Fe(NO)]2+在溶液中呈棕色。
②HNO 在溶液中不稳定,易分解产生NO和NO 气体。
2 2
(3)溶液迅速变为棕色的原因是 。已知棕色溶液变浅是由于生成了 Fe3+,
反应的离子方程式是 。
(4)最终棕褐色溶液中溶质的成分是 Fe(OH) (SO ),测得装置中混合溶液体积为 20 mL,设
x 4 y
计如下实验测定其组成。
资料:充分反应后,Fe2+全部转化为Fe(OH) (SO ) 。
x 4 y
加掩蔽剂KF的原理和目的是(掩蔽Fe3+的颜色除外) 。由上述数据可
知Fe(OH) (SO ) 中x= (用含V 、V 的代数式表示)。
x 4 y 1 2
19.利用电极反应可探究物质氧化性、还原性的变化规律。
已知:酸性介质中,1 mol/L不同电对的电极电势见下表。电极电势越高,其氧化型物质的氧
化性越强;电极电势越低,其还原型物质的还原性越强。
电对(氧化 Fe3+/ H O / O / MnO / I /
2 2 2 2 2
型/还原型) Fe2+ H
2
O H
2
O
2
Mn2+ I-
电极电势
0.771 1.776 0.695 1.224 0.536
φ/V
回答下列问题:
Ⅰ.探究H O 的分解反应
2 2
Fe3+催化H O 分解反应过程包括ⅰ、ⅱ两步:
2 2反应ⅰ:Fe3++H O Fe2++H++ (未配平)
2 2
反应ⅱ:2Fe2++H O +2H+ 2Fe3++2H O
2 2 2
(1)反应ⅰ的离子方程式为 。
(2)验证Fe2+生成:反应过程中,加入 溶液,产生蓝色沉淀,证明有Fe2+生成。
(3)酸性条件下MnO 也可催化 H O 分解。结合表中数据判断,上述条件下H O 、O 、
2 2 2 2 2 2
MnO 的氧化性由强到弱的顺序为 。
2
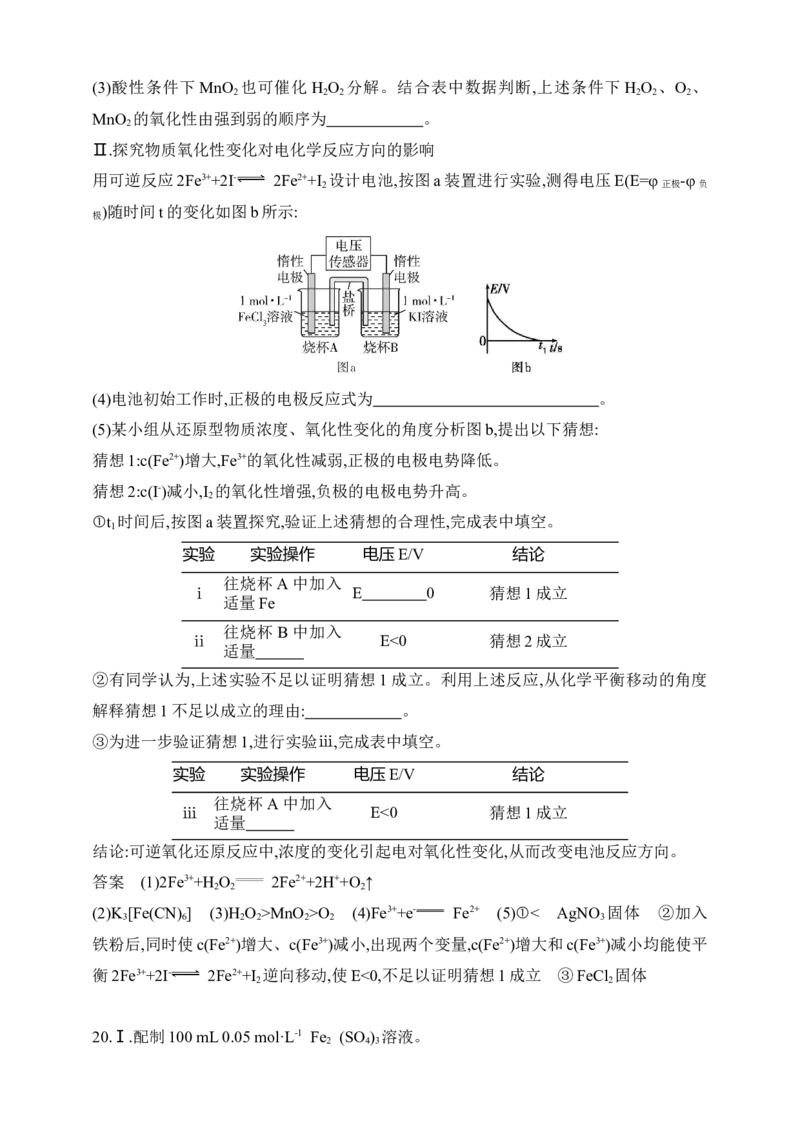
Ⅱ.探究物质氧化性变化对电化学反应方向的影响
用可逆反应2Fe3++2I- 2Fe2++I 设计电池,按图a装置进行实验,测得电压E(E=φ -φ
2 正极 负
)随时间t的变化如图b所示:
极
(4)电池初始工作时,正极的电极反应式为 。
(5)某小组从还原型物质浓度、氧化性变化的角度分析图b,提出以下猜想:
猜想1:c(Fe2+)增大,Fe3+的氧化性减弱,正极的电极电势降低。
猜想2:c(I-)减小,I 的氧化性增强,负极的电极电势升高。
2
①t 时间后,按图a装置探究,验证上述猜想的合理性,完成表中填空。
1
实验 实验操作 电压E/V 结论
往烧杯A中加入
ⅰ E 0 猜想1成立
适量Fe
往烧杯 B 中加入
ⅱ E<0 猜想2成立
适量
②有同学认为,上述实验不足以证明猜想 1成立。利用上述反应,从化学平衡移动的角度
解释猜想1不足以成立的理由: 。
③为进一步验证猜想1,进行实验ⅲ,完成表中填空。
实验 实验操作 电压E/V 结论
往烧杯A中加入
ⅲ E<0 猜想1成立
适量
结论:可逆氧化还原反应中,浓度的变化引起电对氧化性变化,从而改变电池反应方向。20.Ⅰ.配制100 mL 0.05 mol·L-1 Fe (SO ) 溶液。
2 4 3
(1)该实验需要用到的玻璃仪器有:烧杯、量筒、玻璃棒、 、 。
(2)为了防止Fe (SO ) 水解,在配制过程中可以加入少量 。
2 4 3
Ⅱ.探究Fe (SO ) 与Cu的反应。
2 4 3
原理预测:
(3)请写出Fe (SO ) 与Cu反应的离子方程式 。
2 4 3
开展实验并观察现象:
某实验小组在进行Fe (SO ) 与Cu的反应时观察到了异常现象,决定对其进行进一步的
2 4 3
探究。
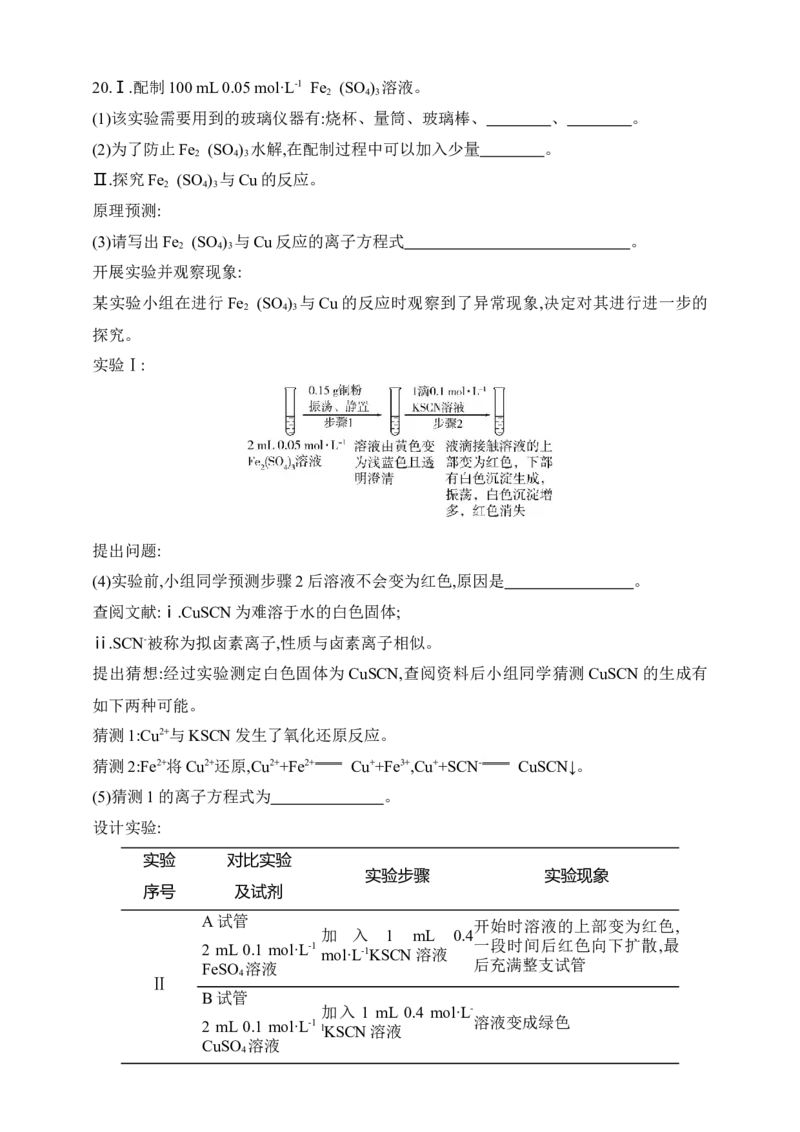
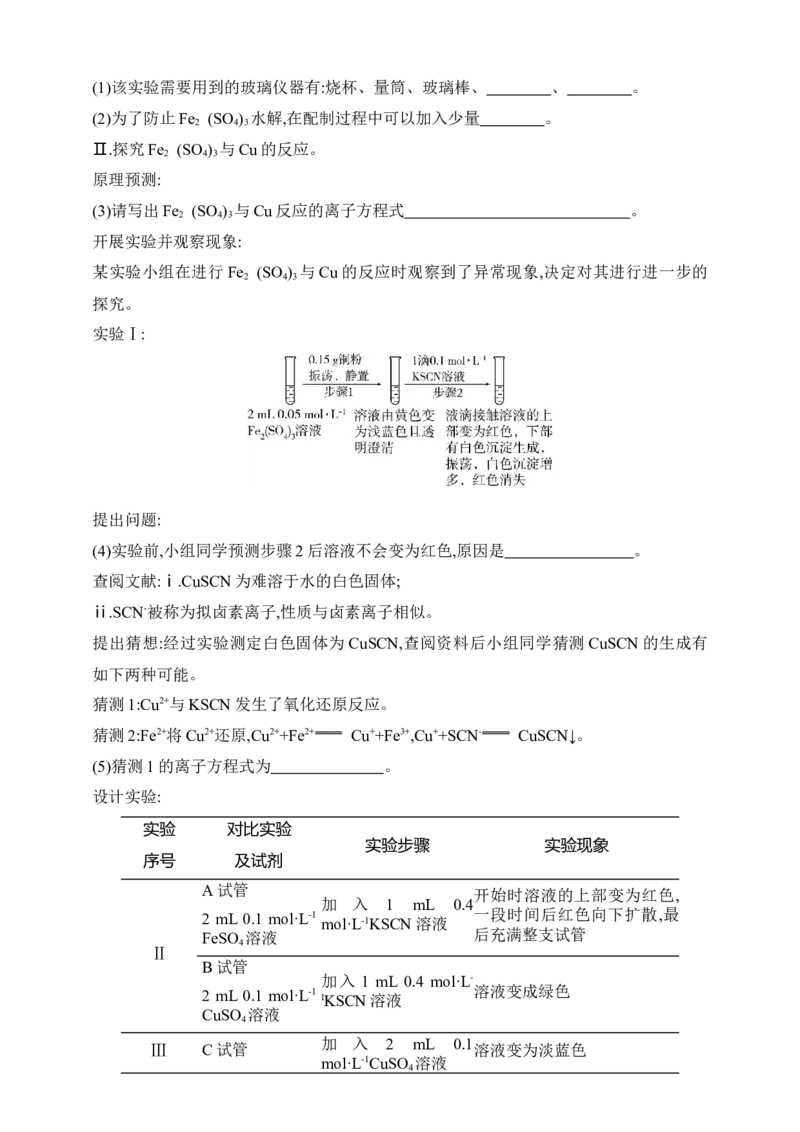
实验Ⅰ:
提出问题:
(4)实验前,小组同学预测步骤2后溶液不会变为红色,原因是 。
查阅文献:ⅰ.CuSCN为难溶于水的白色固体;
ⅱ.SCN-被称为拟卤素离子,性质与卤素离子相似。
提出猜想:经过实验测定白色固体为CuSCN,查阅资料后小组同学猜测CuSCN的生成有
如下两种可能。
猜测1:Cu2+与KSCN发生了氧化还原反应。
猜测2:Fe2+将Cu2+还原,Cu2++Fe2+ Cu++Fe3+,Cu++SCN- CuSCN↓。
(5)猜测1的离子方程式为 。
设计实验:
实验 对比实验
实验步骤 实验现象
序号 及试剂
A试管
开始时溶液的上部变为红色,
加 入 1 mL 0.4
2 mL 0.1 mol·L-1 一段时间后红色向下扩散,最
mol·L-1KSCN溶液
FeSO 溶液 后充满整支试管
4
Ⅱ
B试管
加入 1 mL 0.4 mol·L-
2 mL 0.1 mol·L-1 溶液变成绿色
lKSCN溶液
CuSO 溶液
4加 入 2 mL 0.1
溶液变为淡蓝色
C试管 mol·L-1CuSO 溶液
4
Ⅲ 2 mL 0.1 mol·L-1 溶液的上层变为红色,有白色
再 加 1 mL 0.4
FeSO 溶液 沉淀产生,一段时间后整支试
4 mol·L-1KSCN溶液
管溶液呈深红色
得出结论:
(6)实验Ⅱ中试管 (填字母)中的现象可以证实猜测1不成立。
(7)Fe3+的氧化性本应强于Cu2+,结合实验Ⅲ中的现象解释Cu2++Fe2+ Cu++Fe3+能正向发
生的原因 。
答案 (1)胶头滴管 100 mL容量瓶 (2)稀硫酸 (3)Cu+2Fe3+ Cu2++2Fe2+ (4)Cu粉
过量不会有 Fe3+剩余,不会有红色的 Fe(SCN) 生成 (5)2Cu2++4SCN- 2CuSCN↓+
3
(SCN) ↑ (6)B (7)由于SCN-与Cu+形成沉淀以及SCN-与Fe3+形成配合物,大大降低了产
2
物中Cu+和Fe3+的浓度,使得平衡正向移动
专题十七 实验方案的设计和评价
1.实验室制取乙烯并验证其化学性质,下列装置不正确的是( )
A.制备乙烯 B.除去杂质
C.验证性质 D.收集乙烯
答案 D
2.利用如图所示装置进行 SO 的制备和性质探究实验(夹持装置省略)。下列说法不正确
2
的是( )A.固体X可为Cu
B.若试剂Y为氢硫酸,则试管中可产生淡黄色沉淀
C.为证明SO 具有还原性,试剂Y可为酸性KMnO 溶液
2 4
D.该装置中试管口应塞一团浸有NaOH溶液的棉团
答案 A
3.下列操作能实现相应的实验目的的是( )
选项 实验目的 操作步骤及现象
验证淀粉水 将淀粉和稀硫酸混合水浴加热一段时间;待溶液冷却后,加入
A 解生成葡萄 NaOH溶液,调pH至碱性,再加入新制的Cu(OH) ,加热,有砖红
2
糖 色沉淀产生
向某钠盐中滴加浓盐酸,并将产生的气体通入品红溶液中,品红
证明某钠盐
溶液褪色
B 为 Na SO 或
2 3
NaHSO
3
除去乙醇中
C 混有的少量 向混合液中加入饱和Na CO 溶液,分液
2 3
乙酸
证 明 氧 化 将硫酸酸化的 H O 滴入Fe(NO ) 溶液中,再滴入 KSCN溶液,
D 2 2 3 2
性:H O >Fe3+ 溶液变红
2 2
答案 A
4.实验探究是化学学习的方法之一。下列实验设计、现象和实验结论都正确的是( )
实验设计 现象 实验结论
加热后坩埚内固体为
在坩埚中加入 16.4 g CaC O ·2H O,称取坩埚中剩余物质质量
A 2 4 2 CaO 和 CaC O 的混合
加热一段时间,在干燥器中冷却 为12.8 g 2 4
物
滴加稀硝酸时无明显现象,
向溶液X中先滴加稀硝酸,然后再滴 溶 液 X 中 含 SO2−或
B 滴加 BaCl 溶液时产生白 4
加BaCl 溶液 2 Ag+
2 色沉淀
分别用蒸馏水、1.0 mol·L-1 AlCl 溶喷洒 AlCl 溶液的纸张老
C 3 3 Cl-能促进纸张的老化
液喷洒甲、乙两张白纸,静置、干燥 化明显
在烧瓶中加入木炭颗粒与浓硝酸,然 木炭具有还原性,能还
D 烧瓶中有红棕色气体产生
后加热 原HNO
3
答案 B
5.实验是探究物质性质的重要方法,下列实验中,操作及现象与得出的结论相一致的是(
)选项 实验目的 操作及现象 结论
两支试管中分别盛相同温度、相同浓度、相同体积
探究不同催
的H O 溶液,分别滴加相同浓度、相同体积的FeCl Fe3+对H O 分解
A 化剂的催化 2 2 3 2 2
溶液与CuSO 溶液,滴加FeCl 溶液的试管中产生气的催化效率更高
效率 4 3
体更快
验 证 反 应向2 mL 0.1 mol·L-1 KI溶液中加入1 mL 0.1 mol·L-1
反 应 2Fe3++2I-
2Fe3++2I- FeCl 溶液,充分反应。取反应后试样,滴加KSCN溶
B 3 2Fe2++I 是
2Fe2++I 是可液,溶液变为红色;另取反应后试样,加入K [Fe(CN) ] 2
2 3 6 可逆反应
逆反应 溶液,产生蓝色沉淀
检验Cu O固 若有红色固体剩
2
C 体中是否含取样,加入足量稀盐酸,观察现象 余,则说明样品
有单质Cu 中有单质Cu
证明苯酚与 若出现白色沉
D 溴水发生反向苯酚饱和溶液中滴加少量溴水,充分振荡 淀,说明苯酚与
应 溴发生了反应
答案 B
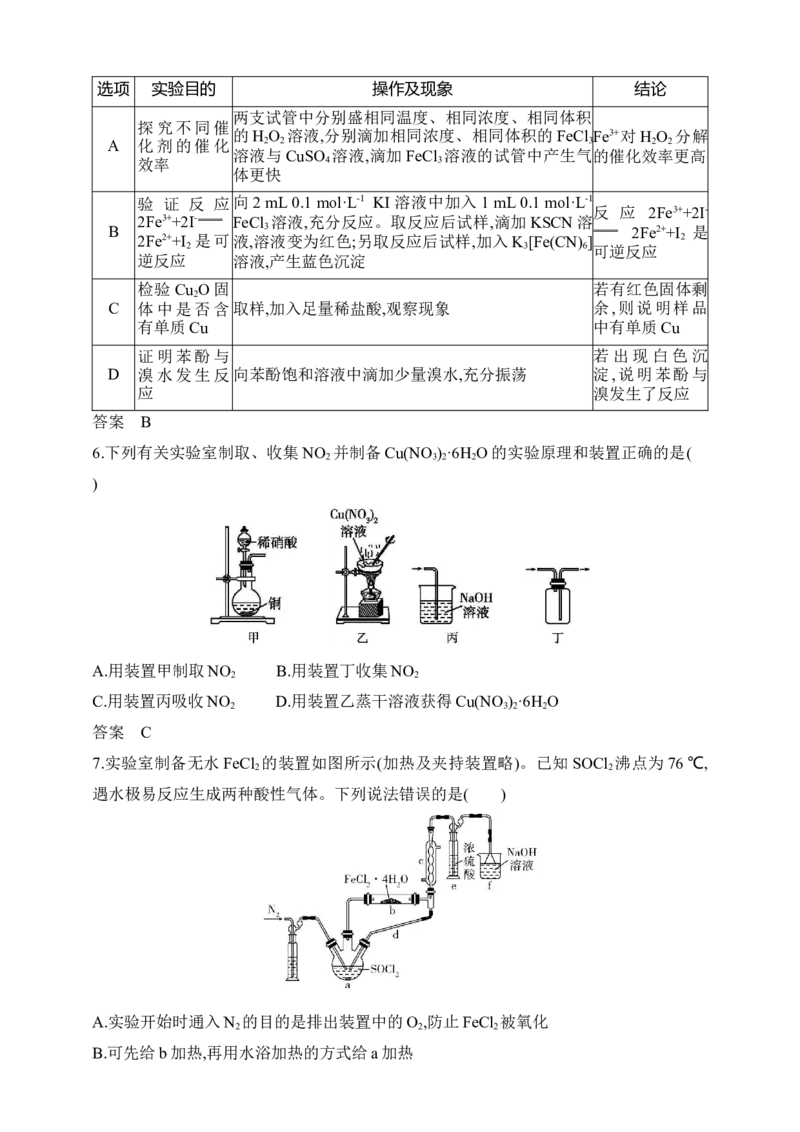
6.下列有关实验室制取、收集 NO 并制备Cu(NO ) ·6H O的实验原理和装置正确的是(
2 3 2 2
)
A.用装置甲制取NO B.用装置丁收集NO
2 2
C.用装置丙吸收NO D.用装置乙蒸干溶液获得Cu(NO ) ·6H O
2 3 2 2
答案 C
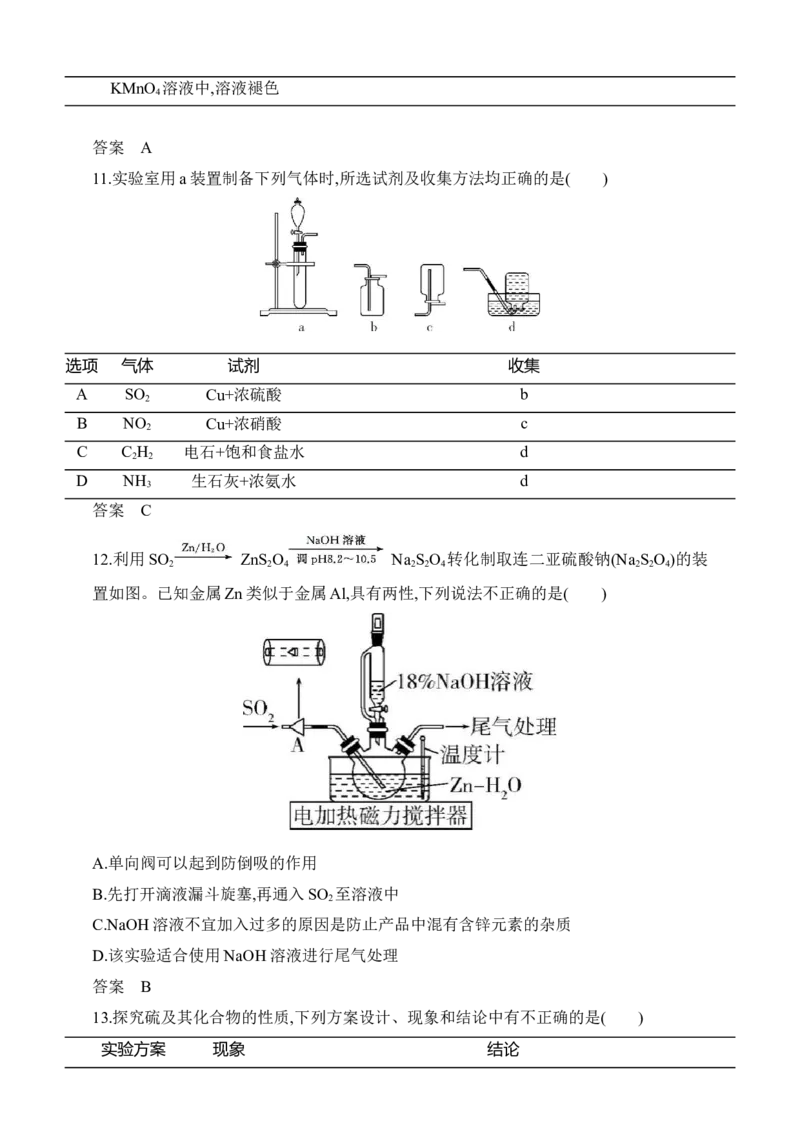
7.实验室制备无水FeCl 的装置如图所示(加热及夹持装置略)。已知SOCl 沸点为76 ℃,
2 2
遇水极易反应生成两种酸性气体。下列说法错误的是( )
A.实验开始时通入N 的目的是排出装置中的O ,防止FeCl 被氧化
2 2 2
B.可先给b加热,再用水浴加热的方式给a加热C.装置c、d的作用是冷凝回流SOCl
2
D.装置f的作用是吸收反应生成的HCl和SO
2
答案 B
8.室温下,下列实验探究方案及现象能达到探究目的的是( )
选项 探究方案及现象 探究目的
用pH计测量 HF溶液、盐酸的 pH,比较溶液
A HF是弱电解质
pH大小
向久置的Na SO 溶液中加入足量BaCl 溶液,
2 3 2
B 出现白色沉淀,再加入足量稀盐酸,部分沉淀溶 Na SO 不能被空气氧化
2 3
解
向NaBr溶液中滴加过量氯水,溶液变橙色,再
氧化性:
C
加入淀粉KI溶液,溶液变蓝色
Cl >Br >I
2 2 2
向盛有 FeSO 溶液的试管中滴加几滴 KSCN
4
D 溶液,振荡,再滴加几滴新制氯水,观察溶液颜色 Fe2+具有还原性
变化
答案 D
9.常温下,根据下列实验操作和现象得出的结论正确的是( )
选项 实验操作和现象 实验结论
分别测量浓度均为 0.1 mol·L-1 Na CO 溶液和
A 2 3 [Al(OH) ]-比CO2−更容易结合H+
Na[Al(OH) ]溶液的pH,后者pH更大 4 3
4
将亚硫酸钠样品溶于水,加入盐酸酸化的
B 亚硫酸钠样品已变质
Ba(NO ) 溶液,出现白色沉淀
3 2
将盐酸滴入Na CO 溶液产生无色气体,将产生
C 2 3 非金属性:Cl>C>Si
的气体直接通入Na SiO 溶液
2 3
向BaCl 溶液中通入SO 和气体X,出现白色沉
D 2 2 气体X一定具有氧化性
淀
答案 A
10.根据下列实验操作和现象得出的结论不正确的是( )
选项 实验操作和现象 实验结论
向溶有 SO 的 BaCl 溶液中通入气体
A 2 2 X具有氧化性
X,出现白色沉淀
向 0.1 mol·L-1 FeCl 溶液中滴加 KI 淀
B 3 氧化性:Fe3+>I
粉溶液,溶液变蓝 2
向 NaHCO 溶液中加入等浓度、等体
C 3 AlO-比CO2−更容易结合H+
积的NaAlO 溶液,出现白色沉淀 2 3
2
将溴乙烷、乙醇和烧碱的混合物加热,
D 溴乙烷发生了消去反应
产生的气体经水洗后,再通入酸性KMnO 溶液中,溶液褪色
4
答案 A
11.实验室用a装置制备下列气体时,所选试剂及收集方法均正确的是( )
选项 气体 试剂 收集
A SO Cu+浓硫酸 b
2
B NO Cu+浓硝酸 c
2
C C H 电石+饱和食盐水 d
2 2
D NH 生石灰+浓氨水 d
3
答案 C
12.利用SO ZnS O Na S O 转化制取连二亚硫酸钠(Na S O )的装
2 2 4 2 2 4 2 2 4
置如图。已知金属Zn类似于金属Al,具有两性,下列说法不正确的是( )
A.单向阀可以起到防倒吸的作用
B.先打开滴液漏斗旋塞,再通入SO 至溶液中
2
C.NaOH溶液不宜加入过多的原因是防止产品中混有含锌元素的杂质
D.该实验适合使用NaOH溶液进行尾气处理
答案 B
13.探究硫及其化合物的性质,下列方案设计、现象和结论中有不正确的是( )
实验方案 现象 结论产生淡黄色
在过硫化钠
沉淀和臭鸡
A (Na S ) 中 加 发生歧化反应:Na S +2HCl 2NaCl+H S↑+S↓
2 2 蛋气味的气 2 2 2
入稀盐酸
体
已 知
溶液先变为
[Fe(SO ) ]3+
2 6 红棕色,过Fe3+与SO 络合反应速率比氧化还原反应速率快,但氧化还原反应的
B 呈红棕色,将 2
一段时间又平衡常数更大
SO 气体通入
2 变成浅绿色
FeCl 溶液中
3
续表
实验方案 现象 结论
燃着的镁条
插 入 盛 有 剧烈燃烧,
SO 的集气瓶 集气瓶口有
2
中。冷却后, 淡黄色固体
往集气瓶中 附着,集气
C 加入适量稀 瓶底有白色镁能在SO 中燃烧:2Mg+SO 2MgO+S
2 2
盐酸,静置,取 固体生成。
少量上层清 试管中没有
液于试管中, 产生黑色沉
滴 加 少 量 淀
CuSO 溶液
4
将电石与饱
和食盐水反
应产生的气
探究电石与
D 体通入酸性若酸性高锰酸钾溶液褪色,说明电石与水反应生成了乙炔
水的反应
高锰酸钾溶
液,观察现
象
答案 D
14.三氯化铬为紫色晶体,熔点为1 152 ℃,易潮解,高温下易被氧气氧化。实验室根据反应
Cr O (s)+3CCl (g) 2CrCl (s)+3COCl (g),利用如下装置制备 CrCl 粗品(加热及夹持装
2 3 4 3 2 3
置略去)。回答下列问题:
已知:CCl 沸点为76.8 ℃;COCl 有毒,沸点为8.2 ℃,遇水剧烈水解生成有刺激性气味的气
4 2体。
制备CrCl 时进行操作:
3
(ⅰ)……;
(ⅱ)将盛有Cr O 粉末的瓷舟置于管式炉中;
2 3
(ⅲ)通入N ,一段时间后接通冷凝装置,加热开始反应,控制温度为750 ℃左右;
2
(ⅳ)反应结束后,停止热水浴和管式炉加热,继续通入N ,直至装置冷却。
2
(1)操作(ⅰ)为 ,判断制备反应结束的实验现象是 。
(2)图示装置存在的缺陷是 。实验过程中通入氮气的目的是
,锥形瓶用来收集 (填化学式)。
(3)装置E中发生反应的离子方程式为 。
答案 (1)检查装置的气密性 当pH传感器读数保持不变时
(2)D、E之间缺少防倒吸装置 开始时把装置中的空气排出,结束时将装置中的COCl 气
2
体排入装置E进行处理 CCl
4
(3)COCl +4OH- CO2−+2Cl-+2H O
2 3 2
15.K [Fe(C O ) ]·xH O(三草酸合亚铁酸钾)是一种橙色固体,能溶于水,难溶于乙醇,在分析
4 2 4 3 2
化学中用作吸氧剂。可通过如下实验装置(夹持装置省略),先制得难溶于水的 FeC O ,再
2 4
制取三草酸合亚铁酸钾。
回答下列问题:
(1)将铁屑放入a中,加入少量蒸馏水,按图连接好装置,进行的操作为①打开K 、K 和K ,
1 3 4
关闭K ;②……;③……;④关闭K 、K 。操作②是 ,目的是 ;经操
2 1 2
作③,B装置中生成FeC O ,此时活塞K 、K 的状态是 。
2 4 2 3
(2)向生成FeC O 的B装置中重新加入H C O -K C O 混合溶液,充分反应后加入乙醇,作
2 4 2 2 4 2 2 4
用是 ,从而获得K [Fe(C O ) ]·xH O沉淀。对所得产
4 2 4 3 2
品洗涤干净后进行如下分析:取m g产品进行含铁量的测定,平均分成三份加入锥形瓶中,
加入稀H SO 溶解后,用c mol·L-1的KMnO 溶液滴定,三次实验消耗 KMnO 溶液的平均
2 4 4 4
体积为V mL。产品中铁元素的质量分数表达式为 %;若产品加入锥形瓶后放置时
间过长,则测定的质量分数将 (填“偏高”“偏低”或“不变”)。
(3)K [Fe(C O ) ]·xH O加热时易分解。现利用如下装置检验其受热分解所得产物是否含
4 2 4 3 2有H O、CO、CO :
2 2
各装置接口的连接顺序为a→hi→ (填标号);实验开始时,
先通一段时间的N 。若气体产物中含有CO,则装置中的现象是 。
2
答案 (1)在尾部检验H 纯度 证明装置内空气已排尽(防止产品被氧化) 打开K ,关闭
2 2
K
3
12cV
(2)降低三草酸合亚铁酸钾的溶解度,便于析出 偏低
m
(3)fg→bc(或cb)→d B中黑色固体变红,E中澄清石灰水不变浑浊,且C中澄清石灰水变
浑浊
16.硫代硫酸钠(Na S O )可用作分析试剂及还原剂,受热、遇酸易分解。学习小组用如图
2 2 3
装置模拟古法制硫酸,同时利用生成的SO 气体制备硫代硫酸钠。
2
已知:
①2FeSO ·7H O Fe O +SO ↑+SO ↑+14H O;
4 2 2 3 2 3 2
②SO 的沸点为44.8 ℃;
3
③Na S O 中S元素的化合价分别为-2价和+6价。
2 2 3
回答下列问题:
(1)检查装置气密性,加入药品。Na S和Na CO 混合溶液用煮沸过的蒸馏水配制,目的是
2 2 3
,D装置中试剂为 。
(2)实验过程操作:①打开活塞K 、K ,关闭活塞K ,通入一段时间N ;②关闭活塞K 、K ,
1 2 3 2 1 2打开活塞K ,加热绿矾;③C处溶液pH约为8时停止加热;④在m处连接盛有NaOH溶液
3
的容器……⑤从锥形瓶中得到Na S O 晶体。使用pH传感器始终监测混合溶液pH的原
2 2 3
因是 ;补充完善操作④: 。
(3)步骤⑤中需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的原因是
。
(4)学习小组探究Na S O 的性质:取Na S O 晶体,溶解配成0.2 mol/L的溶液;取4 mL溶液,
2 2 3 2 2 3
向其中加入1 mL饱和氯水(pH=2.4),溶液立即出现浑浊。对溶液变浑浊的原因提出假设:
假设1:氯水氧化了-2价硫元素;
假设2:酸性条件下Na S O 分解产生S。
2 2 3
实验验证:a、b试管均盛有4 mL 0.2 mol/L Na S O 溶液。
2 2 3
①用胶头滴管向试管b中加入的试剂为 。
②依据现象,S产生的主要原因是 (用离子方程式表示)。
答案 (1)除去水中溶解的氧气 NaOH 溶液 (2)防止 SO 过量使溶液呈酸性,造成
2
Na S O 分解 关闭活塞K ,打开活塞K 、K ,通入一段时间N (3)控制温度,防止温度过
2 2 3 3 1 2 2
高Na S O 分解 (4)①1 mL pH=2.4的盐酸 ②Cl +S O2−+H O SO2−+S↓+2Cl-+2H+
2 2 3 2 2 3 2 4
17.己二酸在有机合成工业等方面有着重要作用,以环己醇( ,M=100,ρ=0.95 g/mL)为
r
原 料 制 取 己 二 酸 [HOOC(CH ) COOH,M=146], 已 知 己 二 酸 和 己 二 酸 钾
2 4 r
[KOOC(CH ) COOK]的溶解度均随温度升高而增大。
2 4
实验步骤:①向250 mL三颈烧瓶中加入搅拌磁子、50 mL 1.0%的KOH溶液和9.0 g高锰
酸钾,按如图所示安装装置,控制滴速并维持温度在45 ℃左右,共滴加环己醇2.0 mL,滴加
结束时需启动加热装置加热一段时间,趁热过滤,洗涤滤渣MnO 。
2②将滤液和洗涤液倒入100 mL 烧杯中,加入适量饱和亚硫酸氢钾溶液,再用约4 mL 浓
HCl溶液,使溶液呈酸性,加热浓缩使溶液体积减少至10 mL,经过冷却结晶、过滤、洗涤,
烘干得到粗产品a g。
③准确称取b g己二酸产品于锥形瓶中,加入少量水溶解,滴入酚酞试剂,用0.1 mol/L的
NaOH溶液滴定。重复上述操作三次,平均消耗NaOH溶液V mL。
(1)装环己醇的仪器名称 ,冷凝水的进水口为 (填“a”或“b”)。
(2)三颈烧瓶内发生反应的化学方程式为 。
(3)步骤①中趁热过滤的优点是 。
(4)下列关于实验操作的相关说法,错误的有 。
A.步骤①中洗涤时可采用少量热水洗涤滤渣三次
B.步骤①如果滴速过快,会导致溶液温度升高,反应过于剧烈
C.步骤②中饱和亚硫酸氢钾溶液的目的是除去多余的KMnO
4
D.步骤②中过滤时,可用玻璃棒搅拌待过滤液,加快过滤速率
(5)如不加入适量饱和亚硫酸氢钾溶液,后续会产生一种有毒气体。在产生该有毒气体的
化学反应中,氧化剂和氧化产物的物质的量之比为 。
(6)如何判断滴定达到终点: 。
(7)己二酸的实际产率是 (用含a、b、V的化简后的式子表示)。
答案 (1)恒压滴液漏斗 b
(2)3 +8KMnO 8MnO ↓+3KOOC(CH ) COOK+2KOH+5H O
4 2 2 4 2
(3)滤去MnO 的同时可以避免溶液冷却导致己二酸钾析出,提高产率
2
(4)D
(5)2∶5
(6)当滴入最后半滴NaOH溶液时,溶液由无色刚好变为粉红色,且半分钟内不褪色
aV
(7) ×100%
380b18.实验小组制备NaNO 并探究其性质。
2
Ⅰ.制备NaNO
2
(1)仪器a的名称是 ;气体b的化学式为 。用漏斗代替导管的目
的是 (答2条)。
(2)为检验B中制得NaNO ,甲进行以下实验:
2
序号 试管 操作 现象
2 mL B 中 加2 mL 0.1 mol/L KI溶
① 不变蓝
溶液 液,滴加几滴淀粉溶液
滴加几滴H SO 溶液至
2 4
2 mL B 中 pH=5,加2 mL 0.1 mol/L
② 变蓝
溶液 KI 溶液,滴加几滴淀粉
溶液
滴加几滴H SO 溶液至
2 4
pH=5,加2 mL 0.1 mol/L
③ 2 mL H O 不变蓝
2 KI 溶液,滴加几滴淀粉
溶液
乙认为上述3组实验无法证明B中一定含NaNO ,还需补充实验,理由是 。
2
Ⅱ.探究NaNO 的性质
2
装置 操作 现象
取10 mL 1 mol/L
NaNO 溶液于试
2
剂瓶中,加入几滴
ⅰ.溶液迅速变为棕色
H SO 溶液酸化,
2 4
再加入 10 mL 1 ⅱ.溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色
mol/L FeSO 溶
4 ⅲ.最终形成棕褐色溶液
液,迅速塞上橡胶
塞,缓缓通入足量
O
2
资料:①[Fe(NO)]2+在溶液中呈棕色。
②HNO 在溶液中不稳定,易分解产生NO和NO 气体。
2 2
(3)溶液迅速变为棕色的原因是 。已知棕色溶液变浅是由于生成了 Fe3+,反应的离子方程式是 。
(4)最终棕褐色溶液中溶质的成分是 Fe(OH) (SO ),测得装置中混合溶液体积为 20 mL,设
x 4 y
计如下实验测定其组成。
资料:充分反应后,Fe2+全部转化为Fe(OH) (SO ) 。
x 4 y
加掩蔽剂KF的原理和目的是(掩蔽Fe3+的颜色除外) 。由上述数据可
知Fe(OH) (SO ) 中x= (用含V 、V 的代数式表示)。
x 4 y 1 2
答案 (1)圆底烧瓶 O 防止倒吸、增大接触面积使其充分反应
2
(2)NO 可能与NaOH反应生成NaNO ,酸性条件下NO-也会氧化I-
2 3 3
(3)酸性条件下,HNO 分解产生的 NO 与溶液中的 Fe2+以配位键结合形成[Fe(NO)]2+
2
4[Fe(NO)]2++O +4H+ 4Fe3++4NO+2H O
2 2
(4)F-能与Fe3+形成稳定的无色配合离子[FeF ]3-,可避免Fe3+与氢氧化钠反应造成实验干扰
6
V -V
1 2
15
19.利用电极反应可探究物质氧化性、还原性的变化规律。
已知:酸性介质中,1 mol/L不同电对的电极电势见下表。电极电势越高,其氧化型物质的氧
化性越强;电极电势越低,其还原型物质的还原性越强。
电对(氧化 Fe3+/ H O / O / MnO / I /
2 2 2 2 2
型/还原型) Fe2+ H
2
O H
2
O
2
Mn2+ I-
电极电势
0.771 1.776 0.695 1.224 0.536
φ/V
回答下列问题:
Ⅰ.探究H O 的分解反应
2 2
Fe3+催化H O 分解反应过程包括ⅰ、ⅱ两步:
2 2
反应ⅰ:Fe3++H O Fe2++H++ (未配平)
2 2
反应ⅱ:2Fe2++H O +2H+ 2Fe3++2H O
2 2 2
(1)反应ⅰ的离子方程式为 。
(2)验证Fe2+生成:反应过程中,加入 溶液,产生蓝色沉淀,证明有Fe2+生成。(3)酸性条件下MnO 也可催化 H O 分解。结合表中数据判断,上述条件下H O 、O 、
2 2 2 2 2 2
MnO 的氧化性由强到弱的顺序为 。
2
Ⅱ.探究物质氧化性变化对电化学反应方向的影响
用可逆反应2Fe3++2I- 2Fe2++I 设计电池,按图a装置进行实验,测得电压E(E=φ -φ
2 正极 负
)随时间t的变化如图b所示:
极
(4)电池初始工作时,正极的电极反应式为 。
(5)某小组从还原型物质浓度、氧化性变化的角度分析图b,提出以下猜想:
猜想1:c(Fe2+)增大,Fe3+的氧化性减弱,正极的电极电势降低。
猜想2:c(I-)减小,I 的氧化性增强,负极的电极电势升高。
2
①t 时间后,按图a装置探究,验证上述猜想的合理性,完成表中填空。
1
实验 实验操作 电压E/V 结论
往烧杯A中加入
ⅰ E 0 猜想1成立
适量Fe
往烧杯 B 中加入
ⅱ E<0 猜想2成立
适量
②有同学认为,上述实验不足以证明猜想 1成立。利用上述反应,从化学平衡移动的角度
解释猜想1不足以成立的理由: 。
③为进一步验证猜想1,进行实验ⅲ,完成表中填空。
实验 实验操作 电压E/V 结论
往烧杯A中加入
ⅲ E<0 猜想1成立
适量
结论:可逆氧化还原反应中,浓度的变化引起电对氧化性变化,从而改变电池反应方向。
答案 (1)2Fe3++H O 2Fe2++2H++O ↑
2 2 2
(2)K [Fe(CN) ] (3)H O >MnO >O (4)Fe3++e- Fe2+ (5)①< AgNO 固体 ②加入
3 6 2 2 2 2 3
铁粉后,同时使c(Fe2+)增大、c(Fe3+)减小,出现两个变量,c(Fe2+)增大和c(Fe3+)减小均能使平
衡2Fe3++2I- 2Fe2++I 逆向移动,使E<0,不足以证明猜想1成立 ③FeCl 固体
2 2
20.Ⅰ.配制100 mL 0.05 mol·L-1 Fe (SO ) 溶液。
2 4 3(1)该实验需要用到的玻璃仪器有:烧杯、量筒、玻璃棒、 、 。
(2)为了防止Fe (SO ) 水解,在配制过程中可以加入少量 。
2 4 3
Ⅱ.探究Fe (SO ) 与Cu的反应。
2 4 3
原理预测:
(3)请写出Fe (SO ) 与Cu反应的离子方程式 。
2 4 3
开展实验并观察现象:
某实验小组在进行Fe (SO ) 与Cu的反应时观察到了异常现象,决定对其进行进一步的
2 4 3
探究。
实验Ⅰ:
提出问题:
(4)实验前,小组同学预测步骤2后溶液不会变为红色,原因是 。
查阅文献:ⅰ.CuSCN为难溶于水的白色固体;
ⅱ.SCN-被称为拟卤素离子,性质与卤素离子相似。
提出猜想:经过实验测定白色固体为CuSCN,查阅资料后小组同学猜测CuSCN的生成有
如下两种可能。
猜测1:Cu2+与KSCN发生了氧化还原反应。
猜测2:Fe2+将Cu2+还原,Cu2++Fe2+ Cu++Fe3+,Cu++SCN- CuSCN↓。
(5)猜测1的离子方程式为 。
设计实验:
实验 对比实验
实验步骤 实验现象
序号 及试剂
A试管
开始时溶液的上部变为红色,
加 入 1 mL 0.4
2 mL 0.1 mol·L-1 一段时间后红色向下扩散,最
mol·L-1KSCN溶液
FeSO 溶液 后充满整支试管
4
Ⅱ
B试管
加入 1 mL 0.4 mol·L-
2 mL 0.1 mol·L-1 溶液变成绿色
lKSCN溶液
CuSO 溶液
4
加 入 2 mL 0.1
Ⅲ C试管 溶液变为淡蓝色
mol·L-1CuSO 溶液
4溶液的上层变为红色,有白色
2 mL 0.1 mol·L-1 再 加 1 mL 0.4
沉淀产生,一段时间后整支试
FeSO 溶液 mol·L-1KSCN溶液
4 管溶液呈深红色
得出结论:
(6)实验Ⅱ中试管 (填字母)中的现象可以证实猜测1不成立。
(7)Fe3+的氧化性本应强于Cu2+,结合实验Ⅲ中的现象解释Cu2++Fe2+ Cu++Fe3+能正向发
生的原因 。
答案 (1)胶头滴管 100 mL容量瓶 (2)稀硫酸 (3)Cu+2Fe3+ Cu2++2Fe2+ (4)Cu粉
过量不会有 Fe3+剩余,不会有红色的 Fe(SCN) 生成 (5)2Cu2++4SCN- 2CuSCN↓+
3
(SCN) ↑ (6)B (7)由于SCN-与Cu+形成沉淀以及SCN-与Fe3+形成配合物,大大降低了产
2
物中Cu+和Fe3+的浓度,使得平衡正向移动