文档内容
专题四 能力提升检测卷
一、选择题(本题共20小题,每小题3分,共60分)
1.常温下,下列各组物质不发生反应的是( )
①硅与NaOH溶液 ②硅与盐酸 ③硅与氢氟酸 ④二氧化硅与碳酸钠 ⑤二氧化硅与 NaOH溶液
⑥二氧化硅与浓硝酸
A.①②④ B.③④⑥ C.②⑤⑥ D.②④⑥
【答案】D
【解析】常温下,能发生反应①Si+2NaOH+HO===Na SiO+2H↑,③Si+4HF===SiF ↑+2H↑,⑤
2 2 3 2 4 2
SiO+2NaOH===Na SiO+HO。
2 2 3 2
2.下列有关硅及其化合物的说法中正确的是( )
A.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中
B.反应①NaSiO +HO+CO===Na CO +HSiO↓,反应②NaCO +SiO=====NaSiO +CO↑,两
2 3 2 2 2 3 2 3 2 3 2 2 3 2
反应是相互矛盾的,不可能都发生
C.普通玻璃、石英玻璃、水泥等均属于硅酸盐材料
D.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
【答案】D
【解析】反应②是在高温下进行的,CO 为气体,逸出可使平衡正向移动,促使反应继续进行,B项
2
错误;石英玻璃不属于硅酸盐材料,C项错误。
3.由下列实验事实得出的结论正确的是( )
A.由SiO 不能与水反应生成HSiO 可知,SiO 不是HSiO 的酸酐
2 2 3 2 2 3
B.由SiO+2C=====Si+2CO↑可知,碳的非金属性强于硅
2
C.CO 通入NaSiO 溶液产生白色沉淀,可知酸性HCO>H SiO
2 2 3 2 3 2 3
D.SiO 可与NaOH溶液反应,也可与氢氟酸反应,可知SiO 为两性氧化物
2 2
【答案】C
【解析】SiO 是HSiO 的酸酐,A错误;SiO+2C=====Si+2CO↑,说明还原性C>Si,但不能比较非
2 2 3 2
金属性,B错误;CO +NaSiO +HO===H SiO↓+NaCO ,说明酸性HCO> H SiO ,C正确;两性氧化
2 2 3 2 2 3 2 3 2 3 2 3
物是指和酸、碱反应生成盐和水的氧化物,二氧化硅和氢氟酸反应是其特殊性质,不能和其他酸发生反应,
二氧化硅和碱溶液反应生成盐和水,是酸性氧化物,D项错误。
4.化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述正确的是( )
A.氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强B.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
C.测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH,测定结果无影响
D.“洁厕灵”不能与“84消毒液”混用,原因是两种溶液混合产生的HClO易分解
【答案】B
【解析】A项,活性炭具有吸附性,可以吸附氯气,错误;B项,氯气与烧碱溶液或石灰乳反应均可
生成次氯酸盐,正确;C项,氯水中的次氯酸具有漂白性,错误;D项,不能混用的原因是消毒液中的
NaClO与“洁厕灵”中的HCl反应生成Cl,错误。
2
5.如图所示。若关闭活塞Ⅰ,打开活塞Ⅱ,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;
若关闭活塞Ⅱ,打开活塞Ⅰ,再通入这种气体,布条褪色。甲瓶中所盛的试剂可能是( )
①浓硫酸 ②饱和氯化钠溶液 ③亚硫酸钠溶液 ④饱和碳酸氢钠溶液
A.①②③ B.②③④
C.①②④ D.①③④
【答案】D
【解析】Cl 与HO反应生成的HClO具有漂白作用。气体通过甲瓶后不能使有色布条褪色,可能有两
2 2
个原因:一是甲瓶中溶液将Cl 干燥,二是甲瓶中溶液能吸收Cl 。浓HSO 具有吸水性,NaSO 溶液、饱
2 2 2 4 2 3
和NaHCO 溶液都能与Cl 发生反应。
3 2
6.硫在空气中燃烧生成气体A,把A溶于水得溶液B,向B中滴加溴水,溴水褪色,B变成C,在C
里加NaS产生气体D,把D通入B溶液得浅黄色沉淀E。A、B、C、D、E都含同一种元素。则A、B、
2
C、D、E分别为( )
A.SO 、HSO 、HSO 、HS、S
2 2 4 2 3 2
B.SO 、HSO 、HSO 、HS、S
2 2 3 2 4 2
C.SO 、HSO 、HSO 、SO 、NaSO
2 2 3 2 4 3 2 2 3
D.SO 、HSO 、HSO 、SO 、NaSO
3 2 4 2 3 2 2 2 3
【答案】B
【解析】硫在空气中燃烧生成SO ,SO 溶于水得HSO ,向HSO 中滴加溴水生成HSO 和HBr,在
2 2 2 3 2 3 2 4
HSO 溶液中加NaS产生气体HS,HS与HSO 反应产生浅黄色沉淀S,故B项正确。
2 4 2 2 2 2 3
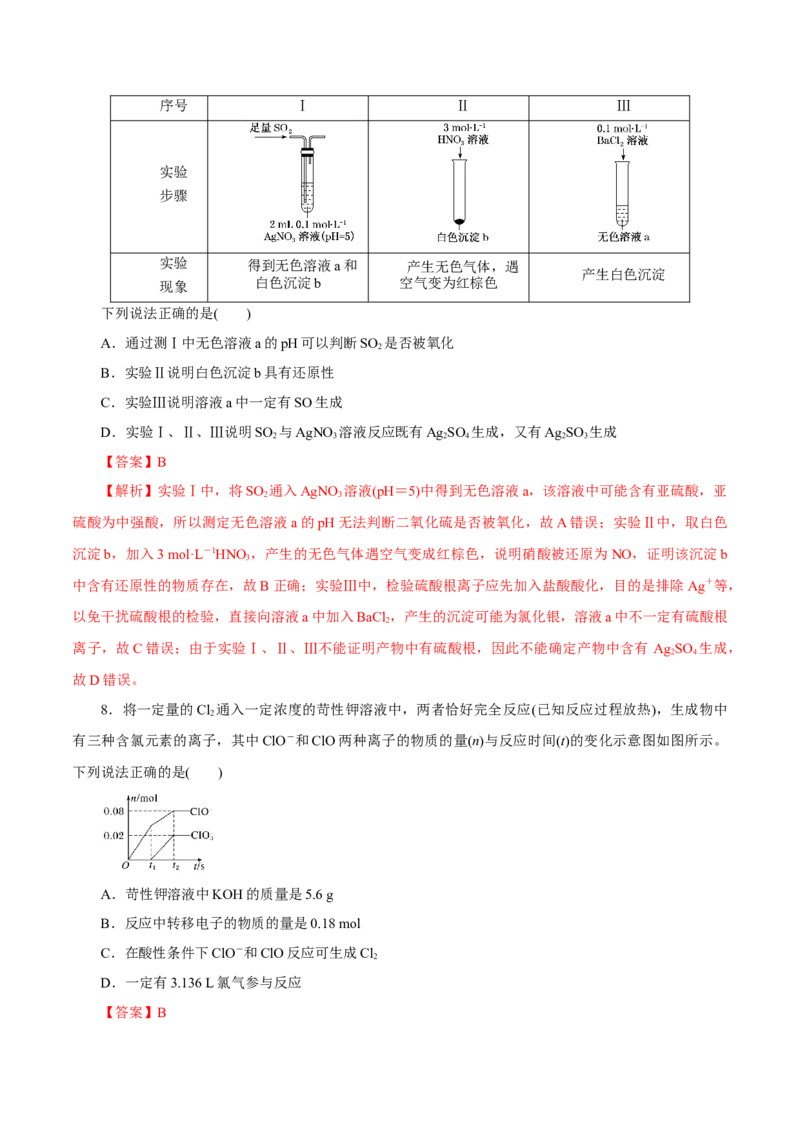
7.某实验小组探究SO 与AgNO 溶液的反应,实验记录如下:
2 3序号 Ⅰ Ⅱ Ⅲ
实验
步骤
实验 得到无色溶液a和 产生无色气体,遇
产生白色沉淀
现象 白色沉淀b 空气变为红棕色
下列说法正确的是( )
A.通过测Ⅰ中无色溶液a的pH可以判断SO 是否被氧化
2
B.实验Ⅱ说明白色沉淀b具有还原性
C.实验Ⅲ说明溶液a中一定有SO生成
D.实验Ⅰ、Ⅱ、Ⅲ说明SO 与AgNO 溶液反应既有Ag SO 生成,又有Ag SO 生成
2 3 2 4 2 3
【答案】B
【解析】实验Ⅰ中,将SO 通入AgNO 溶液(pH=5)中得到无色溶液a,该溶液中可能含有亚硫酸,亚
2 3
硫酸为中强酸,所以测定无色溶液a的pH无法判断二氧化硫是否被氧化,故A错误;实验Ⅱ中,取白色
沉淀b,加入3 mol·L-1HNO ,产生的无色气体遇空气变成红棕色,说明硝酸被还原为NO,证明该沉淀b
3
中含有还原性的物质存在,故B正确;实验Ⅲ中,检验硫酸根离子应先加入盐酸酸化,目的是排除 Ag+等,
以免干扰硫酸根的检验,直接向溶液a中加入BaCl ,产生的沉淀可能为氯化银,溶液a中不一定有硫酸根
2
离子,故C错误;由于实验Ⅰ、Ⅱ、Ⅲ不能证明产物中有硫酸根,因此不能确定产物中含有 Ag SO 生成,
2 4
故D错误。
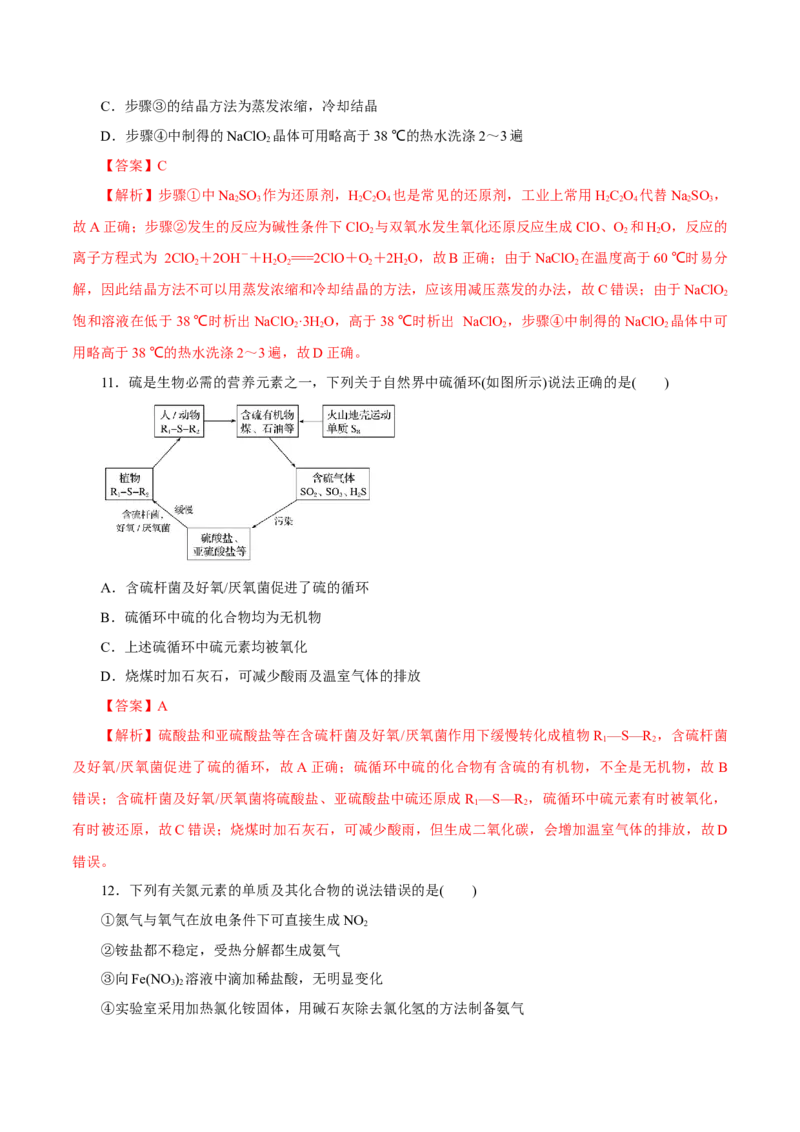
8.将一定量的Cl 通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中
2
有三种含氯元素的离子,其中ClO-和ClO两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。
下列说法正确的是( )
A.苛性钾溶液中KOH的质量是5.6 g
B.反应中转移电子的物质的量是0.18 mol
C.在酸性条件下ClO-和ClO反应可生成Cl
2
D.一定有3.136 L氯气参与反应
【答案】B【解析】氯气和氢氧化钾溶液反应生成次氯酸钾、氯化钾和氯酸钾,根据图像知 n(ClO-)=0.08 mol,
n(ClO)=0.02 mol,根据得失电子守恒可知生成的氯离子 n(Cl-)=0.08 mol×(1-0)+0.02 mol×(5-0)=0.18
mol,转移电子物质的量为0.18 mol,根据物料守恒可知n(K+)=n(Cl-)+n(ClO-)+n(ClO)=0.18 mol+0.08
mol+0.02 mol=0.28 mol。通过以上分析可知,氢氧化钾的物质的量是0.28 mol,质量是0.28 mol×56 g·mol
-1=15.68 g,故A错误;根据上述分析可知,反应中转移电子的物质的量是 0.18 mol,故B正确;因ClO-
中Cl元素的化合价是+1,ClO中Cl元素的化合价是+5,而Cl 中Cl元素的化合价是0,ClO-和ClO中
2
Cl元素的化合价都比Cl 中Cl元素的化合价高,故ClO- 和ClO不可能生成Cl ,C错误;因n(Cl-)+
2 2
n(ClO-)+n(ClO)=0.18 mol+0.08 mol+0.02 mol=0.28 mol,则根据原子守恒可知Cl 的物质的量是0.14
2
mol,但题目未说明是标准状况,无法计算Cl 的体积,故D错误。
2
9.SO 气体与足量Fe (SO ) 溶液完全反应后,再加入KCr O 溶液,发生如下化学反应:①SO +2Fe3
2 2 4 3 2 2 7 2
++2HO===SO+2Fe2++4H+;②CrO+6Fe2++14H+===2Cr3++6Fe3++7HO。则下列有关说法不正确的
2 2 2
是( )
A.氧化性:Cr O>Fe3+>SO
2 2
B.标准状况下,若有6.72 L SO 参加反应,则最终消耗0.2 mol KCr O
2 2 2 7
C.反应②中,每有1 mol K Cr O 参加反应,转移电子的数目为6N
2 2 7 A
D.由上述反应原理推断:KCr O 能将NaSO 氧化成NaSO
2 2 7 2 3 2 4
【答案】B
【解析】由①可知,Fe元素的化合价降低,则氧化性为Fe3+>SO ,由②可知,Cr元素的化合价降低,
2
则氧化性为Cr O>Fe3+,则氧化性:Cr O>Fe3+>SO ,故A正确;6.72 L SO (标准状况)参加反应,n(SO )=
2 2 2 2 2
6.72 L÷22.4 L·mol-1=0.3 mol,由上述两个反应可知,存在3SO ~Cr O,则最终消耗0.1 mol K Cr O ,故
2 2 2 2 7
B错误;每有1 mol K Cr O 参加反应,转移电子为1 mol×2×(6-3)=6 mol,即转移电子的数目为6N ,故
2 2 7 A
C正确;因氧化性:Cr O>SO,则KCr O 能将NaSO 氧化成NaSO ,故D正确。
2 2 2 2 7 2 3 2 4
10.某同学通过以下流程制取 NaClO 晶体:
2
已知:ClO 浓度过高时易发生分解,NaClO 在温度高于60 ℃时易分解, NaClO 饱和溶液在低于38
2 2 2
℃时析出NaClO·3H O,高于38 ℃时析出 NaClO。
2 2 2
下列说法不正确的是( )
A.步骤①中工业上常用HC O 代替NaSO
2 2 4 2 3
B.步骤②发生反应的离子方程式为2ClO +2OH-+HO===2ClO+O+2HO
2 2 2 2 2C.步骤③的结晶方法为蒸发浓缩,冷却结晶
D.步骤④中制得的NaClO 晶体可用略高于38 ℃的热水洗涤2~3遍
2
【答案】C
【解析】步骤①中NaSO 作为还原剂,HC O 也是常见的还原剂,工业上常用HC O 代替NaSO ,
2 3 2 2 4 2 2 4 2 3
故A正确;步骤②发生的反应为碱性条件下ClO 与双氧水发生氧化还原反应生成ClO、O 和HO,反应的
2 2 2
离子方程式为 2ClO +2OH-+HO===2ClO+O+2HO,故B正确;由于NaClO 在温度高于60 ℃时易分
2 2 2 2 2 2
解,因此结晶方法不可以用蒸发浓缩和冷却结晶的方法,应该用减压蒸发的办法,故C错误;由于NaClO
2
饱和溶液在低于38 ℃时析出NaClO·3H O,高于38 ℃时析出 NaClO ,步骤④中制得的NaClO 晶体中可
2 2 2 2
用略高于38 ℃的热水洗涤2~3遍,故D正确。
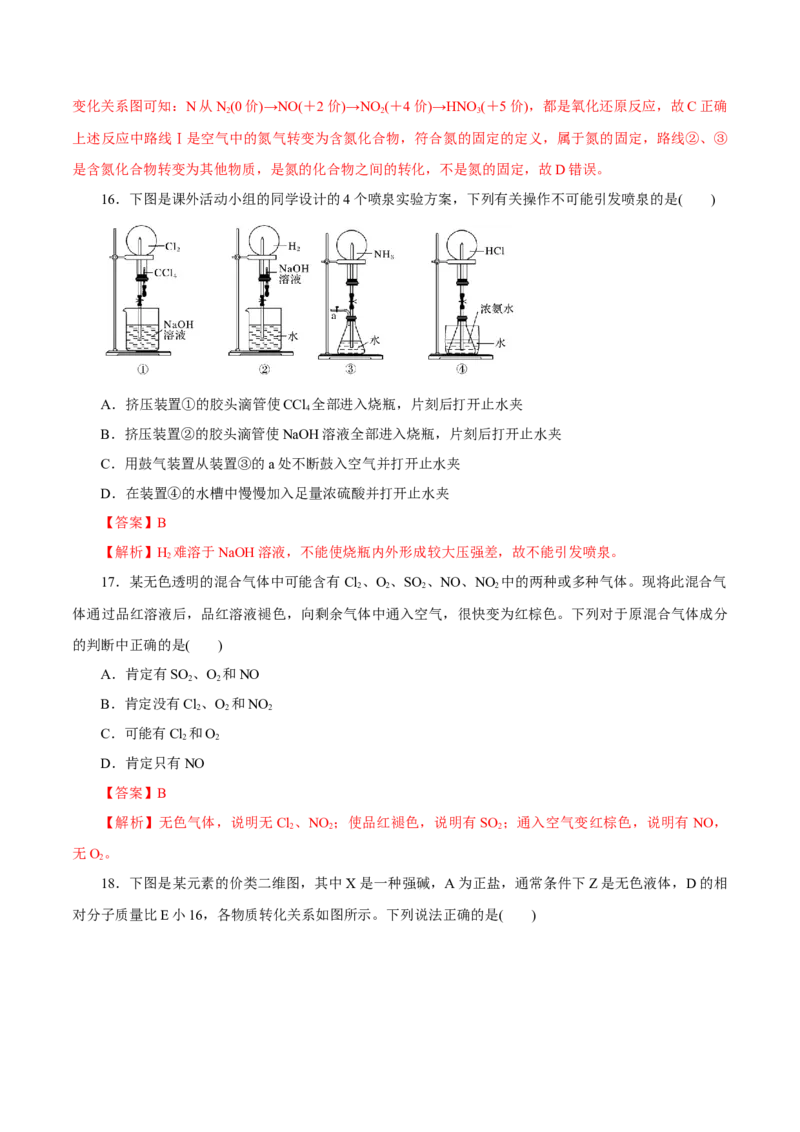
11.硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)说法正确的是( )
A.含硫杆菌及好氧/厌氧菌促进了硫的循环
B.硫循环中硫的化合物均为无机物
C.上述硫循环中硫元素均被氧化
D.烧煤时加石灰石,可减少酸雨及温室气体的排放
【答案】A
【解析】硫酸盐和亚硫酸盐等在含硫杆菌及好氧/厌氧菌作用下缓慢转化成植物R —S—R ,含硫杆菌
1 2
及好氧/厌氧菌促进了硫的循环,故A正确;硫循环中硫的化合物有含硫的有机物,不全是无机物,故 B
错误;含硫杆菌及好氧/厌氧菌将硫酸盐、亚硫酸盐中硫还原成R —S—R ,硫循环中硫元素有时被氧化,
1 2
有时被还原,故C错误;烧煤时加石灰石,可减少酸雨,但生成二氧化碳,会增加温室气体的排放,故D
错误。
12.下列有关氮元素的单质及其化合物的说法错误的是( )
①氮气与氧气在放电条件下可直接生成NO
2
②铵盐都不稳定,受热分解都生成氨气
③向Fe(NO ) 溶液中滴加稀盐酸,无明显变化
3 2
④实验室采用加热氯化铵固体,用碱石灰除去氯化氢的方法制备氨气A.①③④ B.①③
C.①④ D.①②③④
【答案】D
【解析】在放电条件下,氮气与氧气反应生成的是一氧化氮而不是二氧化氮,一氧化氮不稳定,易被
氧气氧化生成二氧化氮,①错误;硝酸铵加强热时剧烈分解发生爆炸生成氮气、二氧化氮和水,②错误;
向硝酸亚铁溶液中加入稀盐酸,酸性条件下,硝酸根离子具有强氧化性,能把亚铁离子氧化成铁离子,同
时自身被还原成一氧化氮,③错误;氯化铵受热易分解,冷却时又生成氯化铵,所以得不到氨气,④错误。
13.某兴趣小组设计用铁粉将NO还原为N(同时生成FeO)。下列说法不正确的是( )
2
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO ,不吸收NO。
2
A.装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d
B.装置E中发生反应的化学方程式为2NO+2Fe=====2FeO+N
2
C.装置D的作用是吸收挥发出来的硝酸和产生的NO
2
D.装置B的作用是干燥,防止水蒸气进入E中干扰反应
【答案】D
【解析】根据实验原理“NO被灼热的铁粉还原为N ,同时生成FeO”,所以首先应制备纯净干燥的
2
NO。利用铜与稀硝酸反应生成NO,由于硝酸具有挥发性,所以制得的NO中会混有硝酸蒸气和产生的
NO ,故先通过装置D除去挥发出的HNO 和产生的NO ,再通过F干燥,得到纯净干燥的NO,然后进入
2 3 2
E中与铁粉反应,最后处理多余的NO,由于NaOH溶液不与NO反应,而浓硝酸可氧化NO生成NO ,所
2
以先通过B氧化NO,再通过C吸收,故上述装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d,
A 项正确;装置 E 中 NO 被灼热的铁粉还原为 N ,同时生成 FeO,反应的化学方程式为 2NO+
2
2Fe=====2FeO+N ,B项正确;装置D盛放的是水,其作用是除去挥发出的HNO 和产生的NO ,C项正
2 3 2
确;装置B盛放的是浓硝酸,可以将NO氧化为NO ,便于氢氧化钠溶液充分吸收,D项错误。
2
14.某学习小组为研究铜与浓、稀HNO 反应的差异,设计了如图所示的实验装置。
3下列说法不正确的是( )
A.反应开始前通入过量的CO 气体,目的是排除装置内的空气
2
B.A中的离子方程式为Cu+2NO+4H+===Cu2++2NO ↑+2HO
2 2
C.当B中0.03 mol铜粉被氧化时,B中产生的NO气体大于0.02 mol
D.C装置中装入一定量的水进行尾气处理
【答案】D
【解析】为便于观察B中生成无色气体,防止NO被氧化,则开始前通入过量的CO 气体,目的是排
2
除装置内的空气,故A正确;A中Cu与浓硝酸反应生成硝酸铜、二氧化氮和水,则离子反应为Cu+2NO
+4H+===Cu2++2HO+2NO ↑,故B正确;B中0.03 mol Cu被氧化时,由电子守恒可知生成NO为=0.02
2 2
mol,且二氧化氮与水反应生成NO,即B中产生的NO气体大于0.02 mol,故C正确;NO与水不反应,
不能用水进行尾气处理,C中应装入NaOH溶液,故D错误。
15.关于氮的变化关系图如图:
则下列说法不正确的是( )
A.路线①②③是工业生产硝酸的主要途径
B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C.上述所有反应都是氧化还原反应
D.上述反应中只有③属于氮的固定
【答案】D
【解析】工业上生产硝酸的流程:氮气和氢气生成氨气,氨气与氧气反应:4NH +5O=====4NO+
3 2
6HO(路线①),一氧化氮与氧气反应:2NO+O===2NO(路线②),二氧化氮被水吸收:3NO +
2 2 2 2
HO===2HNO +NO(路线③),路线①②③是工业生产硝酸的主要途径,故A正确;在放电条件下,氮气
2 3
和氧气发生化合反应:N +O=====2NO(路线Ⅰ);NO 不稳定,易被氧气氧化为二氧化氮:2NO+
2 2
O===2NO(路线Ⅱ),二氧化氮溶于水生成硝酸:3NO +HO===2HNO +NO(路线Ⅲ),故B正确;从氮的
2 2 2 2 3变化关系图可知:N从N(0价)→NO(+2价)→NO (+4价)→HNO(+5价),都是氧化还原反应,故C正确
2 2 3
上述反应中路线Ⅰ是空气中的氮气转变为含氮化合物,符合氮的固定的定义,属于氮的固定,路线②、③
是含氮化合物转变为其他物质,是氮的化合物之间的转化,不是氮的固定,故D错误。
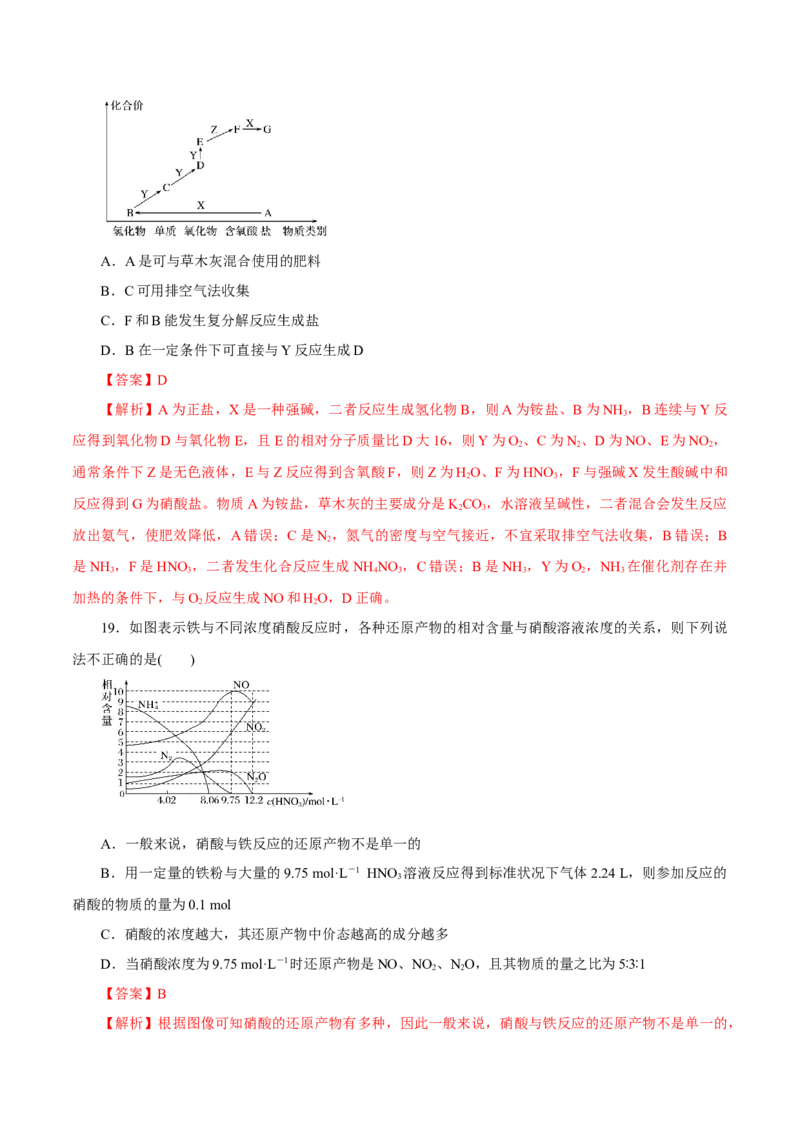
16.下图是课外活动小组的同学设计的4个喷泉实验方案,下列有关操作不可能引发喷泉的是( )
A.挤压装置①的胶头滴管使CCl 全部进入烧瓶,片刻后打开止水夹
4
B.挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹
C.用鼓气装置从装置③的a处不断鼓入空气并打开止水夹
D.在装置④的水槽中慢慢加入足量浓硫酸并打开止水夹
【答案】B
【解析】H 难溶于NaOH溶液,不能使烧瓶内外形成较大压强差,故不能引发喷泉。
2
17.某无色透明的混合气体中可能含有Cl、O、SO 、NO、NO 中的两种或多种气体。现将此混合气
2 2 2 2
体通过品红溶液后,品红溶液褪色,向剩余气体中通入空气,很快变为红棕色。下列对于原混合气体成分
的判断中正确的是( )
A.肯定有SO 、O 和NO
2 2
B.肯定没有Cl、O 和NO
2 2 2
C.可能有Cl 和O
2 2
D.肯定只有NO
【答案】B
【解析】无色气体,说明无Cl 、NO ;使品红褪色,说明有SO ;通入空气变红棕色,说明有NO,
2 2 2
无O。
2
18.下图是某元素的价类二维图,其中X是一种强碱,A为正盐,通常条件下Z是无色液体,D的相
对分子质量比E小16,各物质转化关系如图所示。下列说法正确的是( )A.A是可与草木灰混合使用的肥料
B.C可用排空气法收集
C.F和B能发生复分解反应生成盐
D.B在一定条件下可直接与Y反应生成D
【答案】D
【解析】A为正盐,X是一种强碱,二者反应生成氢化物B,则A为铵盐、B为NH ,B连续与Y反
3
应得到氧化物D与氧化物E,且E的相对分子质量比D大16,则Y为O 、C为N 、D为NO、E为NO ,
2 2 2
通常条件下Z是无色液体,E与Z反应得到含氧酸F,则Z为HO、F为HNO ,F与强碱X发生酸碱中和
2 3
反应得到G为硝酸盐。物质A为铵盐,草木灰的主要成分是KCO ,水溶液呈碱性,二者混合会发生反应
2 3
放出氨气,使肥效降低,A错误;C是N ,氮气的密度与空气接近,不宜采取排空气法收集,B错误;B
2
是NH ,F是HNO ,二者发生化合反应生成NH NO ,C错误;B是NH ,Y为O ,NH 在催化剂存在并
3 3 4 3 3 2 3
加热的条件下,与O 反应生成NO和HO,D正确。
2 2
19.如图表示铁与不同浓度硝酸反应时,各种还原产物的相对含量与硝酸溶液浓度的关系,则下列说
法不正确的是( )
A.一般来说,硝酸与铁反应的还原产物不是单一的
B.用一定量的铁粉与大量的9.75 mol·L-1 HNO 溶液反应得到标准状况下气体2.24 L,则参加反应的
3
硝酸的物质的量为0.1 mol
C.硝酸的浓度越大,其还原产物中价态越高的成分越多
D.当硝酸浓度为9.75 mol·L-1时还原产物是NO、NO 、NO,且其物质的量之比为5∶3∶1
2 2
【答案】B
【解析】根据图像可知硝酸的还原产物有多种,因此一般来说,硝酸与铁反应的还原产物不是单一的,A正确;参加反应的硝酸包括被还原的,以及没有被还原的(转化为硝酸铁),因此参加反应的硝酸的物质
的量大于0.1 mol,B错误;根据图像可知随着硝酸浓度的升高,NO 的含量增大,这说明硝酸的浓度越大,
2
其还原产物中价态越高的成分越多,C正确;根据图像可知当硝酸浓度为9.75 mol·L-1时还原产物是NO、
NO 、NO,且其物质的量之比为10∶6∶2=5∶3∶1,D正确。
2 2
20.从淡化海水中提取溴的流程如下:
下列有关说法不正确的是( )
A.X试剂可用NaSO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:2Br-+Cl===2Cl-+Br
2 2
C.工业上每获得1 mol Br ,需要消耗Cl 44.8 L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏
【答案】C
【解析】NaSO +Br +HO===Na SO +2HBr,A正确;步骤Ⅲ根据氯的非金属性比溴的强,利用置
2 3 2 2 2 4
换反应制取Br ,B正确;反应Ⅰ和反应Ⅲ均使用到Cl ,故制取1 mol Br 消耗2 mol氯气,但未标明氯气
2 2 2
所处的温度和压强,C错误;从浓溴水中提取溴,可利用有机溶剂(如苯)萃取溴,然后分液得到溴的有机
溶液,再经蒸馏可得纯净的溴,D正确。
二、非选择题(本题共4小题,每小题10分,共40分)
21.(10分)水泥是重要的建筑材料。水泥熟料的主要成分为 CaO、SiO ,并含有一定量的铁、铝和
2
镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
__________________,还可以使用____________代替硝酸。
(2)沉淀A的主要成分是__________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为
___________________________________________________________________________
______________________________________________________________________________。
(3)加氨水过程中加热的目的是_____________________________ ______________________。
沉淀B的主要成分为____________、____________(填化学式)。(4)草酸钙沉淀经稀HSO 处理后,用KMnO 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,
2 4 4
滴定反应为:MnO+H++HC O―→Mn2++CO +HO。实验中称取0.400 g水泥样品,滴定时消耗了
2 2 4 2 2
0.050 0 mol·L-1的KMnO 溶液36.00 mL,则该水泥样品中钙元素的质量分数为________。
4
【答案】(1)将样品中可能存在的Fe2+氧化为Fe3+ HO
2 2
(2)SiO SiO+4HF===SiF ↑+2HO (3)防止胶体生成,易于沉淀分离 Al(OH) Fe(OH) (4)45.0%
2 2 4 2 3 3
【解析】(1)水泥样品中含有铁的氧化物。加入盐酸后的溶液中可能含有 Fe3+、Fe2+,Fe2+在pH为4~
5时不能形成沉淀除去,所以需要先加入氧化剂将 Fe2+氧化为Fe3+,故加入硝酸的目的是将样品中可能存
在的Fe2+氧化为Fe3+;双氧水是一种强氧化剂,可将Fe2+氧化为Fe3+,本身被还原为水,不会引入新的杂
质离子,故可用双氧水代替硝酸。
(2)钙、铁、铝和镁等金属的氧化物都能溶于盐酸和硝酸的混合液,而二氧化硅不与盐酸、硝酸反应,
故沉淀A的主要成分为SiO ;二氧化硅可与氢氟酸反应,生成四氟化硅和水,该反应的化学方程式为SiO
2 2
+4HF===SiF ↑+2HO。
4 2
(3)Fe3+和Al3+在pH为4~5时可水解生成氢氧化铁、氢氧化铝,水解过程中会生成氢氧化铁胶体和氢
氧化铝胶体,不利于分离出沉淀,加热可使胶体聚沉,有利于分离出沉淀,所以加热可防止胶体的生成,
易于沉淀分离,故沉淀B的主要成分为Al(OH) 、Fe(OH) 。
3 3
(4)根据化合价升降法、电荷守恒和质量守恒配平可得:2MnO+6H++5HC O===2Mn2++10CO↑+
2 2 4 2
8HO,设含钙的物质的量为x mol,由反应方程式和钙元素守恒可得关系式:
2
5Ca2+ ~ 5HC O ~ 2MnO
2 2 4
5 mol 2 mol
x mol 0.050 0 mol·L-1×36.00×10-3 L
解得x=4.5×10-3,则0.400 g水泥样品中钙元素的质量为4.5×10-3 mol×40 g·mol-1=0.180 g,故该水泥
样品中钙元素的质量分数为×100%=45.0%。
22.(10分)二氧化硫和亚硫酸在工农业生产中具有重要的用途。某化学兴趣小组对 SO 和HSO 的
2 2 3
一些性质进行了探究。
Ⅰ.探究SO 的性质
2
(1)关闭旋塞2,打开旋塞1,注入硫酸至浸没三颈烧瓶中的固体。检验SO 与NaO 反应是否有氧气生
2 2 2成的方法是__________________________________________________________。
(2)装置B中试剂X是________,装置D中NaOH溶液的作用是_________________________。
(3)写出装置C中发生反应的化学方程式:__________________________________________。
(4)关闭旋塞1后,打开旋塞2,装置E中的NaS溶液用于验证SO 的________性,装置F中的现象是
2 2
____________________________________________________________________。
Ⅱ.探究HSO 的酸性强于HClO(可能需要的装置和试剂如图所示)
2 3
(5)所需装置的连接顺序:纯净的 SO ―→________(填字母),装置 K 中反应的离子方程式为
2
______________________________________________________________________________。
(6)能证明HSO 的酸性强于HClO的实验现象是_____________________________________
2 3
_______________________________________________________________________________。
【答案】(1)将带火星的木条放在装置D的试管口,观察木条是否复燃
(2)浓硫酸 吸收未反应的SO 气体,防止污染空气
2
(3)SO +NaO===Na SO
2 2 2 2 4
(4)氧化 溶液红色变浅
(5)HJIK Ca2++2ClO-+CO+HO===CaCO ↓+2HClO
2 2 3
(6)装置I中的品红溶液不褪色,装置K中溶液中出现白色沉淀
【解析】Ⅰ.A中制备二氧化硫:NaSO +HSO (浓)===Na SO +HO+SO ↑,二氧化硫为酸性气体,
2 3 2 4 2 4 2 2
X干燥二氧化硫,选用浓硫酸,C中SO 与NaO 反应,D中氢氧化钠溶液吸收剩余的二氧化硫,防止污染
2 2 2
空气,E装置验证二氧化硫的氧化性,F装置验证二氧化硫为酸性气体,并吸收二氧化硫,防止污染空气。
(1)检验SO 与NaO 反应是否有氧气生成的方法是将带火星的木条放在装置D的试管口,观察木条是否复
2 2 2
燃。
(2)装置B干燥二氧化硫,盛放的试剂X是浓硫酸,D中盛放的NaOH溶液吸收未反应的SO ,防止污
2
染空气。(3)C中SO 与NaO 反应生成NaSO ,反应的化学方程式为SO +NaO===Na SO 。(4)E中为硫
2 2 2 2 4 2 2 2 2 4
化钠与二氧化硫发生价态归中反应生成硫单质,二氧化硫表现氧化性;F装置吸收二氧化硫,二氧化硫为
酸性气体,F中碱性减弱,红色变浅。
Ⅱ.(5)要证明HSO 的酸性强于HClO,因为二氧化硫与次氯酸根离子发生氧化还原反应,不能直接将
2 3
二氧化硫通入漂白粉溶液中,应先用二氧化硫制备二氧化碳,通过证明酸性:HSO >H CO>HClO,从而
2 3 2 3得出结论。将纯净的二氧化硫通过H使二氧化硫和水反应生成亚硫酸,亚硫酸和碳酸氢钠反应制取二氧化
碳,制备的二氧化碳中有二氧化硫,故通入漂白粉溶液之前用酸性高锰酸钾除去二氧化硫气体,再用品红
溶液检验二氧化硫是否除净,再通入漂白粉溶液中,K中反应的离子方程式为Ca2++2ClO-+CO +
2
HO===CaCO ↓+2HClO。(6)I中品红溶液不褪色,K中产生白色沉淀能证明HSO 的酸性强于HClO。
2 3 2 3
23.(10分)某化学研究性学习小组的同学根据理论分析推测出NO具有氧化性,他们设想利用如图
所示装置验证NO的氧化性(已知NO +OH-―→NO+NO+HO,夹持装置已省略)。
2 2
(1)判断 NO 有氧化性的理论依据是________________,本套装置气密性检查较简便的操作是
_______________________________________________________________________________,
装置A中反应的离子方程式为_______________________________________________________。
(2)装置C中试剂X是________,装置B的作用是______________________________________。
(3)本套装置有一个明显的错误,下列分析中正确的是________(填字母)。
A.装置B中导管不应插入液面以下
B.装置E无法吸收NO
C.实验开始后,应不断地向装置E中通入空气
(4)本实验结束时装置D中试管内得到黑色粉末,对黑色粉末的成分,小组的同学提出了不同的看法:
a.是FeO b.是Fe O c.是FeO与Fe O
3 4 3 4
①甲同学认为仅用磁铁就可以确定黑色粉末的成分到底是哪种情况,他判断的依据与结论是
______________________________________________________________________________。
②若用化学方法分析 a 组和 c 组中的黑色粉末,则需要使用三种试剂,这三种试剂是
____________________________________________________________________________。
【答案】(1)NO中氮为+2价,不是氮元素的最低价 关闭分液漏斗活塞,在 E中加水没过导管微热
烧瓶,如果 E 中出现气泡且停止加热后导管中形成一段液柱,则说明气密性良好 3Cu+8H++
2NO===3Cu2++2NO↑+4HO
2
(2)无水CaCl (或其他合理试剂) 吸收装置A中挥发出的HNO(或其他合理答案)
2 3
(3)BC
(4)①若粉末能全部被磁铁吸引,则 b对;若完全不能被吸引,则 a对;若部分能被吸引,则 c对
②HCl、KSCN、K[Fe(CN) ](或稀硫酸、酸性KMnO 溶液、KSCN)
3 6 4【解析】(2)装置C是干燥装置,可用无水CaCl 、PO 等试剂干燥NO。硝酸是挥发性酸,对后续反应
2 2 5
会产生干扰,故装置B的作用是用于吸收装置A中挥发出的HNO 。(3)因要吸收HNO(g),故装置B中导
3 3
管应插入液面下,A项错误;NO是不成盐氧化物,不能与碱反应,B项正确;通入空气后NO被O 氧化
2
为NO ,NO 可被NaOH溶液吸收(或者在O 存在的条件下,NO、O 、OH-反应生成盐),C项正确。(4)①
2 2 2 2
可根据Fe O 能被磁铁吸引,FeO不能被磁铁吸引的性质判断。②用化学方法分析时,先用非氧化性酸将
3 4
固体溶解,然后用KSCN检验有无Fe3+,用K[Fe(CN) ](或酸性KMnO 溶液)检验有无Fe2+,但由于酸性
3 6 4
KMnO 溶液能氧化Cl-,故当用盐酸溶解固体时,不能使用KMnO 溶液。
4 4
24.(10分)三氯化碘(ICl )在药物合成中用途非常广泛。已知ICl 的熔点为33 ℃,沸点为73 ℃,有
3 3
吸湿性,遇水易水解。某小组同学用下列装置制取ICl (部分夹持和加热装置省略)。
3
(1)按照气流方向连接接口顺序为a→______________。
装置A中导管m的作用是_____________________________________________________。
(2)装置C用于除杂,同时作为安全瓶,能监测实验进行时后续装置是否发生堵塞,若发生堵塞,C中
的现象为_____________________________________________________。
(3)氯气与单质碘需在温度稍低于70 ℃下反应,则装置E适宜的加热方式为______________。
装置E中发生反应的化学方程式:________________________________________________。
(4)该装置存在的明显缺陷是______________________________________________________。
【答案】(1)d→e→b→c→g→h→f(接口b与c、g与h可互换) 使浓盐酸顺利滴下 (2)锥形瓶中液面下
降,长颈漏斗中液面上升 (3)水浴加热 3Cl+I=====2ICl (4)缺少尾气处理装置
2 2 3
【解析】(1)在装置A中用浓盐酸与MnO 混合加热制取Cl,浓盐酸易挥发,制取的氯气中会含有氯化
2 2
氢、水蒸气等杂质,通过装置C除去HCl杂质,再通过装置B干燥,得到干燥、纯净的氯气,然后在装置
E中氯气与碘单质反应制得ICl ;为防止ICl 水解,在E后面连接盛有干燥剂的装置D,防止空气中的水蒸
3 3
气进入E装置。故按照气流方向连接装置接口顺序为:a→d→e→b→c→g→h→f,(接口b与c、g与h可互
换);在装置A中导管m使分液漏斗中的液体上下压强一致,这样分液漏斗中的浓盐酸可以顺利滴下。
(2)装置C也是安全瓶,监测实验E中是否发生堵塞,若装置E发生堵塞,则C中气体压强增大,液体
会进入长颈漏斗中,使锥形瓶中液面下降,长颈漏斗中液面上升。
(3)因水浴加热能简便控制加热的温度,且能使反应装置受热均匀,又因为氯气与单质碘需在温度稍低于 70 ℃下反应,故应采取水浴加热的方式;在装置 E 中 Cl 与 I 在低于 70 ℃下发生反应:3Cl +
2 2 2
I=====2ICl 。
2 3
(4)Cl 是有毒气体,通过盛有无水氯化钙的干燥管只能吸收水分,不能吸收氯气,这样就会造成大气
2
污染,故该装置的缺陷是缺少尾气处理装置。