文档内容
(新高考)2021 届高考考前冲刺卷
【解析】A.1mol FeSO ·7H O的质量为296g,失去全部结晶水,质量减少 ,
4 2
化 学(六)
,所以“炒”矾时绿矾没有失去全部结晶水,A项错误;B.强水是指硝酸,加入盐后
注意事项:
形成王水,金能溶于王水,B项正确;C.硝是KNO,含有K+,K+的焰色试验中透过钴玻璃观察到火焰
3
1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴
呈紫色,C项正确;D.开坛则药化为水,而锅亦坏矣,铁被硝酸氧化为Fe3+,是氧化还原反应,D项正
在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写 确;答案选A。
在试题卷、草稿纸和答题卡上的非答题区域均无效。 3.设N 为阿伏加德罗常数的值。下列有关叙述正确的是
A
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿纸和 A.标准状况下,11.2L H18O中含有的中子数为5N
2 A
答题卡上的非答题区域均无效。
B.含1mol HNO 的浓硝酸与足量的Cu反应转移电子数为N
3 A
4.考试结束后,请将本试题卷和答题卡一并上交。
C.2mol NO与lmol O 充分反应后得到的分子数小于2N
2 A
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
D.0.2mol蔗糖完全水解,生成的葡萄糖中含羟基数目为2N
A
【答案】C
一、选择题:每小题3分,共42分。每小题给出的四个选项中,只有一项是符合题目要求的。
【解析】A.标准状况下,水的状态不是气体,不能使用标准状况下的气体摩尔体积计算水的物质的
1.港珠澳大桥是中国建桥史上的又一伟大成就,下列有关说法错误的是
量,A项错误;B.反应过程中浓硝酸变稀,产物是二氧化氮和一氧化氮的混合物,所以反应转移电子
A.用于大桥建设的桥梁钢为合金材料,具有强度大、耐腐蚀等性能
数不是N ,B项错误;C.NO和O 反应生成NO 中存在平衡2NO NO,导致分子数减少,故所
B.用于大桥信息传输的光导纤维主要成分是硅酸盐 A 2 2 2 2 4
得产物分子数小于2N ,C项正确;D.0.2mol蔗糖完全水解生成0.2mol葡萄糖和0.2mol果糖,1mol
C.用于铺设路面的沥青来自石油的分馏 A
葡萄糖含有5mol羟基,即0.2mol葡萄糖含有羟基数为N ,D项错误;答案选C。
D.用于人工岛环岛跃浪沟的热塑长纤维属于高分子材料 A
4.下列实验装置设计正确且能达到目的的是
【答案】B
【解析】A.钢为铁碳合金,属于金属材料,强度大、耐腐蚀,A正确;B.光导纤维主要成分是二氧化
硅,B错误;C.石油分馏可以得到汽油、柴油、润滑油和沥青等馏分,C正确;D.热塑长纤维为纤维的
一种,属于高分子材料,D正确;故选B。
2.中华文化源远流长,对人类进步和社会发展有着巨大影响。《徐光启手记》中载有强水的制备方法:
A.实验I:制取氯气
“绿矾FeSO ·7H O五斤,硝KNO 五斤。将矾炒去,(质量)约折五分之一。将二味同研细,用铁作
4 2 3
B.实验II:加热熔融NaCl固体
锅,锅下起火……,开坛则药化为水,而锅亦坏矣。用水入五金皆成水,惟黄金不化水中,加盐
C.实验III:分离乙酸乙酯和乙醚的混合物
(NaCl)则化……”。下列相关说法错误的是
D.实验IV:证明非金属性:C>Si
A.“炒”矾时绿矾失去全部结晶水
【答案】C
B.强水中加盐后形成王水能溶解金
【解析】A.制取氯气时应使用分液漏斗,防止氯气溢出,故A错误;B.酒精灯火焰的温度低,不能
C.硝的焰色试验中火焰呈紫色
使氯化钠融化,并且不能用玻璃棒搅拌,B错误;C.蒸馏时温度计水银球处于蒸馏烧瓶支管出口处附
D.制备强水过程中涉及氧化还原反应
近,冷凝水需下进上出,C正确;D.盐酸有挥发性,生成的CO 中混有HCl,此装置不能证明碳酸酸性
2
【答案】A
强于硅酸,D错误。故选C。
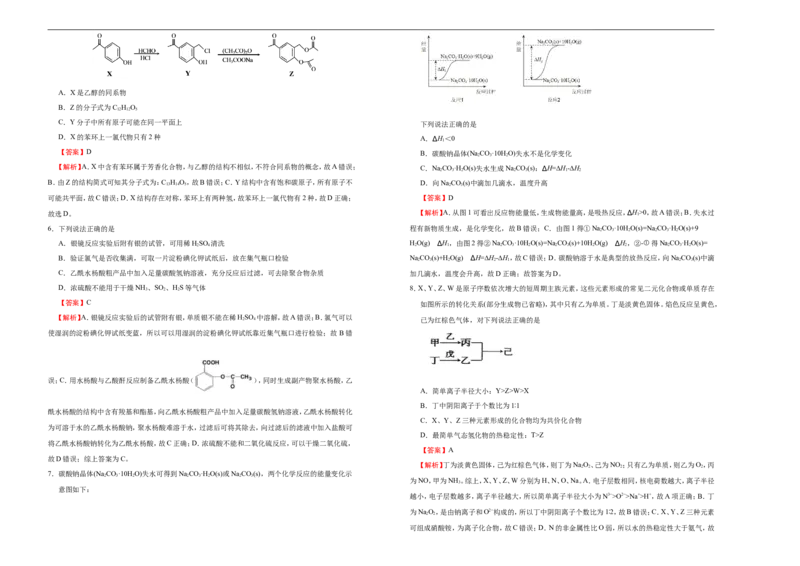
5.Z是合成喘药沙丁胺醇的中间体,可由如下路线合成。下列叙述正确的是
封密不订装只卷此
号位座
号场考
号证考准
名姓
级班A.X是乙醇的同系物
B.Z的分子式为C H O
12 12 5
C.Y分子中所有原子可能在同一平面上 下列说法正确的是
D.X的苯环上一氯代物只有2种 A.∆H<0
1
【答案】D B.碳酸钠晶体(Na CO·10H O)失水不是化学变化
2 3 2
【解析】A.X中含有苯环属于芳香化合物,与乙醇的结构不相似,不符合同系物的概念,故A错误; C.NaCO·H O(s)失水生成NaCO(s):∆H=∆H-∆H
2 3 2 2 3 1 2
B.由Z的结构简式可知其分子式为:C H O,故B错误;C.Y结构中含有饱和碳原子,所有原子不 D.向NaCO(s)中滴加几滴水,温度升高
13 14 5 2 3
可能共平面,故C错误;D.X结构存在对称,苯环上有两种氢,故苯环上一氯代物有2种,故D正确; 【答案】D
故选D。 【解析】A.从图1可看出反应物能量低,生成物能量高,是吸热反应,∆H 1 >0,故A错误;B.失水过
6.下列说法正确的是 程有新物质生成,是化学变化,故B错误;C.由图1得①NaCO·10HO(s)=NaCO·H O(s)+9
2 3 2 2 3 2
A.银镜反应实验后附有银的试管,可用稀HSO 清洗 HO(g) ∆H,由图2得②NaCO·10HO(s)=NaCO(s)+10HO(g) ∆H,②-①得NaCO·H O(s)=
2 4 2 1 2 3 2 2 3 2 2 2 3 2
B.验证氯气是否收集满,可取一片淀粉碘化钾试纸后,放在集气瓶口检验 NaCO(s)+HO(g) ∆H=∆H-∆H,故C错误;D.碳酸钠溶于水是典型的放热反应,向NaCO(s)中滴
2 3 2 2 1 2 3
C.乙酰水杨酸粗产品中加入足量碳酸氢钠溶液,充分反应后过滤,可去除聚合物杂质 加几滴水,温度会升高,故D正确;故答案为D。
D.浓硫酸不能用于干燥NH 、SO 、HS等气体 8.X、Y、Z、W是原子序数依次增大的短周期主族元素,这些元素形成的常见二元化合物或单质存在
3 2 2
【答案】C 如图所示的转化关系(部分生成物已省略),其中只有乙为单质。丁是淡黄色固体。焰色反应呈黄色,
【解析】A.银镜反应实验后的试管附有银,单质银不能在稀HSO 中溶解,故A错误;B.氯气可以
2 4 已为红棕色气体,对下列说法正确的是
使湿润的淀粉碘化钾试纸变蓝,所以可以用湿润的淀粉碘化钾试纸靠近集气瓶口进行检验;故 B错
误;C.用水杨酸与乙酸酐反应制备乙酰水杨酸( ),同时生成副产物聚水杨酸,乙
A.简单离子半径大小:Y>Z>W>X
B.丁中阴阳离子于个数比为1∶1
酰水杨酸的结构中含有羧基和酯基,向乙酰水杨酸粗产品中加入足量碳酸氢钠溶液,乙酰水杨酸转化
C.X、Y、Z三种元素形成的化合物均为共价化合物
为可溶于水的乙酰水杨酸钠,聚水杨酸难溶于水,过滤后可将其除去,向过滤后的滤液中加入盐酸可
D.最简单气态氢化物的热稳定性:T>Z
将乙酰水杨酸钠转化为乙酰水杨酸,故C正确;D.浓硫酸不能和二氧化硫反应,可以干燥二氧化硫,
【答案】A
故D错误;综上答案为C。
【解析】丁为淡黄色固体,己为红棕色气体,则丁为NaO、己为NO ;只有乙为单质,则乙为O,丙
2 2 2 2
7.碳酸钠晶体(Na CO·10H O)失水可得到NaCO·H O(s)或NaCO(s),两个化学反应的能量变化示
2 3 2 2 3 2 2 3
为NO,甲为NH 。综上,X、Y、Z、W分别为H、N、O、Na。A.电子层数相同,核电荷数越大,离子半径
3
意图如下:
越小,电子层数越多,离子半径越大,所以简单离子半径大小为N3−>O2−>Na+>H+,故A项正确;B.丁
为NaO,是由钠离子和O2−构成的,所以丁中阴阳离子个数比为1∶2,故B错误;C.X、Y、Z三种元素
2 2
可组成硝酸铵,为离子化合物,故C错误;D.N的非金属性比O弱,所以水的热稳定性大于氨气,故D错误;答案选A。
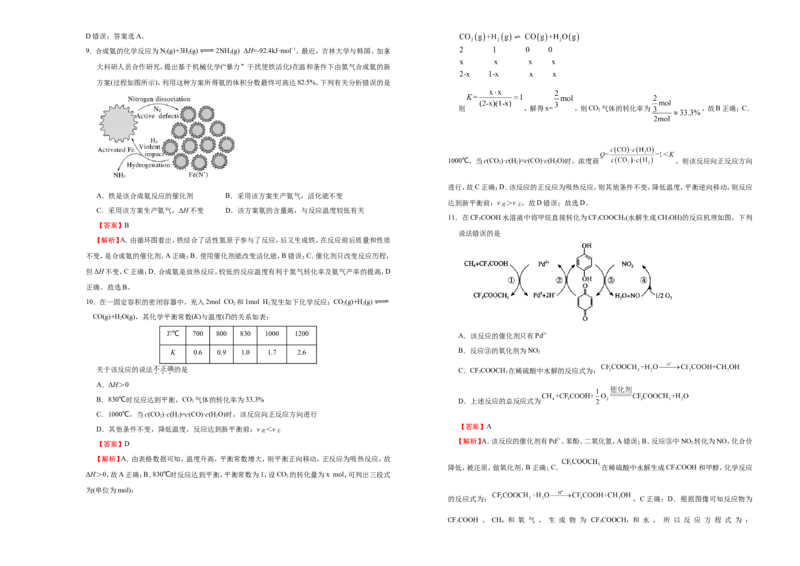
9.合成氨的化学反应为N(g)+3H(g) 2NH (g) ΔH=-92.4kJ·mol−1。最近,吉林大学与韩国、加拿
2 2 3
大科研人员合作研究,提出基于机械化学(“暴力”干扰使铁活化)在温和条件下由氮气合成氨的新
方案(过程如图所示),利用这种方案所得氨的体积分数最终可高达82.5%。下列有关分析错误的是
则 ,解得x= ,则CO 气体的转化率为 ,故B正确;C.
2
1000℃,当c(CO)·c(H )=c(CO)·c(H O)时,浓度商 ,则该反应向正反应方向
2 2 2
进行,故C正确;D.该反应的正反应为吸热反应,则其他条件不变,降低温度,平衡逆向移动,则反应
A.铁是该合成氨反应的催化剂 B.采用该方案生产氨气,活化能不变
达到新平衡前:v >v ,故D错误;故选D。
逆 正
C.采用该方案生产氨气,ΔH不变 D.该方案氨的含量高,与反应温度较低有关
11.在CFCOOH水溶液中将甲烷直接转化为CFCOOCH (水解生成CHOH)的反应机理如图,下列
3 3 3 3
【答案】B
说法错误的是
【解析】A.由循环图看出,铁结合了活性氮原子参与了反应,后又生成铁,在反应前后质量和性质
不变,是合成氨的催化剂,A正确;B.使用催化剂能改变活化能,B错误;C.催化剂只改变反应历程,
但ΔH不变,C正确;D.合成氨是放热反应,较低的反应温度有利于氮气转化率及氨气产率的提高,D
正确。故选B。
10.在一固定容积的密闭容器中,充入2mol CO 和1mol H 发生如下化学反应:CO(g)+H(g)
2 2 2 2
CO(g)+HO(g),其化学平衡常数(K)与温度(T)的关系如表:
2
T/℃ 700 800 830 1000 1200 A.该反应的催化剂只有Pd2+
K 0.6 0.9 1.0 1.7 2.6 B.反应③的氧化剂为NO 2
关于该反应的说法不正确的是
C.CFCOOCH 在稀硫酸中水解的反应式为:
3 3
A.ΔH>0
B.830℃时反应达到平衡,CO 2 气体的转化率为33.3% D.上述反应的总反应式为
C.1000℃,当c(CO)·c(H )=c(CO)·c(H O)时,该反应向正反应方向进行
2 2 2
【答案】A
D.其他条件不变,降低温度,反应达到新平衡前:v <v
逆 正
【解析】A.该反应的催化剂有Pd2+、苯酚、二氧化氮,A错误;B.反应③中NO 转化为NO,化合价
【答案】D 2
【解析】A.由表格数据可知,温度升高,平衡常数增大,则平衡正向移动,正反应为吸热反应,故
降低,被还原,做氧化剂,B正确;C. 在稀硫酸中水解生成CFCOOH和甲醇,化学反应
3
ΔH>0,故A正确;B.830℃时反应达到平衡,平衡常数为1,设CO 的转化量为x mol,可列出三段式
2
为(单位为mol):
的反应式为: ,C正确;D.根据图像可知反应物为
CFCOOH 、 CH 和 氧 气 , 生 成 物 为 CFCOOCH 和 水 , 所 以 反 应 方 程 式 为 :
3 4 3 3C.每生成1mol ,阴极区消耗3mol H+
,D正确;答案选A。
D.起始时,若在Y电极附近加入适量Fe3+,装置不能正常工作
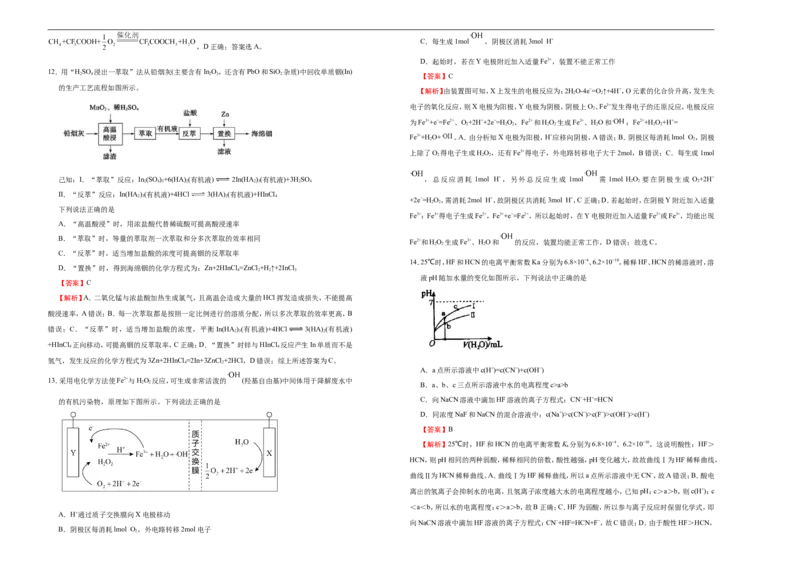
12.用“HSO 浸出一萃取”法从铅烟灰(主要含有InO,还含有PbO和SiO 杂质)中回收单质铟(In)
2 4 2 3 2 【答案】C
的生产工艺流程如图所示。
【解析】由装置图可知,X上发生的电极反应为:2HO-4e−=O ↑+4H+,O元素的化合价升高,发生失
2 2
电子的氧化反应,则X电极为阳极,Y电极为阴极,阴极上O、Fe3+发生得电子的还原反应,电极反应
2
为Fe3++e−=Fe2+、O+2H++2e−=H O,Fe2+ 和HO 生成Fe3+、HO和 :Fe2++H O+H+=
2 2 2 2 2 2 2 2
Fe3++H O+ 。A.由分析知X电极为阳极,H+应移向阴极,A错误;B.阴极区每消耗lmol O,阴极
2 2
上除了O 得电子生成HO,还有Fe3+得电子,外电路转移电子大于2mol,B错误;C.每生成1mol
2 2 2
己知:I.“萃取”反应:In(SO )+6(HA) (有机液) 2In(HA )(有机液)+3H SO ,总反应消耗 1mol H+,另外总反应生成 1mol 需 1mol HO 要在阴极生成 O+2H+
2 4 3 2 2 3 2 4 2 2 2
II.“反萃”反应:In(HA )(有机液)+4HCl 3(HA) (有机液)+HInCl
2 3 2 4
+2e−=H O,需消耗2mol H+,故阴极区共消耗3mol H+,C正确;D.若起始时,在阴极Y附近加入适量
2 2
下列说法正确的是
Fe3+:Fe3+得电子生成Fe2+,Fe3++e−=Fe2+,所以起始时,在Y电极附近加入适量Fe2+或Fe3+,均能出现
A.“高温酸浸”时,用浓盐酸代替稀硫酸可提高酸浸速率
B.“萃取”时,等量的萃取剂一次萃取和分多次萃取的效率相同
Fe2+和HO 生成Fe3+、HO和 的反应,装置均能正常工作,D错误;故选C。
2 2 2
C.“反萃”时,适当增加盐酸的浓度可提高铟的反萃取率
14.25℃时,HF和HCN的电离平衡常数Ka分别为6.8×10−4、6.2×10−10,稀释HF、HCN的稀溶液时,溶
D.“置换”时,得到海绵铟的化学方程式为:Zn+2HInCl =ZnCl +H ↑+2InCl
4 2 2 3
液pH随加水量的变化如图所示,下列说法中正确的是
【答案】C
【解析】A.二氧化锰与浓盐酸加热生成氯气,且高温会造成大量的HCl挥发造成损失,不能提高
酸浸速率,A错误;B.每一次萃取都是按照一定比例进行的溶质分配,所以多次萃取的效率更高,B
错误;C.“反萃”时,适当增加盐酸的浓度,平衡In(HA )(有机液)+4HCl 3(HA) (有机液)
2 3 2
+HInCl 正向移动,可提高铟的反萃取率,C正确;D.“置换”时锌与HInCl 反应产生In单质而不是
4 4
氢气,发生反应的化学方程式为3Zn+2HInCl =2In+3ZnCl +2HCl,D错误;综上所述答案为C。
4 2
A.a点所示溶液中c(H+)=c(CN−)+c(OH−)
13.采用电化学方法使Fe2+与HO 反应,可生成非常活泼的 (羟基自由基)中间体用于降解废水中
2 2 B.a、b、c三点所示溶液中水的电离程度c>a>b
的有机污染物,原理如下图所示。下列说法正确的是
C.向NaCN溶液中滴加HF溶液的离子方程式:CN−+H+=HCN
D.同浓度NaF和NaCN的混合溶液中:c(Na+)>c(CN−)>c(F−)>c(OH−)>c(H+)
【答案】B
【解析】25℃时,HF和HCN的电离平衡常数K 分别为6.8×10−4、6.2×10−10,这说明酸性:HF>
a
HCN,则pH相同的两种弱酸,稀释相同的倍数,酸性越强,pH变化越大,故故曲线Ⅰ为HF稀释曲线,
曲线Ⅱ为HCN稀释曲线。A.曲线Ⅰ为HF稀释曲线,所以a点所示溶液中无CN−,故A错误;B.酸电
离出的氢离子会抑制水的电离,且氢离子浓度越大水的电离程度越小,已知pH:c>a>b,则c(H+):c
<a<b,所以水的电离程度:c>a>b,故B正确;C.HF为弱酸,所以参与离子反应时保留化学式,即
A.H+通过质子交换膜向X电极移动
向NaCN溶液中滴加HF溶液的离子方程式:CN−+HF=HCN+F−,故C错误;D.由于酸性HF>HCN,
B.阴极区每消耗lmol O,外电路转移2mol电子
2则相同条件下水解程度:CN−>F−,则溶液中的离子浓度:F−>CN−,由于两者都水解,溶液显碱性,故
混合溶液中离子浓度由大到小的顺序为:c(Na+)>c(F−)>c(CN−)>
c(OH−)>c(H+),故D错误。答案选B。
二、非选择题:包括必考题和选考题两部分。第15题~第17题为必考题,每个试题考生都必须作答。
第18题~第19题为选考题,考生根据要求做答。
(一)必考题:共43分。
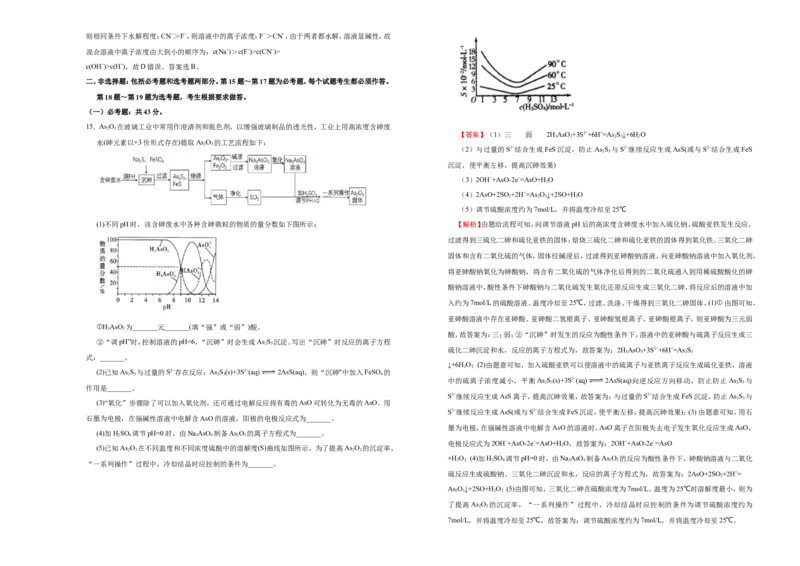
15.As O 在玻璃工业中常用作澄清剂和脱色剂,以增强玻璃制品的透光性,工业上用高浓度含砷废
2 3
【答案】(1)三 弱 2HAsO +3S2−+6H+=AsS↓+6H O
3 3 2 3 2
水(砷元素以+3价形式存在)提取As O 的工艺流程如下:
2 3
(2)与过量的S2−结合生成FeS沉淀,防止As S 与S2−继续反应生成AsS(或与S2−结合生成FeS
2 3
沉淀,使平衡左移,提高沉砷效果)
(3)2OH−+AsO-2e−=AsO+H O
2
(4)2AsO+2SO +2H+=AsO↓+2SO+H O
2 2 3 2
(5)调节硫酸浓度约为7mol/L,并将温度冷却至25℃
(1)不同pH时,该含砷废水中各种含砷微粒的物质的量分数如下图所示: 【解析】由题给流程可知,向调节溶液pH后的高浓度含砷废水中加入硫化钠、硫酸亚铁发生反应,
过滤得到三硫化二砷和硫化亚铁的固体;焙烧三硫化二砷和硫化亚铁的固体得到氧化铁、三氧化二砷
固体和含有二氧化硫的气体,固体经碱浸后,过滤得到亚砷酸钠溶液,向亚砷酸钠溶液中加入氧化剂,
将亚砷酸钠氧化为砷酸钠,将含有二氧化硫的气体净化后得到的二氧化硫通入到用稀硫酸酸化的砷
酸钠溶液中,酸性条件下砷酸钠与二氧化硫发生氧化还原反应生成三氧化二砷,将反应后的溶液中加
入约为7mol/L的硫酸溶液、温度冷却至25℃,过滤、洗涤、干燥得到三氧化二砷固体。(1)①由图可知,
亚砷酸溶液中存在亚砷酸、亚砷酸二氢根离子、亚砷酸氢根离子、亚砷酸根离子,则亚砷酸为三元弱
①HAsO 为_______元_______(填“强”或“弱”)酸。
3 3
酸,故答案为:三;弱;②“沉砷”时发生的反应为酸性条件下,溶液中的亚砷酸与硫离子反应生成三
②“调pH”时,控制溶液的pH=6,“沉砷”时会生成As S 沉淀。写出“沉砷”时反应的离子方程
2 3
硫化二砷沉淀和水,反应的离子方程式为,故答案为:2HAsO +3S2−+6H+=AsS
3 3 2 3
式:_______。
↓+6H O;(2)由题意可知,加入硫酸亚铁可以使溶液中的硫离子与亚铁离子反应生成硫化亚铁,溶液
2
(2)已知As S 与过量的S2−存在反应:As S(s)+3S2−(aq) 2AsS(aq),则“沉砷"中加入FeSO 的
2 3 2 3 4
中的硫离子浓度减小,平衡As S(s)+3S2−(aq) 2AsS(aq)向逆反应方向移动,防止防止As S 与
2 3 2 3
作用是_______。
S2−继续反应生成AsS离子,提高沉砷效果,故答案为:与过量的S2−结合生成FeS沉淀,防止As S 与
2 3
(3)“氧化”步骤除了可以加入氧化剂,还可通过电解反应将有毒的AsO可转化为无毒的AsO。用
S2−继续反应生成AsS(或与S2−结合生成FeS沉淀,使平衡左移,提高沉砷效果);(3) 由题意可知,用石
石墨为电极,在强碱性溶液中电解含AsO的溶液,阳极的电极反应式为_______。
墨为电极,在强碱性溶液中电解含AsO的溶液时,AsO离子在阳极失去电子发生氧化反应生成AsO,
(4)加HSO 调节pH=0时,由NaAsO 制备As O 的离子方程式为_______。
2 4 3 4 2 3
电极反应式为2OH−+AsO-2e−=AsO+H O,故答案为:2OH−+AsO-2e−=AsO
(5)已知As O 在不同温度和不同浓度硫酸中的溶解度(S)曲线如图所示,为了提高As O 的沉淀率, 2
2 3 2 3
+H O;(4)加HSO 调节pH=0时,由NaAsO 制备As O 的反应为酸性条件下,砷酸钠溶液与二氧化
2 2 4 3 4 2 3
“一系列操作”过程中,冷却结晶时应控制的条件为_______。
硫反应生成硫酸钠、三氧化二砷沉淀和水,反应的离子方程式为,故答案为:2AsO+2SO +2H+=
2
As O↓+2SO+H O;(5)由图可知,三氧化二砷在硫酸浓度为7mol/L、温度为25℃时溶解度最小,则为
2 3 2
了提高As O 的沉淀率,“一系列操作”过程中,冷却结晶时应控制的条件为调节硫酸浓度约为
2 3
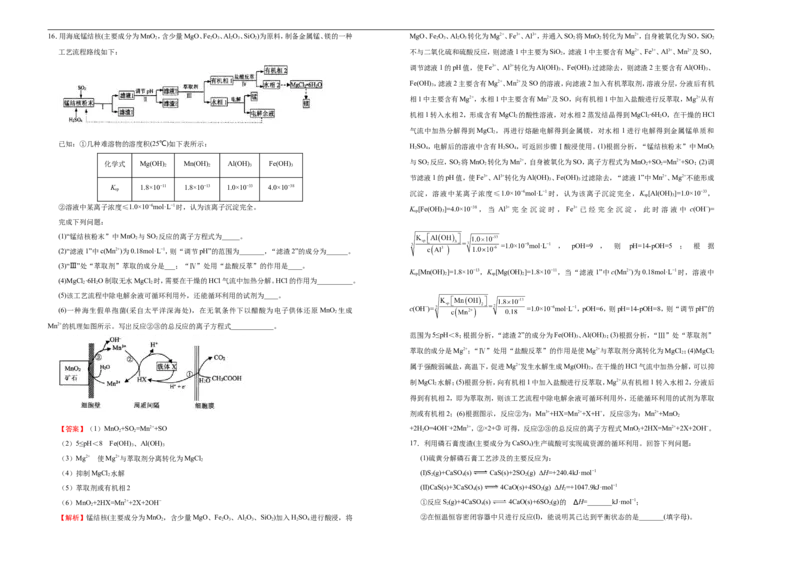
7mol/L,并将温度冷却至25℃,故答案为:调节硫酸浓度约为7mol/L,并将温度冷却至25℃。16.用海底锰结核(主要成分为MnO ,含少量MgO、Fe O、Al O、SiO)为原料,制备金属锰、镁的一种 MgO、Fe O、Al O 转化为Mg2+、Fe3+、Al3+,并通入SO 将MnO 转化为Mn2+,自身被氧化为SO,SiO
2 2 3 2 3 2 2 3 2 3 2 2 2
工艺流程路线如下: 不与二氧化硫和硫酸反应,则滤渣1中主要为SiO,滤液1中主要含有Mg2+、Fe3+、Al3+、Mn2+及SO,
2
调节滤液1的pH值,使Fe3+、Al3+转化为Al(OH) 、Fe(OH) 过滤除去,则滤渣2主要含有Al(OH) 、
3 3 3
Fe(OH) ,滤液2主要含有Mg2+、Mn2+及SO的溶液,向滤液2加入有机萃取剂,溶液分层,分液后有机
3
相1中主要含有Mg2+,水相1中主要含有Mn2+及SO,向有机相1中加入盐酸进行反萃取,Mg2+从有
机相1转入水相2,形成含有MgCl 的酸性溶液,对水相2蒸发结晶得到MgCl ∙6H O,在干燥的HCl
2 2 2
气流中加热分解得到MgCl ,再进行熔融电解得到金属镁,对水相 1进行电解得到金属锰单质和
2
已知:①几种难溶物的溶度积(25℃)如下表所示:
HSO ,电解后的溶液中含有HSO ,可返回步骤Ⅰ酸浸使用。(1)根据分析,“锰结核粉末”中MnO
2 4 2 4 2
化学式 Mg(OH) 2 Mn(OH) 2 Al(OH) 3 Fe(OH) 3 与SO 2 反应,SO 2 将MnO 2 转化为Mn2+,自身被氧化为SO,离子方程式为MnO 2 +SO 2 =Mn2++SO;(2)调
节滤液1的pH值,使Fe3+、Al3+转化为Al(OH) 、Fe(OH) 过滤除去,“滤液1”中Mn2+、Mg2+不能形成
3 3
K 1.8×10−11 1.8×10−13 1.0×10−33 4.0×10−38
sp
沉淀,溶液中某离子浓度≤1.0×10−6mol·L−1时,认为该离子沉淀完全,K [Al(OH) ]=1.0×10−33,
sp 3
②溶液中某离子浓度≤1.0×10−6mol·L−1时,认为该离子沉淀完全。
K [Fe(OH) ]=4.0×10−38,当 Al3+完全沉淀时, Fe3+已经完全沉淀,此时溶 液中 c(OH−)=
sp 3
完成下列问题:
(1)“锰结核粉末”中MnO 与SO 反应的离子方程式为_____。
2 2
=1.0×10−9mol·L−1 , pOH=9 , 则 pH=14-pOH=5 ; 根 据
(2)“滤液1”中c(Mn2+)为0.18mol·L−1,则“调节pH”的范围为_______,“滤渣2”的成分为______。
(3)“Ⅲ”处“萃取剂”萃取的成分是___;“Ⅳ”处用“盐酸反萃”的作用是____。
K [Mn(OH) ]=1.8×10−13,K [Mg(OH) ]=1.8×10−11,当“滤液1”中c(Mn2+)为0.18mol·L−1时,溶液中
sp 2 sp 2
(4)MgCl ·6H O制取无水MgCl 时,需要在干燥的HCl气流中加热分解。HCl的作用为__________。
2 2 2
(5)该工艺流程中除电解余液可循环利用外,还能循环利用的试剂为____。
(6)一种海生假单孢菌(采自太平洋深海处),在无氧条件下以醋酸为电子供体还原MnO 生成
c(OH−)= =1.0×10−6mol·L−1,pOH=6,则pH=14-pOH=8,则“调节pH”的
2
Mn2+的机理如图所示。写出反应②③的总反应的离子方程式____________。
范围为5≤pH<8;根据分析,“滤渣2”的成分为Fe(OH) 、Al(OH) ;(3)根据分析,“Ⅲ”处“萃取剂”
3 3
萃取的成分是Mg2+;“Ⅳ”处用“盐酸反萃”的作用是使Mg2+与萃取剂分离转化为MgCl ;(4)MgCl
2 2
属于强酸弱碱盐,高温下,促进Mg2+发生水解生成Mg(OH) ,在干燥的HCl气流中加热分解,可以抑
2
制MgCl 水解;(5)根据分析,向有机相1中加入盐酸进行反萃取,Mg2+从有机相1转入水相2,分液后
2
得到有机相2,即为萃取剂,则该工艺流程中除电解余液可循环利用外,还能循环利用的试剂为萃取
剂或有机相2;(6)根据图示,反应②为:Mn3++HX=Mn2++X+H+,反应③为:Mn2++MnO
2
【答案】(1)MnO +SO=Mn2++SO +2H O=4OH−+2Mn3+,②×2+③可得,反应②③的总反应的离子方程式MnO +2HX=Mn2++2X+2OH−。
2 2 2 2
(2)5≤pH<8 Fe(OH) 、Al(OH) 17.利用磷石膏废渣(主要成分为CaSO)生产硫酸可实现硫资源的循环利用。回答下列问题:
3 3 4
(3)Mg2+ 使Mg2+与萃取剂分离转化为MgCl (1)硫黄分解磷石膏工艺涉及的主要反应为:
2
(4)抑制MgCl 水解 (I)S (g)+CaSO (s) CaS(s)+2SO (g) ∆H=+240.4kJ·mol−1
2 2 4 2
(5)萃取剂或有机相2 (II)CaS(s)+3CaSO (s) 4CaO(s)+4SO (g) ∆H=+1047.9kJ·mol−1
4 2 2
(6)MnO +2HX=Mn2++2X+2OH− ①反应S(g)+4CaSO (s) 4CaO(s)+6SO (g)的 ∆H=_______kJ·mol−1;
2 2 4 2
【解析】锰结核(主要成分为MnO ,含少量MgO、Fe O、Al O、SiO)加入HSO 进行酸浸,将 ②在恒温恒容密闭容器中只进行反应(I),能说明其已达到平衡状态的是_______(填字母)。
2 2 3 2 3 2 2 4A.v (SO )=2v (S ) B.气体中含硫原子总数不随时间变化
正 2 正 2
=134.5kPa-94.7kPa=39.8kPa,则平衡时p(NO )=107.6kPa-2×39.8kPa=28kPa,则该反应的
2
C.容器内固体总质量不再随时间变化 D.容器内气体总压强不再随时间变化
③在恒温恒容密闭容器中进行的反应(II)达到平衡时,向容器中(CaS、CaSO、CaO均足量)再充入
4
平衡常数 。
少量SO ,达到新平衡后,与原平衡相比c(SO )_______(填“增大”“减小”或“不变”),原因为
2 2
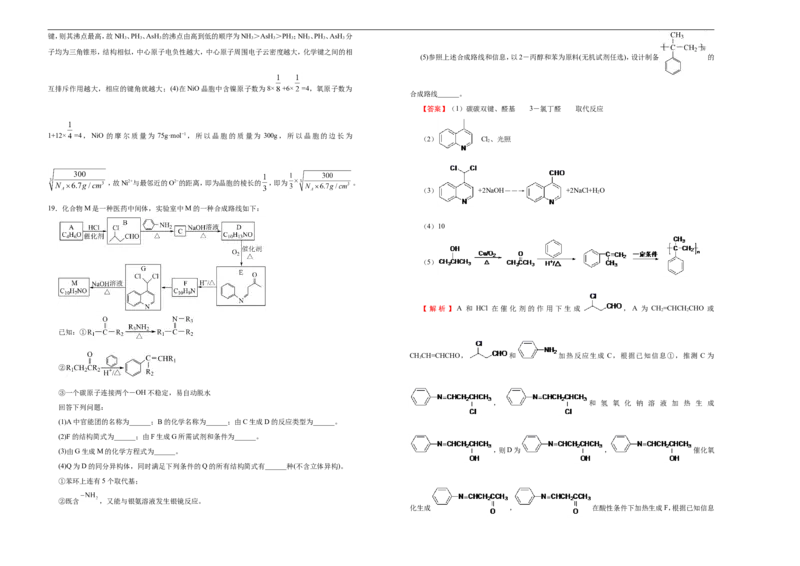
18.云南师范大学杨智教授合成了一种以醚键桥联型双吡啶羧酸为配体的金属镍配合物(分子式为
_______。
C H NNiO·2H O)。本配合物具有一定的光催化效果,在光催化还原二氧化碳方面具有潜在的应
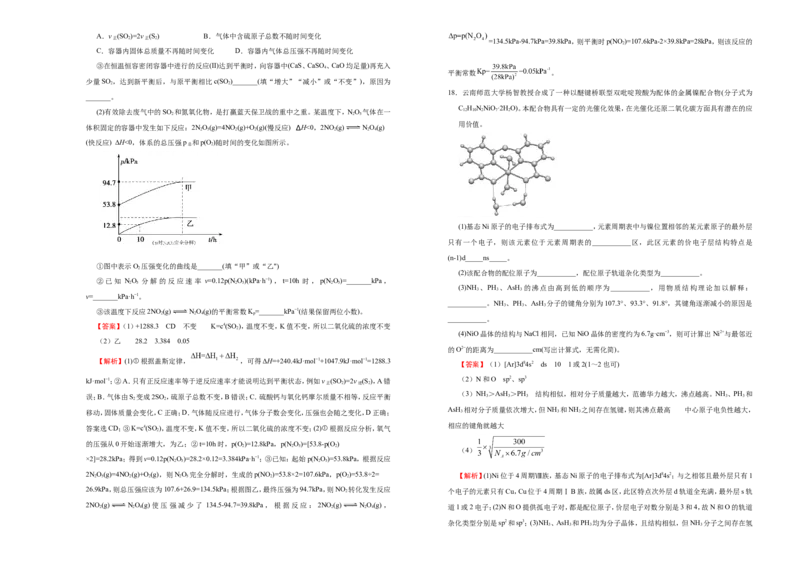
(2)有效除去废气中的SO 和氮氧化物,是打贏蓝天保卫战的重中之重。某温度下,NO 气体在一 12 10 2 7 2
2 2 5
用价值。
体积固定的容器中发生如下反应:2NO(g)=4NO (g)+O(g)(慢反应) ∆H<0,2NO (g) NO(g)
2 5 2 2 2 2 4
(快反应) ∆H<0,体系的总压强p 和p(O )随时间的变化如图所示。
总 2
(1)基态Ni原子的电子排布式为___________,元素周期表中与镍位置相邻的某元素原子的最外层
只有一个电子,则该元素位于元素周期表的___________区,此区元素的价电子层结构特点是
(n-1)d_____ns_____。
①图中表示O 压强变化的曲线是_______(填“甲”或“乙")
2
(2)该配合物的配位原子为___________,配位原子轨道杂化类型为___________。
②已知 NO 分解的反应速率 v=0.12p(N O)(kPa·h−1),t=10h 时,p(N O)=_______kPa,
2 5 2 5 2 5
(3)NH 、PH 、AsH 的沸点由高到低的顺序为___________,用物质结构理论加以解释:
3 3 3
v=_______kPa·h−1。
___________。NH 、PH 、AsH 分子的键角分别为107.3°、93.3°、91.8°,其键角逐渐减小的原因是
3 3 3
③该温度下反应2NO (g) NO(g)的平衡常数K=_______kPa−1(结果保留两位小数)。
2 2 4 p
___________。
【答案】(1)+1288.3 CD 不变 K=c4(SO ),温度不变,K值不变,所以二氧化硫的浓度不变
2
(4)NiO晶体的结构与NaCl相同,已知NiO晶体的密度约为6.7g·cm−3,则可计算出Ni2+与最邻近
(2)乙 28.2 3.384 0.05
的O2−的距离为___________cm(写出计算式,无需化简)。
【解析】(1)①根据盖斯定律, ,可得ΔH=+240.4kJ·mol−1+1047.9kJ·mol−1=1288.3
【答案】(1)[Ar]3d84s2 ds 10 1或2(1~2也可)
kJ·mol−1;②A.只有正反应速率等于逆反应速率才能说明达到平衡状态,例如v (SO )=2v (S ),A错 (2)N和O sp2、sp3
正 2 逆 2
(3)NH >AsH >PH 结构相似,相对分子质量越大,范德华力越大,沸点越高。NH 、PH 和
误;B.气体由S 变成2SO ,硫原子总数不变,B错误;C.硫酸钙与氧化钙摩尔质量不相等,反应平衡 3 3 3 3 3
2 2
AsH 相对分子质量依次增大,但NH 和NH 之间存在氢键,则其沸点最高 中心原子电负性越大,
移动,固体质量会变化,C正确;D.气体随反应进行,气体分子数会变化,压强也会随之变化,D正确; 3 3 3
相应的键角就越大
答案选CD;③K=c4(SO ),温度不变,K值不变,所以二氧化硫的浓度不变;(2)①根据反应分析,氧气
2
的压强从0开始逐渐增大,为乙;②t=10h时,p(O )=12.8kPa,p(N O)=[53.8-p(O )
2 2 5 2
(4)
×2]=28.2kPa;得到v=0.12p(N O)=28.2×0.12=3.384kPa·h−1;③已知:起始p(N O)=53.8kPa,根据反应
2 5 2 5
2N
2
O
5
(g)=4NO
2
(g)+O
2
(g),则N
2
O
5
完全分解时,生成的p(NO
2
)=53.8×2=107.6kPa,p(O
2
)=53.8÷2= 【解析】(1)Ni位于4周期Ⅷ族,基态Ni原子的电子排布式为[Ar]3d84s2;与之相邻且最外层只有1
26.9kPa,则总压强应该为107.6+26.9=134.5kPa;根据图乙,最终压强为94.7kPa,则NO 转化发生反应
2 个电子的元素只有Cu,Cu位于4周期ⅠB族,故属ds区,此区特点次外层d轨道全充满,最外层s轨
2NO (g) NO(g)使压强减少了 134.5-94.7=39.8kPa,根据反应:2NO (g) NO(g),
2 2 4 2 2 4 道1或2电子;(2)N和O提供孤电子对,都是配位原子,价层电子对数分别是3和4,故N和O的轨道
杂化类型分别是sp2和sp3;(3)NH 、AsH 和PH 均为分子晶体,且结构相似,但NH 分子之间存在氢
3 3 3 3键,则其沸点最高,故NH 、PH 、AsH 的沸点由高到低的顺序为NH >AsH >PH ;NH 、PH 、AsH 分
3 3 3 3 3 3 3 3 3
子均为三角锥形,结构相似,中心原子电负性越大,中心原子周围电子云密度越大,化学键之间的相
(5)参照上述合成路线和信息,以2-丙醇和苯为原料(无机试剂任选),设计制备 的
互排斥作用越大,相应的键角就越大;(4)在NiO晶胞中含镍原子数为8× +6× =4,氧原子数为
合成路线______。
【答案】(1)碳碳双键、醛基 3-氯丁醛 取代反应
1+12× =4,NiO 的摩尔质量为 75g·mol−1,所以晶胞的质量为 300g,所以晶胞的边长为
(2) Cl 、光照
2
,故Ni2+与最邻近的O2−的距离,即为晶胞的棱长的 ,即为 。
(3) +2NaOH――→ +2NaCl+HO
2
19.化合物M是一种医药中间体,实验室中M的一种合成路线如下:
(4)10
(5)
【 解 析 】 A 和 HCl 在 催 化 剂 的 作 用 下 生 成 , A 为 CH=CHCHCHO 或
2 2
已知:①
CHCH=CHCHO, 和 加热反应生成 C,根据已知信息①,推测 C 为
3
②
③一个碳原子连接两个-OH不稳定,易自动脱水
, 和 氢 氧 化 钠 溶 液 加 热 生 成
回答下列问题:
(1)A中官能团的名称为______;B的化学名称为______;由C生成D的反应类型为______。
(2)F的结构简式为______;由F生成G所需试剂和条件为______。
(3)由G生成M的化学方程式为______。 ,则D为 , 催化氧
(4)Q为D的同分异构体,同时满足下列条件的Q的所有结构简式有______种(不含立体异构)。
①苯环上连有5个取代基;
②既含 ,又能与银氨溶液发生银镜反应。
化生成 , 在酸性条件下加热生成F,根据已知信息②,推出F为 , 和氢氧化钠溶液加热生成 ,根据已知信息③,
、 、 、 、 ,
共 10 种;(5) 催化氧化生成 , 和 在酸性条件下加热生成
不 稳 定 , 易 自 动 脱 水 , 则 M 为 。 (1)A 为 CH=CHCHCHO 或
2 2
CHCH=CHCHO , 含 有 的 官 能 团 为 碳 碳 双 键 、 醛 基 ; B 的 化 学 名 称 为 3- 氯 丁 醛 ;
3
, 发 生 加 聚 反 应 生 成 , 合 成 路 线 为
和氢氧化钠溶液加热生成 ,该反应为取代反应;(2)F
的结构简式为 ;由F生成G为取代反应,反应试剂及条件为Cl、光照;(3)由G生成M的
2
。
化学方程式为 +2NaOH――→ +2NaCl+HO;(4)①苯环上连有5个取代基;
2
②既含 ,又能与银氨溶液发生银镜反应,说明含有-CHO;符合条件的同分异构体有:
、 、 、 、 、