文档内容
热点强化 14 微粒空间结构 大 π 键的判断
(一)微粒空间结构的判断
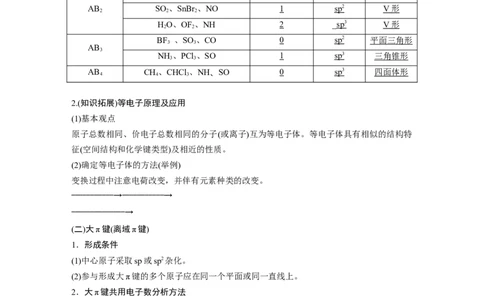
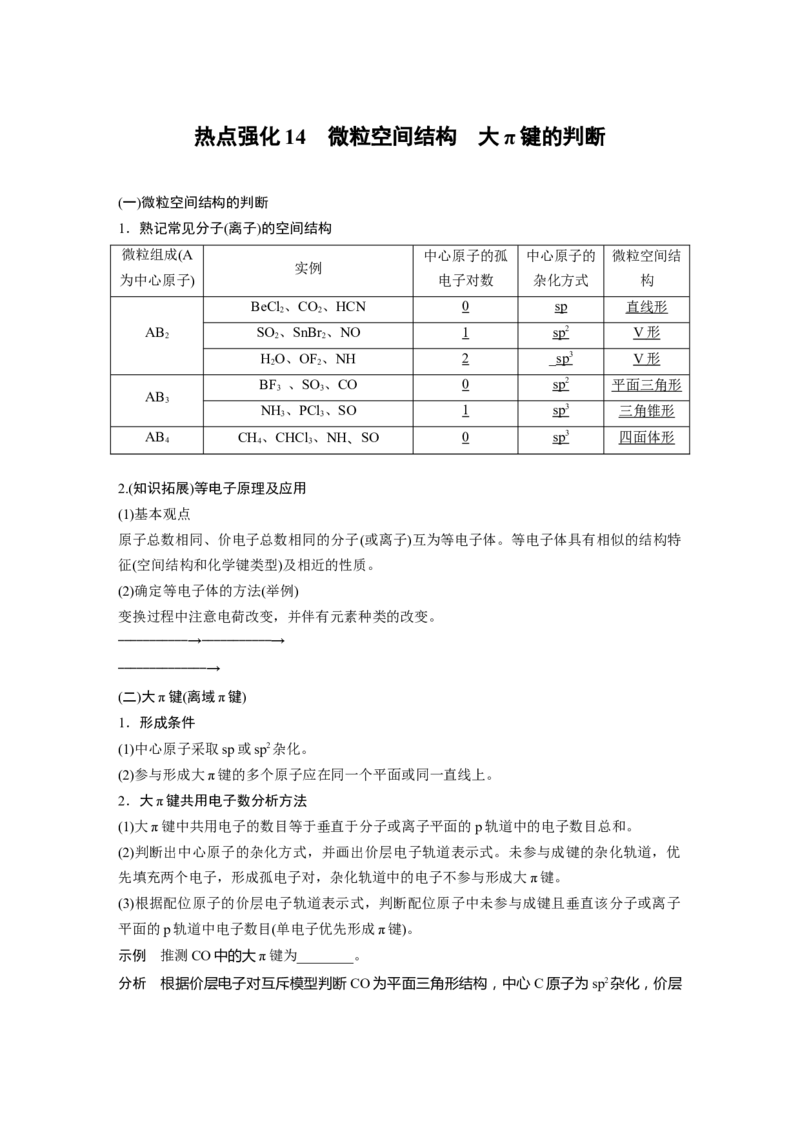
1.熟记常见分子(离子)的空间结构
微粒组成(A 中心原子的孤 中心原子的 微粒空间结
实例
为中心原子) 电子对数 杂化方式 构
BeCl 、CO、HCN 0 sp 直线形
2 2
AB SO 、SnBr 、NO 1 sp 2 V 形
2 2 2
HO、OF 、NH 2 _ sp 3 V 形
2 2
BF 、SO 、CO 0 sp 2 平面三角形
3 3
AB
3
NH 、PCl 、SO 1 sp 3 三角锥形
3 3
AB CH、CHCl 、NH、SO 0 sp 3 四面体形
4 4 3
2.(知识拓展)等电子原理及应用
(1)基本观点
原子总数相同、价电子总数相同的分子(或离子)互为等电子体。等电子体具有相似的结构特
征(空间结构和化学键类型)及相近的性质。
(2)确定等电子体的方法(举例)
变换过程中注意电荷改变,并伴有元素种类的改变。
―――――――――――→―――――――――――→
――――――――――――――→
(二)大π键(离域π键)
1.形成条件
(1)中心原子采取sp或sp2杂化。
(2)参与形成大π键的多个原子应在同一个平面或同一直线上。
2.大π键共用电子数分析方法
(1)大π键中共用电子的数目等于垂直于分子或离子平面的p轨道中的电子数目总和。
(2)判断出中心原子的杂化方式,并画出价层电子轨道表示式。未参与成键的杂化轨道,优
先填充两个电子,形成孤电子对,杂化轨道中的电子不参与形成大π键。
(3)根据配位原子的价层电子轨道表示式,判断配位原子中未参与成键且垂直该分子或离子
平面的p轨道中电子数目(单电子优先形成π键)。
示例 推测CO中的大π键为________。
分析 根据价层电子对互斥模型判断CO为平面三角形结构,中心C原子为sp2杂化,价层电子轨道表示式为 ,每个O原子有两个单电子,三个O分别用一
个单电子与中心C原子形成三个C—O σ键,另一个单电子参与形成大π键,形成两个负电
荷的电子也参与形成大π键。则大π键的电子总数为1+3+2=6,表示为Π。
1.(2020·山东,7)B NH(无机苯)的结构与苯类似,也有大π键。下列关于B NH 的说法错
3 3 6 3 3 6
误的是( )
A.其熔点主要取决于所含化学键的键能
B.形成大π键的电子全部由N提供
C.分子中B和N的杂化方式相同
D.分子中所有原子共平面
答案 A
解析 无机苯属于分子晶体,其熔点与分子间作用力有关,与键能无关,A项错误;B的最
外层电子排布式为2s22p1,N的最外层电子排布式为2s22p3,经过sp2轨道杂化后,N原子剩
下1个孤电子对,B原子剩下1个空的p轨道,所以形成大π键的电子全部由N提供,B项
正确;B和N都是sp2杂化,键角为120°,分子中所有原子共平面,C、D项正确。
2.(2023·菏泽二模)胍( )是一种平面形分子。胍盐在碱性条件下不稳定,易水
解产生尿素和氨气,其盐酸盐( )是核酸检测液的主要成分。下列说法错误
的是( )
A.胍的水溶液呈碱性
B.胍中C、N杂化方式均为sp2
C.胍中存在Π大π键
D.胍盐中含有的化学键均为极性键
答案 D
解析 胍含有碱性基团氨基,可以和盐酸反应生成胍盐,胍的水溶液呈碱性,A正确;胍是
平面形分子,C、N均采取sp2杂化,B正确;胍中存在Π大π键,C正确;胍盐中含有共价
键和离子键,D错误。
3.5-氨基四唑硝酸盐受热迅速生成以N 为主的环境友好型气体,并放出大量的热,是制造
2
HTPB火箭推进剂的重要原料。该盐结构简式如图,其中五元环为平面结构,下列说法正确的是( )
A.阴离子的空间结构为三角锥形
B.该化合物难溶于水
C.该化合物中五元环上的5个原子的杂化方式都相同
D.该化合物存在类似于苯分子的大π键,化学性质比较稳定
答案 C
解析 硝酸根离子中,成键电子对为3,孤电子对数为×(5+1-3×2)=0,因此其空间结构
为平面三角形,A错误;硝酸盐易溶于水,B错误;五元环为平面结构,可知该化合物中五
元环上的5个原子均为sp2杂化,它们的杂化方式相同,C正确;该化合物受热迅速生成
N,化学性质不稳定,D错误。
2
4.(1)[2020·全国卷Ⅰ,35(3)]磷酸根离子的空间结构为________,其中P的价层电子对数为
________,杂化轨道类型为________。
(2)[2018·全国卷Ⅰ,35(3)节选]LiAlH 中的阴离子空间结构是________、中心原子的杂化形
4
式为________。
答案 (1)正四面体形 4 sp3 (2)正四面体 sp3
解析 (1)PO的中心原子P的价层电子对数为4,孤电子对数为0,中心原子P为sp3杂化,
故PO的空间结构为正四面体形。(2)LiAlH 中的阴离子是AlH,中心原子铝原子含有的价层
4
电子对数是4,且不存在孤电子对,所以空间结构是正四面体,中心原子的杂化轨道类型是
sp3杂化。
5.(1)(2023·杭州模拟)含有碳元素的有机化合物分布极广,最简单的为碳正离子(CH),该离
子的空间结构为__________;如图是叶绿素的结构示意图,配体是一种平面大环有机物,该
结构中N原子的杂化方式为__________,C—N σ键有________个。
(2)(2023·天津模拟)常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大
的顺序为________(用元素符号表示),SCN-的空间结构为________,中心原子的杂化类型
为________。
(3)(2023·杭州模拟)已知RbHPO 是次磷酸的正盐,HPO 的结构式为 ________,其中P采
2 2 3 2取________杂化方式。
(4)(2023·济南模拟)非金属氮化物在生产、生活和科研中应用广泛。回答下列问题:
氟化硝酰(NO F)可用作火箭推进剂中的氧化剂,NO F 中心原子的杂化方式为
2 2
________________________________________________________________________。
气态NO 的分子结构为 ,而固态NO 则由一种直线形的阳离子X与一种
2 5 2 5
平面正三角形的阴离子Y构成,X的化学式为________,Y的离域π键可表示为 ________。
答案 (1)平面三角形 sp2、sp3 8
(2)K