文档内容
第 19 讲 硫及其氧化物
[复习目标] 1.了解硫的存在及其单质的性质和用途。2.掌握硫的氧化物的主要性质及应用。
3.了解空气中SO 的测定及治理。
2
考点一 硫单质的性质
1.硫元素的存在形态
2.硫单质的物理性质
溶解性
俗称 颜色状态
水 酒精 CS
2
硫黄 黄色晶体 难溶 微溶 易溶
思考 (1)硫有S 、S 、S 、S 等多种单质,它们的关系是什么?加热时,S 转化为S 、
2 4 6 8 8 6
S、S 属于什么变化?
4 2
(2)硫单质难溶于水,易溶于CS,其原因是什么?
2
提示 (1)S 、S 、S 、S 属于同一元素的不同种单质,它们互为同素异形体,S 转化为S 、
2 4 6 8 8 6
S、S 属于化学变化。
4 2
(2)硫单质、CS 均属于非极性分子,而HO属于极性分子,根据“相似相溶”规律,非极性
2 2
分子易溶于非极性分子形成的溶剂中。
3.从化合价的角度认识硫单质的化学性质
S←―― ――→S1.硫在空气中燃烧的产物是SO ,在纯氧中燃烧的产物是SO ( )
2 3
2.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物( )
答案 1.× 2.×
硫及多硫化物的性质
1.在下列反应中硫元素只表现氧化性的是( )
A.2Al+3S=====Al S
2 3
B.S+2HSO (浓)=====2HO+3SO ↑
2 4 2 2
C.HS=====H+S
2 2
D.3S+6NaOH=====2NaS+NaSO +3HO
2 2 3 2
答案 A
解析 A项,该反应中S的化合价由0价变为-2价,S只体现氧化性,正确;B项,该反
应中S的化合价由0价、+6价变为+4价,S体现还原性和氧化性,错误;C项,该反应中
S的化合价由-2价变为0价,S只体现还原性,错误;D项,该反应中S的化合价由0价变
为-2价、+4价,S体现氧化性和还原性,错误。
2.硫元素最常见和最稳定的一种同素异形体是黄色的正交 α-型,1912年E.Beckmann由硫
在碘中的冰点降低法测得它含有S 分子。1891年,M.R.Engel用浓盐酸和硫代硫酸盐的饱和
8
溶液在0 ℃下作用首次制得了一种菱形的ε-硫,后来证明含有S 分子。下列说法正确的是(
6
)
A.S 和S 分子都是由S原子组成,所以它们是一种物质
6 8
B.S 和S 分子分别与铁粉反应,所得产物不同
6 8
C.S 和S 分子分别与过量的氧气反应可以得到SO
6 8 3
D.等质量的S 和S 分子分别与足量的KOH溶液反应,消耗KOH的物质的量相同
6 8
答案 D
解析 S 和S 分子都是由S原子组成,但它们是不同的物质,互为同素异形体,故 A错误;
6 8
S 和S 是硫元素的不同单质,化学性质相似,因此它们分别与铁粉反应,所得产物相同,
6 8
故B错误;不管氧气过量还是少量,S 和S 分子分别与氧气反应均得到SO ,故C错误;等
6 8 2
质量的S 和S 分子,其硫原子的物质的量相同,因此它们分别与足量的 KOH溶液反应,消
6 8
耗KOH的物质的量相同,故D正确。
3.单质硫与可溶性硫化物溶液作用生成多硫化物,如NaS(aq)+(x-1)S===NaS(x一般为2
2 2 x
~6);多硫化物在酸性溶液中不稳定,易歧化;As S +2NaS(aq)===As S +2NaS。下列说
2 3 2 2 2 5 2
法错误的是( )
A.As S (其中As显+3价)是多硫化物
2 3B.As S 是氧化产物
2 5
C.NaS 中阴、阳离子个数比为1∶2
2 2
D.久置NaS溶液遇酸可能变浑浊
2
答案 A
解析 由题干信息知,多硫离子S中S元素化合价为-价>-2价,而As S 中S元素为-2
2 3
价,是正常硫化物,A错误; As S 发生氧化反应生成氧化产物As S ,B正确;NaS 中阴、
2 3 2 5 2 2
阳离子分别为S、Na+,个数比为1∶2,C正确;久置NaS溶液被空气中氧气氧化后生成单
2
质硫,S与NaS溶液进一步反应生成多硫化物,多硫化物在酸性条件下易歧化,可能生成
2
单质硫,溶液变浑浊,D正确。
考点二 二氧化硫和三氧化硫
1.二氧化硫
(1)物理性质
色、味、态 密度 溶解性
无色、有刺激性气味的有毒气 易溶于水,通常状况下,1体积的水溶解
比空气的大
体 约40 体积的SO
2
(2)化学性质
按要求完成下列化学方程式:
SO
2
(3)实验室制法
①固体NaSO 与较浓HSO 反应,化学方程式为NaSO +HSO ===NaSO +SO ↑+HO。
2 3 2 4 2 3 2 4 2 4 2 2
②铜与浓HSO 混合加热,化学方程式为Cu+2HSO (浓)=====CuSO +SO ↑+2HO。
2 4 2 4 4 2 2
2.三氧化硫
(1)物理性质
熔点:16.8 ℃,沸点:44.8 ℃,常温常压下为液态,标准状况下为固态。
(2)化学性质
三氧化硫具有酸性氧化物的通性,主要反应如下:3.硫的氧化物对环境的影响
(1)硫的氧化物的来源、危害及治理
(2)硫酸型酸雨的形成过程
4.三类漂白剂的比较
类型 原理 举例 特点
将有机色质内部“生色团”
氧化型 次氯酸及盐、过氧化物、O 等 不可逆、持久
2
破坏掉
与有色物质内部“生色团”
加合型 SO 可逆、不持久
2
“化合”成无色物质
吸附型 将有色物质吸附而褪色 活性炭 物理变化
1.标准状况下,2.24 L SO 中含有硫原子数为N ( )
3 A
2.将SO 通入紫色石蕊溶液中,紫色石蕊溶液先变红后褪色( )
2
3.SO 使滴有酚酞的NaOH溶液褪色,体现了SO 的漂白性( )
2 2
4.SO 和Cl 等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好( )
2 2
5.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同( )
2 2 2
答案 1.× 2.× 3.× 4.× 5.×
一、SO 的制取与性质探究
2
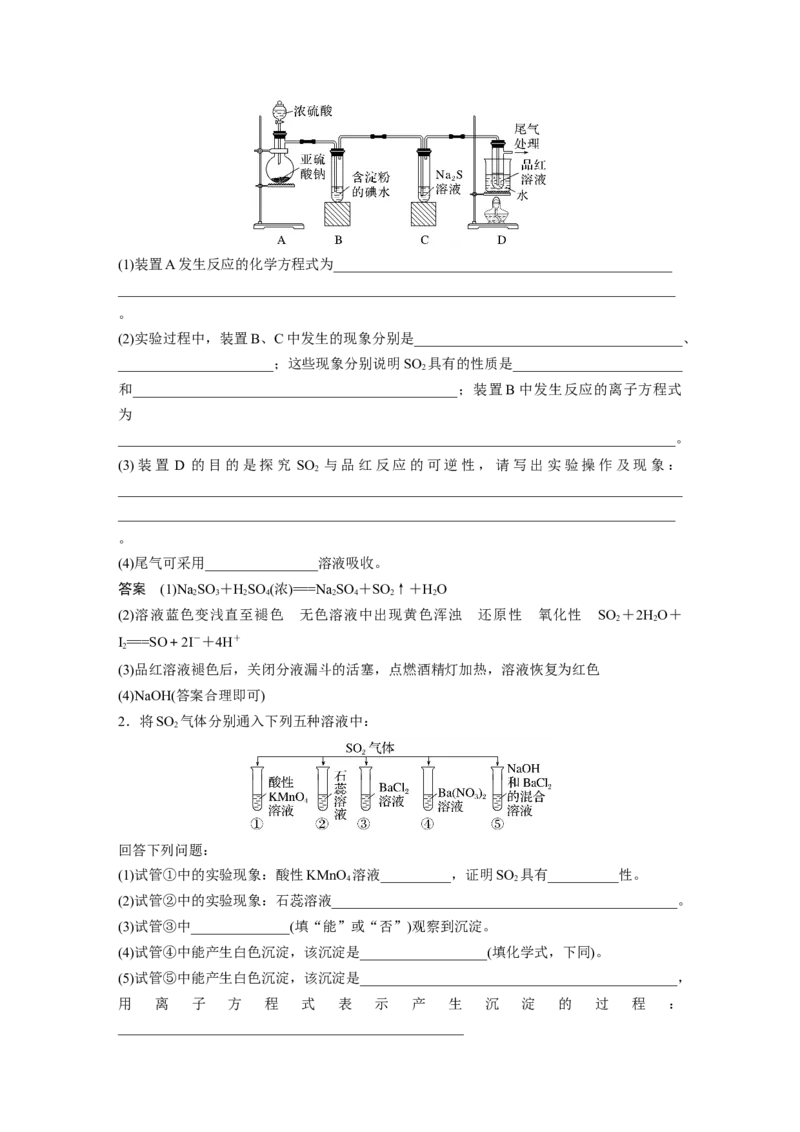
1.某研究性学习小组用如图装置制取少量二氧化硫并探究其某些性质。(1)装置A发生反应的化学方程式为________________________________________________
_______________________________________________________________________________
。
(2)实验过程中,装置B、C中发生的现象分别是______________________________________、
______________________;这些现象分别说明SO 具有的性质是________________________
2
和______________________________________________;装置B中发生反应的离子方程式
为
_______________________________________________________________________________。
(3)装置 D 的目的是探究 SO 与品红反应的可逆性,请写出实验操作及现象:
2
________________________________________________________________________________
_______________________________________________________________________________
。
(4)尾气可采用________________溶液吸收。
答案 (1)Na SO +HSO (浓)===NaSO +SO ↑+HO
2 3 2 4 2 4 2 2
(2)溶液蓝色变浅直至褪色 无色溶液中出现黄色浑浊 还原性 氧化性 SO +2HO+
2 2
I===SO+2I-+4H+
2
(3)品红溶液褪色后,关闭分液漏斗的活塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH(答案合理即可)
2.将SO 气体分别通入下列五种溶液中:
2
回答下列问题:
(1)试管①中的实验现象:酸性KMnO 溶液__________,证明SO 具有__________性。
4 2
(2)试管②中的实验现象:石蕊溶液_________________________________________________。
(3)试管③中______________(填“能”或“否”)观察到沉淀。
(4)试管④中能产生白色沉淀,该沉淀是__________________(填化学式,下同)。
(5)试管⑤中能产生白色沉淀,该沉淀是_____________________________________________,
用 离 子 方 程 式 表 示 产 生 沉 淀 的 过 程 :
________________________________________________________________________________________________________________________________
。
答案 (1)褪色 还原 (2)变红 (3)否
(4)BaSO (5)BaSO SO +2OH-===SO+HO、Ba2++SO===BaSO↓
4 3 2 2 3
二、CO、SO 混合气体中各成分的检验
2 2
3.如图是检验某无色气体A是SO 和CO 的混合气体的装置图,按要求回答下列问题:
2 2
(1)B 中 加 入 的 试 剂 是 ________ , 作 用 是
______________________________________________。
(2)C 中 加 入 的 试 剂 是 __________ , 作 用 是
_____________________________________________
________________________。
(3)D 中 加 入 的 试 剂 是 ________________ , 作 用 是
______________________________________
________________________。
(4) 实 验 时 , C 中 应 观 察 到 的 现 象 是
__________________________________________________
________________________。
答案 (1)品红溶液 检验SO
2
(2)酸性KMnO 溶液 除去SO 并检验SO 是否除尽
4 2 2
(3)澄清石灰水 检验CO
2
(4)酸性KMnO 溶液的颜色变浅但不褪成无色
4
解析 检验二氧化硫用品红溶液,吸收二氧化硫用酸性KMnO 溶液,检验二氧化碳用澄清
4
石灰水;在检验二氧化碳之前,必须除尽二氧化硫,因为二氧化硫也能使澄清石灰水变浑浊。
C装置的作用是除去SO 并检验SO 是否除尽,所以酸性高锰酸钾溶液颜色变浅,但不能褪
2 2
成无色,若褪成无色则不能证明二氧化硫已除尽。
(1)SO 具有漂白性,但不能漂白酸碱指示剂,如紫色石蕊溶液中通入SO ,溶液变红,但不
2 2
褪色。
(2)检验SO 和CO 同时存在的一般流程
2 2
SO 和CO 都可使澄清石灰水变浑浊,检验二者同时存在的一般流程为检验SO ⇒除去SO ⇒
2 2 2 2
检验SO 是否除尽⇒检验CO。
2 21.正误判断,正确的打“√”,错误的打“×”。
(1)向盛有SO 水溶液的试管中滴加几滴品红溶液,振荡,加热试管,通过观察溶液颜色变
2
化,来探究SO 具有漂白性(2022·江苏,11B)( )
2
(2)SO 可漂白纸浆,不可用于杀菌、消毒(2021·湖南,2C)( )
2
(3)可用澄清石灰水检验SO 气体(2020·天津,6B)( )
2
(4)温室气体是形成酸雨的主要物质(2022·全国甲卷,7B)( )
(5)用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏(2022·浙江6月选考,8D)( )
(6)燃煤中加入CaO可以减少酸雨的形成及温室气体的排放(2017·全国卷Ⅲ,7C)( )
答案 (1)√ (2)× (3)× (4)× (5)√ (6)×
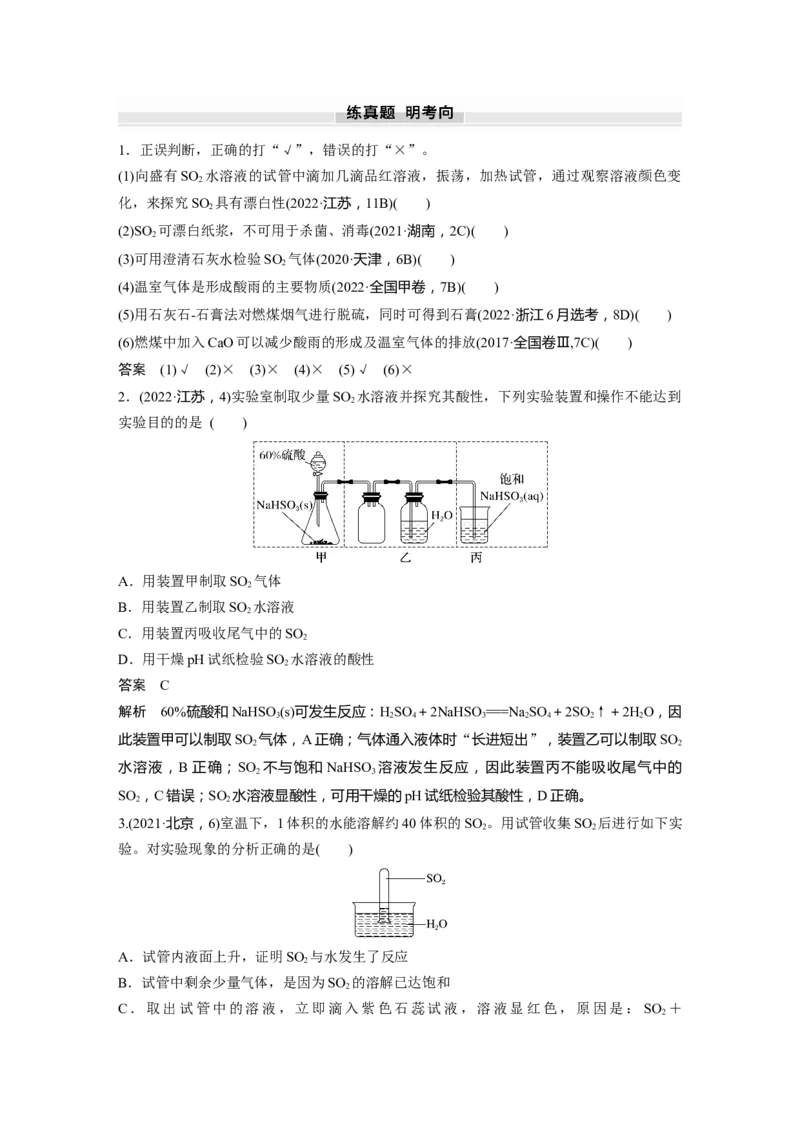
2.(2022·江苏,4)实验室制取少量SO 水溶液并探究其酸性,下列实验装置和操作不能达到
2
实验目的的是 ( )
A.用装置甲制取SO 气体
2
B.用装置乙制取SO 水溶液
2
C.用装置丙吸收尾气中的SO
2
D.用干燥pH试纸检验SO 水溶液的酸性
2
答案 C
解析 60%硫酸和NaHSO(s)可发生反应:HSO +2NaHSO===NaSO +2SO ↑+2HO,因
3 2 4 3 2 4 2 2
此装置甲可以制取SO 气体,A正确;气体通入液体时“长进短出”,装置乙可以制取SO
2 2
水溶液,B正确;SO 不与饱和NaHSO 溶液发生反应,因此装置丙不能吸收尾气中的
2 3
SO ,C错误;SO 水溶液显酸性,可用干燥的pH试纸检验其酸性,D正确。
2 2
3.(2021·北京,6)室温下,1体积的水能溶解约40体积的SO 。用试管收集SO 后进行如下实
2 2
验。对实验现象的分析正确的是( )
A.试管内液面上升,证明SO 与水发生了反应
2
B.试管中剩余少量气体,是因为SO 的溶解已达饱和
2
C.取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO +
2HOHSO ,HSO H++HSO,HSOH++SO
2 2 3 2 3
D.取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO 挥发
2
答案 C
4.(2021·广东1月适应性测试,14)推理是一种重要的能力。打开分液漏斗活塞,进行如图
所示的探究实验,对实验现象的预测及分析错误的是( )
A.试管内CCl 层溶液褪色,说明Br 具有氧化性
4 2
B.试管中的红色花瓣褪色,说明SO 具有漂白性
2
C.试管中产生大量气泡,说明NaSO 被氧化产生SO
2 3 3
D.一段时间后试管内有白色沉淀,说明有SO生成
答案 C
解析 锥形瓶内发生反应:NaSO +HSO ===NaSO +SO ↑+HO ,产生的SO 进入到试
2 3 2 4 2 4 2 2 2
管中,CCl 层溶液褪色,发生反应:SO +Br +2HO===HSO +2HBr,证明Br 具有氧化
4 2 2 2 2 4 2
性,A项正确;试管中花瓣褪色,说明SO 可以漂白花瓣中的有色物质,证明SO 具有漂白
2 2
性,B项正确;试管中产生大量气泡是锥形瓶中产生的SO 进入到试管中引起的,NaSO 与
2 2 3
HSO 发生复分解反应,C项错误;试管中Br 可将SO 氧化,生成HSO 和HBr,SO 可以
2 4 2 2 2 4
和Ba2+结合生成不溶于酸的白色沉淀,D项正确。
课时精练
1.下列关于硫的叙述正确的是( )
A.硫的非金属性较强,在自然界中只以化合态存在
B.可用水溶解过滤分离硝酸钾和硫黄的混合物
C.硫与金属或非金属反应时都作氧化剂
D.硫的氧化性比氯气强
答案 B
解析 硫的非金属性虽然较强,但在自然界中的存在形态既有化合态又有游离态,故 A错
误;硝酸钾易溶于水,而硫难溶于水,所以可用水溶解过滤分离硝酸钾和硫黄的混合物,故
B正确;硫与金属反应时作氧化剂,与非金属反应时既可作氧化剂,也可作还原剂,故C错
误;硫的非金属性比氯弱,所以硫的氧化性比氯气弱,故D错误。
2.下列说法错误的是( )
A.残留在试管内壁上的硫可用热的NaOH溶液除去B.硫单质与变价金属反应时一般生成低价态的金属硫化物
C.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理
D.单质硫或含硫物质燃烧时,氧气少量时生成SO ,氧气足量时生成SO
2 3
答案 D
3.下列有关硫及其化合物的说法或描述正确的是( )
A.硫黄矿制备硫酸经历两步:S――→SO ――→HSO
3 2 4
B.酸雨与土壤中的金属氧化物反应后,硫元素以单质的形式进入土壤中
C.在燃煤中加入石灰石可减少SO 的排放,发生的反应为2CaCO +2SO +O=====2CO +
2 3 2 2 2
2CaSO
4
D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原
性
答案 C
解析 硫元素以硫酸盐的形式进入土壤,B项错误;CuS中S的化合价为-2价,具有还原
性,D项错误。
4.(2023·豫北名校高三调研)正交硫(也称菱形硫、斜方硫)与单斜硫是硫元素的两种常见单质,
均由S 分子(结构如图所示)组成,两者结构中S 分子的排列方式不同,相互之间可以转化:
8 8
单斜硫正交硫。下列有关说法错误的是( )
A.正交硫与单斜硫互为同素异形体
B.S 分子中每个“S”均满足8电子结构
8
C.正交硫转化为单斜硫发生了化学变化
D.正交硫与单斜硫均完全燃烧生成SO 时,单斜硫放出的能量多
2
答案 D
解析 正交硫与单斜硫都是由硫元素组成的单质,所以两者互为同素异形体,A正确;由结
构示意图可知,S 分子中每个硫原子与2个硫原子形成共价键,则每个硫原子均满足8电子
8
稳定结构,B正确;同素异形体之间的转化属于化学变化,C正确。
5.下列关于SO 、SO 的说法正确的是( )
2 3
A.SO 与SO 均为极性分子
2 3
B.SO 能与水形成分子间氢键
3
C.SO 分子中S的杂化方式为sp3
3
D.SO 分子中键角小于SO 分子中的键角
2 3
答案 D
解析 SO 分子中S原子为sp2杂化,孤电子对数为1,分子空间结构为V形,SO 为极性分
2 2
子,SO 分子中S原子为sp2杂化,孤电子对数为0,分子空间结构为平面三角形,SO 为非
3 3极性分子,A、C错误;SO 遇水迅速反应生成硫酸,SO 与HO不能形成分子间氢键,但
3 3 2
HSO 与HO能形成分子间氢键,B错误。
2 4 2
6.根据SO 通入不同溶液中的实验现象,所得结论不正确的是( )
2
实验 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2
B HS溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D NaSiO 溶液 产生胶状沉淀 酸性:HSO >H SiO
2 3 2 3 2 3
答案 C
解析 A项,溶液中SO 被FeCl 氧化生成SO,再与BaCl 反应产生白色沉淀,体现了SO
2 3 2 2
的还原性;B项,SO 与HS溶液发生反应:SO +2HS===3S↓+2HO,体现了SO 的氧化
2 2 2 2 2 2
性;C项,SO 使酸性KMnO 溶液褪色,体现了SO 的还原性;D项,SO 与NaSiO 溶液
2 4 2 2 2 3
反应产生胶状沉淀,根据强酸制弱酸,则酸性:HSO >HSiO。
2 3 2 3
7.如图是研究二氧化硫性质的微型实验装置(实验时用另一表面皿扣在上面)。现用75%硫
酸溶液和亚硫酸钠晶体反应制取SO 气体并进行实验,实验现象很明显。下列说法错误的是
2
( )
A.品红溶液褪色
B.紫色石蕊溶液先变红后褪色
C.酸性KMnO 溶液紫色褪去
4
D.含酚酞的NaOH溶液红色变浅
答案 B
解析 SO 能漂白品红,不能漂白指示剂,SO 是酸性氧化物,与水反应生成亚硫酸,能使
2 2
紫色石蕊溶液变红但不会褪色,A项正确,B项错误;SO 具有还原性,能与酸性高锰酸钾
2
溶液发生氧化还原反应,使酸性KMnO 溶液紫色褪去,C项正确;SO 能与NaOH溶液反应
4 2
生成亚硫酸钠和水,能使含酚酞的NaOH溶液红色变浅,D项正确。
8.为确定某纯净的气体Q的成分,进行了如下几种实验,其中不正确的是( )
选项 操作及现象 结论
A 闻Q气味(有刺激性)――→酸性KMnO 溶液(褪色) Q一定是SO
4 2
B 闻Q气味(有刺激性)――→澄清石灰水(变浑浊) Q可能是SO
2C Q――→品红溶液(褪色)――→变红色 Q一定是SO
2
D Q――→紫色石蕊溶液(先变红后褪色) Q一定不是SO
2
答案 A
解析 硫化氢、二氧化硫等均能被高锰酸钾氧化,由现象可知Q不一定是SO ,故A错误。
2
9.SO 属于大气污染物,可用H 与SO 在加热条件下反应消除SO 的污染,其反应原理可
2 2 2 2
分为两步,过程如图所示。
下列说法正确的是( )
A.SO 排放到空气中会形成pH≈5.6的酸雨
2
B.可用CuSO 溶液检验是否有气体X生成
4
C.在100~200 ℃时发生的是置换反应
D.工业上可用浓硝酸处理尾气中的SO
2
答案 B
解析 酸雨的pH<5.6,A错误;气体X为HS,能与CuSO 溶液反应生成黑色的硫化铜沉
2 4
淀,所以可用CuSO 溶液检验是否有气体X生成,B正确;在100~200 ℃时发生的反应为
4
2HS+SO ========3S+2HO,不是置换反应,C错误;若用浓硝酸处理工业尾气中的
2 2 2
SO ,会产生含氮元素的大气污染物(即氮的氧化物),D错误。
2
10.向酸化的KI溶液中通入SO ,溶液变黄并出现浑浊,发生反应Ⅰ:SO +4H++4I-
2 2
===2I +S↓+2HO,继续通入SO ,溶液变为无色,发生反应Ⅱ:I +SO +2HO===SO+
2 2 2 2 2 2
4H++2I-。下列说法错误的是( )
A.SO 、I 的氧化性强弱与外界条件有关
2 2
B.每生成0.1 mol SO,整个过程中转移0.4 mol电子,同时消耗0.2 mol KI
C.该过程的总反应为3SO +2HO===2SO+S↓+4H+
2 2
D.该反应过程中KI作催化剂
答案 B
解析 由反应Ⅰ可知,SO 的氧化性强于I,由反应Ⅱ可知,I 的氧化性强于SO ,故可说明
2 2 2 2
SO 、I 的氧化性强弱与外界条件有关,A正确;由反应Ⅱ可知,每生成0.1 mol SO,转移电
2 2
子为0.2 mol,同时生成0.2 mol I-,反应0.1 mol I ,由反应Ⅰ可知生成0.1 mol I 消耗0.2
2 2
mol I-,转移电子为0.2 mol,故整个过程中转移0.4 mol电子,不消耗KI,B错误;由题干
信息可知,反应Ⅰ+2反应Ⅱ可得该过程的总反应为3SO +2HO===2SO+S↓+4H+,C正
2 2
确;由C项分析可知,该反应过程中KI作催化剂,D正确。
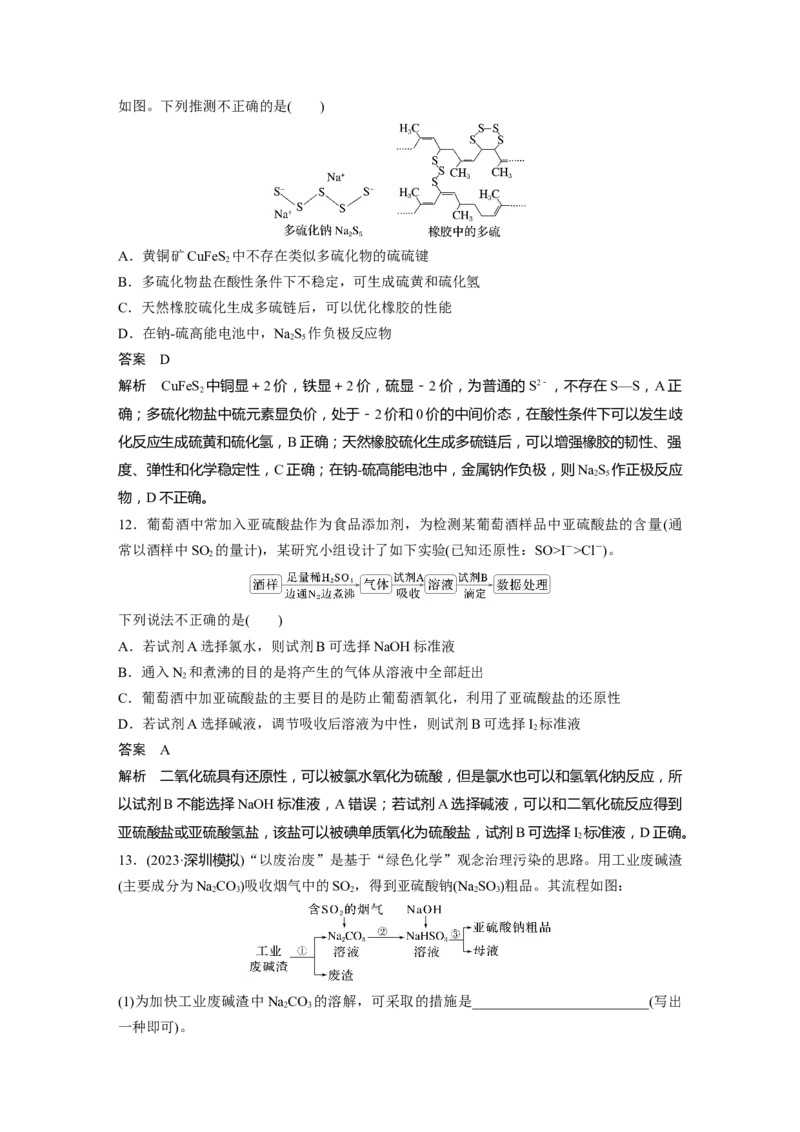
11.多硫化物是指含有硫硫键的化合物,在电池、橡胶等多种工业中均有重要用途,其结构如图。下列推测不正确的是( )
A.黄铜矿CuFeS 中不存在类似多硫化物的硫硫键
2
B.多硫化物盐在酸性条件下不稳定,可生成硫黄和硫化氢
C.天然橡胶硫化生成多硫链后,可以优化橡胶的性能
D.在钠-硫高能电池中,NaS 作负极反应物
2 5
答案 D
解析 CuFeS 中铜显+2价,铁显+2价,硫显-2价,为普通的S2-,不存在S—S,A正
2
确;多硫化物盐中硫元素显负价,处于-2价和0价的中间价态,在酸性条件下可以发生歧
化反应生成硫黄和硫化氢,B正确;天然橡胶硫化生成多硫链后,可以增强橡胶的韧性、强
度、弹性和化学稳定性,C正确;在钠-硫高能电池中,金属钠作负极,则NaS 作正极反应
2 5
物,D不正确。
12.葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫酸盐的含量(通
常以酒样中SO 的量计),某研究小组设计了如下实验(已知还原性:SO>I->Cl-)。
2
下列说法不正确的是( )
A.若试剂A选择氯水,则试剂B可选择NaOH标准液
B.通入N 和煮沸的目的是将产生的气体从溶液中全部赶出
2
C.葡萄酒中加亚硫酸盐的主要目的是防止葡萄酒氧化,利用了亚硫酸盐的还原性
D.若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I 标准液
2
答案 A
解析 二氧化硫具有还原性,可以被氯水氧化为硫酸,但是氯水也可以和氢氧化钠反应,所
以试剂B不能选择NaOH标准液,A错误;若试剂A选择碱液,可以和二氧化硫反应得到
亚硫酸盐或亚硫酸氢盐,该盐可以被碘单质氧化为硫酸盐,试剂B可选择I 标准液,D正确。
2
13.(2023·深圳模拟)“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣
(主要成分为NaCO)吸收烟气中的SO ,得到亚硫酸钠(Na SO )粗品。其流程如图:
2 3 2 2 3
(1)为加快工业废碱渣中NaCO 的溶解,可采取的措施是_________________________(写出
2 3
一种即可)。(2)过程①进行的操作是__________________________________________________________。
(3)上述流程中,加入NaOH后,发生反应的化学方程式为_____________________________。
(4) 亚 硫 酸 钠 粗 品 中 含 有 少 量 NaSO , 原 因 是
2 4
__________________________________________
_______________________________________________________________________________
。
(5)设计实验证明亚硫酸钠粗品中含有少量NaSO 的方案:在一支试管中,加入少量亚硫酸
2 4
钠 粗 品 , 用 适 量 蒸 馏 水 溶 解 ,
________________________________________________________
_______________________________________________________________________________
,
出现白色沉淀,则证明含有NaSO 。
2 4
答案 (1)搅拌(或粉碎、加热) (2)过滤
(3)NaHSO+NaOH===NaSO +HO
3 2 3 2
(4)Na SO 具有较强还原性,易被空气中的氧气氧化 (5)加入过量盐酸,再加入BaCl 溶液
2 3 2
14.碳、硫的含量对钢铁性能影响很大,其含量的一种测定方法是将钢样中碳、硫转化为气
体,再用测碳、测硫装置进行测定。实验流程如图:
(1) 煅 烧 装 置 中 采 用 纯 氧 , 目 的 是
____________________________________________________
_______________________________________________________________________________
。
气体a的主要成分有______、CO 和未反应的O。
2 2
(2)为充分吸收气体a,下列吸收装置合适的是________________________________________
(填字母)。
(3)气体a被HO 溶液吸收转化为硫酸(溶液b),用已知浓度的NaOH溶液滴定生成的溶液
2 2
b,根据消耗NaOH溶液的体积可确定钢样中硫的质量分数。
①滴定时NaOH溶液置于________(填仪器名称)中,若以酚酞为指示剂,滴定终点时的现象
为______________________________________________________________________________
_______________________________________________________________________________
。
②若称取1 g钢样进行实验,滴定消耗0.01 mol·L-1 NaOH溶液2.0 mL,则该钢样中硫的质量分数为________。
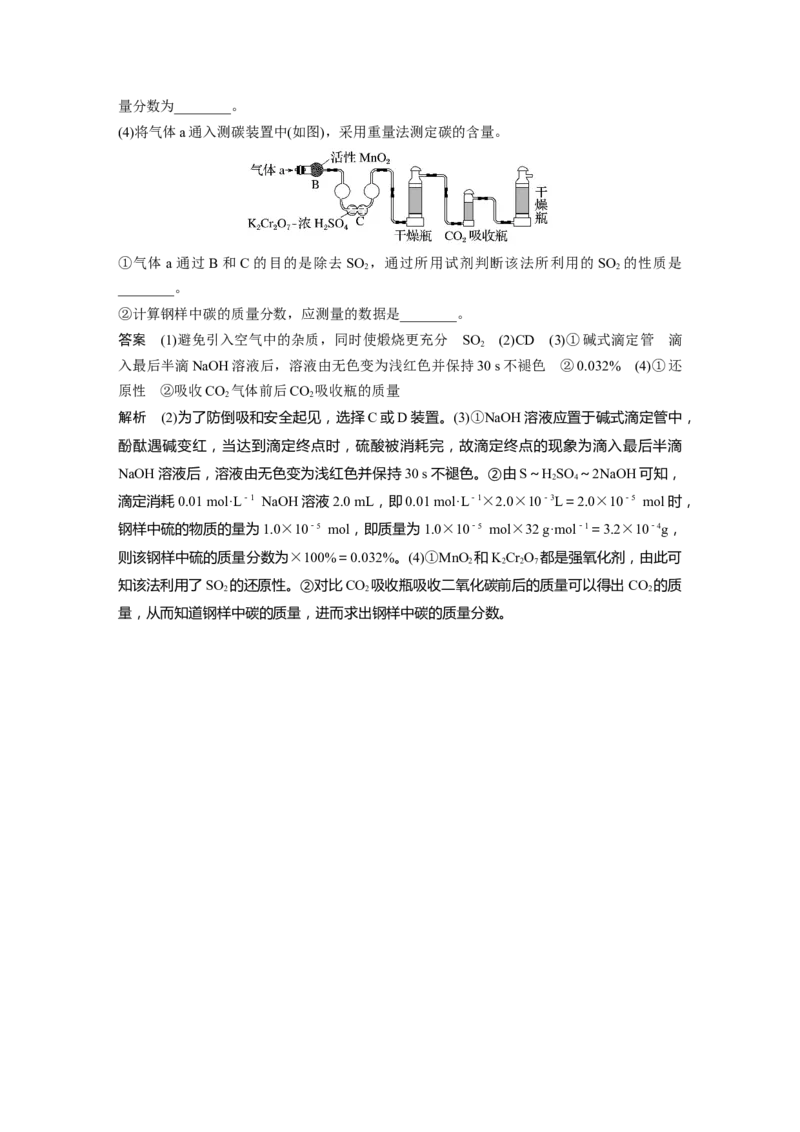
(4)将气体a通入测碳装置中(如图),采用重量法测定碳的含量。
①气体a通过B和C的目的是除去SO ,通过所用试剂判断该法所利用的 SO 的性质是
2 2
________。
②计算钢样中碳的质量分数,应测量的数据是________。
答案 (1)避免引入空气中的杂质,同时使煅烧更充分 SO (2)CD (3)①碱式滴定管 滴
2
入最后半滴NaOH溶液后,溶液由无色变为浅红色并保持30 s不褪色 ②0.032% (4)①还
原性 ②吸收CO 气体前后CO 吸收瓶的质量
2 2
解析 (2)为了防倒吸和安全起见,选择C或D装置。(3)①NaOH溶液应置于碱式滴定管中,
酚酞遇碱变红,当达到滴定终点时,硫酸被消耗完,故滴定终点的现象为滴入最后半滴
NaOH溶液后,溶液由无色变为浅红色并保持30 s不褪色。②由S~HSO ~2NaOH可知,
2 4
滴定消耗0.01 mol·L-1 NaOH溶液2.0 mL,即0.01 mol·L-1×2.0×10-3L=2.0×10-5 mol时,
钢样中硫的物质的量为1.0×10-5 mol,即质量为1.0×10-5 mol×32 g·mol-1=3.2×10-4g,
则该钢样中硫的质量分数为×100%=0.032%。(4)①MnO 和KCr O 都是强氧化剂,由此可
2 2 2 7
知该法利用了SO 的还原性。②对比CO 吸收瓶吸收二氧化碳前后的质量可以得出CO 的质
2 2 2
量,从而知道钢样中碳的质量,进而求出钢样中碳的质量分数。