文档内容
第 27 讲 常见物质(离子)的检验与推断
[复习目标] 1.掌握常见物质(离子)检验的方法,能利用物质(离子)的性质设计检验指定物质
或特定离子。2.能通过实验事实推断物质(离子)。
考点一 常见物质(离子)的检验
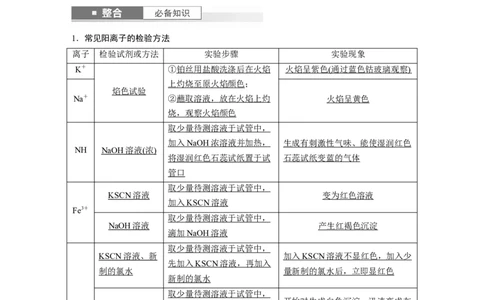
1.常见阳离子的检验方法
离子 检验试剂或方法 实验步骤 实验现象
K+ ①铂丝用盐酸洗涤后在火焰 火焰呈紫色 ( 通过蓝色钴玻璃观察 )
上灼烧至原火焰颜色;
焰色试验
Na+ ②蘸取溶液,放在火焰上灼 火焰呈黄色
烧,观察火焰颜色
取少量待测溶液于试管中,
加入 NaOH 浓溶液并加热, 生成有刺激性气味、能使湿润红色
NH NaOH 溶液 ( 浓 )
将湿润红色石蕊试纸置于试 石蕊试纸变蓝的气体
管口
取少量待测溶液于试管中,
KSCN 溶液 变为红色溶液
加入 KSCN 溶液
Fe3+
取少量待测溶液于试管中,
NaOH 溶液 产生红褐色沉淀
滴加 NaOH 溶液
取少量待测溶液于试管中,
KSCN 溶液、新 加入 KSCN 溶液不显红色,加入少
先加入 KSCN 溶液,再加入
制的氯水 量新制的氯水后,立即显红色
新制的氯水
取少量待测溶液于试管中,
开始时生成白色沉淀,迅速变成灰
NaOH 溶液 加入 NaOH 溶液并露置在空
Fe2+ 绿色,最后变成红褐色沉淀
气中
酸性 KMnO 溶 取少量待测溶液于试管中,
4
溶液紫红色褪去
液 加入酸性 KMnO 溶液
4
取少量待测溶液于试管中,
K[Fe(CN) ] 溶液 生成蓝色沉淀
3 6
加入 K [Fe(CN) ] 溶液
3 6
2.常见阴离子的检验方法离子 检验试剂或方法 实验现象
Cl- 加入AgNO 溶液、稀硝酸 生成白色沉淀(AgCl)
3
加入AgNO 溶液、稀硝酸 生成淡黄色沉淀(AgBr)
3
Br-
加入氯水后振荡,滴入四氯化碳 四氯化碳层(下层)呈橙红色
加入AgNO 溶液、稀硝酸 生成黄色沉淀(AgI)
3
I- 加入氯水后振荡,滴入四氯化碳 四氯化碳层(下层)呈紫红色
加入氯水和淀粉溶液 溶液变蓝
SO 先加入稀盐酸,再加入 BaC l 溶液 生成白色沉淀(BaSO)
2 4
先生成白色沉淀(CaCO 或BaCO ),将沉淀
3 3
加入CaCl 或BaCl 溶液、稀盐酸、
2 2
溶于稀盐酸,产生无色、无味的气体
澄清石灰水
(CO),该气体能使澄清石灰水变浑浊
2
CO
产生无色、无味的气体,该气体能使澄清
加入盐酸、澄清石灰水;CaCl 溶液 石灰水变浑浊;向原溶液中加入稀CaCl
2 2
溶液,产生白色沉淀
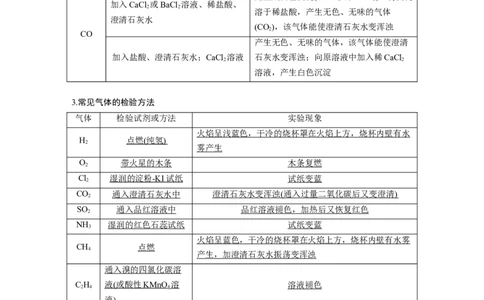
3.常见气体的检验方法
气体 检验试剂或方法 实验现象
火焰呈浅蓝色,干冷的烧杯罩在火焰上方,烧杯内壁有水
H 点燃 ( 纯氢 )
2
雾产生
O 带火星的木条 木条复燃
2
Cl 湿润的淀粉 - K I 试纸 试纸变蓝
2
CO 通入澄清石灰水中 澄清石灰水变浑浊 ( 通入过量二氧化碳后又变澄清 )
2
SO 通入品红溶液中 品红溶液褪色,加热后又恢复红色
2
NH 湿润的红色石蕊试纸 试纸变蓝
3
火焰呈蓝色,干冷的烧杯罩在火焰上方,烧杯内壁有水雾
CH 点燃
4
产生,加澄清石灰水振荡变浑浊
通入溴的四氯化碳溶
C H 液 ( 或酸性 KMnO 溶 溶液褪色
2 4 4
液 )
通入溴的四氯化碳溶
C H 液 ( 或酸性 KMnO 溶 溶液褪色
2 2 4
液 )
1.(2020·天津,6)检验下列物质所选用的试剂正确的是( )
选项 待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水
D 溶液中的NH NaOH溶液,湿润的蓝色石蕊试纸
答案 C
解析 淀粉溶液可以检验碘单质,不能检验碘元素,故 A错误;能使澄清石灰水变浑浊的
气体可以是二氧化硫或二氧化碳,应该用品红溶液检验二氧化硫气体,故B错误;铜离子
遇到氨水会先产生氢氧化铜蓝色沉淀,继续加氨水会生成四氨合铜离子,检验铜离子可以用
氨水,故C正确;铵根离子遇氢氧化钠溶液(加热)生成氨气,氨气能使湿润的红色石蕊试纸
变蓝,不能使用湿润的蓝色石蕊试纸检验氨气,故D错误。
2.(2022·浙江6月选考,25)亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误
服会中毒。现将适量某样品(成分为亚硝酸钠或氯化钠)溶于水配成溶液,分别取少量该溶液
于试管中进行实验。下列方案设计、现象和结论都正确的是( )
方案设计 现象和结论
先加入少量KClO 溶液,再加AgNO
3 3
A 若产生白色沉淀,则样品为亚硝酸钠
溶液和足量稀硝酸,振荡
加到少量KMnO 溶液中,再加硫酸酸
4
B 若溶液褪色,则样品为亚硝酸钠
化,振荡
先加到少量FeCl 溶液中,再加入稀盐
2
C 若溶液变黄色,则样品为亚硝酸钠
酸酸化,振荡
先加入少量NaSO 溶液,再加入BaCl
2 3 2
D 若产生白色沉淀,则样品为亚硝酸钠
溶液和稀硝酸,振荡
答案 C
解析 氯化钠电离出的氯离子也可以被酸性高锰酸钾氧化,而使其褪色,B错误;NO在酸
性条件下有较强的氧化性,可以把二价铁氧化为三价铁,溶液变为黄色,C正确;稀硝酸可
以把亚硫酸根离子氧化为硫酸根离子,再加入氯化钡可以生成硫酸钡白色沉淀,D错误。
3.(2022·海南,6)依据下列实验,预测的实验现象正确的是( )
选项 实验内容 预测的实验现象
A MgCl 溶液中滴加NaOH溶液至过量 产生白色沉淀后沉淀消失
2
B FeCl 溶液中滴加KSCN溶液 溶液变红色
2
C AgI悬浊液中滴加NaCl溶液至过量 黄色沉淀全部转化为白色沉淀
D 酸性KMnO 溶液中滴加乙醇至过量 溶液紫红色褪色
4
答案 D解析 MgCl 溶液中滴加NaOH溶液至过量,两者发生反应产生白色沉淀,白色沉淀为氢氧
2
化镁,氢氧化镁为中强碱,其不与过量的NaOH溶液发生反应,因此沉淀不消失,A不正确;
FeCl 溶液中滴加KSCN溶液,溶液不变色,B不正确;AgI的溶解度远远小于AgCl,因此,
2
向AgI悬浊液中滴加NaCl溶液至过量,黄色沉淀不可能全部转化为白色沉淀,C不正确;
酸性KMnO 溶液呈紫红色,其具有强氧化性,而乙醇具有较强的还原性,因此,酸性
4
KMnO 溶液中滴加乙醇至过量后溶液紫红色褪色,D正确。
4
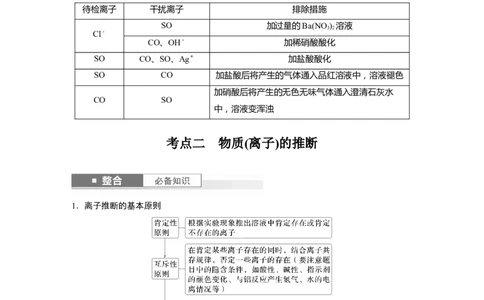
离子检验中的常见干扰离子以及排除措施
待检离子 干扰离子 排除措施
SO 加过量的Ba(NO ) 溶液
3 2
Cl-
CO、OH- 加稀硝酸酸化
SO CO、SO、Ag+ 加盐酸酸化
SO CO 加盐酸后将产生的气体通入品红溶液中,溶液褪色
加硝酸后将产生的无色无味气体通入澄清石灰水
CO SO
中,溶液变浑浊
考点二 物质(离子)的推断
1.离子推断的基本原则
2.离子推断的解题技巧
(1)推断结论时,应该考虑三个方面,即肯定存在的离子、肯定不存在的离子、不能判定存
在与否的离子。这三个方面的离子应是相互独立的;任何一种离子只能出现一次,不能重复
出现。(2)定量型离子推断试题常根据离子的物质的量(或浓度)定量推断最后一种离子的存在;如果
多种离子共存,且只有一种离子的物质的量未知,可以用电荷守恒来确定最后一种离子是否
存在,即阳离子所带的正电荷总数等于阴离子所带的负电荷总数。
1.(2020·全国卷Ⅱ,8)某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进
4 3
行如下实验:①混合物溶于水,得到澄清透明溶液;②做焰色试验,通过钴玻璃可观察到紫
色;③向溶液中加碱,产生白色沉淀。根据实验现象可判断其组成为( )
A.KCl、NaCl B.KCl、MgSO
4
C.KCl、CaCO D.MgSO 、NaCl
3 4
答案 B
解析 由信息①得到澄清透明溶液,可排除碳酸钙;由信息②焰色试验透过钴玻璃可观察到
紫色,说明含有钾离子,可推测含有氯化钾;由信息③向溶液中加入碱产生白色沉淀,可推
测含有硫酸镁,所以B正确。
2.(2022·全国乙卷,9)某白色粉末样品,可能含有NaSO 、NaSO 、NaSO 和NaCO。取
2 4 2 3 2 2 3 2 3
少量样品进行如下实验:
①溶于水,得到无色透明溶液;②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气
体逸出,离心分离;③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中确定存在的是( )
A.NaSO 、NaSO B.NaSO 、NaSO
2 4 2 2 3 2 3 2 2 3
C.NaSO 、NaCO D.NaSO 、NaCO
2 4 2 3 2 3 2 3
答案 A
解析 向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出,说明固体中存在
NaSO ,发生反应:SO+2H+===S↓+HO+SO ↑,由于盐酸过量,向②的上层清液中
2 2 3 2 2 2
滴加BaCl 溶液,有沉淀生成,则沉淀为BaSO ,说明固体中存在NaSO ,不能确定是否有
2 4 2 4
NaSO 和NaCO ,NaSO 、NaCO 与过量稀盐酸反应的现象可以被NaSO 与过量稀盐酸
2 3 2 3 2 3 2 3 2 2 3
反应的现象覆盖掉。
3.一瓶无色澄清的溶液,其中可能含有H+、NH、Na+、Al3+、Fe3+、I-、NO、CO、SO、
AlO。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性 ②取溶液适量,加入少量CCl 和数滴新制氯水,振荡,
4
CCl 层呈紫红色 ③该溶液的焰色试验没有黄色;根据以上实验结果,下列推断正确的是(
4
)
A.向该溶液中加入BaCl 溶液不一定能观察到白色沉淀
2
B.可以确定没有Na+、Fe3+、CO、AlO,不能确定是否有NO
C.该溶液可能是NH NO 与HI的混合液
4 3D.一定没有Al3+、CO和NO
答案 A
解析 不能确定是否含SO,则向该溶液中加入BaCl 溶液不一定能观察到白色沉淀,故A
2
正确;一定不含Na+、Fe3+、NO、CO、AlO,故B、C错误;不能确定是否含Al3+,故D
错误。
4.(2023·安徽六安高三模拟)某固体中可能含有Fe (SO ) 、FeCl 、PbSO 、NaCl中一种或者
2 4 3 2 4
几种,现通过如下实验确定其成分。①取少量该固体,加稀硫酸溶解,得到澄清溶液;②取
实验①所得澄清溶液,先加足量稀盐酸酸化,再加BaCl 溶液,产生白色沉淀;③另取少量
2
实验①所得澄清溶液,加入NaOH溶液,产生的沉淀经过滤、洗涤后,向沉淀中加入足量
稀盐酸和KSCN溶液,溶液变红色;④另取少量实验①所得澄清溶液,做焰色试验,火焰
呈黄色。下列说法正确的是( )
A.该固体中Fe (SO ) 和FeCl 至少有一种
2 4 3 2
B.该固体中一定没有PbSO 和FeCl
4 2
C.该固体中一定有NaCl和Fe (SO )
2 4 3
D.因为铁元素的干扰,根据实验④无法确定NaCl的存在
答案 A
解析 根据实验①可以直接确定没有难溶物PbSO 存在;因为实验①使用了稀硫酸溶解固体,
4
引入了SO,故实验②无法确定Fe (SO ) 的存在;根据实验③可以确定该固体中存在Fe元素,
2 4 3
但是无法确定Fe元素来自Fe (SO ) 还是FeCl ,故只能确定二者之中至少有一个;根据实验
2 4 3 2
④可以确定含有Na元素,则含有NaCl,实验室可用无锈铁丝做焰色试验,说明铁元素不会
干扰Na元素的焰色试验。综上所述,A正确,B、C、D错误。
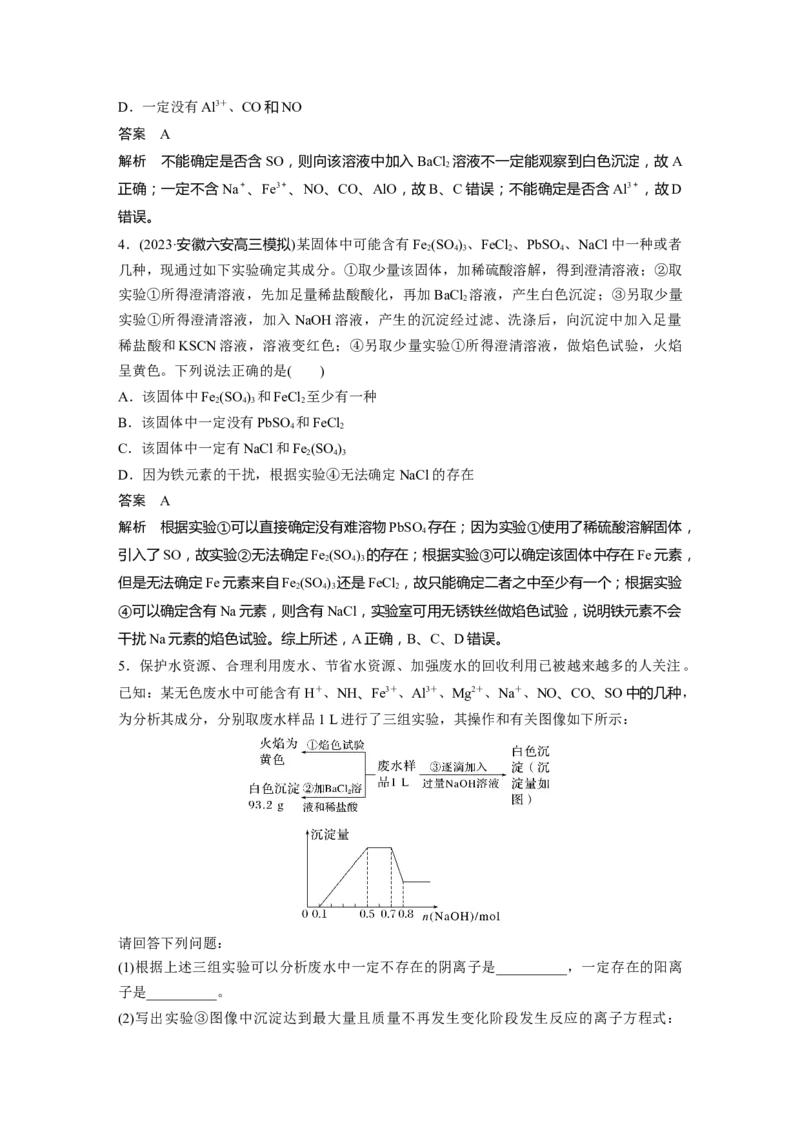
5.保护水资源、合理利用废水、节省水资源、加强废水的回收利用已被越来越多的人关注。
已知:某无色废水中可能含有H+、NH、Fe3+、Al3+、Mg2+、Na+、NO、CO、SO中的几种,
为分析其成分,分别取废水样品1 L进行了三组实验,其操作和有关图像如下所示:
请回答下列问题:
(1)根据上述三组实验可以分析废水中一定不存在的阴离子是__________,一定存在的阳离
子是__________。
(2)写出实验③图像中沉淀达到最大量且质量不再发生变化阶段发生反应的离子方程式:________________________________________________________________________________
_______________________________________________________________________________
。
(3)分析图像,在原溶液中c(NH)与c(Al3+)的比值为__________,所得沉淀的最大质量是
__________g。
(4)若通过实验确定原废水中 c(Na+)=0.18 mol·L-1,试判断原废水中 NO 是否存在?
__________(填“存在”“不存在”或“不确定”)。若存在,c(NO)=__________mol·L-1(若
不存在或不确定则此空不填)。
答案 (1)CO Na+、H+、Al3+、Mg2+、NH
(2)NH+OH-===NH ·H O
3 2
(3)2∶1 10.7 (4)存在 0.08
解析 无色废水中肯定不存在Fe3+,根据实验①确定存在Na+,根据实验②确定存在SO,
根据实验③结合图像可知,溶液中有H+、NH、Al3+、Mg2+,因为CO与H+、Al3+不能共
存,所以无CO。n(SO)==0.4 mol,根据图像求出n(Al3+)=n[Al(OH)]=0.8 mol-0.7 mol=
3
0.1 mol,n(NH)=0.7 mol-0.5 mol=0.2 mol,n(H+)=0.1 mol,生成0.1 mol Al(OH) 消耗0.3
3
mol NaOH,则生成Mg(OH) 消耗的氢氧化钠为0.5 mol-0.1 mol-0.3 mol=0.1 mol,即含有
2
Mg2+的物质的量是0.05 mol。(3)根据上述分析,在原溶液中==,沉淀最多时含有0.1 mol
Al(OH) 和0.05 mol Mg(OH) ,其质量为0.1 mol×78 g·mol-1+0.05 mol×58 g·mol-1=10.7 g。
3 2
(4)根据上述分析,若通过实验确定原废水中c(Na+)=0.18 mol·L-1,即含有Na+为0.18 mol,根
据电荷守恒,则含有NO为0.08 mol,c(NO)==0.08 mol·L-1。
答题规范(3) 离子检验操作、现象描述
(1)解答此类题的思维过程
(2)规范答题
检验某溶液中是否含有××的操作方法:取待测液少许置于试管中,先加××试剂无明显现
象(若有沉淀则静置后取上层清液继续实验,说明:本步骤为排除干扰离子);再加入××溶
液,若产生××则证明溶液中含有××离子,反之则证明溶液中不含××离子。1.某含碘废水(pH约为8)中一定存在I ,可能存在I-、IO中的一种或两种。请补充完整检
2
验含碘废水中是否含有I-、IO的实验方案:取适量含碘废水,用CCl 多次萃取、分液直到
4
水层用淀粉溶液检验不出有碘单质存在;____________________________________________
________________________________________________________________________________
_______________________________________________________________________________
。
已知:5SO+2IO+2H+===I +5SO+HO;可供选择的试剂:稀盐酸、淀粉溶液、FeCl 溶
2 2 3
液、NaSO 溶液。
2 3
答案 从水层取少量溶液,加入1~2 mL淀粉溶液,加稀盐酸酸化,滴加FeCl 溶液,若溶
3
液变蓝,说明废水中含有I-。另从水层取少量溶液,加入1~2 mL淀粉溶液,加稀盐酸酸
化,滴加NaSO 溶液,若溶液变蓝,说明废水中含有IO
2 3
2.按要求回答下列问题。
(1)结晶析出NaSO·5H O,其中可能含有NaSO 、NaSO 等杂质。利用所给试剂设计实验,
2 2 3 2 2 3 2 4
检 验 产 品 中 是 否 存 在 NaSO , 简 要 说 明 实 验 操 作 、 现 象 和 结 论 :
2 4
_________________________
_______________________________________________________________________________
。
已知:NaSO·5H O遇酸易分解:SO+2H+===S↓+SO ↑+HO;
2 2 3 2 2 2 2
可供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl 溶液、AgNO 溶液。
2 3
(2)榴石矿石可以看作由CaO、FeO、Fe O 、Al O 、SiO 组成。试设计实验证明榴石矿石中
2 3 2 3 2
含有FeO(试剂任选,说明实验操作与现象):
________________________________________________________________________________
_______________________________________________________________________________
。
答案 (1)取少量产品溶于足量稀盐酸,静置,取上层清液(或过滤,取滤液)于一试管中,滴
加BaCl 溶液,若产生白色沉淀,则说明含有NaSO 杂质(合理即可)
2 2 4
(2)取矿石少许,加稀硫酸充分溶解后,向其中滴加酸性高锰酸钾溶液,若紫色褪去,证明
矿石中含有FeO(不能加盐酸溶解)
3.(NH )SO 是常用的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
4 2 4
【查阅资料】(NH )SO 在260 ℃和400 ℃时分解产物不同。
4 2 4
【实验探究】该小组拟选用如图所示装置进行实验(夹持和加热装置略)。连接装置A→D→B,检查气密性,按图示加入试剂。通入N 排尽空气后,于400 ℃加热装
2
置A至(NH )SO 完全分解无残留物,停止加热,冷却,停止通入 N 。观察到装置A、D之
4 2 4 2
间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO,无SO。进
一步研究发现,气体产物中无氮氧化物。
检验装置D内溶液中有SO而无SO的实验操作和现象是_____________________________
_______________________________________________________________________________
。
答案 取少量装置D内溶液于试管中,滴加BaCl 溶液,生成白色沉淀,加入足量稀盐酸后,
2
沉淀完全溶解,放出无色有刺激性气味的气体
课时精练
1.为确定下列久置于空气中的物质是否变质,所选检验试剂(括号内物质)能达到目的的是(
)
A.NaOH溶液[Ba(OH) 溶液]
2
B.漂粉精(Na CO 溶液)
2 3
C.氯水(AgNO 溶液)
3
D.NaSO 溶液(BaCl 溶液)
2 3 2
答案 A
解析 NaOH溶液若变质会混有碳酸钠,NaCO 与氢氧化钡反应生成白色沉淀,故A正确;
2 3
漂粉精含氯化钙、次氯酸钙,无论次氯酸钙是否变质,氯化钙可电离出钙离子,加碳酸钠溶
液均产生沉淀,不能检验是否变质,故B错误;氯水及盐酸中均含氯离子,与硝酸银反应
均生成白色沉淀,不能检验是否变质,故 C错误;NaSO 溶液变质会混有硫酸钠,亚硫酸
2 3
钠和硫酸钠均与氯化钡反应生成白色沉淀,不能检验是否变质,故D错误。
2.通过实验得出的结论正确的是( )
A.将某固体试样完全溶于盐酸,再滴加Ba(NO ) 溶液,出现白色沉淀,则该固体试样中存
3 2
在SO
B.将某固体试样完全溶于盐酸,再滴加KSCN溶液,没有出现红色,则该固体试样中不存
在Fe3+
C.在某固体试样加水后的溶液中,滴加NaOH溶液,没有产生使湿润红色石蕊试纸变蓝的
气体,该固体试样中仍可能存在NH
D.在某固体试样加水后的上层清液中,滴加盐酸出现白色沉淀,再加NaOH溶液沉淀溶解,
则该固体试样中存在SiO
答案 C
解析 当固体中含有SO时,在酸性条件下滴加Ba(NO ) 溶液会被氧化生成硫酸根离子,有
3 2相同现象,故不一定存在SO,A错误;若固体为FeCl 和Fe的混合物时,也有相同的现象,
3
故固体试样中可能存在Fe3+,B错误;检验NH时应加NaOH溶液,加热,产生使湿润红色
石蕊试纸变蓝的气体,选项中没有加热,故不能确定有没有铵根离子,C正确;滴加盐酸出
现白色沉淀,再加NaOH溶液沉淀溶解,可能原固体中有AlO,不一定为SiO,D错误。
3.仅用一种试剂鉴别如下物质:苯、CCl 、NaI溶液、NaCl溶液、NaSO 溶液,下列试剂
4 2 3
中不能选用的是( )
A.溴水 B.FeCl 溶液
3
C.酸性KMnO 溶液 D.AgNO 溶液
4 3
答案 D
4.(2023·山东日照高三模拟)鉴别下列物质采用的试剂不可行的是( )
A.AgNO、MgCl 、BaCl 三种溶液:浓氨水
3 2 2
B.BaCl 、Ca(OH) 、Ba(NO ) 三种溶液:SO 气体
2 2 3 2 2
C.CaCl 、Ba(OH) 、Al (SO ) 三种溶液:NaCO 溶液
2 2 2 4 3 2 3
D.浓度均为0.1 mol·L-1的NaClO、Ba(OH) 、Al (SO ) 三种溶液:酚酞试剂
2 2 4 3
答案 C
解析 过量浓氨水和AgNO 、MgCl 、BaCl 三种溶液混合的现象分别为先产生白色沉淀后
3 2 2
沉淀溶解、产生白色沉淀、无明显现象,可以鉴别,故 A不选;SO 气体通入 BaCl 、
2 2
Ca(OH) 、Ba(NO ) 三种溶液的现象分别为无明显现象、产生白色沉淀继续通入沉淀溶解、
2 3 2
产生白色沉淀,可以鉴别,故B不选;NaCO 溶液和CaCl 、Ba(OH) 、Al (SO ) 三种溶液
2 3 2 2 2 4 3
的现象分别为产生白色沉淀、产生白色沉淀、产生白色沉淀并有气体生成,不能鉴别,故 C
选;酚酞试剂加入浓度均为0.1 mol·L-1的NaClO、Ba(OH) 、Al (SO ) 三种溶液的现象分别
2 2 4 3
为先变红后褪色、变红、无明显现象,可以鉴别,故D不选。
5.(2023·江西校联考模拟)鉴别等浓度的Al (SO ) 、AgNO 、苯酚三种溶液,仅用下列一种
2 4 3 3
方法不可行的是( )
A.加入浓溴水 B.通入SO 气体
2
C.通入足量氨气 D.加入FeCl 溶液
3
答案 B
解析 加入浓溴水后,Al (SO ) 溶液无明显现象,AgNO 溶液中有淡黄色沉淀生成,苯酚溶
2 4 3 3
液中有白色沉淀生成,A项可行;通入SO 后,Al (SO ) 溶液无明显现象,AgNO 溶液中出
2 2 4 3 3
现白色浑浊,苯酚溶液无明显现象,B项不可行;通入足量氨气后,Al (SO ) 溶液中有白色
2 4 3
沉淀生成,AgNO 溶液中先有白色沉淀生成,后沉淀消失,苯酚溶液无明显变化,C项可行。
3
6.(2023·珠海高三摸底测试)化学是以实验为基础的科学。下列检验实验操作或做法正确且
能达到目的的是( )
选项 操作或做法 目的
A 溴乙烷和NaOH乙醇溶液共热,所产 检验反应生成乙烯生气体直接通入酸性高锰酸钾溶液
中,溶液褪色
B 将SO 通入溴水中,溶液褪色 检验SO 的漂白性
2 2
在待测液中先用稀硝酸酸化,再滴加
C 检验溶液中是否含有Cl-
AgNO 溶液,生成白色沉淀
3
D 向丙烯醛溶液中滴加溴水,溶液褪色 检验丙烯醛中是否含有碳碳双键
答案 C
解析 溴乙烷和NaOH乙醇溶液共热,所产生气体中含有乙醇蒸气,乙醇、乙烯都能使酸
性高锰酸钾溶液褪色,高锰酸钾溶液褪色不能证明有乙烯生成,故A错误;将SO 通入溴水
2
中生成硫酸和氢溴酸,该反应体现SO 的还原性,不能体现SO 的漂白性,故B错误;在待
2 2
测液中先用稀硝酸酸化,再滴加AgNO 溶液,生成白色沉淀,该沉淀是氯化银,证明原溶
3
液中含有Cl-,故C正确;碳碳双键、醛基都能与溴水反应,向丙烯醛溶液中滴加溴水,溶
液褪色,不能证明丙烯醛中含有碳碳双键,故D错误。
7.下列离子在未知溶液中的检验方法正确的是( )
选项 离子 检验方法
向样品中加入足量盐酸,将生成的无色无味的气体通入澄清石灰水中,
A CO
观察溶液是否变浑浊
向样品中先加入稀硝酸酸化,再滴加氯化钡溶液,观察是否有白色沉淀
B SO
生成
C Fe2+ 取少量溶液于试管中,加入酸性高锰酸钾溶液,观察溶液紫色是否褪去
取少量溶液于试管中,加入新制氯水,再加入淀粉溶液,观察溶液是否
D I-
变蓝色
答案 D
解析 A项,HCO会产生干扰,错误;B项,SO会产生干扰,错误;C项,使酸性高锰酸
钾溶液褪色的不一定是Fe2+,如SO等,错误;D项,新制氯水能把I-氧化成I ,淀粉遇碘
2
变蓝,因此可以检验I-的存在,正确。
8.某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解,再加入足量稀盐酸,有气泡产生,固体全部
溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为( )
A.NaHCO 、Al(OH) B.AgCl、NaHCO
3 3 3
C.NaSO 、BaCO D.NaCO、CuSO
2 3 3 2 3 4
答案 C9.下列关于离子检验的说法不正确的是( )
A.取某盐溶液加入浓NaOH溶液,加热,产生的气体可使湿润的红色石蕊试纸变蓝,该溶
液中含有NH
B.取某溶液滴加KSCN溶液,无明显现象,滴加氯水,溶液变红色,该溶液中含有Fe2+
C.取某溶液加入BaCl 溶液,产生不溶于稀硝酸的白色沉淀,该溶液中一定含有SO
2
D.取某无色溶液通入Cl,再加入CCl ,振荡,静置,下层呈紫色,该溶液中一定含有I-
2 4
答案 C
解析 氯化银也是不溶于稀硝酸的白色沉淀,该溶液中可能含有SO或Ag+,故C错误。
10.某溶液X中可能含有下列离子中的若干种:Fe3+、Na+、Ba2+、I-、H+、CO,下列有
关溶液X的假设与溶液成分的分析正确的是( )
选项 假设 溶液成分
A 溶液X遇酚酞变红色 溶质一定是NaCO
2 3
B 加入氨水后得到红褐色沉淀 一定不含I-
C 若加入铝粉后有Al3+生成 一定含有H+
D 若加入淀粉后溶液不显蓝色 一定不含有I-、一定含有CO
答案 B
解析 溶液X遇酚酞变红色说明其呈碱性,溶液中一定有CO,Fe3+、Ba2+、H+均不能与
CO共存,但I-能与CO共存,溶质可能为NaI和NaCO 的混合物,故A错误;由产生沉淀
2 3
的颜色得出一定有Fe3+,Fe3+不能与I-大量共存,故B正确;H+、Fe3+都能将铝粉氧化为
Al3+,故C错误;淀粉可检验出溶液中是否有I 而不是I-,若加入淀粉后溶液不显蓝色,不
2
能确定不含I-,故D错误。
11.某溶液可能含有等物质的量的Ba2+、Na+、NH、H+、Cl-、I-、SO、SO中的几种,向
该溶液中滴加少量新制氯水,所得溶液为无色。下列判断不正确的是( )
A.肯定不含NH B.肯定不含H+
C.肯定含有SO D.肯定不含Cl-
答案 A
解析 亚硫酸根离子的还原性强于碘离子,优先与少量氯水反应,由向溶液中滴加少量新制
氯水,所得溶液为无色可知,溶液中一定含有亚硫酸根离子,一定不含氢离子和钡离子;溶
液中各离子物质的量相等,由电荷守恒可知,溶液中一定含有钠离子和铵根离子,一定不含
有氯离子、碘离子和硫酸根离子,故选A。
12.某溶液中可能存在Br-、CO、SO、Al3+、I-、Mg2+、Na+七种离子中的某几种。现取
该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;②向所得橙色溶液中加入足
量BaCl 溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
2已知:5Cl+I+6HO===10HCl+2HIO
2 2 2 3
据此可以判断,该溶液中肯定不存在的离子组是( )
A.Al3+、Mg2+、SO B.Mg2+、CO、I-
C.Al3+、SO、I- D.Al3+、Br-、SO
答案 A
解析 根据①可判断溶液中有Br-和CO,根据离子共存原则,不存在Al3+、Mg2+;根据②
可判断溶液中无SO;根据③不能确定是否含有I-,因为在①中氯水可能把I-氧化成了IO,
致使淀粉溶液不变蓝色。
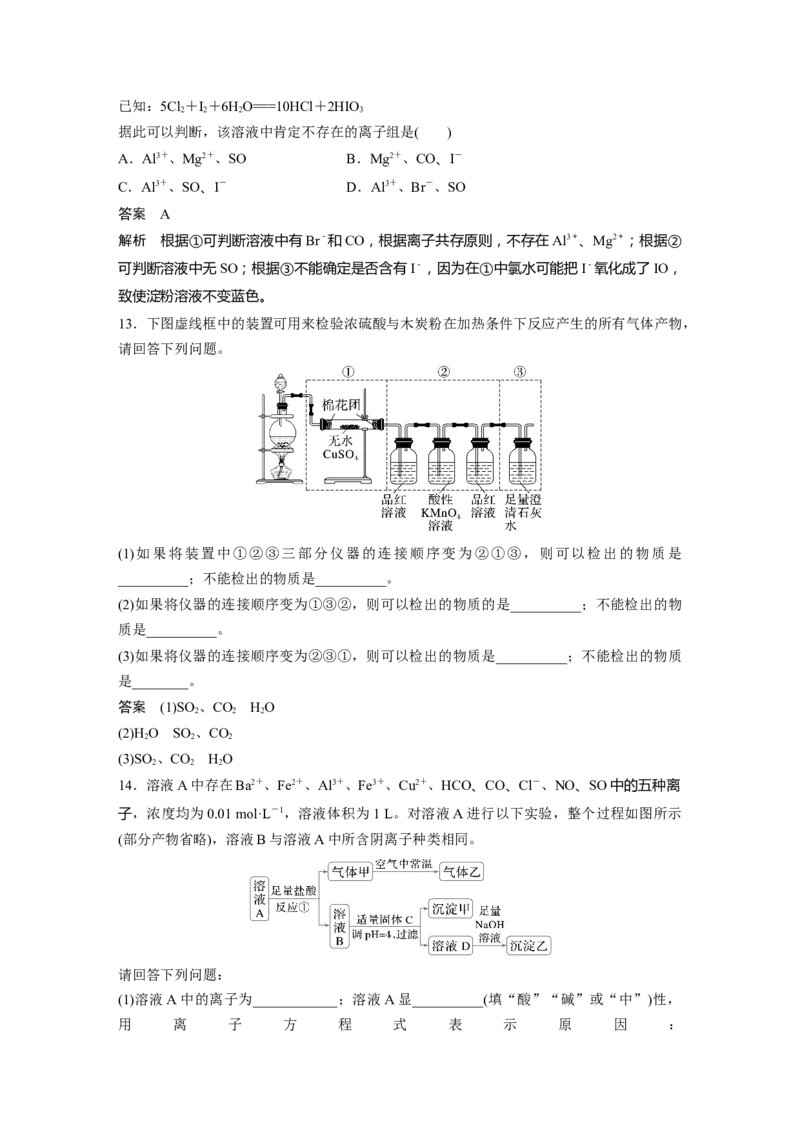
13.下图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,
请回答下列问题。
(1)如果将装置中①②③三部分仪器的连接顺序变为②①③,则可以检出的物质是
__________;不能检出的物质是__________。
(2)如果将仪器的连接顺序变为①③②,则可以检出的物质的是__________;不能检出的物
质是__________。
(3)如果将仪器的连接顺序变为②③①,则可以检出的物质是__________;不能检出的物质
是________。
答案 (1)SO 、CO HO
2 2 2
(2)H O SO 、CO
2 2 2
(3)SO 、CO HO
2 2 2
14.溶液A中存在Ba2+、Fe2+、Al3+、Fe3+、Cu2+、HCO、CO、Cl-、NO、SO中的五种离
子,浓度均为0.01 mol·L-1,溶液体积为1 L。对溶液A进行以下实验,整个过程如图所示
(部分产物省略),溶液B与溶液A中所含阴离子种类相同。
请回答下列问题:
(1)溶液A中的离子为____________;溶液A显__________(填“酸”“碱”或“中”)性,
用 离 子 方 程 式 表 示 原 因 :_____________________________________________________________
_________________________________________________________________(写出一个即可)。
(2)反应①的离子方程式为_________________________________________________________
_______________________________________________________________________________
。
(3)沉淀甲是__________(填化学式,下同),沉淀乙是__________。
(4)固体C可能是__________(填字母)。
a.CuO b.Cu(OH)
2
c.CuSO d.CuCl
4 2
(5)气体甲、气体乙都能造成环境问题,将等体积的气体甲和乙通入足量 NaOH溶液中,被
完 全 吸 收 , 写 出 反 应 的 离 子 方 程 式 :
_________________________________________________
_______________________________________________________________________________
。
答案 (1)Fe2+、Cu2+、Cl-、NO、SO 酸 Fe2++2HOFe(OH) +2H+、Cu2++
2 2
2HOCu(OH) +2H+(任写一个)
2 2
(2)3Fe2++4H++NO===3Fe3++NO↑+2HO
2
(3)Fe(OH) Cu(OH)
3 2
(4)ab
(5)NO+NO +2OH-===2NO+HO
2 2