文档内容
“学情空间”区域教研共同体高三入学检测
化学试题
可能用到的相对原子质量:
一、选择题:本题共10个小题,每小题2分,每个小题只有一个选项符合题目要求。
1. 化学与生产、生活、社会密切相关。下列有关说法中正确的是( )
A. 服用铬含量超标的药用胶囊会对人体健康造成危害
B. 酒精可以使蛋白质变性,酒精纯度越高杀菌消毒效果越好
C. 食品袋中放置的CaO可直接防止食品氧化变质
D. “酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成的
2. 下图是某84消毒液(有效成分为次氯酸钠)标签的部分内容。下列说法正确的是
84消毒液
[性状]本品为无色透明液体
[规格]250 mL、252.50 g
[含量]氯含量为5.00%
[贮藏]密封保存
A. 密封保存的目的是防止 分解
B. 该84消毒液中含 的质量为
C. 该84消毒液的密度为
D. 该84消毒液中含氯微粒的物质的量浓度约为
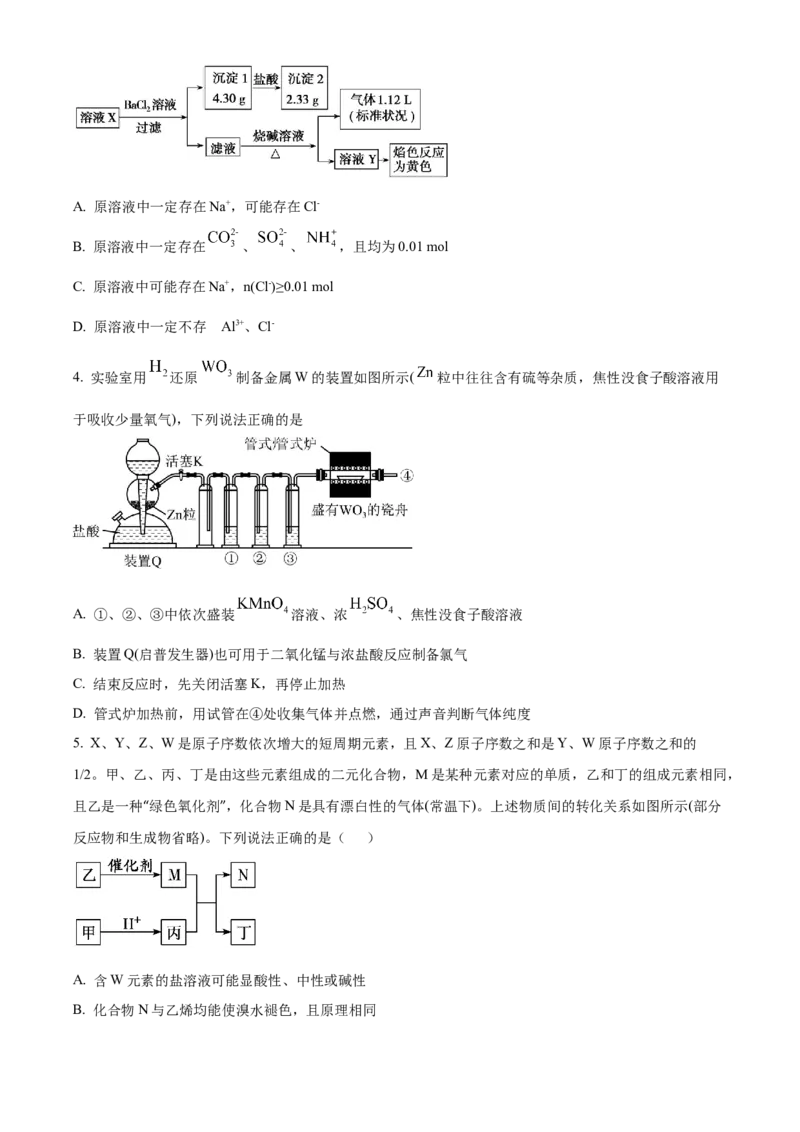
3. 某未知溶液X可能含有Al3+、Na+、 、Cl-、 、 中的若干种,取该溶液进行如下实验,若
实验过程中所加试剂均过量,产生的气体全部逸出。则下列说法正确的是
下载最新免费模拟卷,到公众号:一枚试卷君A. 原溶液中一定存在Na+,可能存在Cl-
B. 原溶液中一定存在 、 、 ,且均为0.01 mol
C. 原溶液中可能存在Na+,n(Cl-)≥0.01 mol
在
D. 原溶液中一定不存 Al3+、Cl-
4. 实验室用 还原 制备金属W的装置如图所示( 粒中往往含有硫等杂质,焦性没食子酸溶液用
于吸收少量氧气),下列说法正确的是
A. ①、②、③中依次盛装 溶液、浓 、焦性没食子酸溶液
B. 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
C. 结束反应时,先关闭活塞K,再停止加热
D. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
5. X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的
1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元素对应的单质,乙和丁的组成元素相同,
且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分
反应物和生成物省略)。下列说法正确的是( )
A. 含W元素的盐溶液可能显酸性、中性或碱性
B. 化合物N与乙烯均能使溴水褪色,且原理相同C. 原子半径:r(Y)>r(Z)>r(W)
D. Z与X、Y、W形成的化合物中,各元素均满足8电子结构
的
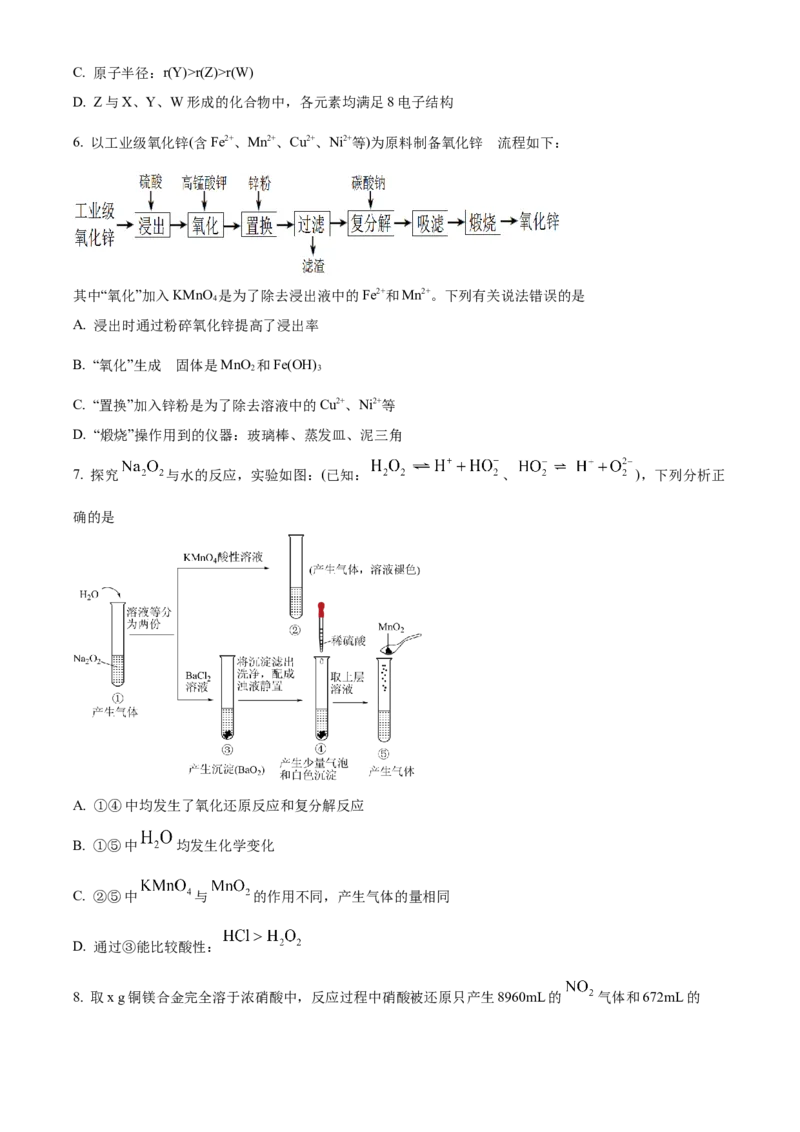
6. 以工业级氧化锌(含Fe2+、Mn2+、Cu2+、Ni2+等)为原料制备氧化锌 流程如下:
其中“氧化”加入KMnO 是为了除去浸出液中的Fe2+和Mn2+。下列有关说法错误的是
4
A. 浸出时通过粉碎氧化锌提高了浸出率
的
B. “氧化”生成 固体是MnO 和Fe(OH)
2 3
C. “置换”加入锌粉是为了除去溶液中的Cu2+、Ni2+等
D. “煅烧”操作用到的仪器:玻璃棒、蒸发皿、泥三角
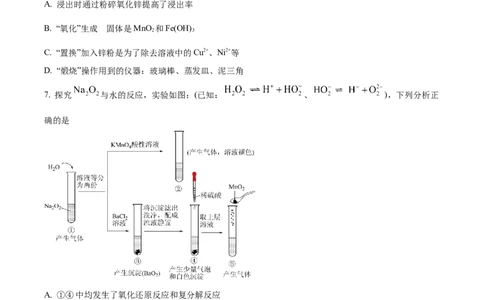
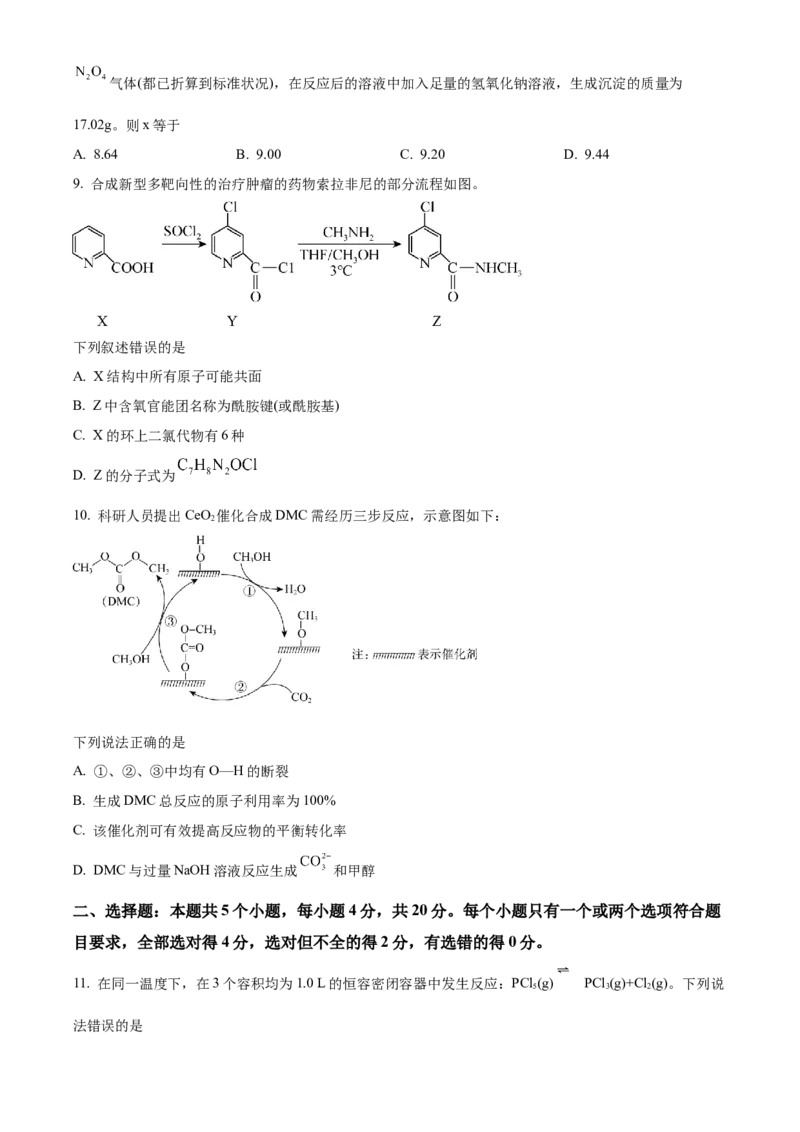
7. 探究 与水的反应,实验如图:(已知: 、 ),下列分析正
确的是
A. ①④中均发生了氧化还原反应和复分解反应
B. ①⑤中 均发生化学变化
C. ②⑤中 与 的作用不同,产生气体的量相同
D. 通过③能比较酸性:
8. 取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8960mL的 气体和672mL的气体(都已折算到标准状况),在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀的质量为
17.02g。则x等于
A. 8.64 B. 9.00 C. 9.20 D. 9.44
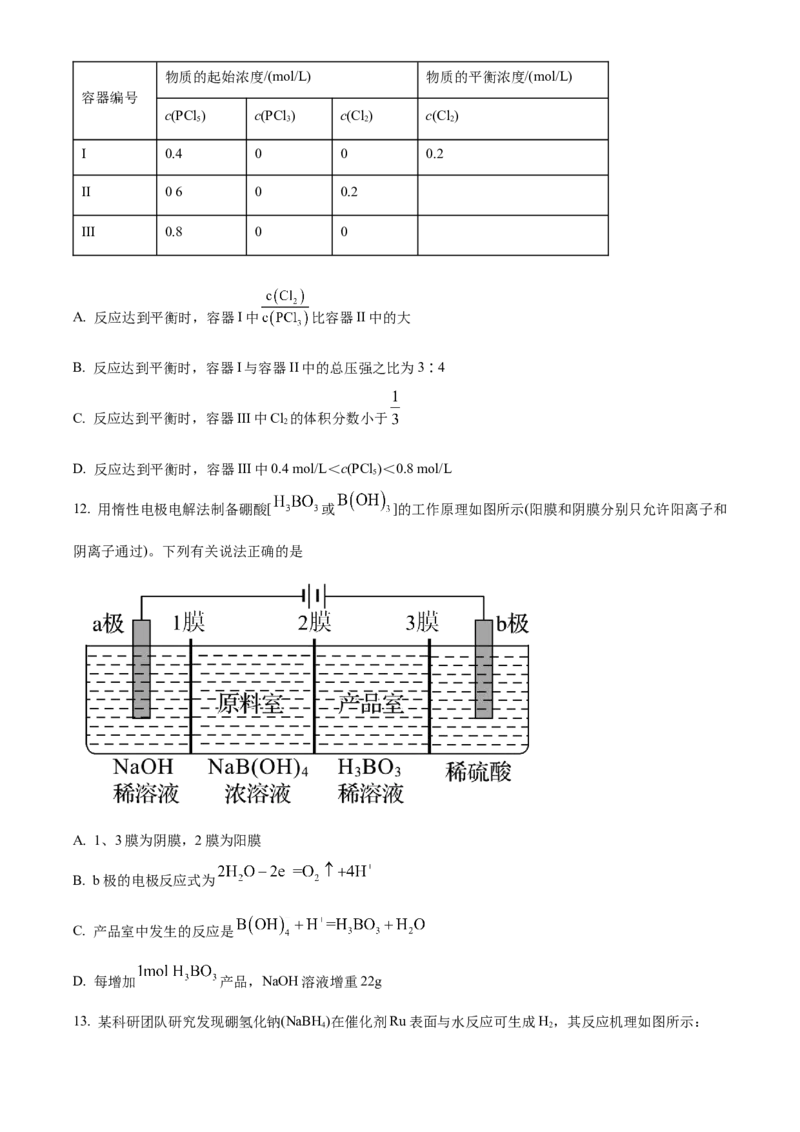
9. 合成新型多靶向性的治疗肿瘤的药物索拉非尼的部分流程如图。
下列叙述错误的是
A. X结构中所有原子可能共面
B. Z中含氧官能团名称为酰胺键(或酰胺基)
C. X的环上二氯代物有6种
D. Z的分子式为
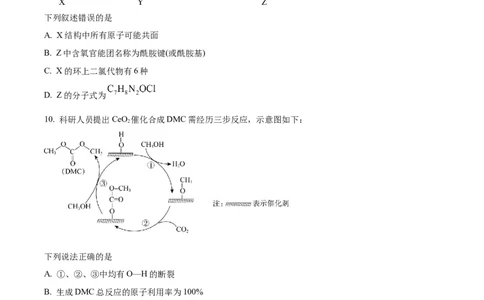
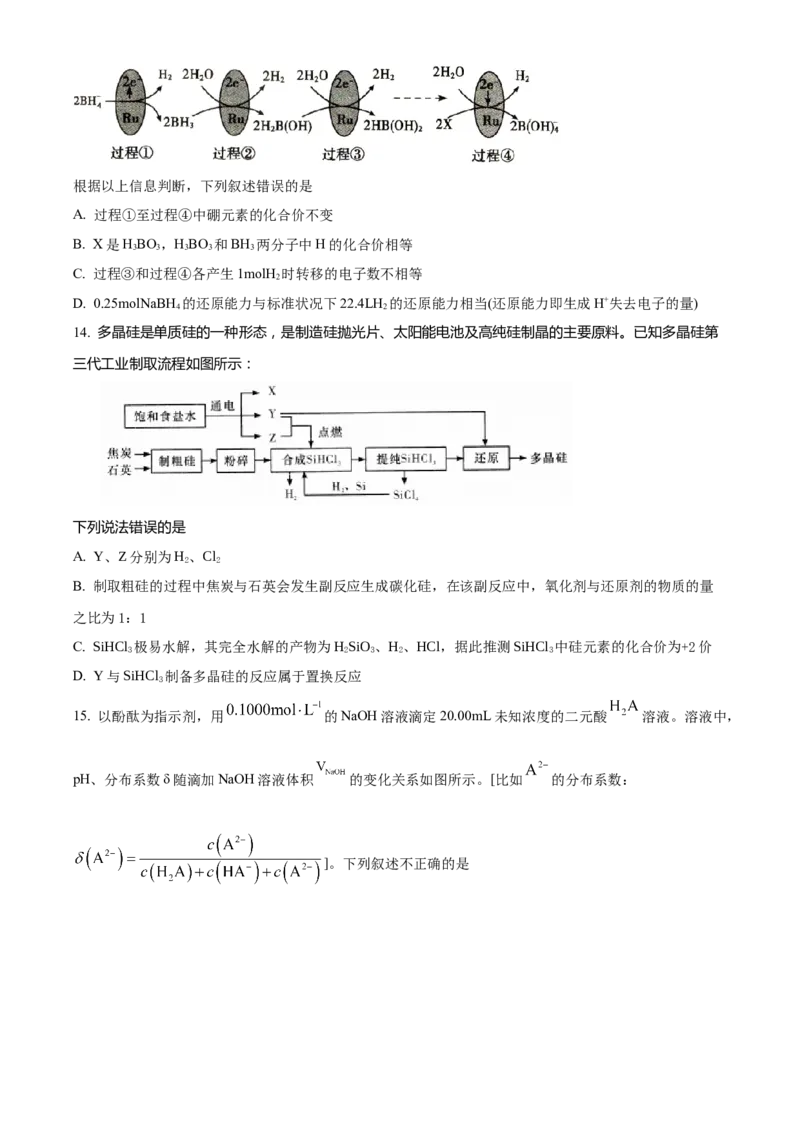
10. 科研人员提出CeO 催化合成DMC需经历三步反应,示意图如下:
2
下列说法正确的是
A. ①、②、③中均有O—H的断裂
B. 生成DMC总反应的原子利用率为100%
C. 该催化剂可有效提高反应物的平衡转化率
D. DMC与过量NaOH溶液反应生成 和甲醇
二、选择题:本题共5个小题,每小题4分,共20分。每个小题只有一个或两个选项符合题
目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11. 在同一温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl (g) PCl (g)+Cl (g)。下列说
5 3 2
法错误的是物质的起始浓度/(mol/L) 物质的平衡浓度/(mol/L)
容器编号
c(PCl ) c(PCl ) c(Cl ) c(Cl )
5 3 2 2
I 0.4 0 0 0.2
.
II 06 0 0.2
III 0.8 0 0
A. 反应达到平衡时,容器I中 比容器II中的大
B. 反应达到平衡时,容器I与容器II中的总压强之比为3∶4
C. 反应达到平衡时,容器III中Cl 的体积分数小于
2
D. 反应达到平衡时,容器III中0.4 mol/L<c(PCl )<0.8 mol/L
5
12. 用惰性电极电解法制备硼酸[ 或 ]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和
阴离子通过)。下列有关说法正确的是
A. 1、3膜为阴膜,2膜为阳膜
B. b极的电极反应式为
C. 产品室中发生的反应是
D. 每增加 产品,NaOH溶液增重22g
13. 某科研团队研究发现硼氢化钠(NaBH )在催化剂Ru表面与水反应可生成H,其反应机理如图所示:
4 2根据以上信息判断,下列叙述错误的是
A. 过程①至过程④中硼元素的化合价不变
B. X是HBO,HBO 和BH 两分子中H的化合价相等
3 3 3 3 3
C. 过程③和过程④各产生1molH 时转移的电子数不相等
2
D. 0.25molNaBH 的还原能力与标准状况下22.4LH 的还原能力相当(还原能力即生成H+失去电子的量)
4 2
14. 多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制晶的主要原料。已知多晶硅第
三代工业制取流程如图所示:
下列说法错误的是
A. Y、Z分别为H、Cl
2 2
B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量
之比为1:1
C. SiHCl 极易水解,其完全水解的产物为HSiO、H、HCl,据此推测SiHCl 中硅元素的化合价为+2价
3 2 3 2 3
D. Y与SiHCl 制备多晶硅的反应属于置换反应
3
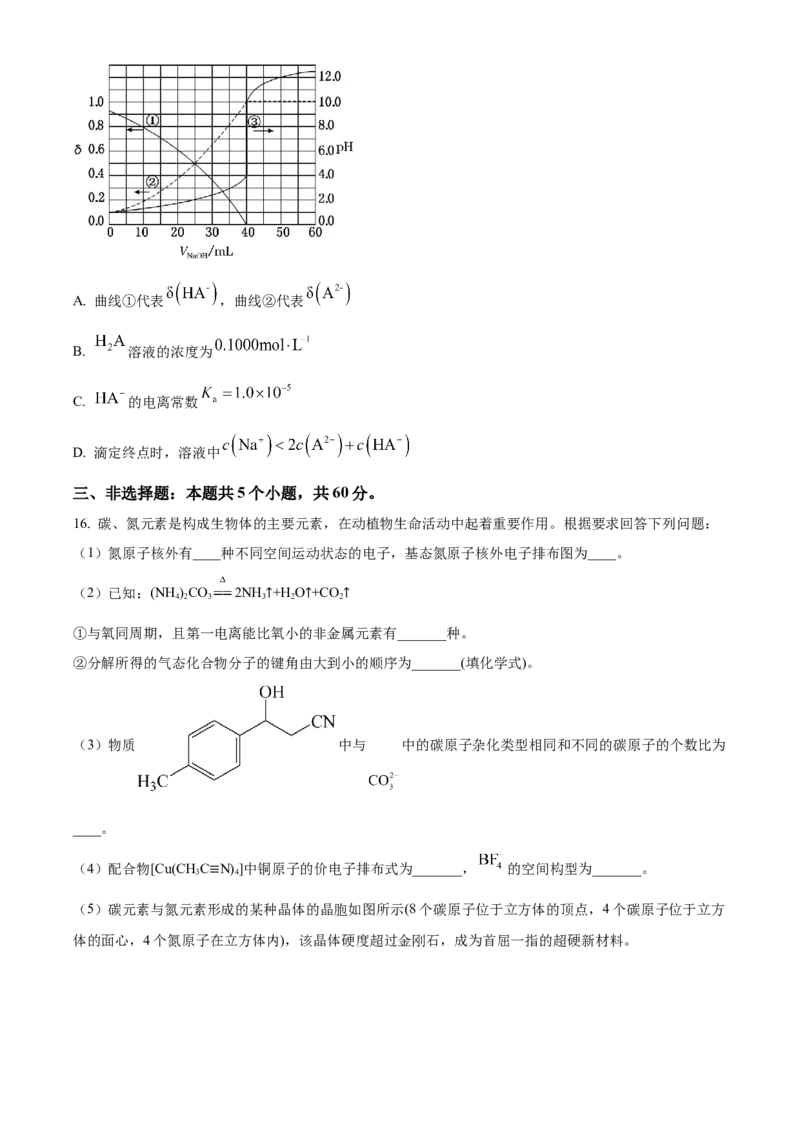
15. 以酚酞为指示剂,用 的NaOH溶液滴定20.00mL未知浓度的二元酸 溶液。溶液中,
pH、分布系数δ随滴加NaOH溶液体积 的变化关系如图所示。[比如 的分布系数:
]。下列叙述不正确的是A. 曲线①代表 ,曲线②代表
B. 溶液的浓度为
C. 的电离常数
D. 滴定终点时,溶液中
三、非选择题:本题共5个小题,共60分。
16. 碳、氮元素是构成生物体的主要元素,在动植物生命活动中起着重要作用。根据要求回答下列问题:
(1)氮原子核外有____种不同空间运动状态的电子,基态氮原子核外电子排布图为____。
(2)已知:(NH )CO 2NH +H O +CO
4 2 3 3 2 2
↑ ↑ ↑
①与氧同周期,且第一电离能比氧小的非金属元素有_______种。
②分解所得的气态化合物分子的键角由大到小的顺序为_______(填化学式)。
(3)物质 中与 中的碳原子杂化类型相同和不同的碳原子的个数比为
____。
(4)配合物[Cu(CHC N) ]中铜原子的价电子排布式为_______, 的空间构型为_______。
3 4
≡
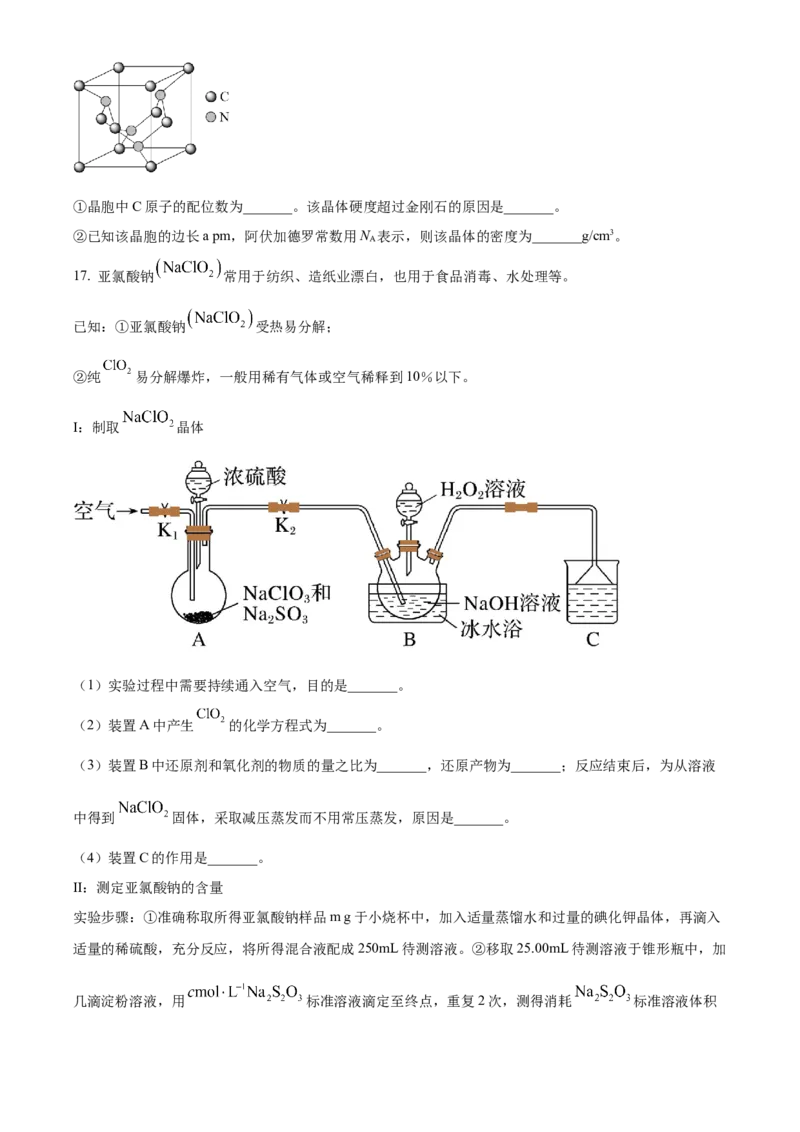
(5)碳元素与氮元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方
体的面心,4个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。①晶胞中C原子的配位数为_______。该晶体硬度超过金刚石的原因是_______。
②已知该晶胞的边长a pm,阿伏加德罗常数用N 表示,则该晶体的密度为_______g/cm3。
A
17. 亚氯酸钠 常用于纺织、造纸业漂白,也用于食品消毒、水处理等。
已知:①亚氯酸钠 受热易分解;
②纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
I:制取 晶体
(1)实验过程中需要持续通入空气,目的是_______。
(2)装置A中产生 的化学方程式为_______。
(3)装置B中还原剂和氧化剂的物质的量之比为_______,还原产物为_______;反应结束后,为从溶液
中得到 固体,采取减压蒸发而不用常压蒸发,原因是_______。
(4)装置C的作用是_______。
II:测定亚氯酸钠的含量
实验步骤:①准确称取所得亚氯酸钠样品m g于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入
适量的稀硫酸,充分反应,将所得混合液配成250mL待测溶液。②移取25.00mL待测溶液于锥形瓶中,加
几滴淀粉溶液,用 标准溶液滴定至终点,重复2次,测得消耗 标准溶液体积的平均值为V mL。(已知: 、 )
(5)达到滴定终点时的现象为_______。
(6)该样品中 的质量分数为_______%(用含m、c、V的代数式表示)。在滴定操作正确的情况下,
此实验测得结果偏高,可能原因为_______(用离子方程式表示)。
18. 草酸钴可用于指示剂和催化剂的制备。用含钴废料(主要成分为Co,含有一定量的NiO、 、
Fe、 等),制备草酸钴晶体 的流程如下:
已知:①草酸钴晶体难溶于水;②RH为有机物(难电离)。回答下列问题:
的
(1)酸浸时钴溶解反应 化学方程式为_______,浸出液中加入 后发生反应的离子方程式为_______。
(2)加入氧化钴的目的是_______,滤渣II高温灼烧的产物主要有_______。
(3)操作①为_______(填操作名称)。
(4)已知: ;
;
。
该流程中所用 溶液的pH_______7(填“>”“<”或“=”)。
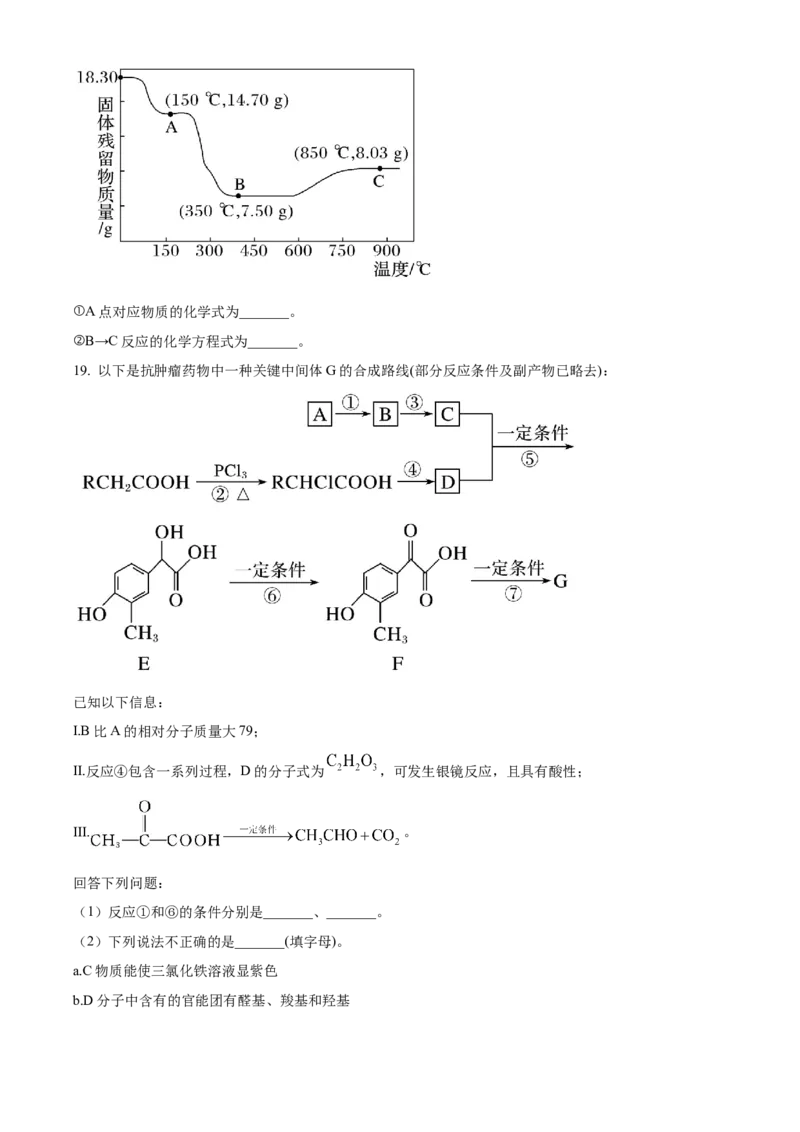
(5)钴的含氧酸盐受热分解最终产物多为氧化物,已知 热分解质量变化过程如图
所示(其中600℃以前是隔绝空气加热,600℃以后是在空气中加热),A、B、C均为纯净物。①A点对应物质的化学式为_______。
②B→C反应的化学方程式为_______。
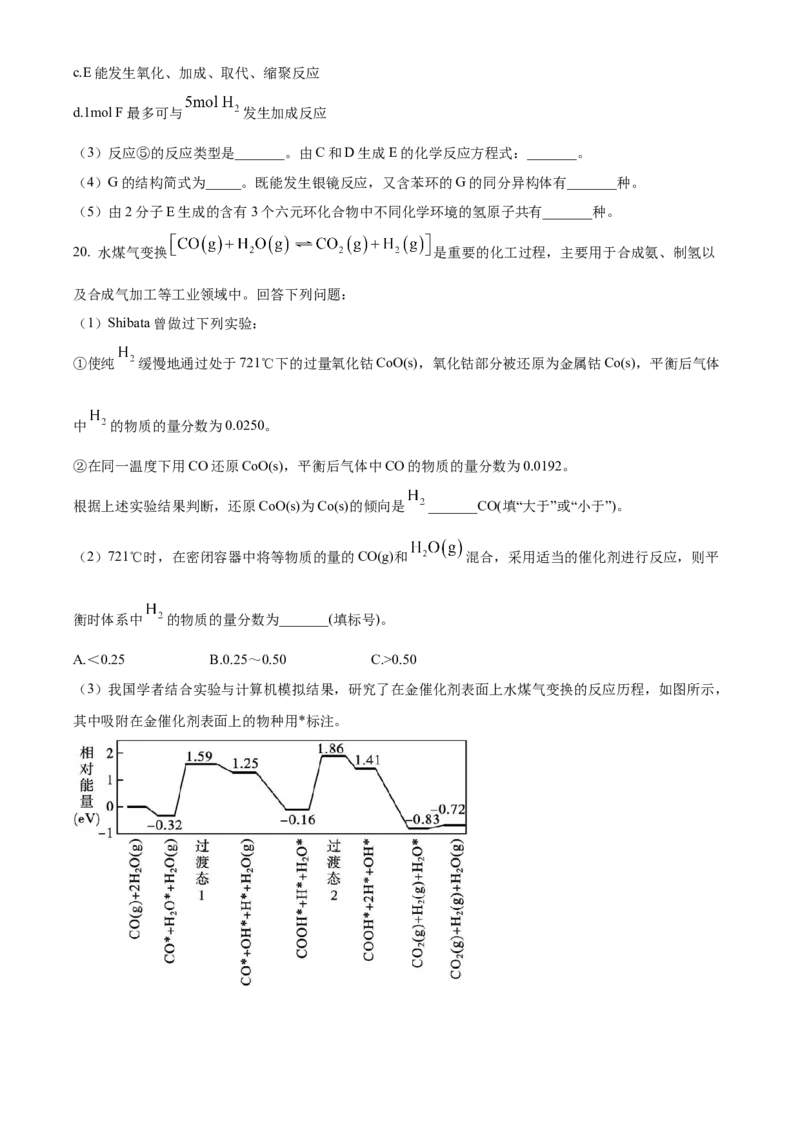
19. 以下是抗肿瘤药物中一种关键中间体G的合成路线(部分反应条件及副产物已略去):
已知以下信息:
I.B比A的相对分子质量大79;
II.反应④包含一系列过程,D的分子式为 ,可发生银镜反应,且具有酸性;
III. 。
回答下列问题:
(1)反应①和⑥的条件分别是_______、_______。
(2)下列说法不正确的是_______(填字母)。
a.C物质能使三氯化铁溶液显紫色
b.D分子中含有的官能团有醛基、羧基和羟基c.E能发生氧化、加成、取代、缩聚反应
d.1mol F最多可与 发生加成反应
(3)反应⑤的反应类型是_______。由C和D生成E的化学反应方程式:_______。
(4)G的结构简式为_____。既能发生银镜反应,又含苯环的G的同分异构体有_______种。
(5)由2分子E生成的含有3个六元环化合物中不同化学环境的氢原子共有_______种。
20. 水煤气变换 是重要的化工过程,主要用于合成氨、制氢以
及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:
①使纯 缓慢地通过处于721℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴Co(s),平衡后气体
中 的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是 _______CO(填“大于”或“小于”)。
(2)721℃时,在密闭容器中将等物质的量的CO(g)和 混合,采用适当的催化剂进行反应,则平
衡时体系中 的物质的量分数为_______(填标号)。
A.<0.25 B.0.25~0.50 C.>0.50
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,
其中吸附在金催化剂表面上的物种用*标注。可知水煤气变换的 _______0(填“>”或“<”),该历程中最大能垒(活化能) _______eV,写出该步骤
的化学方程式_______。
(4)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数 。
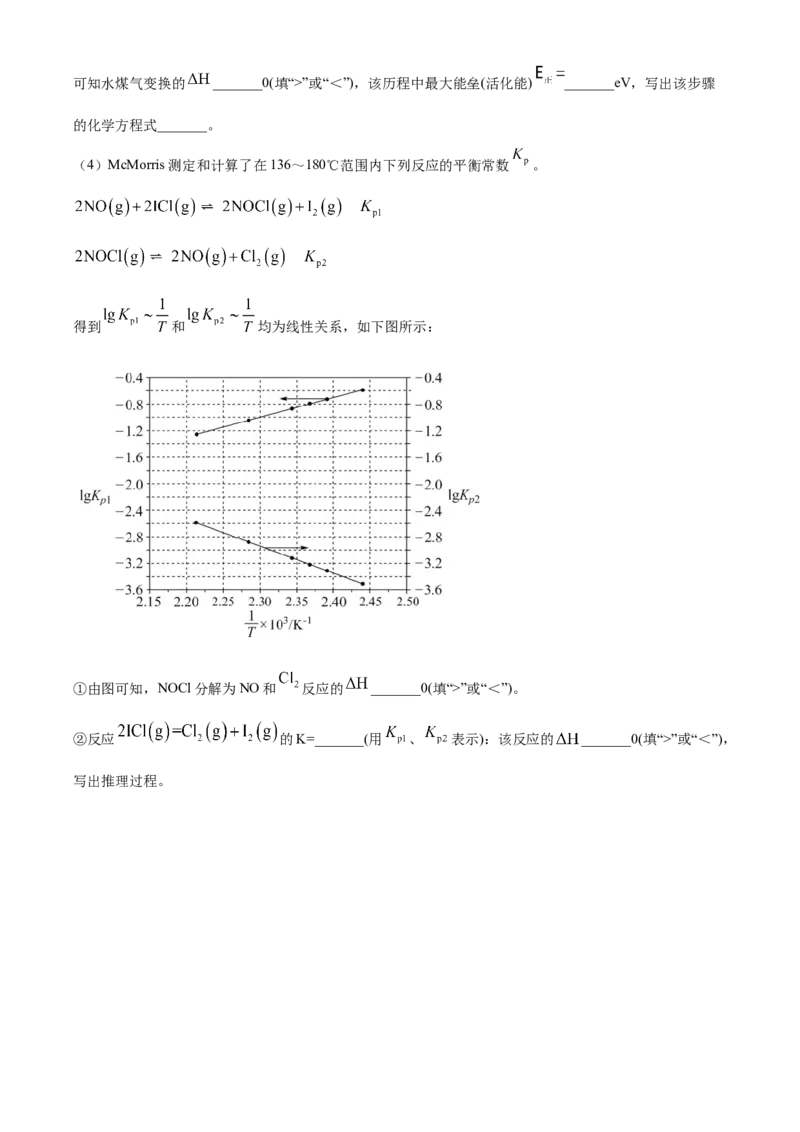
得到 和 均为线性关系,如下图所示:
①由图可知,NOCl分解为NO和 反应的 _______0(填“>”或“<”)。
②反应 的K=_______(用 、 表示):该反应的 _______0(填“>”或“<”),
写出推理过程。下载最新免费模拟卷,到公众号:一枚试卷君