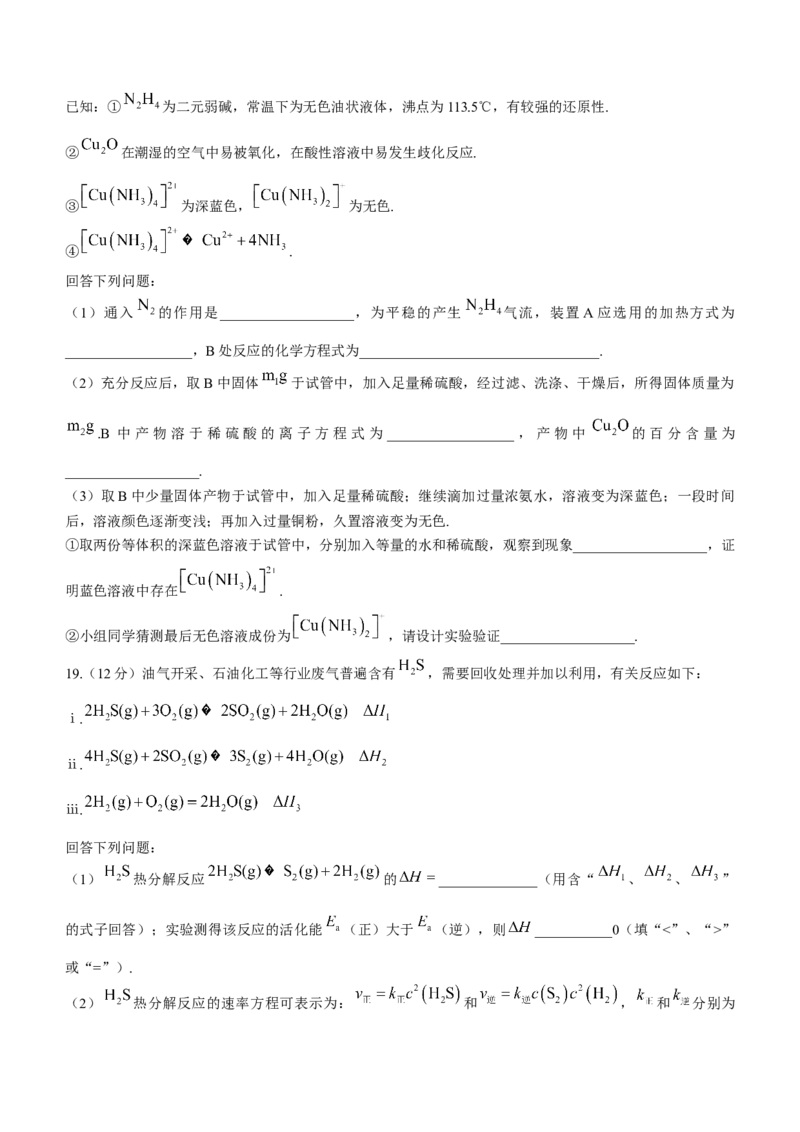文档内容
2022 年 10 月份过程性检测
化学试题
2022.10
注意事项:
1.答题前,考生先将自己的学校、班级、姓名、考生号、座号填写在相应位置.
2.选择题答案必须使用2B铅笔(按填涂样例)正确填涂;非选择题答案必须使用 0.5毫米黑色签字笔书写,
字体工整、笔迹清楚.
3.请按照题号在各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试题卷答题无效.保持
卡面清洁,不折叠,不破损.
可能用到的相对原子质量:H-1 C-12 N-14 O-18 F-19 Cl-35.5 Fe-56 Cu-64
一、选择题:本题共10小题,每小题2分,共20分.每小题只有一个选项符合题目要求.
1.化学无处不在.下列叙述正确的是( )
A.催化剂能改变可逆反应达到平衡的时间
B.84消毒液与洁厕灵混合使用去污杀菌效果更好
C.将海水经过一系列处理得到 溶液,电解可得到金属镁
D.碳酸氢钠和碳酸钠均能与酸反应调节面团酸度,都可用作膨松剂
2.下列实验方法或操作叙述正确的是( )
A.用湿润的蓝色石蕊试纸检验氨气
B.萃取实验中,振荡后需打开分液漏斗活塞放气
C.将 溶液保存在带玻璃塞的试剂瓶中
D.将实验用剩的金属钠块放入废物缸
3.《开宝本草》载:“硝石( )所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”.下列叙述
正确的是( )
A.温度降低,硝石的溶解度增大 B.硝石易溶于水,且水溶液显碱性
C.产生“霜”的过程涉及化学变化 D.上述提纯过程涉及溶解、蒸发、结晶
4. 表示阿伏加德罗常数的值.下列说法正确的是( )
A.18g重水( )中含有的中子数为
B.常温下,5.6g铁与 硝酸反应,铁失去的电子数为
C. 和 于密闭容器中充分反应生成的 分子总数小于
D.标准状况下,5.6L CO和 混合气体中分子数目与碳原子数目均为
5.含S元素的某钠盐a能发生如图转化.下列说法错误的是( )A.a可能为正盐,也可能为酸式盐
B.c为不溶于盐酸的白色沉淀
C.反应①中氧化剂和还原剂物质的量之比为1∶1
D.反应②中还可能生成淡黄色沉淀
6.下列实验装置或操作均正确,且能达到预期目的的是( )
A B C D
吸收HCl气体 稀释浓硫酸与铜的反应混合液 检验溶液中是否含有钾元素
制备少量
7.下列反应的离子方程式正确的是( )
A.用惰性电极电解饱和食盐水:
B. 放入水中:
C. 通过灼热铁粉:
D.氯气通入石灰乳中:
8.C和 在生产、生活、科技中是非常重要的燃料.已知:
①
②
下列推断正确的是( )
A. 的摩尔燃烧焓为
B.
C.D.由②可知该反应中,反应物化学键中储存的总能量比产物化学键储存的能量高
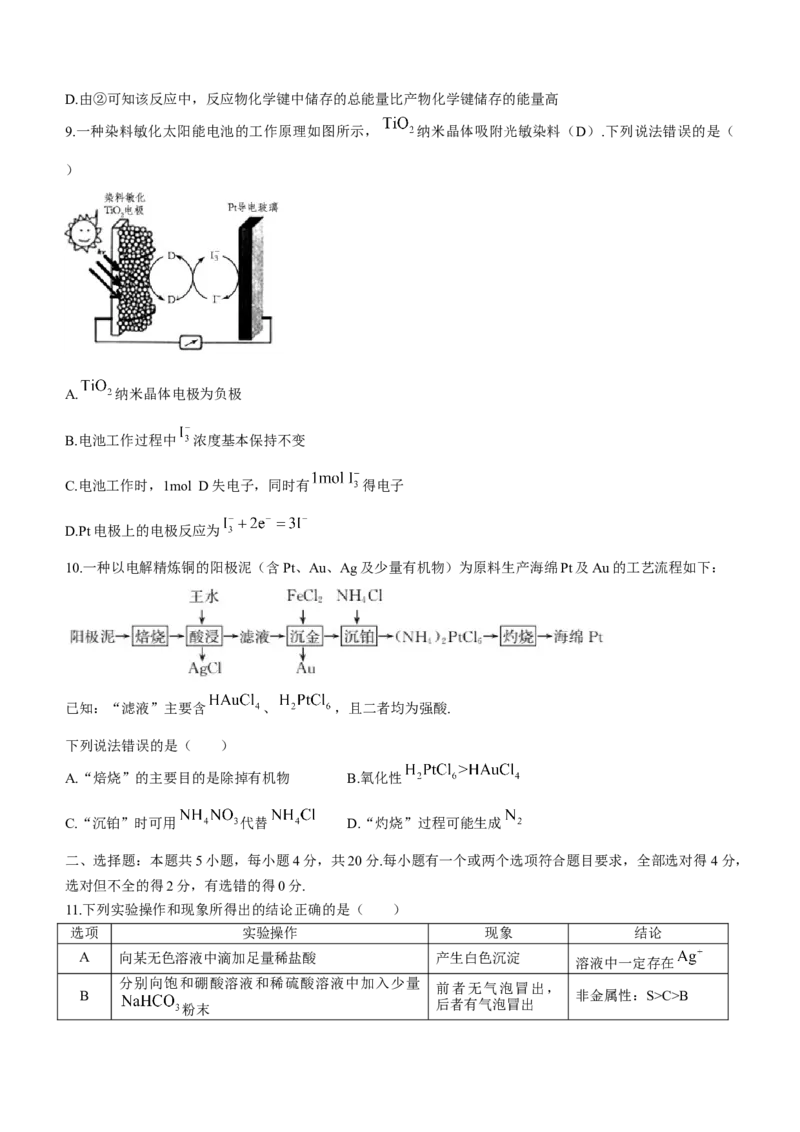
9.一种染料敏化太阳能电池的工作原理如图所示, 纳米晶体吸附光敏染料(D).下列说法错误的是(
)
A. 纳米晶体电极为负极
B.电池工作过程中 浓度基本保持不变
C.电池工作时,1mol D失电子,同时有 得电子
D.Pt电极上的电极反应为
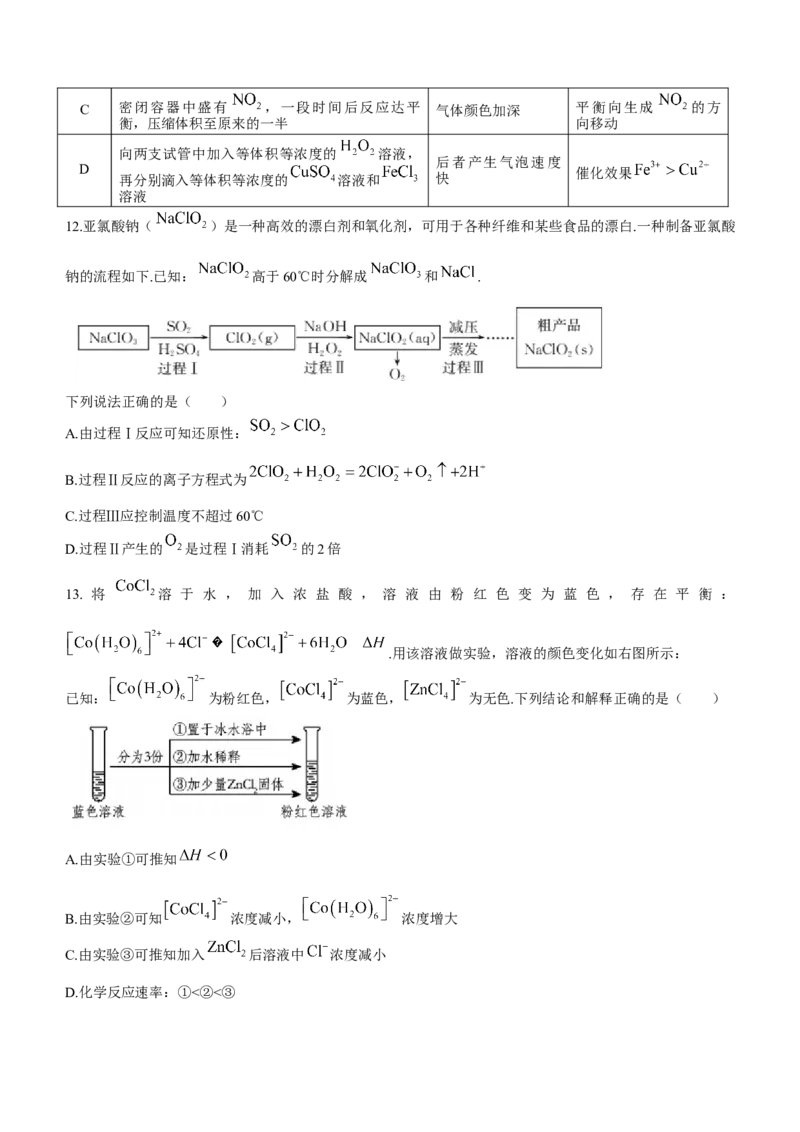
10.一种以电解精炼铜的阳极泥(含Pt、Au、Ag及少量有机物)为原料生产海绵Pt及Au的工艺流程如下:
已知:“滤液”主要含 、 ,且二者均为强酸.
下列说法错误的是( )
A.“焙烧”的主要目的是除掉有机物 B.氧化性
C.“沉铂”时可用 代替 D.“灼烧”过程可能生成
二、选择题:本题共5小题,每小题4分,共20分.每小题有一个或两个选项符合题目要求,全部选对得4分,
选对但不全的得2分,有选错的得0分.
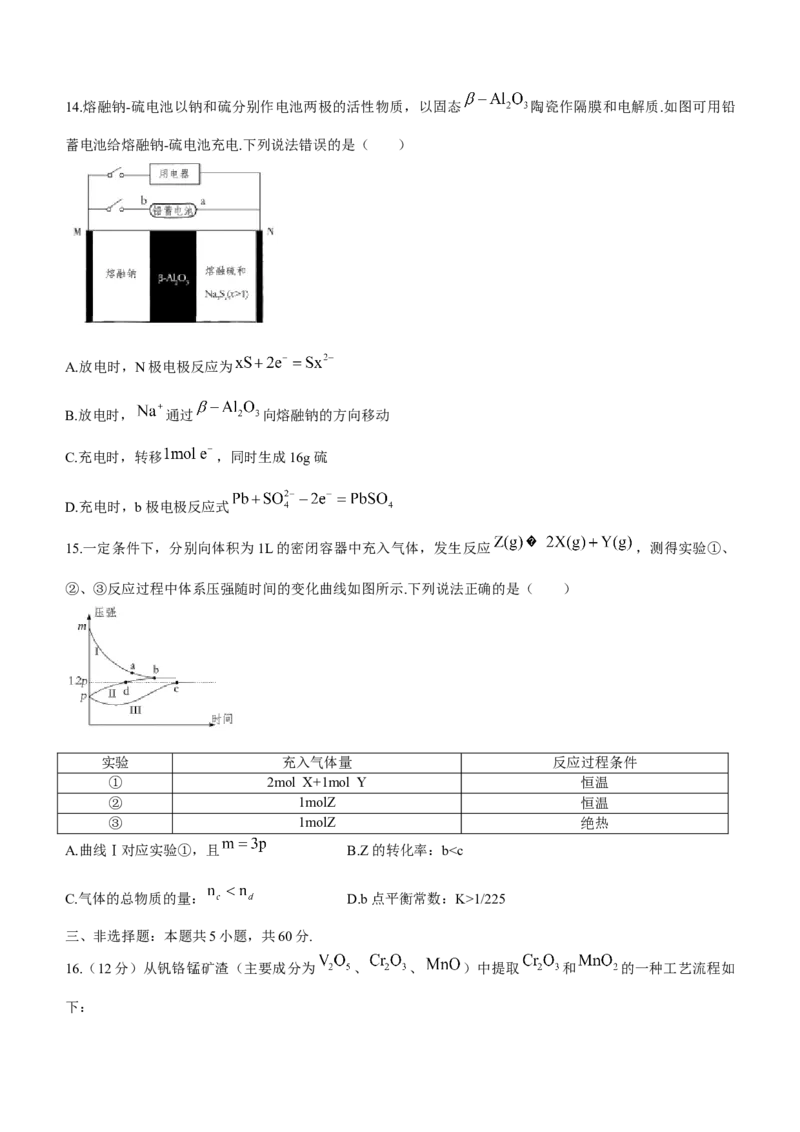
11.下列实验操作和现象所得出的结论正确的是( )
选项 实验操作 现象 结论
A 向某无色溶液中滴加足量稀盐酸 产生白色沉淀
溶液中一定存在
分别向饱和硼酸溶液和稀硫酸溶液中加入少量
前者无气泡冒出,
B 非金属性:S>C>B
后者有气泡冒出
粉末C 密闭容器中盛有 ,一段时间后反应达平 气体颜色加深 平衡向生成 的方
衡,压缩体积至原来的一半 向移动
向两支试管中加入等体积等浓度的 溶液,
后者产生气泡速度
D 催化效果
再分别滴入等体积等浓度的 溶液和 快
溶液
12.亚氯酸钠( )是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白.一种制备亚氯酸
钠的流程如下.已知: 高于60℃时分解成 和 .
下列说法正确的是( )
A.由过程Ⅰ反应可知还原性:
B.过程Ⅱ反应的离子方程式为
C.过程Ⅲ应控制温度不超过60℃
D.过程Ⅱ产生的 是过程Ⅰ消耗 的2倍
13. 将 溶 于 水 , 加 入 浓 盐 酸 , 溶 液 由 粉 红 色 变 为 蓝 色 , 存 在 平 衡 :
.用该溶液做实验,溶液的颜色变化如右图所示:
已知: 为粉红色, 为蓝色, 为无色.下列结论和解释正确的是( )
A.由实验①可推知
B.由实验②可知 浓度减小, 浓度增大
C.由实验③可推知加入 后溶液中 浓度减小
D.化学反应速率:①<②<③14.熔融钠-硫电池以钠和硫分别作电池两极的活性物质,以固态 陶瓷作隔膜和电解质.如图可用铅
蓄电池给熔融钠-硫电池充电.下列说法错误的是( )
A.放电时,N极电极反应为
B.放电时, 通过 向熔融钠的方向移动
C.充电时,转移 ,同时生成16g硫
D.充电时,b极电极反应式
15.一定条件下,分别向体积为1L的密闭容器中充入气体,发生反应 ,测得实验①、
②、③反应过程中体系压强随时间的变化曲线如图所示.下列说法正确的是( )
实验 充入气体量 反应过程条件
① 2mol X+1mol Y 恒温
② 1molZ 恒温
③ 1molZ 绝热
A.曲线Ⅰ对应实验①,且 B.Z的转化率:b1/225
三、非选择题:本题共5小题,共60分.
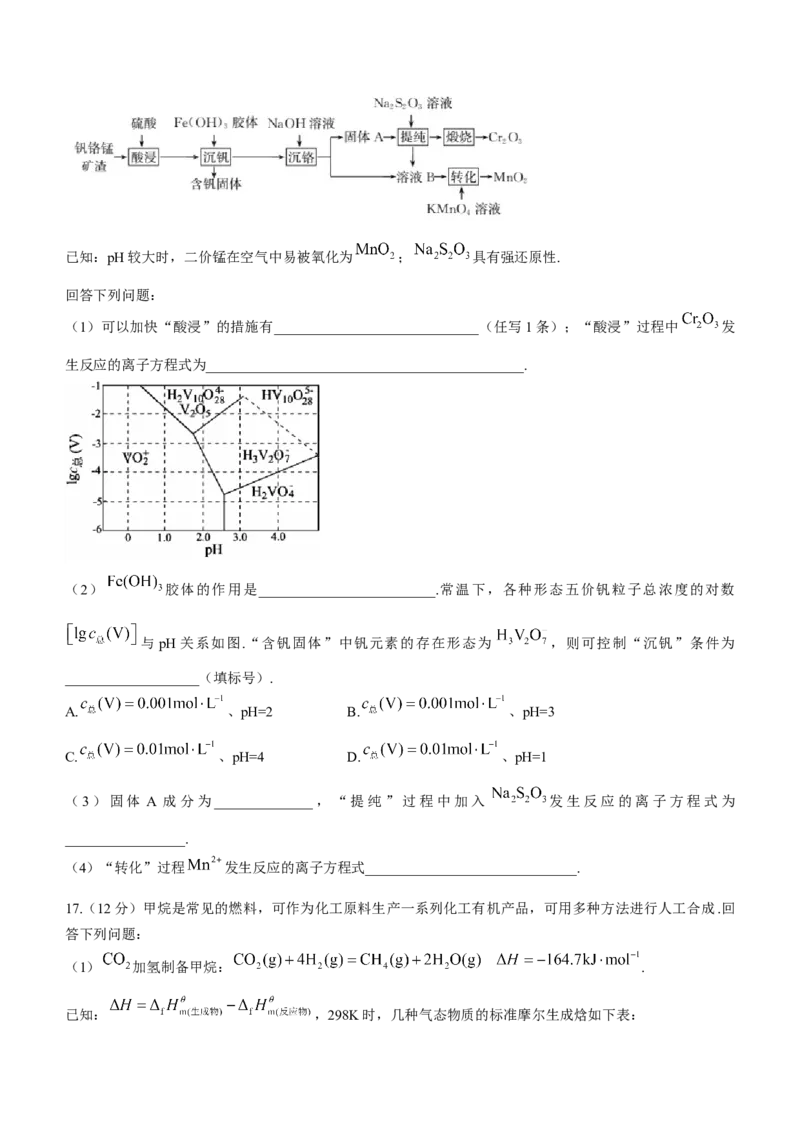
16.(12分)从钒铬锰矿渣(主要成分为 、 、 )中提取 和 的一种工艺流程如
下:已知:pH较大时,二价锰在空气中易被氧化为 ; 具有强还原性.
回答下列问题:
(1)可以加快“酸浸”的措施有_____________________________(任写1条);“酸浸”过程中 发
生反应的离子方程式为_____________________________________________.
(2) 胶体的作用是_________________________.常温下,各种形态五价钒粒子总浓度的对数
与 pH 关系如图.“含钒固体”中钒元素的存在形态为 ,则可控制“沉钒”条件为
___________________(填标号).
A. 、pH=2 B. 、pH=3
C. 、pH=4 D. 、pH=1
(3)固体 A 成分为______________,“提纯”过程中加入 发生反应的离子方程式为
_________________.
(4)“转化”过程 发生反应的离子方程式______________________________.
17.(12分)甲烷是常见的燃料,可作为化工原料生产一系列化工有机产品,可用多种方法进行人工合成.回
答下列问题:
(1) 加氢制备甲烷: .
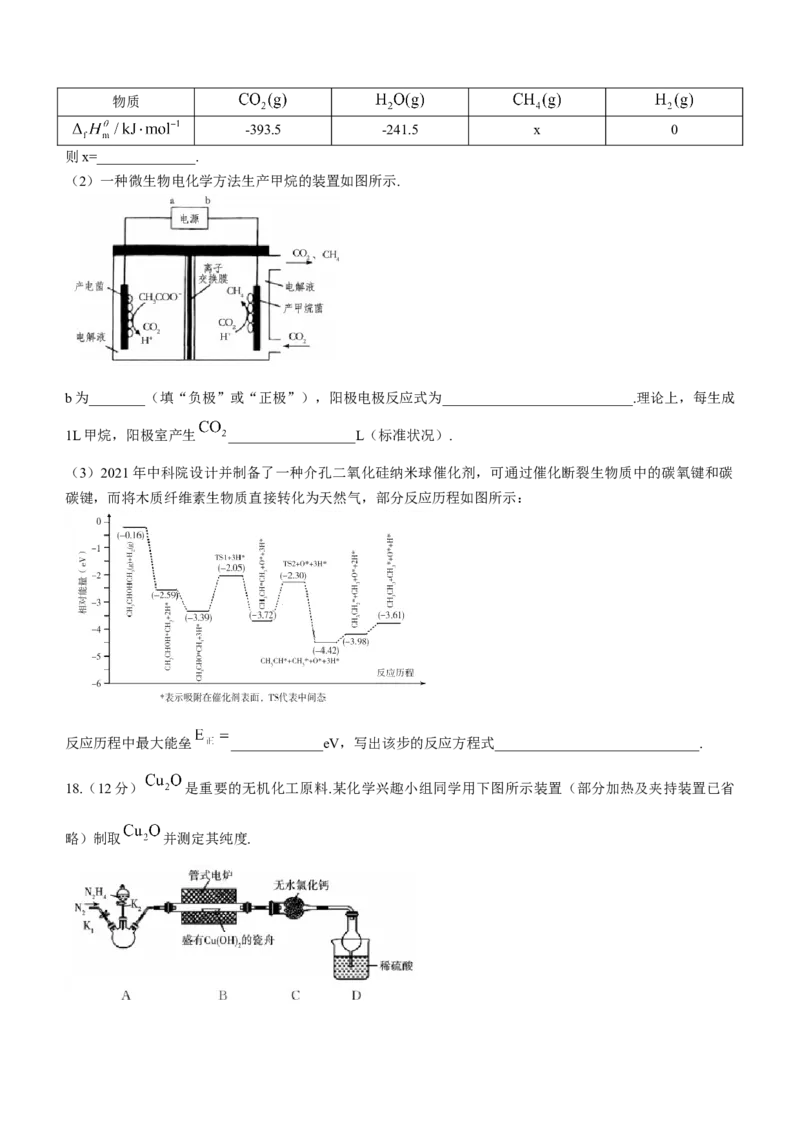
已知: ,298K时,几种气态物质的标准摩尔生成焓如下表:物质
-393.5 -241.5 x 0
则x=______________.
(2)一种微生物电化学方法生产甲烷的装置如图所示.
b为________(填“负极”或“正极”),阳极电极反应式为___________________________.理论上,每生成
1L甲烷,阳极室产生 __________________L(标准状况).
(3)2021年中科院设计并制备了一种介孔二氧化硅纳米球催化剂,可通过催化断裂生物质中的碳氧键和碳
碳键,而将木质纤维素生物质直接转化为天然气,部分反应历程如图所示:
反应历程中最大能垒 _____________eV,写出该步的反应方程式_____________________________.
18.(12分) 是重要的无机化工原料.某化学兴趣小组同学用下图所示装置(部分加热及夹持装置已省
略)制取 并测定其纯度.已知:① 为二元弱碱,常温下为无色油状液体,沸点为113.5℃,有较强的还原性.
② 在潮湿的空气中易被氧化,在酸性溶液中易发生歧化反应.
③ 为深蓝色, 为无色.
④ .
回答下列问题:
(1)通入 的作用是___________________,为平稳的产生 气流,装置 A 应选用的加热方式为
__________________,B处反应的化学方程式为__________________________________.
(2)充分反应后,取B中固体 于试管中,加入足量稀硫酸,经过滤、洗涤、干燥后,所得固体质量为
.B 中产物溶于稀硫酸的离子方程式为__________________,产物中 的百分含量为
___________________.
(3)取B中少量固体产物于试管中,加入足量稀硫酸;继续滴加过量浓氨水,溶液变为深蓝色;一段时间
后,溶液颜色逐渐变浅;再加入过量铜粉,久置溶液变为无色.
①取两份等体积的深蓝色溶液于试管中,分别加入等量的水和稀硫酸,观察到现象___________________,证
明蓝色溶液中存在 .
②小组同学猜测最后无色溶液成份为 ,请设计实验验证___________________.
19.(12分)油气开采、石油化工等行业废气普遍含有 ,需要回收处理并加以利用,有关反应如下:
ⅰ.
ⅱ.
ⅲ.
回答下列问题:
(1) 热分解反应 的 ______________(用含“ 、 、 ”
的式子回答);实验测得该反应的活化能 (正)大于 (逆),则 ___________0(填“<”、“>”
或“=”).
(2) 热分解反应的速率方程可表示为: 和 , 和 分别为正、逆反应速率常数.T℃时, , ,则该温度下 热分解反应的平衡常数
K=___________.
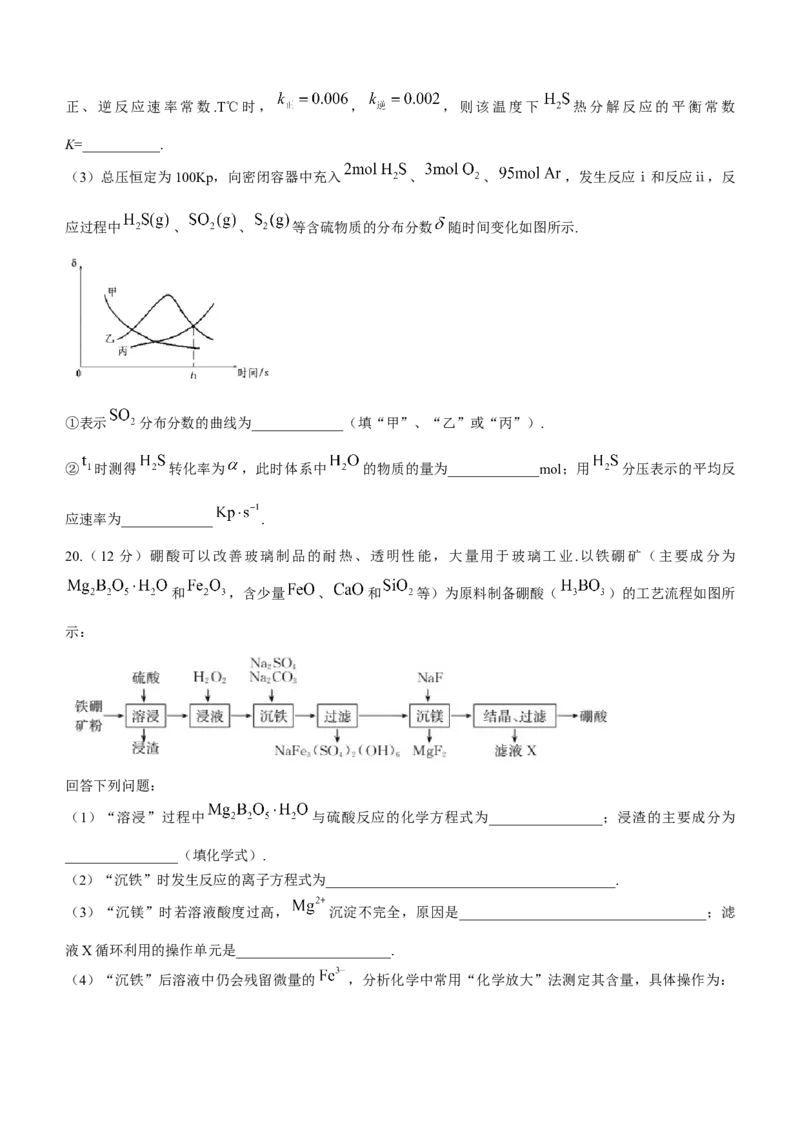
(3)总压恒定为100Kp,向密闭容器中充入 、 、 ,发生反应ⅰ和反应ⅱ,反
应过程中 、 、 等含硫物质的分布分数 随时间变化如图所示.
①表示 分布分数的曲线为_____________(填“甲”、“乙”或“丙”).
② 时测得 转化率为 ,此时体系中 的物质的量为_____________mol;用 分压表示的平均反
应速率为_____________ .
20.(12 分)硼酸可以改善玻璃制品的耐热、透明性能,大量用于玻璃工业.以铁硼矿(主要成分为
和 ,含少量 、 和 等)为原料制备硼酸( )的工艺流程如图所
示:
回答下列问题:
(1)“溶浸”过程中 与硫酸反应的化学方程式为________________;浸渣的主要成分为
________________(填化学式).
(2)“沉铁”时发生反应的离子方程式为_________________________________________.
(3)“沉镁”时若溶液酸度过高, 沉淀不完全,原因是___________________________________;滤
液X循环利用的操作单元是______________________.
(4)“沉铁”后溶液中仍会残留微量的 ,分析化学中常用“化学放大”法测定其含量,具体操作为:取100mL“沉铁”后溶液,酸化后加入过量的KI,再用 萃取、分液;有机相用 水溶液进行还原
并反萃取,反萃取生成的 再加入过量的 将其氧化为 ,煮沸除去 ,加入过量的KI,酸化后用
标准溶液进行滴定,达到滴定终点时消耗 V mL.则“沉铁”后溶液中 的浓度为
_______________ (已知: , ).
高三化学试题参考答案及评分标准
一、选择题(每小题2分,共20分)
1-10ABDCC CACCB
二、选择题(每小题4分,共20分;每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全
的得2分,有选错的得0分)
11-15B AC C BC AD
三、非选择题:本题共5小题,共60分.
16.(12分)
(1)粉碎、适当增大酸的浓度、升温等(1分); (2分)
(2)吸附含钒离子生成沉淀(1分)AB(2分)
(3) 、 (2分) (2分)
(4) (2分)
17.(12分)(1)-74.6(2分)
(2)负极(2分) (2分)2(2分)
(3)1.42(2分) (2分)
18.(12分)(1)排净装置空气;(1分)油浴加热;(1分)
(2分)
(2) (2分) (2分)
(3)①加入稀硫酸的溶液颜色比加水的溶液颜色变得更浅;(2分)
②取少量无色溶液于试管中,通入氧气,一段时间后,溶液颜色由无色变为深蓝色,证明无色溶液为
.(2分)
19.(12分)(1) (2分)>(2分)
(2)3(2分)
(3)①乙(2分)② (2分) (2分)
20.(12分)(1) (2分) 和 (2分)
(2) (2分)
(3) 与 结合形成弱电解质HF,使 浓度减小,不能使 完全沉淀(2分)沉铁(2分)
(4) (2分)