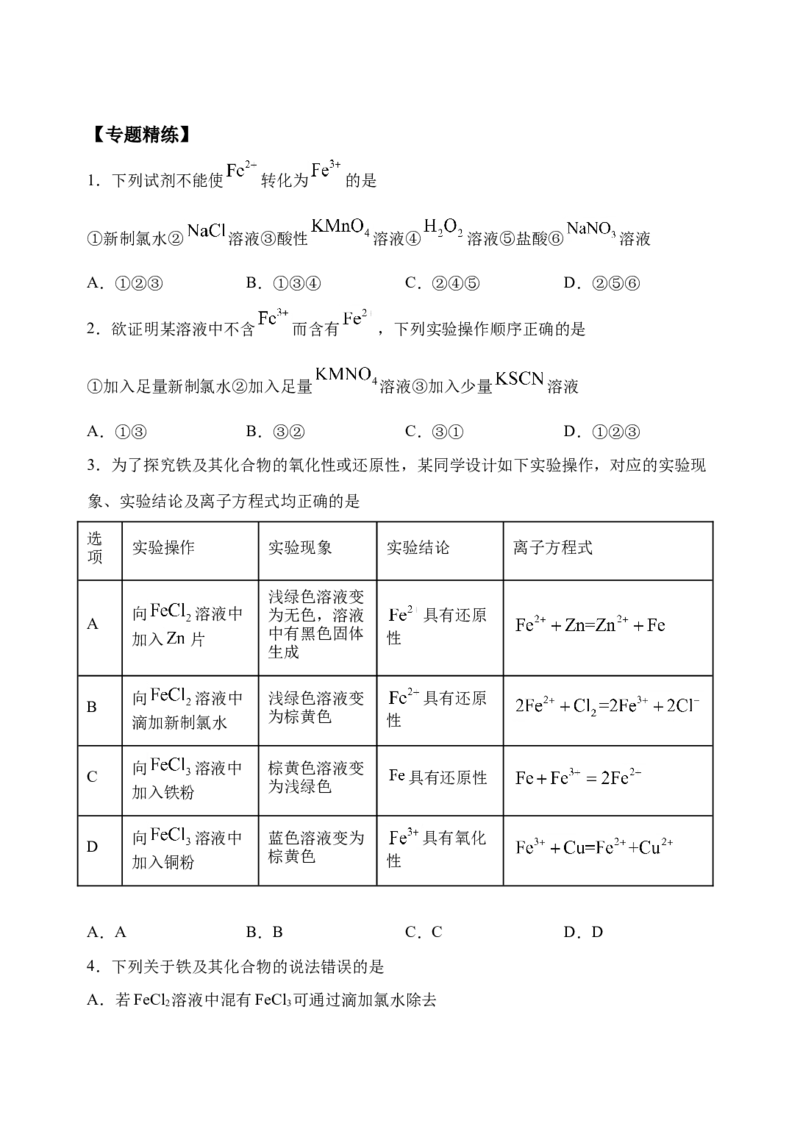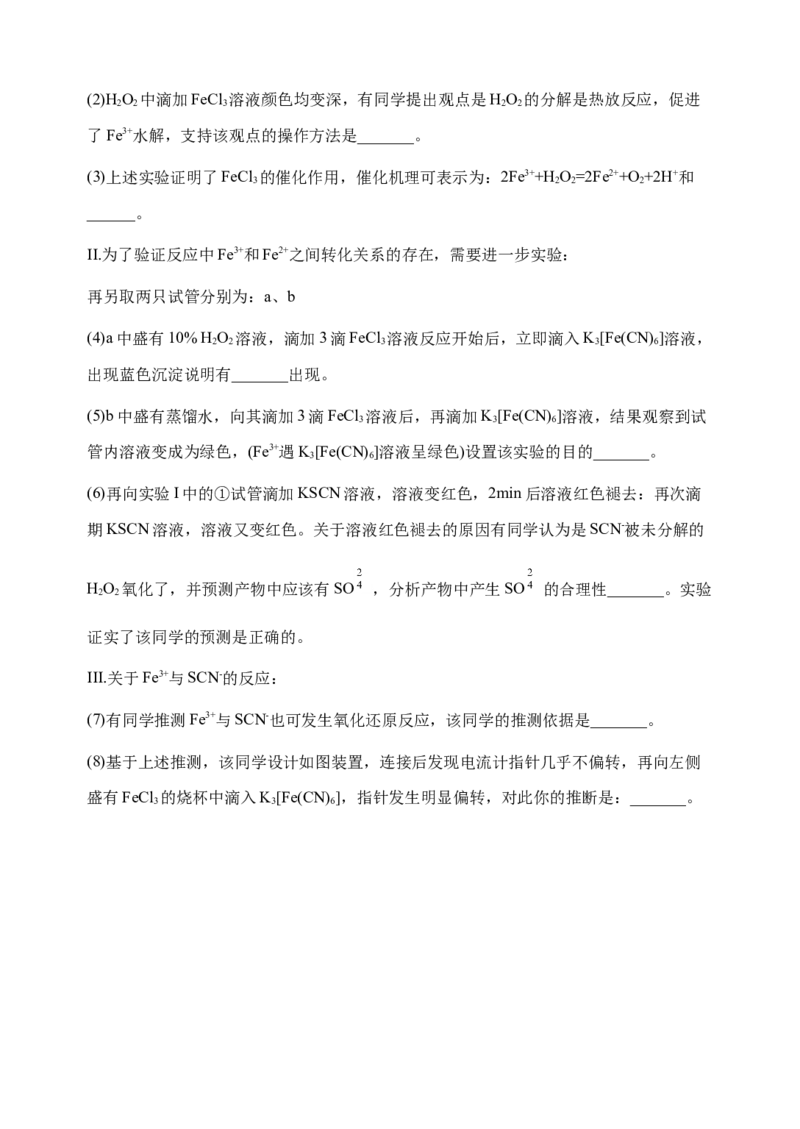文档内容
微专题13 Fe2+、Fe3+的性质及检验
【知识点梳理】
1.亚铁盐
含有Fe2+的溶液呈浅绿色,既有氧化性,又有还原性。
(1)Fe2+的还原性:
Fe2+的酸性溶液与HO 反应的离子方程式:
2 2
2Fe2++HO+2H+===2Fe3++2HO。
2 2 2
(2)Fe2+的弱氧化性:Fe2+ Fe
2.铁盐
含Fe3+的溶液呈棕黄色,Fe3+具有较强的氧化性。
写出下列转化的离子方程式:
(1)Fe3+ Fe2+:
2Fe3++SO+HO===2Fe2++SO+2H+
2
(2)Fe3+ Fe2+:2Fe3++2I-===2Fe2++I
2
3.Fe2+、Fe3+的检验方法
(1)用KSCN溶液和氯水
(2)用NaOH溶液
检验Fe3+也可用苯酚溶液,在FeCl 溶液中滴加苯酚溶液,溶液变紫色。
3
(3)含Fe2+、Fe3+的混合溶液中Fe3+、Fe2+的检验―――――――→溶液变血红色,说明含有Fe3+
―――――→KMnO 溶液紫红色褪去,说明含有Fe2+。
4
(4)Fe2+的特征检验方法
溶液 产生蓝色沉淀,说明溶液中含有Fe2+,有关反应离子方程式为
3Fe2++2[Fe(CN) ]3-===Fe [Fe(CN) ]↓。
6 3 6 2
(5)盐溶液的配制与保存
(6)物质的制备
4.混合溶液中Fe3+、Fe2+除去的实验
(1)除去Mg2+中混有的Fe3+的方法
向混合溶液中加入MgO、MgCO 、Mg(OH) 中之一,与Fe3+水解产生的H+反应,促进
3 2
Fe3+的水解,将Fe3+转化为Fe(OH) 沉淀除去。
3
(2)除去Cu2+中混有的Fe3+的方法
向混合溶液中加入CuO、CuCO、Cu(OH) 、Cu (OH) CO 中之一,与Fe3+水解产生的H+
3 2 2 2 3
反应,促进Fe3+的水解,将Fe3+转化为Fe(OH) 沉淀而除去。
3
(3)除去Mg2+中混有的Fe2+的方法
先加入氧化剂(如HO)将溶液中的Fe2+氧化成Fe3+,然后再按(1)的方法除去溶液中的Fe3
2 2
+。
(4)除去Cu2+中混有的Fe2+的方法
先加入氧化剂(如HO)将溶液中的Fe2+氧化成Fe3+,然后再按(2)的方法除去溶液中的Fe3
2 2
+。
(5)除杂
溶液 杂质 除杂方法
FeCl FeCl 加过量铁粉后过滤
2 3
FeCl FeCl 加氯水或HO
3 2 2 2
FeCl CuCl 加过量铁粉后过滤
2 2【专题精练】
1.下列试剂不能使 转化为 的是
①新制氯水② 溶液③酸性 溶液④ 溶液⑤盐酸⑥ 溶液
A.①②③ B.①③④ C.②④⑤ D.②⑤⑥
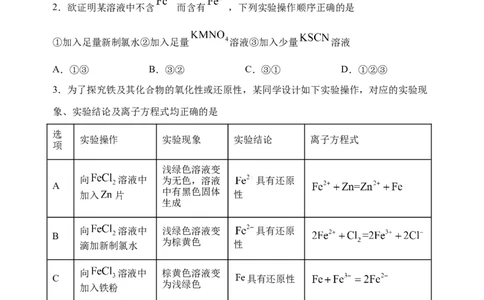
2.欲证明某溶液中不含 而含有 ,下列实验操作顺序正确的是
①加入足量新制氯水②加入足量 溶液③加入少量 溶液
A.①③ B.③② C.③① D.①②③
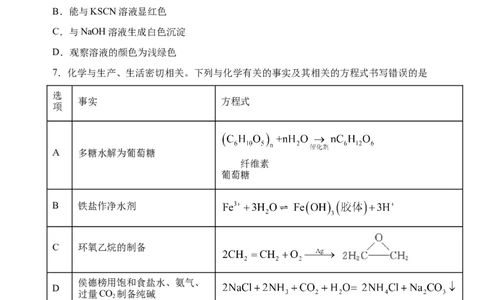
3.为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验操作,对应的实验现
象、实验结论及离子方程式均正确的是
选
实验操作 实验现象 实验结论 离子方程式
项
浅绿色溶液变
向 溶液中 为无色,溶液 具有还原
A
加入 片 中有黑色固体 性
生成
向 溶液中 浅绿色溶液变 具有还原
B
滴加新制氯水 为棕黄色 性
向 溶液中 棕黄色溶液变
C 具有还原性
为浅绿色
加入铁粉
向 溶液中 蓝色溶液变为 具有氧化
D
加入铜粉 棕黄色 性
A.A B.B C.C D.D
4.下列关于铁及其化合物的说法错误的是
A.若FeCl 溶液中混有FeCl 可通过滴加氯水除去
2 3B.可用KSCN溶液检验FeCl 溶液是否变质
2
C.实验室保存FeCl 溶液时常加入铁粉
2
D.向FeCl 溶液中加入NaOH溶液,最终可观察到红褐色沉淀
2
5.某同学设计的制备氯化铁溶液的方案中,分别采用下列物品,其中能实现的是
A.氢氧化铁和硫酸 B.铁和盐酸 C.氧化亚铁和盐酸 D.氧化铁和盐酸
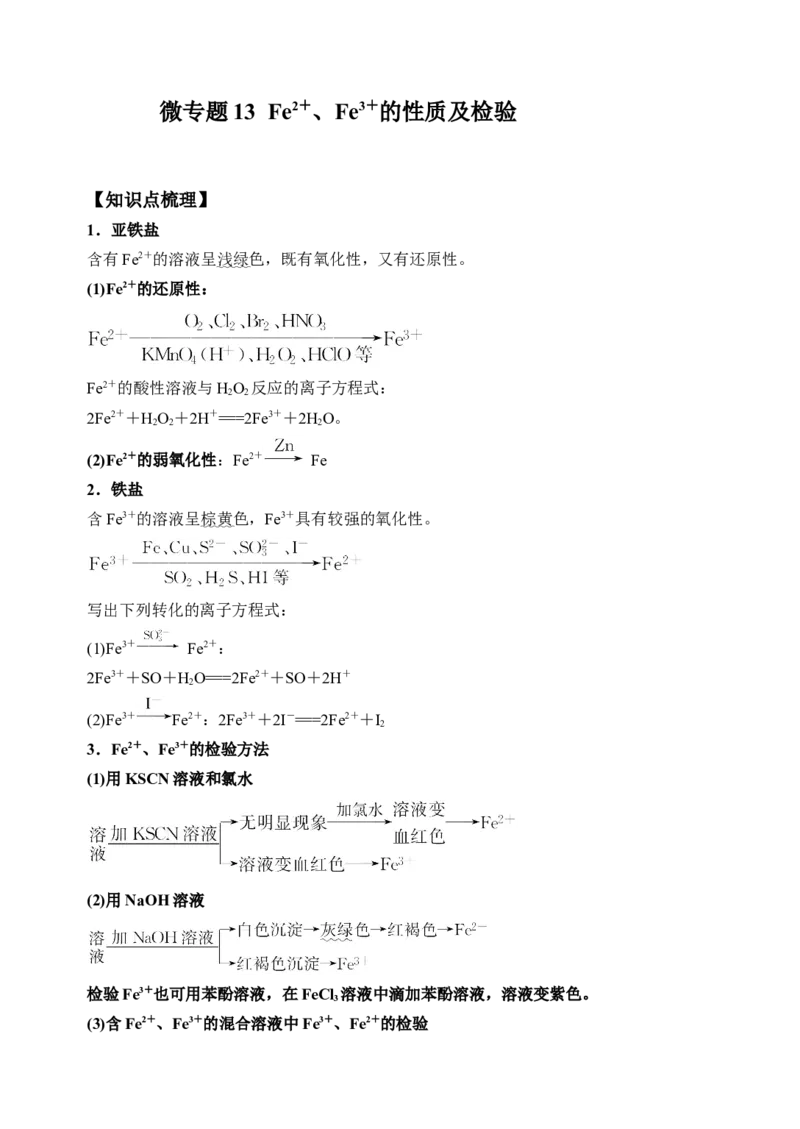
6.实验室有一瓶失去标签的溶液,以下方法能证明溶液中含有Fe3+的是
A.品尝味道
B.能与KSCN溶液显红色
C.与NaOH溶液生成白色沉淀
D.观察溶液的颜色为浅绿色
7.化学与生产、生活密切相关。下列与化学有关的事实及其相关的方程式书写错误的是
选
事实 方程式
项
A 多糖水解为葡萄糖
纤维素
葡萄糖
B 铁盐作净水剂
C 环氧乙烷的制备
侯德榜用饱和食盐水、氨气、
D
过量CO 制备纯碱
2
A.A B.B C.C D.D
8.下列有关离子共存或离子方程式的叙述正确的是
A.Na+、K+、ClO-、 不能大量共存
B.K+、Fe3+、SCN−、Cl−能大量共存C.Fe(OH) 溶于氢碘酸:Fe(OH) +3H+=Fe3++3H O
3 3 2
D.向碳酸氢铵稀溶液中加入过量烧碱溶液: +OH−=NH·H O
3 2
9.将Cu片放入0.1mol/L的FeCl 溶液中,一段时间后取出Cu片,溶液中
3
c(Fe3+)∶c(Fe2+)=2∶3,则反应后溶液中n(Cu2+)∶n(Fe3+)为
A.3∶4 B.3∶5 C.4∶3 D.3∶2
10.下列关于“摩尔盐”[(NH )Fe(SO )·6H O]的说法不正确的是
4 2 4 2 2
A.具有较强的还原性,可使高锰酸钾酸性溶液褪色
B.可用于治疗缺铁性贫血,还可用于制造红色颜料铁红(Fe O)、磁性氧化铁(Fe O)等
2 3 3 4
C.加水溶解,再滴加KSCN溶液,若溶液变红色,说明摩尔盐已氧化变质
D.加水溶解,与过量NaOH溶液反应的离子方程式:Fe2++2OH-=Fe(OH) ↓
2
11.要证明某溶液中不含Fe3+而可能含有Fe2+进行如下实验操作时,最佳顺序为
①加入足量氯水 ②加入足量KMnO 溶液 ③加入少量NH SCN溶液
4 4
A.①③ B.③② C.③① D.①②③
12.下列离子的检验方法合理的是
A.向某溶液中通入氯气,然后再加入KSCN溶液变红色,不能说明原溶液中含Fe2+
B.向某溶液中加入NaOH溶液,最终得到红褐色沉淀,说明溶液中含Fe3+
C.向某溶液中滴加 KSCN溶液呈红色,说明不含Fe2+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到逐渐变成红褐色,说明只含Fe2+不
含Mg2+
【Fe2+、Fe3+性质的有关实验】
1.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L的溶液。为防止Fe2+被氧化,
FeCl 溶液中需加入___________反应的化学方程式为___________。
2
(2)甲组同学取2 mL FeCl 溶液,加入1滴KSCN溶液,再加入几滴氯水,溶液变红,说
2
明Cl 可将Fe2+氧化。
2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mLFeCl 溶液中先加入0.5 mL煤油,
2再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是___________。
(4)丙组同学取5 mL 0.1 mol/LKI溶液,加入6 mL 0.1 mol/LFeCl 溶液混合。分别取2 mL
3
此溶液于3支试管中进行如下实验:
①第一支试管中加入1滴淀粉溶液,溶液显___________色;
②第二支试管中加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子可能是___________(填离子符号);写出KI与FeCl 反应的离子方程式
3
___________。
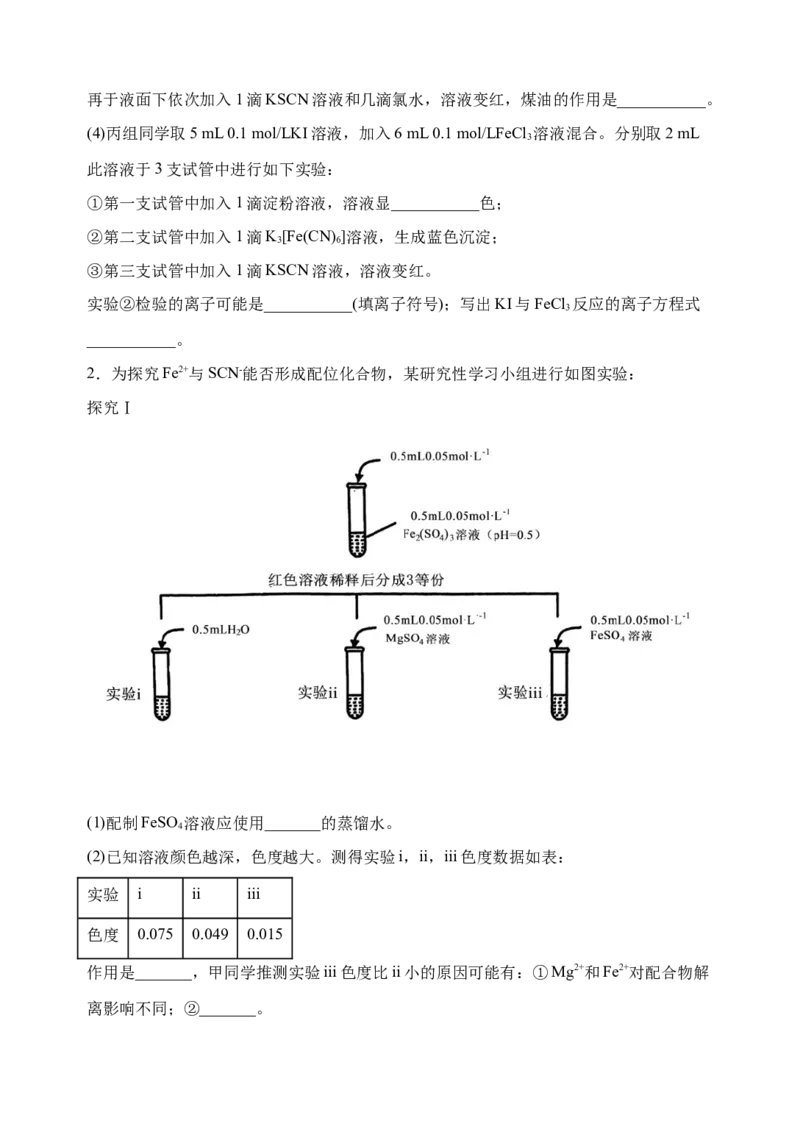
2.为探究Fe2+与SCN-能否形成配位化合物,某研究性学习小组进行如图实验:
探究Ⅰ
(1)配制FeSO 溶液应使用_______的蒸馏水。
4
(2)已知溶液颜色越深,色度越大。测得实验i,ii,iii色度数据如表:
实验 i ii iii
色度 0.075 0.049 0.015
作用是_______,甲同学推测实验iii色度比ii小的原因可能有:①Mg2+和Fe2+对配合物解
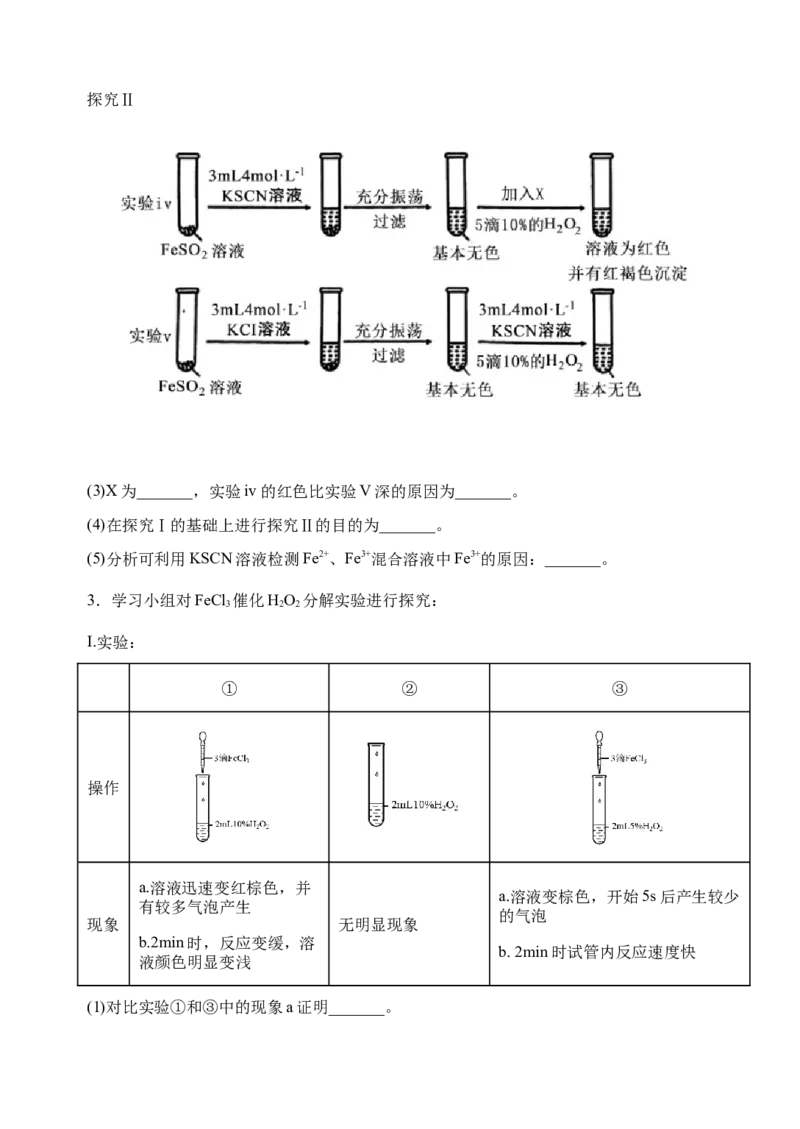
离影响不同;②_______。探究Ⅱ
(3)X为_______,实验iv的红色比实验V深的原因为_______。
(4)在探究Ⅰ的基础上进行探究Ⅱ的目的为_______。
(5)分析可利用KSCN溶液检测Fe2+、Fe3+混合溶液中Fe3+的原因:_______。
3.学习小组对FeCl 催化HO 分解实验进行探究:
3 2 2
I.实验:
① ② ③
操作
a.溶液迅速变红棕色,并
a.溶液变棕色,开始5s后产生较少
有较多气泡产生
的气泡
现象 无明显现象
b.2min时,反应变缓,溶
b. 2min时试管内反应速度快
液颜色明显变浅
(1)对比实验①和③中的现象a证明_______。(2)HO 中滴加FeCl 溶液颜色均变深,有同学提出观点是HO 的分解是热放反应,促进
2 2 3 2 2
了Fe3+水解,支持该观点的操作方法是_______。
(3)上述实验证明了FeCl 的催化作用,催化机理可表示为:2Fe3++H O=2Fe2++O +2H+和
3 2 2 2
______。
II.为了验证反应中Fe3+和Fe2+之间转化关系的存在,需要进一步实验:
再另取两只试管分别为:a、b
(4)a中盛有10% H O 溶液,滴加3滴FeCl 溶液反应开始后,立即滴入K[Fe(CN) ]溶液,
2 2 3 3 6
出现蓝色沉淀说明有_______出现。
(5)b中盛有蒸馏水,向其滴加3滴FeCl 溶液后,再滴加K[Fe(CN) ]溶液,结果观察到试
3 3 6
管内溶液变成为绿色,(Fe3+遇K[Fe(CN) ]溶液呈绿色)设置该实验的目的_______。
3 6
(6)再向实验I中的①试管滴加KSCN溶液,溶液变红色,2min后溶液红色褪去:再次滴
期KSCN溶液,溶液又变红色。关于溶液红色褪去的原因有同学认为是SCN-被未分解的
HO 氧化了,并预测产物中应该有SO ,分析产物中产生SO 的合理性_______。实验
2 2
证实了该同学的预测是正确的。
III.关于Fe3+与SCN-的反应:
(7)有同学推测Fe3+与SCN-也可发生氧化还原反应,该同学的推测依据是_______。
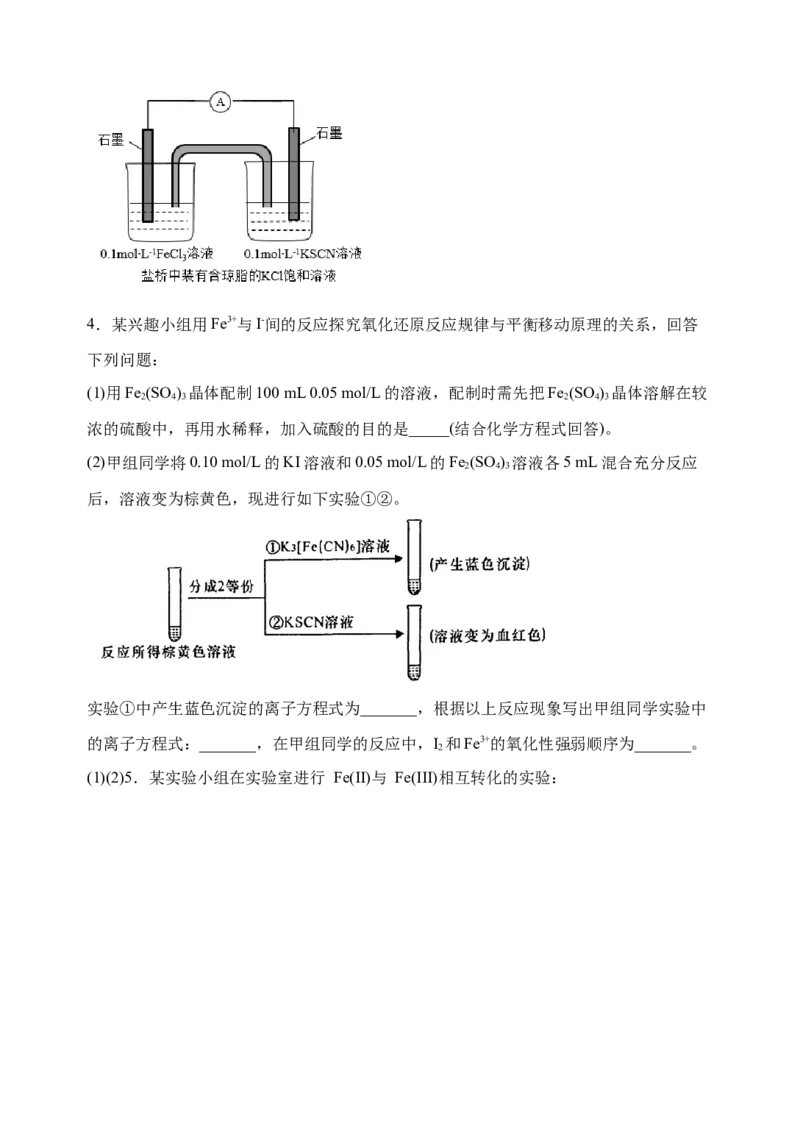
(8)基于上述推测,该同学设计如图装置,连接后发现电流计指针几乎不偏转,再向左侧
盛有FeCl 的烧杯中滴入K[Fe(CN) ],指针发生明显偏转,对此你的推断是:_______。
3 3 64.某兴趣小组用Fe3+与I-间的反应探究氧化还原反应规律与平衡移动原理的关系,回答
下列问题:
(1)用Fe (SO ) 晶体配制100 mL 0.05 mol/L的溶液,配制时需先把Fe (SO ) 晶体溶解在较
2 4 3 2 4 3
浓的硫酸中,再用水稀释,加入硫酸的目的是_____(结合化学方程式回答)。
(2)甲组同学将0.10 mol/L的KI溶液和0.05 mol/L的Fe (SO ) 溶液各5 mL混合充分反应
2 4 3
后,溶液变为棕黄色,现进行如下实验①②。
实验①中产生蓝色沉淀的离子方程式为_______,根据以上反应现象写出甲组同学实验中
的离子方程式:_______,在甲组同学的反应中,I 和Fe3+的氧化性强弱顺序为_______。
2
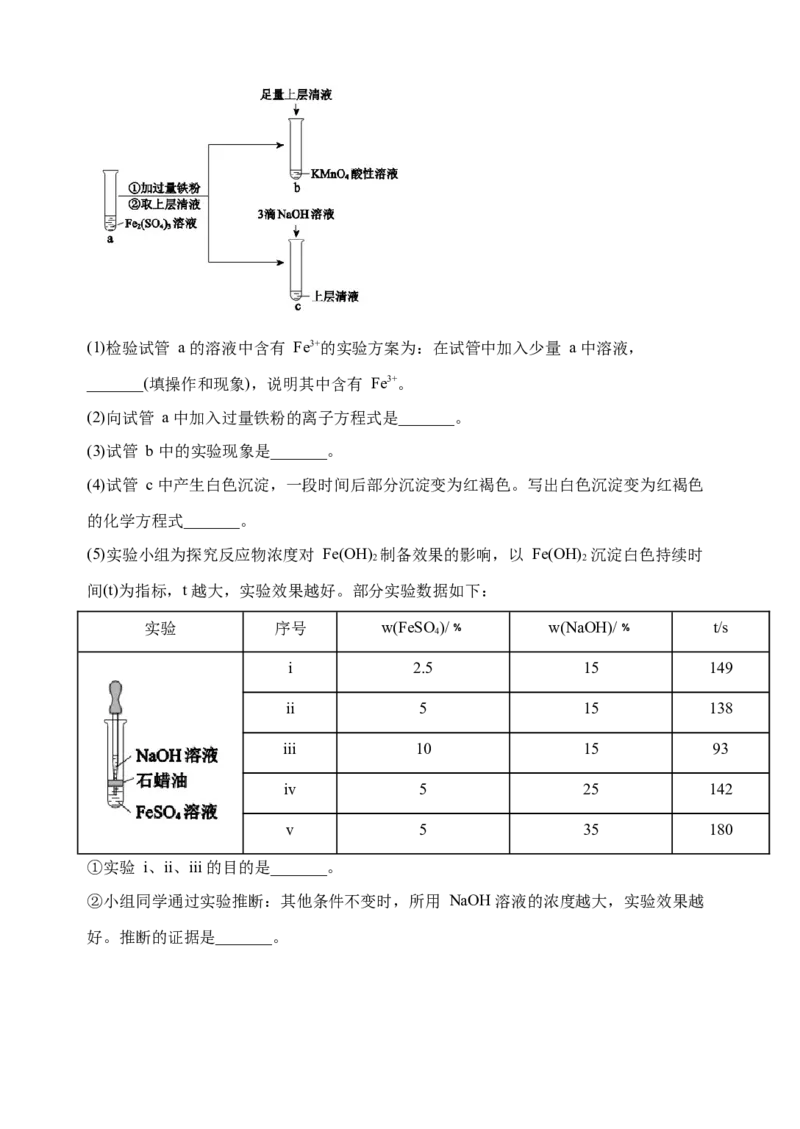
(1)(2)5.某实验小组在实验室进行 Fe(II)与 Fe(III)相互转化的实验:(1)检验试管 a 的溶液中含有 Fe3+的实验方案为:在试管中加入少量 a 中溶液,
_______(填操作和现象),说明其中含有 Fe3+。
(2)向试管 a 中加入过量铁粉的离子方程式是_______。
(3)试管 b 中的实验现象是_______。
(4)试管 c 中产生白色沉淀,一段时间后部分沉淀变为红褐色。写出白色沉淀变为红褐色
的化学方程式_______。
(5)实验小组为探究反应物浓度对 Fe(OH) 制备效果的影响,以 Fe(OH) 沉淀白色持续时
2 2
间(t)为指标,t 越大,实验效果越好。部分实验数据如下:
实验 序号 w(FeSO )/﹪ w(NaOH)/﹪ t/s
4
i 2.5 15 149
ii 5 15 138
iii 10 15 93
iv 5 25 142
v 5 35 180
①实验 i、ii、iii 的目的是_______。
②小组同学通过实验推断:其他条件不变时,所用 NaOH 溶液的浓度越大,实验效果越
好。推断的证据是_______。