文档内容
微专题突破16 归因类问题考点透视二
一、选择题
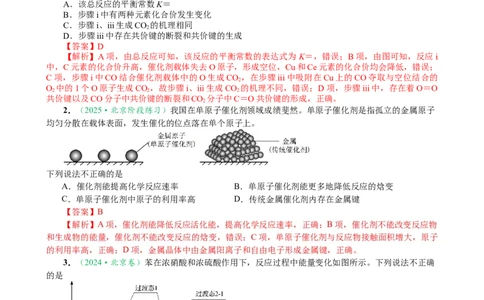
1.(2024·南京、盐城一模)利用铜-铈氧化物(xCuO·yCeO),Ce是活泼金属)催化氧化除去H
2 2
中少量CO,总反应为2CO(g)+O(g)=2CO(g) ΔH,反应机理如图所示。下列说法正确的是
2 2
A.该总反应的平衡常数K=
B.步骤i中有两种元素化合价发生变化
C.步骤i、iii生成CO 的机理相同
2
D.步骤iii中存在共价键的断裂和共价键的生成
【答案】D
【解析】A项,由总反应可知,该反应的平衡常数的表达式为 K=,错误;B项,由图可知,反应i
中,C元素的化合价升高,催化剂载体失去O原子,形成空位,Cu和Ce元素的化合价均会降低,错误;
C项,步骤i中CO结合催化剂载体中的O生成CO ,在步骤iii中吸附在Cu上的CO夺取与空位结合的
2
O 中的1个O原子生成CO ,故步骤i、iii生成CO 的机理不同,错误;D项,步骤iii中,存在着O=O
2 2 2
共价键以及CO分子中共价键的断裂和CO 分子中C=O共价键的形成,正确。
2
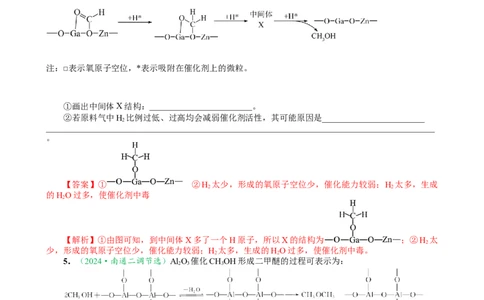
2.(2025·北京阶段练习)我国在单原子催化剂领域成绩斐然。单原子催化剂是指孤立的金属原子
均匀分散在载体表面,发生催化的位点落在单个原子上。
下列说法不正确的是
A.催化剂能提高化学反应速率 B.单原子催化剂能更多地降低反应的焓变
C.单原子催化剂中原子的利用率高 D.传统金属催化剂内存在金属键
【答案】B
【解析】A项,催化剂能降低反应活化能,提高化学反应速率,正确;B项,催化剂不能改变反应物
和生成物的能量,催化剂不能改变反应的焓变,错误;C项,单原子催化剂与反应物接触面积增大,原子
的利用率高,正确;D项,金属晶体中由金属阳离子和自由电子形成金属键,正确。
3.(2024·北京卷)苯在浓硝酸和浓硫酸作用下,反应过程中能量变化如图所示。下列说法不正确
的是
A.从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ
B.X为苯的加成产物,Y为苯的取代产物
C.由苯得到M时,苯中的大π键没有变化
D.对于生成Y的反应,浓硫酸作催化剂
【答案】C
【解析】A项,由图可知,生成产物Ⅱ的反应的活化能更低,反应速率更快,且产物Ⅱ的能量更低,微专题突破16 归因类问题考点透视
即产物Ⅱ更稳定,正确;B项,根据前后结构对照可知,X为苯的加成产物,Y为苯的取代产物,正确;
C项,由图可知,M的六元环中与—NO 相连的C为sp3杂化,C的杂化方式改变,苯中大π键发生改变,
2
错误;D项,苯的硝化反应中浓硫酸作催化剂,正确。
二、填空题
4.(2025·南通市海安市开学考)研发CO 碳利用技术是实现“碳中和”的重要方向。
2
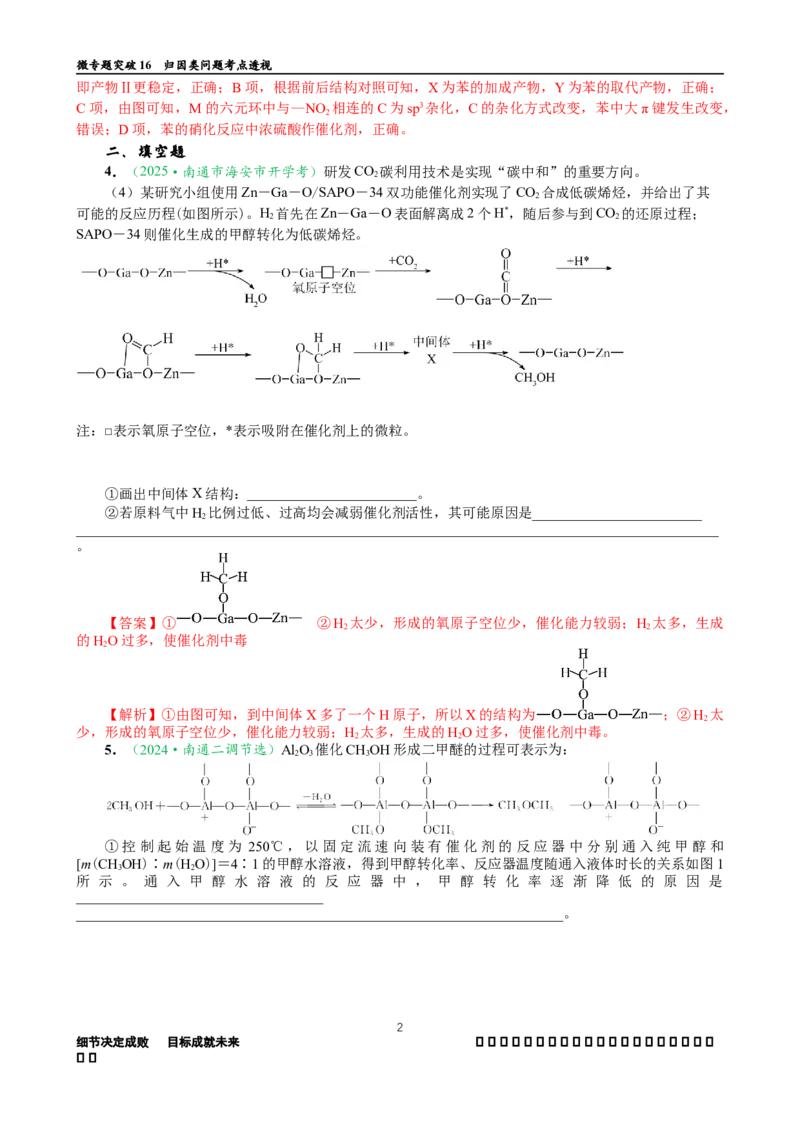
(4)某研究小组使用Zn-Ga-O/SAPO-34双功能催化剂实现了CO 合成低碳烯烃,并给出了其
2
可能的反应历程(如图所示)。H 首先在Zn-Ga-O表面解离成2个H*,随后参与到CO 的还原过程;
2 2
SAPO-34则催化生成的甲醇转化为低碳烯烃。
注:□表示氧原子空位,*表示吸附在催化剂上的微粒。
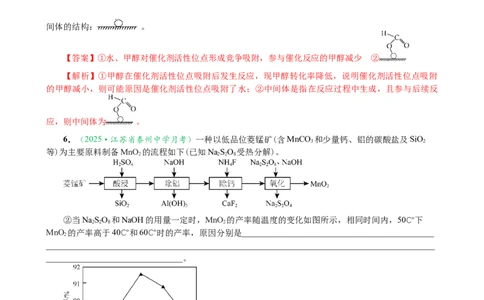
①画出中间体X结构:________________________。
②若原料气中H 比例过低、过高均会减弱催化剂活性,其可能原因是________________________
2
___________________________________________________________________________________________
。
【答案】① ②H 太少,形成的氧原子空位少,催化能力较弱;H 太多,生成
2 2
的HO过多,使催化剂中毒
2
【解析】①由图可知,到中间体X多了一个H原子,所以X的结构为 ;②H 太
2
少,形成的氧原子空位少,催化能力较弱;H 太多,生成的HO过多,使催化剂中毒。
2 2
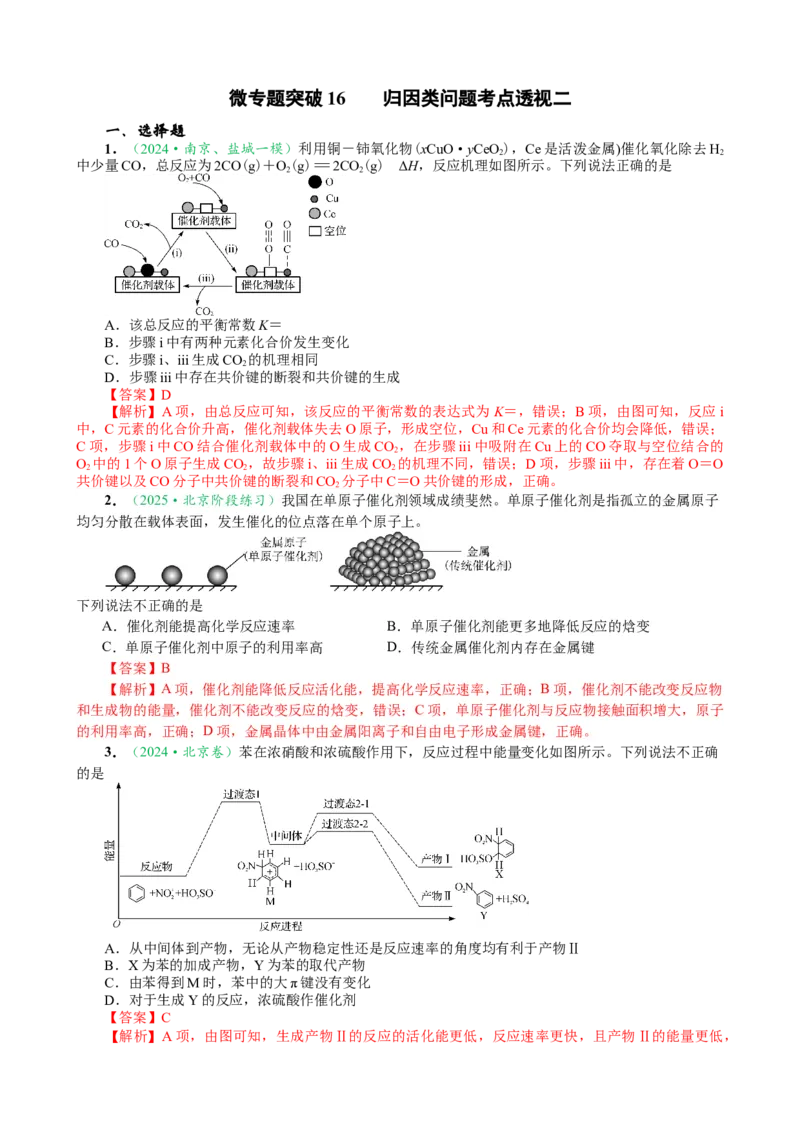
5.(2024·南通二调节选)Al O 催化CHOH形成二甲醚的过程可表示为:
2 3 3
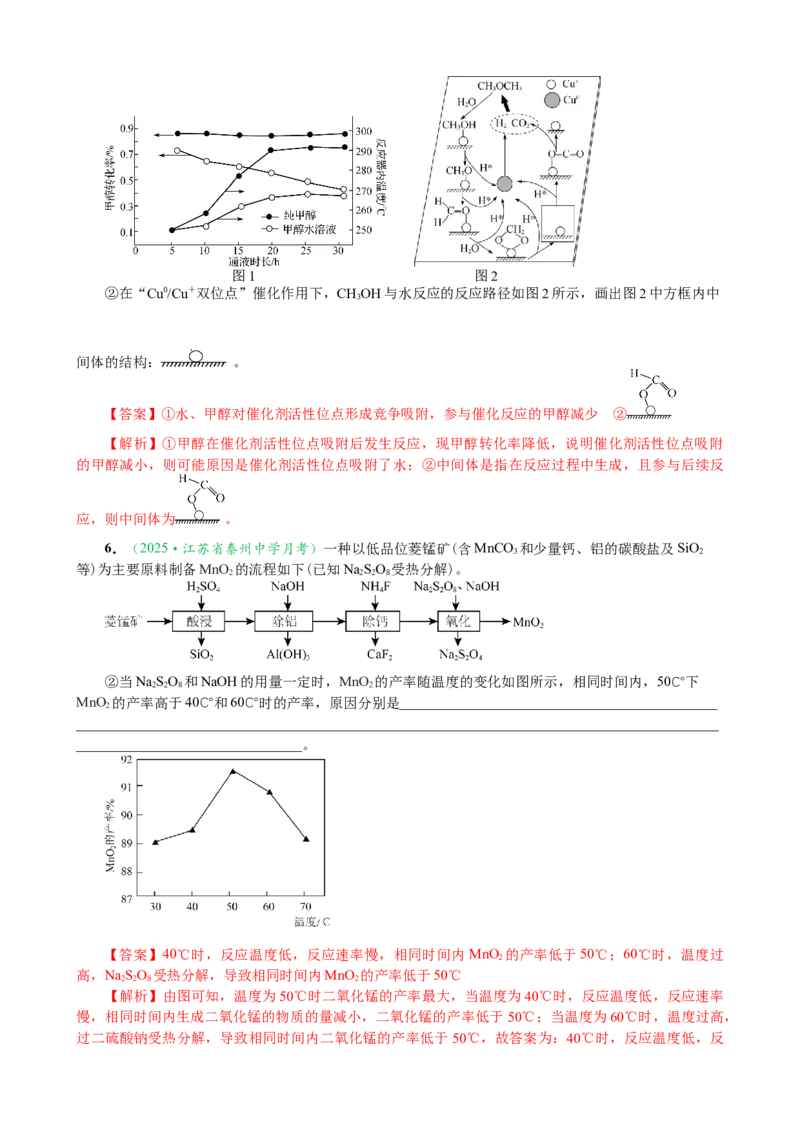
①控制起始温度为 250℃,以固定流速向装有催化剂的反应器中分别通入纯甲醇和
[m(CHOH)∶m(HO)]=4∶1的甲醇水溶液,得到甲醇转化率、反应器温度随通入液体时长的关系如图1
3 2
所 示 。 通 入 甲 醇 水 溶 液 的 反 应 器 中 , 甲 醇 转 化 率 逐 渐 降 低 的 原 因 是
___________________________________
_____________________________________________________________________。
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找图1 图2
②在“Cu0/Cu+双位点”催化作用下,CHOH与水反应的反应路径如图2所示,画出图2中方框内中
3
间体的结构: 。
【答案】①水、甲醇对催化剂活性位点形成竞争吸附,参与催化反应的甲醇减少 ②
【解析】①甲醇在催化剂活性位点吸附后发生反应,现甲醇转化率降低,说明催化剂活性位点吸附
的甲醇减小,则可能原因是催化剂活性位点吸附了水;②中间体是指在反应过程中生成,且参与后续反
应,则中间体为 。
6.(2025·江苏省泰州中学月考)一种以低品位菱锰矿(含MnCO 和少量钙、铝的碳酸盐及SiO
3 2
等)为主要原料制备MnO 的流程如下(已知NaSO 受热分解)。
2 2 2 8
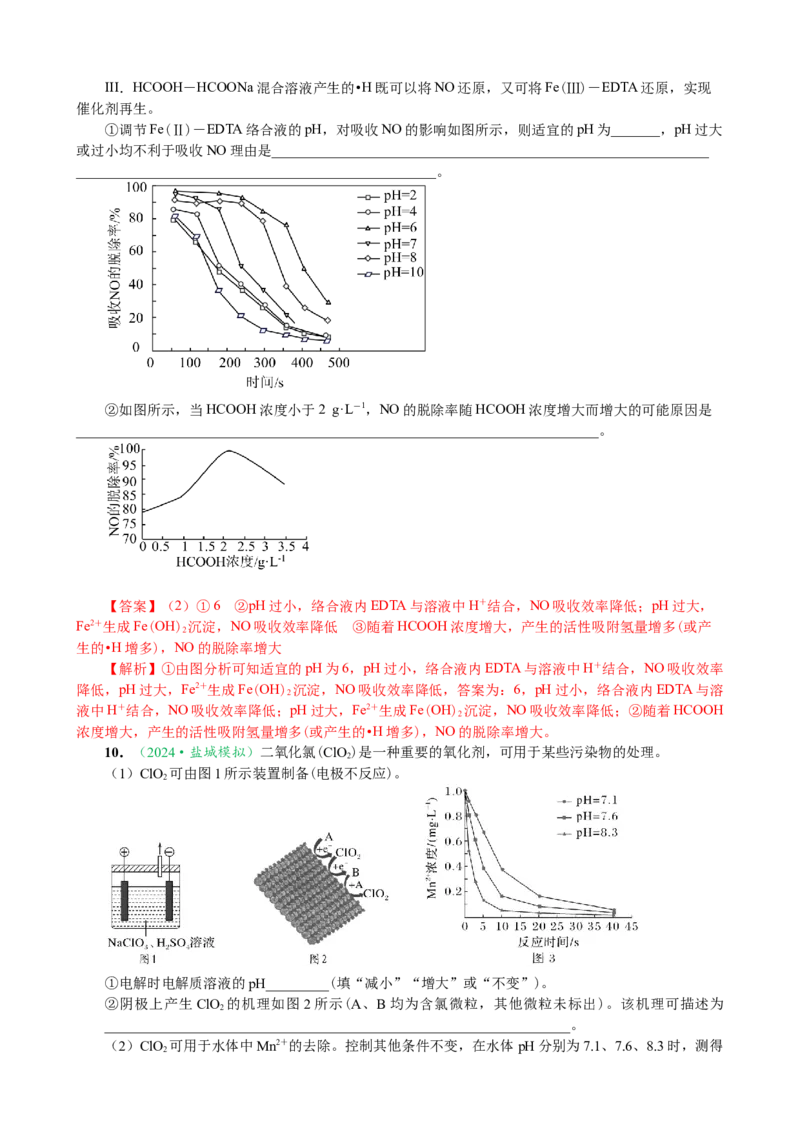
②当NaSO 和NaOH的用量一定时,MnO 的产率随温度的变化如图所示,相同时间内,50℃下
2 2 8 2
MnO 的产率高于40℃和60℃时的产率,原因分别是_____________________________________________
2
___________________________________________________________________________________________
________________________________。
【答案】40℃时,反应温度低,反应速率慢,相同时间内MnO 的产率低于50℃;60℃时,温度过
2
高,NaSO 受热分解,导致相同时间内MnO 的产率低于50℃
2 2 8 2
【解析】由图可知,温度为50℃时二氧化锰的产率最大,当温度为40℃时,反应温度低,反应速率
慢,相同时间内生成二氧化锰的物质的量减小,二氧化锰的产率低于50℃;当温度为60℃时,温度过高,
过二硫酸钠受热分解,导致相同时间内二氧化锰的产率低于50℃,故答案为:40℃时,反应温度低,反微专题突破16 归因类问题考点透视
应速率慢,相同时间内MnO 的产率低于50℃;60℃时,温度过高,NaSO 受热分解,导致相同时间内
2 2 2 8
MnO 的产率低于50℃。
2
7.(2025·镇江市上学期期中)CO 的资源化利用是化学研究的热点。
2
(1)C H 催化脱氢可制备丙烯。反应为C H(g)=C H(g)+H(g) ∆H=+123.8 kJ·mol-1
3 8 3 8 3 6 2 1
①该反应高温下能自发进行的原因为_______________________________________________________
__________________________________________。
②工业生产反应温度选择600℃,温度过高,反应速率和丙烯选择性均快速下降,原因可能为
___________________________________________________________________________________________
________________________________________。
(4)InO 催化CO 加氢制甲醇。H 在InO 表面吸附后活化生成HCOO*中间体的机理如图所示。
2 3 2 2 2 3
①转化1中,In元素的化合价会_________。(选填“升高”、“降低”或“不变”)
②根据元素电负性的变化规律,用文字描述转化Ⅱ和Ⅲ的机理_________________________________
___________________________________________________________________________________________
___________________________________________________________________________________________
___________________________________________________________________。
【答案】(1)①该反应的∆H>0,∆S>0,高温下∆H-T∆S<0,反应可自发进行 ②温度过高,丙
烷裂解产生CH 、C H 、C和氢气等副产物,使丙烯的选择性下降;同时高温下产生积碳使催化剂快速失
4 2 4
活,反应速率快速下降;(4)①降低 ②CO 分子中的一个O原子填充到氧空位,促进CO 分子中C=O
2 2
键断裂;In的电负性小于H,与In相连的H原子带负电,C的电负性小于O,与O相连的C原子带正电;
带负电的H进攻带正电的C原子生成HCOO* (吸附在InO 表面)
2 3
【解析】(1)①该反应高温下能自发进行的原因为:该反应的∆H>0,∆S>0,∆H-T∆S<0,反应
可自发进行;②工业生产反应温度选择600℃,温度过高,反应速率和丙烯选择性均快速下降,原因可能
为:温度过高,丙烷裂解产生CH 、C H 、C和氢气等副产物,使丙烯的选择性下降;同时高温下产生积
4 2 4
碳使催化剂快速失活,反应速率快速下降;(4)①转化1中,InO 中产生了氧空位,由化合价代数和为
2 3
零可知,In元素的化合价会降低;②根据元素电负性的变化规律,用文字描述转化Ⅱ和Ⅲ的机理为:CO
2
分子中的一个O原子填充到氧空位,促进CO 分子中C=O键断裂;In的电负性小于H,与In相连的H
2
原子带负电,C的电负性小于O,与O相连的C原子带正电;带负电的 H进攻带正电的C原子生成
HCOO*(吸附在InO 表面)。
2 3
9.(2024·徐州上学期期中)HCOOH-HCOONa混合溶液可脱除烟气中NO。其机理如图所示:
已知:I.脱除过程中,Fe(Ⅱ)-EDTA络合液部分易被烟气中的O 氧化成Fe(Ⅲ)-EDTA;
2
II.酸性较强环境下,EDTA易与溶液中H+结合;
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找III.HCOOH-HCOONa混合溶液产生的•H既可以将NO还原,又可将Fe(Ⅲ)-EDTA还原,实现
催化剂再生。
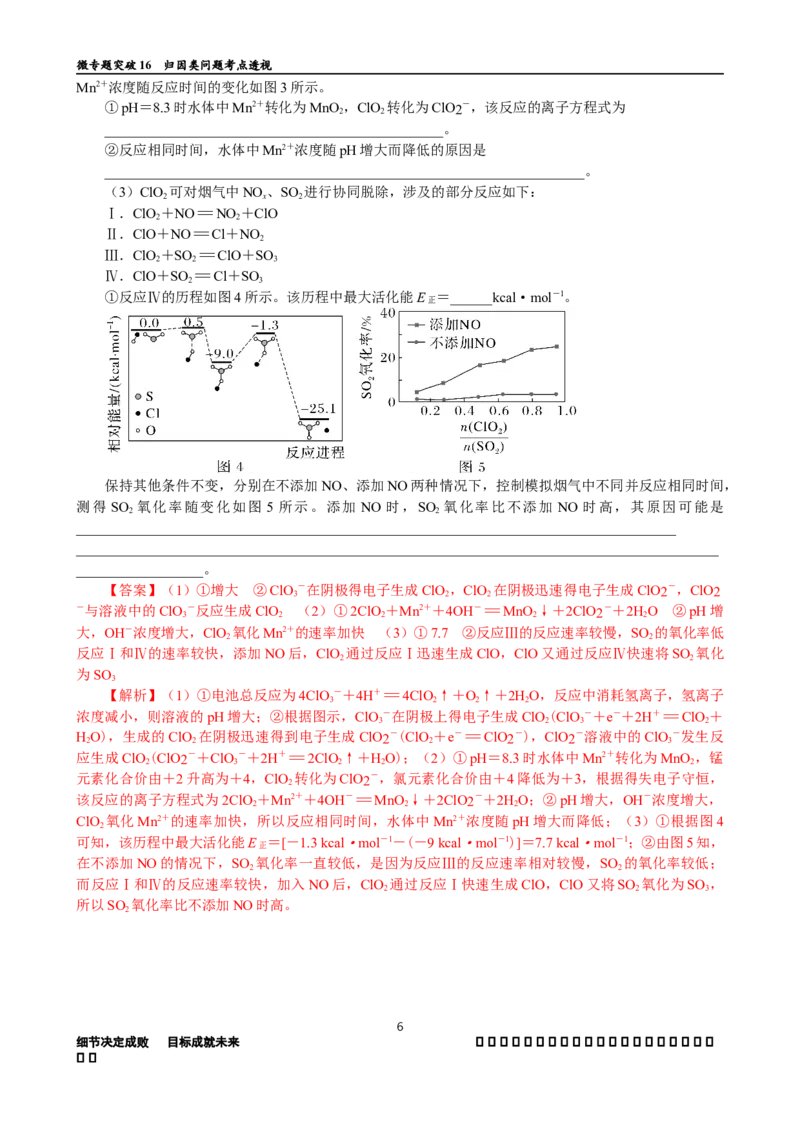
①调节Fe(Ⅱ)-EDTA络合液的pH,对吸收NO的影响如图所示,则适宜的pH为_______,pH过大
或过小均不利于吸收NO理由是______________________________________________________________
___________________________________________________。
②如图所示,当HCOOH浓度小于2 g·L-1,NO的脱除率随HCOOH浓度增大而增大的可能原因是
__________________________________________________________________________。
【答案】(2)①6 ②pH过小,络合液内EDTA与溶液中H+结合,NO吸收效率降低;pH过大,
Fe2+生成Fe(OH) 沉淀,NO吸收效率降低 ③随着HCOOH浓度增大,产生的活性吸附氢量增多(或产
2
生的•H增多),NO的脱除率增大
【解析】①由图分析可知适宜的pH为6,pH过小,络合液内EDTA与溶液中H+结合,NO吸收效率
降低,pH过大,Fe2+生成Fe(OH) 沉淀,NO吸收效率降低,答案为:6,pH过小,络合液内EDTA与溶
2
液中H+结合,NO吸收效率降低;pH过大,Fe2+生成Fe(OH) 沉淀,NO吸收效率降低;②随着HCOOH
2
浓度增大,产生的活性吸附氢量增多(或产生的•H增多),NO的脱除率增大。
10.(2024·盐城模拟)二氧化氯(ClO )是一种重要的氧化剂,可用于某些污染物的处理。
2
(1)ClO 可由图1所示装置制备(电极不反应)。
2
①电解时电解质溶液的pH_________(填“减小”“增大”或“不变”)。
②阴极上产生ClO 的机理如图2所示(A、B均为含氯微粒,其他微粒未标出)。该机理可描述为
2
__________________________________________________________________。
(2)ClO 可用于水体中Mn2+的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得
2微专题突破16 归因类问题考点透视
Mn2+浓度随反应时间的变化如图3所示。
①pH=8.3时水体中Mn2+转化为MnO ,ClO 转化为ClO2-,该反应的离子方程式为
2 2
________________________________________________。
②反应相同时间,水体中Mn2+浓度随pH增大而降低的原因是
____________________________________________________________________。
(3)ClO 可对烟气中NO、SO 进行协同脱除,涉及的部分反应如下:
2 x 2
Ⅰ.ClO +NO=NO +ClO
2 2
Ⅱ.ClO+NO=Cl+NO
2
Ⅲ.ClO +SO =ClO+SO
2 2 3
Ⅳ.ClO+SO =Cl+SO
2 3
①反应Ⅳ的历程如图4所示。该历程中最大活化能E =______kcal·mol-1。
正
保持其他条件不变,分别在不添加NO、添加NO两种情况下,控制模拟烟气中不同并反应相同时间,
测得 SO 氧化率随变化如图 5 所示。添加 NO 时,SO 氧化率比不添加 NO 时高,其原因可能是
2 2
_____________________________________________________________________________________
___________________________________________________________________________________________
__________________。
【答案】(1)①增大 ②ClO -在阴极得电子生成ClO ,ClO 在阴极迅速得电子生成ClO2-,ClO2
3 2 2
-与溶液中的ClO -反应生成ClO (2)①2ClO +Mn2++4OH-=MnO ↓+2ClO2-+2HO ②pH增
3 2 2 2 2
大,OH-浓度增大,ClO 氧化Mn2+的速率加快 (3)①7.7 ②反应Ⅲ的反应速率较慢,SO 的氧化率低
2 2
反应Ⅰ和Ⅳ的速率较快,添加NO后,ClO 通过反应Ⅰ迅速生成ClO,ClO又通过反应Ⅳ快速将SO 氧化
2 2
为SO
3
【解析】(1)①电池总反应为4ClO -+4H+=4ClO ↑+O↑+2HO,反应中消耗氢离子,氢离子
3 2 2 2
浓度减小,则溶液的pH增大;②根据图示,ClO -在阴极上得电子生成ClO (ClO -+e-+2H+=ClO +
3 2 3 2
HO),生成的ClO 在阴极迅速得到电子生成ClO2-(ClO +e-=ClO2-),ClO2-溶液中的ClO -发生反
2 2 2 3
应生成ClO (ClO2-+ClO -+2H+=2ClO ↑+HO);(2)①pH=8.3时水体中Mn2+转化为MnO ,锰
2 3 2 2 2
元素化合价由+2升高为+4,ClO 转化为ClO2-,氯元素化合价由+4降低为+3,根据得失电子守恒,
2
该反应的离子方程式为2ClO +Mn2++4OH-=MnO ↓+2ClO2-+2HO;②pH增大,OH-浓度增大,
2 2 2
ClO 氧化Mn2+的速率加快,所以反应相同时间,水体中Mn2+浓度随pH增大而降低;(3)①根据图4
2
可知,该历程中最大活化能E =[-1.3 kcal·mol-1-(-9 kcal·mol-1)]=7.7 kcal·mol-1;②由图5知,
正
在不添加NO的情况下,SO 氧化率一直较低,是因为反应Ⅲ的反应速率相对较慢,SO 的氧化率较低;
2 2
而反应Ⅰ和Ⅳ的反应速率较快,加入NO后,ClO 通过反应Ⅰ快速生成ClO,ClO又将SO 氧化为SO ,
2 2 3
所以SO 氧化率比不添加NO时高。
2
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找