文档内容
押江苏卷第 6-8 题
元素及其化合物
核心考点 考情统计 考向预测 备考策略
2023·江苏卷,6
化学反应
2022·江苏卷,6
1.重点关注元素化合物与基本概
结合离子反应、氧化还原反应相关 念和基本理论的融合考查;
物质结构与性 2023·江苏卷,7
质或物质性质 知识综合考查,注重物质间的转化 2.掌握元素化合物之间的转化关
与用途 2022·江苏卷,7 考查 系以及常见物质结构与性质、物质
性质与用途之间的关系
元素化合物的 2023·江苏卷,8
转化 2022·江苏卷,8
1.(2023·江苏卷,6)氢元素及其化合物在自然界广泛存在且具有重要应用。 、 、 是氢元素的
3种核素,基态H原子 的核外电子排布,使得H既可以形成 又可以形成 ,还能形成 、 、
、 、 等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法制氢反
应中, 与足量 反应生成 和 吸收131.3kJ的热量。 在金属冶炼、新能
源开发、碳中和等方面具有重要应用,如 在催化剂作用下与 反应可得到 。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
A.水煤气法制氢:
B. 催化加氢生成 的反应:
C.电解水制氢的阳极反应:
D. 与水反应:
2.(2023·江苏卷,7)氢元素及其化合物在自然界广泛存在且具有重要应用。 、 、 是氢元素的
3种核素,基态H原子 的核外电子排布,使得H既可以形成 又可以形成 ,还能形成 、 、
、 、 等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法制氢反
应中, 与足量 反应生成 和 吸收131.3kJ的热量。 在金属冶炼、新能
源开发、碳中和等方面具有重要应用,如 在催化剂作用下与 反应可得到 。我国科学家在
氢气的制备和应用等方面都取得了重大成果。下列物质结构与性质或物质性质与用途具有对应关系的是
A. 具有还原性,可作为氢氧燃料电池的燃料
B.氨极易溶于水,液氨可用作制冷剂
C. 分子之间形成氢键, 的热稳定性比 的高
D. 中的N原子与 形成配位键, 具有还原性
3.(2023·江苏卷,8)氮及其化合物的转化具有重要应用。下列说法不正确的是
A.实验室探究稀硝酸与铜反应的气态产物:
B.工业制硝酸过程中的物质转化:C.汽车尾气催化转化器中发生的主要反应:
D.实验室制备少量 的原理:
4.(2022·江苏,6)周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热 ,
是常见燃料;Si、Ge是重要的半导体材料,硅晶体表面 能与氢氟酸(HF,弱酸)反应生成 (
在水中完全电离为 和 );1885年德国化学家将硫化锗 与 共热制得了门捷列夫预言
的类硅—锗;下列化学反应表示正确的是
A. 与HF溶液反应:
B.高温下 还原 :
C.铅蓄电池放电时的正极反应:
D.甲烷的燃烧:
5.(2022·江苏,7)我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;
Pb、 是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料,下列物质性
质与用途具有对应关系的是
A.石墨能导电,可用作润滑剂
B.单晶硅熔点高,可用作半导体材料
C.青铜比纯铜熔点低、硬度大,古代用青铜铸剑
D.含铅化合物颜色丰富,可用作电极材料
6.(2022·江苏,8)氮及其化合物的转化具有重要应用。下列说法不正确的是
A.自然固氮、人工固氮都是将 转化为
B.侯氏制碱法以 、 、 、 为原料制备 和C.工业上通过 催化氧化等反应过程生产
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
1.化学反应的书写与正误判断
(1)离子方程式正误判断的三个关键
易溶强电解质拆,弱电解质、难溶物不拆
微溶物清拆浊不拆
化学式拆写“四原则”
单质、氧化物不拆
浓硫酸不拆,浓盐酸、浓硝酸拆
分析量不同时的产物
反应产物“三分析” 分析是否漏掉同步反应
分析变价元素的产物
原子守恒
方程式遵循“三守恒” 电荷守恒
得失电子守恒
(2)热化学方程式书写易出现的错误
①未标明反应物或生成物的状态而造成错误。
②反应热的符号使用不正确,即吸热反应未标出“+”号,放热反应未标出“-”号,从而导致错误。
③漏写ΔH的单位,或者将ΔH的单位写为kJ,从而造成错误。
④反应热的数值与方程式的计量数不对应而造成错误。
⑤对燃烧热的概念理解不到位,忽略其标准是1 mol 可燃物而造成错误。
⑥对中和反应反应热理解不准确。
a.强酸与强碱中和反应的反应热ΔH=-57.3 kJ·mol-1,若用弱酸代替强酸(或用弱碱代替强碱),因电
离吸热,放出的热量减少。
b.若用浓硫酸(或NaOH固体)作反应物,放出热量增多。
c.若是稀硫酸和Ba(OH) 反应,生成1 mol HO(l)时所释放的热量会比57.3 kJ多,原因是
2 2
H+与OH-结合成1 mol HO(l)的同时,Ba2+和SO结合成BaSO 沉淀也会放热。
2 4
(3)氧化还原反应方程式的书写(4)电极反应式书写技巧
方法一:直接书写
方法二:间接书写
第一步,写出电池总反应式。
第二步,写出电极的正极反应式。
第三步,负极反应式=总反应式-正极反应式。
2.常见无机物性质与用途的对应关系
物质性质 生活中的应用
生理盐水是消毒后的0.9%的氯化钠溶液 用于静脉注射、冲洗隐形眼镜和鼻腔冲洗等
生石灰、无水氯化钙能与水反应 可用作(食品)干燥剂
PO 能与水反应 可用作(不可用作食品)干燥剂
2 5
硅胶能吸收水分 可用作(袋装食品)干燥剂
ClO 具有较强的氧化性 用于自来水的杀菌消毒
2
次氯酸(盐)具有强氧化性 可作杀菌消毒剂,还可作漂白剂
碘酸钾在常温下稳定 食盐中的加碘物质
水玻璃(NaSiO 的水溶液)不燃不爆 可用作防火材料
2 3硅酸钠的水溶液是一种无机黏合剂 盛放碱性溶液的试剂瓶不能用玻璃塞
锂质量轻、比能量大 可用作电池负极材料
Al具有良好的延展性和抗腐蚀性 常用铝箔包装物品
常温下铝、铁遇浓硫酸、浓硝酸钝化 铝和铁制容器可盛装或运输浓硫酸、浓硝酸
铝有还原性,与氧化铁反应放出大量的热 可用于焊接铁轨
MgO、AlO 熔点高 作耐高温材料
2 3
明矾溶液中Al3+水解生成氢氧化铝胶体,具
明矾作净水剂(混凝剂)
有吸附性
小苏打和硫酸铝反应生成二氧化碳 可以作泡沫灭火器
明矾溶液显酸性 中国古代利用明矾溶液清除铜镜表面的铜锈
Al(OH) 有弱碱性 可用于中和胃酸
3
镁铝合金质量轻、强度大 可用作高铁车厢材料
KFeO 是强氧化剂,还原产物Fe3+水解生成
2 4
KFeO 作新型净水剂
2 4
氢氧化铁胶体
CuSO 使蛋白质变性 误服CuSO 溶液,喝蛋清或豆浆解毒
4 4
医疗上进行胃部造影前,BaSO 做患者服用的
4
BaSO 不溶于水,不与胃酸反应
4
“钡餐”
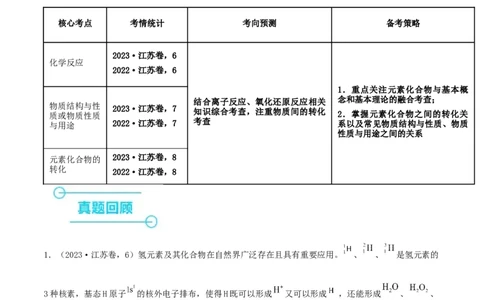
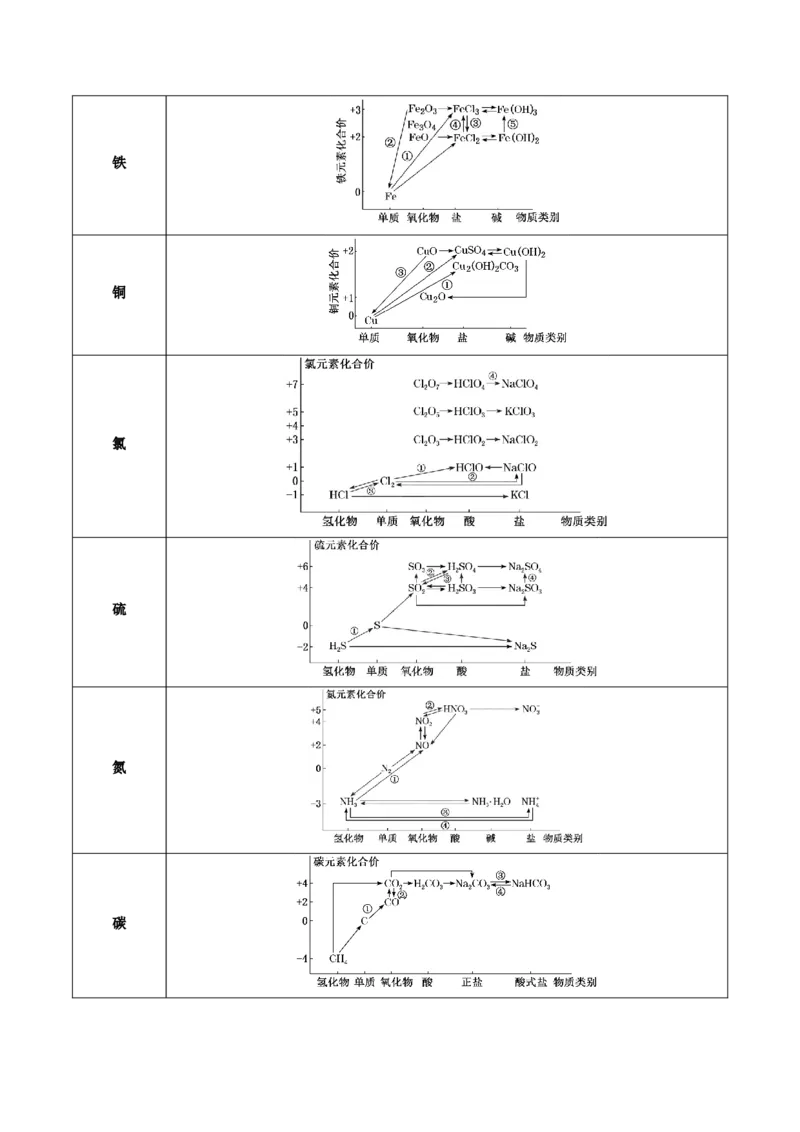
3.元素及其化合物的价—类二维图
元素 价—类二维图
钠
镁
铝铁
铜
氯
硫
氮
碳硅
考点一 化学反应
1.(2024·江苏常州第一中学高三期初检测,6)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合:HCO +Ca2++OH﹣=CaCO ↓+H O
3 2
B.将少量SO 通入NaClO溶液:SO +H O+2ClO﹣=SO +2HClO
2 2 2
C.用过量氨水吸收工业尾气中的SO :
2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH•H O=[Ag(NH)]++2H O
3 2 3 2 2
2.(2024·江苏海安高级中学高三11月月考,6)在元素周期表中,某些主族元素与右下方的主族元素的
某些性质是相似的。 和 均为两性氢氧化物, 溶于强碱形成 。 和
都具有难溶于水、高熔点等性质。 和 在气态时通常以二聚体的形式存在, 的结
构如图所示。B和 均能溶于 溶液生成盐和氢气。工业上用焦炭和石英砂(主要成分为 )在高
温条件下反应制得粗硅。硼酸 和硅酸都是弱酸,硼酸晶体有类似于石墨的层状结构,常用作消毒
剂、润滑剂等。下列化学反应表示不正确的是
A.氢氧化铍溶于强碱:
B.可溶性铝盐净水原理:
C.硅与氢氧化钠溶液反应:
D.焦炭与石英砂反应:
3.(2024·江苏苏锡常镇四市高三教学情况调研一,6)氮的常见氢化物有氨(NH )和肼(N H)。MgN 与水
3 2 4 3 2
反应可产生NH ,液氨发生微弱电离产生NH,液氨能与碱金属(如Na、K)反应产生H 。NH 中一个H被
3 2 3
—NH 取代可得NH ,常温下NH 为液体,具有很高的燃烧热(622.1 kJ·mol-1)。以硫酸为电解质,通过催
2 2 4 2 4
化电解可将N 转化为NH;碱性条件下,NaClO氧化NH 也可制备NH。
2 2 4 3 2 4
下列化学反应表示正确的是( )
A. 肼在氧气中燃烧:NH(l)+O(g)===N (g)+2HO(g);ΔH=622.1 kJ·mol-1
2 4 2 2 2
B. 液氨与钠反应:2Na+2NH ===2NaNH +H↑
3 2 2
C. NaClO氧化NH 制备NH:4NH +ClO-+2OH-===2N H+Cl-+3HO
3 2 4 3 2 4 2
D. 电解法制备NH 的阴极反应:N+4H+-4e-===N H
2 4 2 2 4
4.(2024·江苏南京盐城高三一模,6) 能将溶液中的 还原为 ,生成黑色沉淀,该反应可用于
检验 。燃煤烟气中的 可用 饱和溶液进行捕集。下列化学反应表示项正确的是
A.焦炭与石英砂反应:
B. 与酸性 溶液反应:C. 的水解反应:
D. 饱和溶液与足量 反应:
5.(2024·江苏海安高级中学高三开学考试,6)甲醇是易燃液体,能与水、乙醇、丙酮等混溶。甲醇燃烧
热为 。工业使用原料气 、 气相法合成甲醇的主反应:
。有少量 存在时,会发生副反应:
。甲醇是一种重要的工业原料,可用于制备二甲醚
、甲醛、甲酸等有机物。下列化学反应或转化过程表示正确的是
A. 燃烧热的热化学方程式:
B.气相法合成甲醇的副反应:
C.实验室由甲醇制备二甲醚:
D.甲醇转化为甲酸:
6.(2024·江苏连云港五校高三12月联考,8)1mol液态肼完全燃烧生成 气体和液态水放出577kJ的热
量。工业上利用 和 制取尿素[ ],尿素在高温条件下可将汽车尾气中的 转化为无毒
气体 。下列化学反应表示正确的是
A. 燃烧的热化学方程式:
B.碱性 燃料电池负极发生的电极反应式:
C.NaClO氧化氨气制取 的离子方程式:D. 与 高温下反应的化学方程式:
7.(2024·江苏南通海门高三第二次调研,7)周期表第ⅤA族元素及其化合物用途广泛。 在强碱性
条件下能被NaClO氧化生成肼( ),常温下 呈液态,是常用的火箭燃料。 的燃烧热为
624kJ/mol, 可被NaClO氧化生成 ,也可被 氧化生成 , 是一种弱酸,酸性与醋酸
相当。 与 高温条件下可制备半导体材料砷化镓, 的沸点为55℃。下列化学反应
或说法不正确的是
A.制备 时,应将 缓缓通入NaClO溶液中
B. 与 反应方程式为
C.向 溶液中通入HCl可以制得
D. 燃烧的热化学方程式为:
8.(2024·江苏镇江丹阳高三10月期中,7)从废定影液[主要含有H+、 、HSO 、Br-等微
2 3
粒]中回收Ag和Br 的主要步骤:向该废定影液中加入NaOH调节pH在7.5~8.5之间,然后再加入稍过
2
量NaS溶液沉银,过滤、洗涤及干燥,灼烧Ag S制Ag;滤液中通入Cl 氧化Br-,用苯萃取分液。下列化
2 2 2
学反应表示正确的是
A. 废液用过量的硝酸处理:
B.用铜电极电解CuSO 溶液:
4
C.稀硝酸洗涤做过银镜反应的试管:
D.CuSO 溶液中加入小粒金属钠:
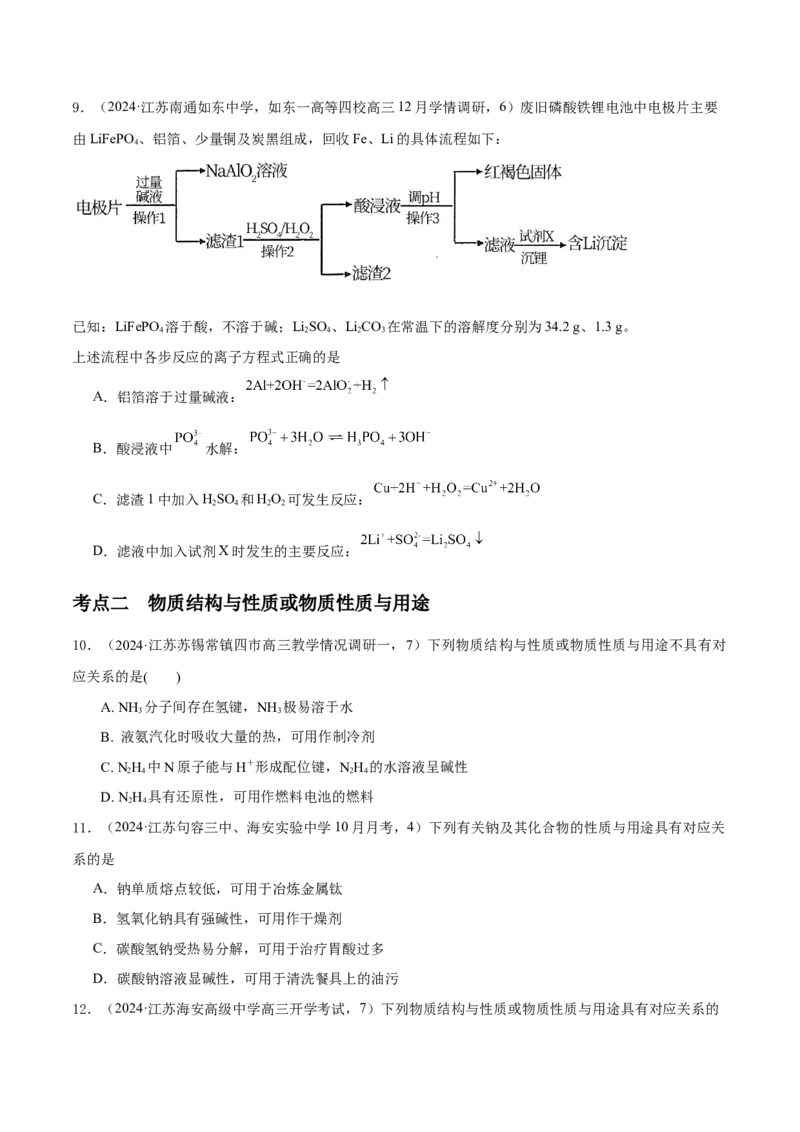
49.(2024·江苏南通如东中学,如东一高等四校高三12月学情调研,6)废旧磷酸铁锂电池中电极片主要
由LiFePO 、铝箔、少量铜及炭黑组成,回收Fe、Li的具体流程如下:
4
已知:LiFePO 溶于酸,不溶于碱;LiSO 、LiCO 在常温下的溶解度分别为34.2 g、1.3 g。
4 2 4 2 3
上述流程中各步反应的离子方程式正确的是
A.铝箔溶于过量碱液:
B.酸浸液中 水解:
C.滤渣1中加入HSO 和HO 可发生反应:
2 4 2 2
D.滤液中加入试剂X时发生的主要反应:
考点二 物质结构与性质或物质性质与用途
10.(2024·江苏苏锡常镇四市高三教学情况调研一,7)下列物质结构与性质或物质性质与用途不具有对
应关系的是( )
A. NH 分子间存在氢键,NH 极易溶于水
3 3
B. 液氨汽化时吸收大量的热,可用作制冷剂
C. NH 中N原子能与H+形成配位键,NH 的水溶液呈碱性
2 4 2 4
D. N H 具有还原性,可用作燃料电池的燃料
2 4
11.(2024·江苏句容三中、海安实验中学10月月考,4)下列有关钠及其化合物的性质与用途具有对应关
系的是
A.钠单质熔点较低,可用于冶炼金属钛
B.氢氧化钠具有强碱性,可用作干燥剂
C.碳酸氢钠受热易分解,可用于治疗胃酸过多
D.碳酸钠溶液显碱性,可用于清洗餐具上的油污
12.(2024·江苏海安高级中学高三开学考试,7)下列物质结构与性质或物质性质与用途具有对应关系的是
A.甲醇分子间能形成氢键,可与水任意比例互溶
B. 具有氧化性,可用于冶金工业
C.干冰能溶于水,可用作制冷剂
D.二甲醚具有可燃性,可用作燃料
13.(2024·江苏海安高级中学12月月考,7)下列物质的性质与用途具有对应关系的是
A.臭氧有强氧化性,可用于水体杀菌消毒
B.浓硫酸有脱水性,可用于干燥某些气体
C.二氧化硫有还原性,可用于织物的漂白
D.硫化氢具有酸性,可用于沉淀重金属离子
14.(2024·江苏连云港五校高三12月联考,7)下列钠及其化合物的性质与用途具有对应关系的是
A.Na质软,可用于冶炼金属钛
B. 溶液显碱性,可用于去除物品表面的油污
C. 具有还原性,可用于吸收 尾气
D. 呈淡黄色,可用于呼吸面罩中作供氧剂
15.(2024·江苏南通如东中学,如东一高等四校高三12月学情调研,7)下列有关物质的性质与用途具有
对应关系的是
A.Al(OH) 具有两性,可用作塑料制品的阻燃剂
3
B.HO 具有强氧化性,可用于杀菌消毒
2 2
C.炭黑硬度大,可用于电极材料
D.铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀速率
16.(2024·江苏南通如皋高三2月适应性考试(一),4)下列物质的结构与性质或性质与用途具有对应
关系的是
A. 中化学键非常牢固,可用作保护气
B.乙醇易溶于水,可用于消毒杀菌
C.浓硫酸具有强氧化性,可用于与 反应制
D. 是极性分子,可用于漂白纸浆考点三 元素化合物的转化
17.(2024·江苏宿迁3月学情调研,8)下列有关氮、硫、氯的单质及其化合物的转化正确的是( )
A. 工业制备漂白粉:饱和食盐水――→Cl――→漂白粉
2
B. 工业制备硫酸:FeS――→SO――→HSO
2 3 2 4
C. 实验室制备NH:Ca(OH)+2NHCl=====CaCl+2NH↑+2HO
3 2 4 2 3 2
D. 实验室制备SO:NaSO+2HNO===2NaNO+SO↑+HO
2 2 3 3 3 2 2
18.(2024·江苏句容三中、海安实验中学10月月考,6)氯及其化合物应用广泛。氯的单质Cl 可由MnO
2 2
与浓盐酸共热得到,Cl 能氧化Br-,可从海水中提取Br ;氯的氧化物ClO 可用于自来水消毒,ClO 是一
2 2 2 2
种黄绿色气体,易溶于水,与碱反应会生成ClO 与ClO ,在稀硫酸和NaClO 的混合溶液中通入SO 气体
3 2
可制得ClO ;漂白液和漂白粉的有效成分是次氯酸盐,可作棉、麻的漂白剂。下列含氯物质的转化正确的
2
是
A.漂白粉 HClO(aq) Cl(g)
2
B.MgCl (aq) 无水MgCl Mg
2 2
C.NaCl(aq) Cl(g) FeC1
2 3
D.NaCl(aq) NaHCO (aq) NaCO(s)
3 2 3
19.(2024·江苏连云港五校高三12月联考,9)元素及其化合物的转化在工业生产中具有极其重要的用途。
下列物质间转化能实现的是
A.工业制取漂白粉:饱和食盐水 漂白粉
B.工业制取镁: 溶液 无水 Mg
C.工业制取硫酸:
D.工业制取纯碱:饱和食盐水 固体 固体
20.(2024·江苏南通海门高三第二次调研,5)在给定条件下,下列关于物质间的转化能实现的是
A.B.
C.
D.
21.(2024·江苏南通名校联盟高三12月学业质量联合监测,9)氮及其化合物的转化具有重要应用。下列
说法不正确的是
A.实验室探究稀硝酸与铜反应的气态产物:
B.工业制硝酸过程中的物质转化:
C.汽车尾气催化转化器中发生的主要反应:
D.实验室制备少量 的原理:
22.(2024·江苏南通如东中学,如东一高等四校高三12月学情调研,8)钠及其化合物的转化具有重要应
用。下列说法正确的是
A.金属钠制取 :
B.工业上制取 :饱和 溶液
C.工业上制取 :
D.用金属钠检验乙醚中是否含有少量乙醇的离子方程式:
23.(2024·江苏南通如皋高三2月适应性考试(一),8) 的燃烧热为 ,具有强还原性,
可由尿素 和 溶液一起反应制得。下列说法正确的是
A.侯氏制碱的原理可表示为 饱和 溶液
B.氨气催化氧化制取 属于氮的固定中的一种C.由尿素、 和 溶液制 时,应将 溶液滴加到尿素溶液中
D.浓氨水与浓硫酸靠近时会有白烟生成
24.(2024·江苏镇江丹阳高三10月期中,8)硫及其化合物的转化具有重要应用。下列说法不正确的是
A.硫酸型酸雨产生的途径:
B.工业制备硫酸过程中的物质转化:
C.钙基固硫过程中发生的总反应:
D.实验室制备少量 的原理: (固体) (浓)
25.(2024·江苏泰州中学、宿迁中学、宜兴中学高三12月调研,5)在指定条件下,下列物质间转化不能
实现的是
A. B.
C. D.