文档内容
新和县实验中学 2022-2023 学年第一学期月考考试试卷
高三年级学科: 化学 (时间90分钟分值:100分) 5. 下表列出了某短周期元素R的各级电离能数据(用I 1 、I 2 表示,单位为kJ/mol)。
I I I I ……
常用到的相对原子质量:H---1 C---12 O---16 Na--23 I---127 1 2 3 4
R 740 1500 7700 10500 ……
一、选择题(共 14 小题,每小题 3 分,共 42 分)
下列关于元素R的判断中一定正确的是( )
1. 下列电子排布图中违反洪特规则的是( )
A.R的最高正价为+3 B.R元素位于元素周期表中第IIA族
C.R元素的原子最外层共有4个电子 D.R元素基态原子的电子排布式为1s22s2
6. 下列说法中正确的是( )
A.气体单质中,一定有σ键,可能有π键
B.PCl 分子是非极性分子
3
C. 甲醛(HCHO)、苯和二氧化碳中碳原子均采用sp2杂化
2. 下面的排序不正确的是( )
D. ClO- 的 VSEPR模型与离子的空间立体构型一致
4
A.氢键属于一种较强的分子间作用力,只能存在于分子之间
7. 下列各组物质的晶体类型相同的是( )
B.硬度由大到小:金刚石>碳化硅>晶体硅
A.SiO 和SO B.I 和NaCl C.Cu和Ag D.SiC和MgO
2 3 2
C. 熔点由高到低:NaNaCl>NaBr>Nal
A.σ键比π键的电子云重叠程度大,形成的共价键强
3. 如图为周期表的一小部分,A、B、C、D、E的位置关系如图所示。其中B元素最高化合价是最低化
B.s—sσ键与 s—pσ键的电子云形状对称性相同
合价绝对值的3倍,它的最高价氧化物中含氧60%。下列说法正确的是( )
C.丙烯(CH —CH=CH )分子有 8 个σ键 1 个π键
3 2
A.D、B、E 三种元素的第一电离能逐渐减小
D.N 分子中有一个σ键,2 个π键;CH 中 4 个C—H 键的键能不相同 2 4
B. B.电负性:C>E
9. Al O 的下列性质能用晶格能解释的是( ) C.D、B、E 三种元素形成的简单离子的半径逐渐增大 2 3
D.气态氢化物的稳定性顺序:D<B<E A.Al2O3可用作耐火材料 B.固态时不导电,熔融时能导电
4. 关于[Cr(H O) Br ]Br·2H O的说法正确的是( ) C.Al2O3是两性氧化物 D.晶体Al2O3可以作宝石
2 4 2 2
A.配体为水分子,外界为Br- B.中心离子的配位数为6
10. 化学与人体健康及环境保护息息相关。下列叙述正确的是( )
C.中心离子Cr3+提供孤电子对 D.中心离子的化合价为+2
A.食品加工时不可添加任何防腐剂 B.掩埋废旧电池不会造成环境污染
C.天然气不完全燃烧会产生有毒气体 D.使用含磷洗涤剂不会造成水体污染
下载最新免费模拟卷,到公众号:一枚试卷君
:
名姓生学
:号考
(班级)年
高 A
D B E
C11. N 为阿伏加德罗常数的值。下列叙述正确的是( )
A 学元素。
A. 8g重水( D O)中含有的质子数为10N
2 A
B. 3mol的NO 与H O完全反应时转移的电子数为4N
2 2 A
C. 32g环状S( )分子中含有的S-S键数为1N
8 A
请回答下列问题:
D. 1LpH=4的溶液中离子数为
(1)元素b位于周期表中 区,其基态原子核外有 种运动状态不同的电子。
12. 一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的
(2)基态c原子中有 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为 形。
原子序数依次增大、且总和为24。下列有关叙述错误的是( ) (3)ca 理论上为离子化合物,猜测其电子式为 。
5
A.该化合物中,W、X、Y 之间均为共价键 (4)基态f2外围电子的电子排布图为 ,已知高温下化合物f
2
d比化合物fd更稳定,试从核外电子
B.Z 的单质既能与水反应,也可与甲醇反应 排布的角度解释原因 。 (2 分 )
C.Y的最高化合价氧化物的水化物为强酸 D.X的氟化物XF 中原子均为8电子稳定结构 (5)b、c、d三种元素的第一电离能由大到小的顺序为 (填元素符号)。(2分)
3
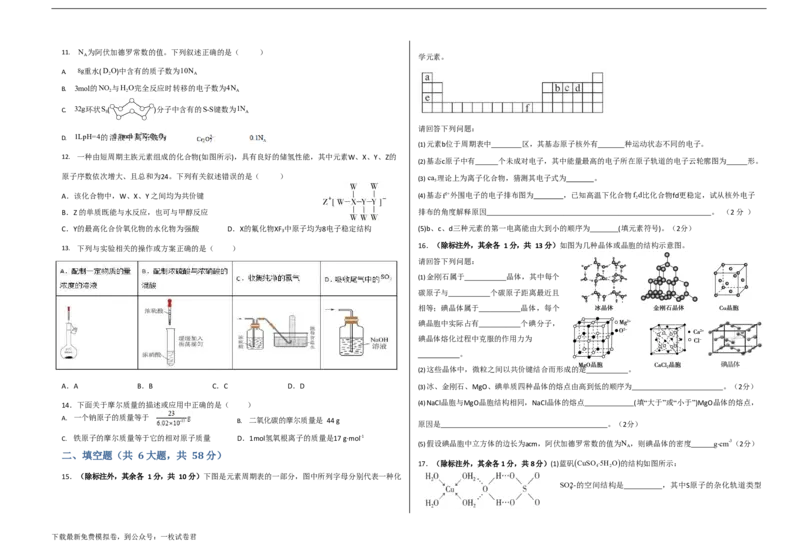
13. 下列与实验相关的操作或方案正确的是( ) 16.(除标注外,其余各 1 分,共 13 分)如图为几种晶体或晶胞的结构示意图。
请回答下列问题:
(1)金刚石属于 晶体,其中每个
碳原子与 个碳原子距离最近且
相等;碘晶体属于 晶体,每个
碘晶胞中实际占有 个碘分子,
碘晶体熔化过程中克服的作用力为
。
(2)这些晶体中,微粒之间以共价键结合而形成的是 。
A.A B.B C.C D.D (3)冰、金刚石、MgO、碘单质四种晶体的熔点由高到低的顺序为 。(2分)
14.下面关于摩尔质量的描述或应用中正确的是( )
(4)NaCl晶胞与MgO晶胞结构相同,NaCl晶体的熔点 (填“大于”或“小于”)MgO晶体的熔点,
A. 一个钠原子的质量等于 B. 二氧化碳的摩尔质量是 44 g
原因是 。(2分)
C. 铁原子的摩尔质量等于它的相对原子质量 D.1mol氢氧根离子的质量是17 g·mol-1
(5)假设碘晶胞中立方体的边长为acm,阿伏加德罗常数的值为N ,则碘晶体的密度 gcm-3(2分)
A
二、填空题(共 6 大题,共 58 分)
17.(除标注外,其余各1分,共8分)(1)蓝矾CuSO 5H O的结构如图所示:
4 2
15.(除标注外,其余各 1 分,共 10 分)下图是元素周期表的一部分,图中所列字母分别代表一种化
SO2-的空间结构是 ,其中S原子的杂化轨道类型
4
下载最新免费模拟卷,到公众号:一枚试卷君是 ;基态O原子的价层电子排布图为 。
据此回答下列问题:
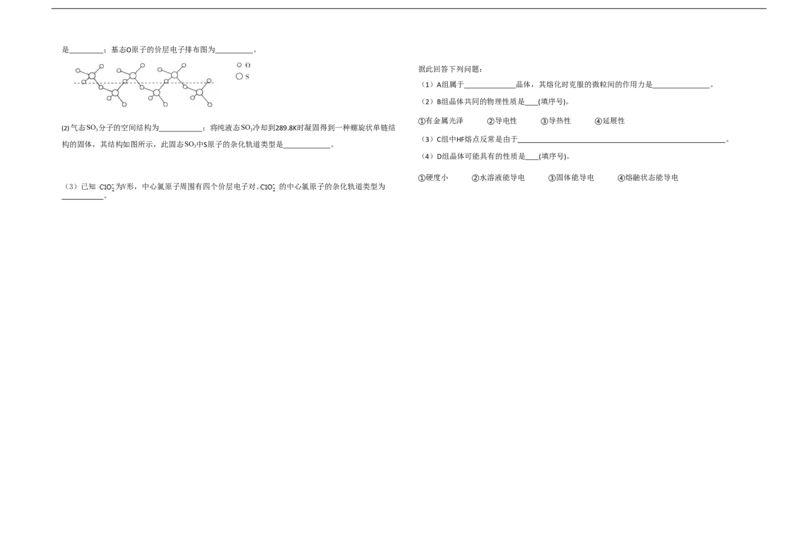
(1)A组属于 晶体,其熔化时克服的微粒间的作用力是 。
(2)B组晶体共同的物理性质是 (填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(2)气态SO 分子的空间结构为 ;将纯液态SO 冷却到289.8K时凝固得到一种螺旋状单链结
3 3
(3)C组中HF熔点反常是由于 。
构的固体,其结构如图所示,此固态SO 中S原子的杂化轨道类型是 。
3
(4)D组晶体可能具有的性质是 (填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(3)已知 为V形,中心氯原子周围有四个价层电子对。 的中心氯原子的杂化轨道类型为
。(3)二氧化钛TiO是常用的具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米
2
TiO 催化的一个实例如图所示。
2
化合物甲的分子中采取sp2
杂化方式的碳原子个数为 (2分)
18.(每空 2 分,共 8 分)完成下列问题:法匹拉韦是治疗新冠肺炎的一种药物,结构简式
如图。
(1)该药物分子中,电负性最大的元素是 。 (2)该分子的所有原子(填“是”或“否”)共平面。
(3)分子中氧原子参与形成 键(填“极性”或“非极性”)
(4)C、N、O、F四种元素的简单氢化物中沸点最低的是 (填化学式)。
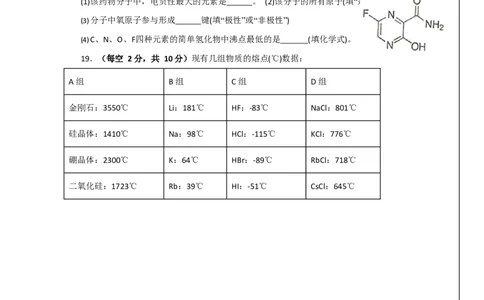
19.(每空 2 分,共 10 分)现有几组物质的熔点(℃)数据:
A 组 B 组 C 组 D 组
金刚石:3550℃ Li:181℃ HF:-83℃ NaCl:801℃
硅晶体:1410℃ Na:98℃ HCl:-115℃ KCl:776℃
硼晶体:2300℃ K:64℃ HBr:-89℃ RbCl:718℃
二氧化硅:1723℃ Rb:39℃ HI:-51℃ CsCl:645℃20.(除标注外,其余各 1 分,共 9 分)
Ⅰ.化合物 YX 、ZX 中,X、Y、Z 的核电荷数小于 18;X 原子最外能层的 p 能级中有一个轨
2 2
道充填了 2 个电子,Y 原子的最外层中 p 能级的电子数等于前一能层电子总数,且 X 和 Y
具有相同的电子层数;Z 与 X 在周期表中位于同一主族。回答下列问题:
(1)X的电子排布式为 ,Y的轨道表示式为 。
(2)ZX 的分子式是 ,YX 电子式是 。
2 2
(3)Z形成的简单阴离子的结构示意图是 。
(4)Y和Z一定条件下形成简单分子的结构式是 。
Ⅱ.目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨
大潜力。
(1)硫酸镍溶于氨水形成[Ni(NH ) ]SO 蓝色溶液。
3 6 4
①基态Ni2+的核外电子排布式为 。
②在[Ni(NH)]2+中存在的化学键有( )(2分)
3 6
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
参考答案:
1.C
【解析】洪特规则:当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占
据一个轨道,而且自旋方向相同。
【详解】A. C原子的2p能级的2个电子单独占据一个轨道,而且自旋方向相同,没有违反洪
特规则,A选项不符合题意;
B. P原子的3p能级的3个电子单独占据一个轨道,而且自旋方向相同,没有违反洪特规则,B
选项不符合题意;
C. N原子的2p能级的3个电子没有单独占据轨道,违反洪特规则,C选项符合题意;
D. Mg原子的3s电子自旋相同,违反了泡利原理,不是违反洪特规则,D选项不符合题意;
答案选C。
2.A
【详解】A.邻羟基苯甲醛分子( )内的羟基与醛基之间存在氢键,对羟基苯甲醛分子()之间存在氢键,所以氢键既可存在于分子之间,也可存在于分子之内,故A
错误;
B.原子晶体中共价键越短则键能越大,键能越大共价键越强,三者的结构是类似的,但是硅原子
比碳原子要大,则硬度由大到小:金刚石碳化硅晶体硅,故B正确;
AlMgNa
C.金属离子的电荷越大、半径越小,其熔点越大,则熔点由高到低为 ,故C正确;
D.离子晶体中离子键越短,晶格能越大,因为卤族元素从上到下是半径不断增大的,则晶格能由
大到小:NaFNaClNaBrNaI,故D正确;
答案选A。
3.D
【解析】B元素最高价是最低负价绝对值的3倍,则B元素最高正价为+6价,其最高价氧化物化
学式表示为BO ,又最高氧化物中含氧60%,令B元素相对原子质量为b,则
3
163
100%=60%,解得b=32,故B为S元素,由元素在周期表中相对位置可知,A为O元
b+163
素、C为Se、D为P元素、E为Cl,
【详解】由上述分析可知,A为O,B为S,C为Se,D为P,E为Cl,
A.非金属性越强,第一电离能越大,但P的3p电子半满为稳定结构,则D、E、B三种元素的
第一电离能逐渐减小,故A错误;
B.同主族元素从上到下,元素的电负性减弱,同周期从左到右,电负性增大,则电负性E>C,
故B错误;
C.D、B、E三种元素形成的简单离子具有相同的核外电子排布,核电荷数越大离子半径越小,
故C错误;
D.非金属性:D(P)<B(S)<E(Cl),故氢化物稳定性:D<B<E,故D正确;
故选:D。
4.B
【详解】A.[Cr(H O) Br ]Br•2H O中配位体是H O、Br,外界为Br-,选项A错误;
2 4 2 2 2
B.[Cr(H O) Br ]-中的中心离子的配体是H O、Br,该配离子中含有4个H O、2个Br,所以配位
2 4 2 2 2
数是6,选项B正确;
C. [Cr(H O) Br ]Br·2H O中内界为[Cr(H O) Br ]+,Cr3+为中心离子,配体为H O、Br-,配位数为
2 4 2 2 2 4 2 2
6,外界为Br-,Cr3+提供的空轨道,选项C错误;D.[Cr(H O) Br ]Br•2H O中阴离子是溴离子,溴离子的化合价是-1价,所以铬离子的化合价是+3
2 4 2 2
价,选项D错误;
答案选B。
5.B
【分析】从表中原子的第一至第四电离能可以看出,元素的第一、第二电离能都较小,可失去2
个电子,最高化合价为+2价,即最外层应有2个电子,应为第IIA族元素。
【详解】A.根据分析可知,R的最高正价为+2,故A错误;
B.根据分析可知,R元素位于元素周期表中第IIA族,故B正确;
C.根据分析可知,R元素的原子最外层共有2个电子,故C错误;
D.根据分析可知,短周期元素R为第IIA族元素,可能是Mg或Be,即R元素基态原子的电子
排布式可能为1s22s22p63s2,故D错误;
答案选B。
6.D
【详解】A.稀有气体单质是单原子分子,分子中无化学键,故A项说法错误;
531
B.PCl 中P原子孤对电子对数为 =1,δ键数目为3,则P原子价电子对数为4,因此PCl
3 2 3
分子空间构型为三角锥型,因此PCl 是极性分子,故B项说法错误;
3
C.甲醛(HCHO)、苯均为平面结构,碳原子均采用 sp2杂化,二氧化碳为直线型结构,碳原子均
采用 sp杂化,故C项说法错误;
7142
D. ClO- 中Cl原子孤对电子对数为 2 =0,因此 ClO- 的 VSEPR 模型与离子的空间立体构
4 4
型一致,故D项说法正确;
综上所述,说法中正确的是D项,故答案为:D。
7.C
【详解】A.SiO 为原子晶体,SO 为分子晶体,晶体类型不同,故A错误;
2 3
B.I 为分子晶体,NaCl为离子晶体,晶体类型不同,故B错误;
2
C.Cu和Ag都为金属晶体,晶体类型相同,故C正确;
D.SiC为原子晶体,MgO为离子晶体,晶体类型不同,故D错误;
故选C。
8.D
【详解】A.σ键是电子云“头碰头”的方式重叠,π键是电子云“肩并肩”的方式重叠,σ键比
π键的电子云重叠程度大,形成的共价键强,A正确;B.s—sσ键与s—pσ键都是轴对称的,所以s—sσ键与s—pσ键的电子云形状对称性相同,B正确;
C.丙烯(CH —CH=CH )分子有8个σ键1个π键,C正确;
3 2
D.N 分子的结构式为NN,有1个σ键,2个π键,CH 中4个C—H键的键能完全相同,D错
2 4
误;
故选D。
9.A
【详解】A.Al O 中Al3+和O2-所带电荷都比较多,半径又都很小,因此Al O 的晶格能很大,熔
2 3 2 3
点很高,故Al O 可作耐火材料,能用晶格能解释,故A选;
2 3
B.Al O 固态时不导电,熔融时能导电,说明熔融状态能够电离出自由移动的离子,与晶格能无
2 3
关,故B不选;
C.Al O 是两性氧化物是指氧化铝能够与强酸反应,也能与强碱反应,与晶格能无关,故C不选;
2 3
D.晶体Al O 俗称刚玉,导热好,硬度高,透红外,化学稳定性好,具有较好的光学性能,可
2 3
以用作宝石,与晶格能无关,故D不选;
故选A。
10.C
【详解】A.食品加工时,可适当添加食品添加剂和防腐剂等,如苯甲酸钠,故A错误;
B.废旧电池中含有重金属等金属离子,会造成土壤污染,水体污染等,故B错误;
C.天然气主要成分为甲烷,不完全燃烧会产生一氧化碳等有毒气体,故C正确;
D.含磷洗涤剂的排放,使水中磷过多,造成水中藻类疯长,消耗水中溶解的氧,水体变浑浊,
故D错误;
故选C。
11.C
18g
=
【详解】A. D 2 O 的质子数为10,18g D 2 O 的物质的量为20g/mol 0.9mol, 则18g重水( D 2 O )
9N
中所含质子数为 A,A错误;
NO H O
B. 2与 2 反应的化学方程式为:3NO +H O=2HNO +NO,该反应消耗3个NO 分子转移的电
2 2 3 2
2N
子数为2个,则有3mol的NO 参与反应时,转移的电子数为 A,B错误;
232g 1
=
C.一个S ( )分子中含有的S-S键数为8个,32gS 的物质的量为832g/mol 8
8 8
1
mol,则含有的
S-S
键数为
8
8N
A
=N
A
,C正确;
K CrO CrO2-+H O 2CrO2-+2H+ Cr O2- CrO2-
D.酸性 2 2 7溶液中存在: 2 7 2 4 ,含Cr元素微粒有 2 7 和 4 ,则
1L pH=4 0.1molL-1K CrO Cr O2- 0.1N
的 2 2 7溶液中 2 7 离子数应小于 A,D错误;
故选C。
12.D
【分析】一种由短周期主族元素形成的化合物,具有良好的储氢性能,其中元素W、X、Y、Z的
原子序数依次增大,且总和为24,根据图示,W为1价形成共价键,W为氢,Z为+1价阳离子,
Z为Na,Y为3价,Y为N,24-1-11-7=5,X为B元素。
【详解】A.该化合物中,H、B、N之间均以共用电子对形成共价键,故A正确;
B.Na单质既能与水反应生成氢氧化钠和氢气,也能与甲醇反应生成甲醇钠和氢气,故B正确;
C.N的最高价氧化物的水化物HNO 为强酸,故C正确;
3
D.B的氟化物BF 中B原子最外层只有6个电子,达不到8电子稳定结构,故D错误;
3
故选D。
13.B
【详解】A.配制一定物质的量浓度的溶液时,不能在容量瓶里溶解固体,应在烧杯中溶解固体
并冷却至室温,再转移到容量瓶中定容,图中操作不合理,A错误;
B.浓硫酸和浓硝酸混合时放热,浓硫酸密度大于浓硝酸,所以要把浓硫酸缓慢加入浓硝酸中配
制二者的混酸溶液,B正确;
Cl Cl
C.实验室中一般用向上排空气法收集 2,若用题图所示方法收集,收集到的 2中会混有少量
Cl
的水蒸气,使收集到的 2不纯,C错误;
SO
2
D.题图所示装置吸收尾气中 时,容易引起倒吸,且装置不应密封,D错误;
故选B。
14.A【解析】略
H
H:N:H :H
15. p 6 3 哑铃(或纺锤)
H
Cu+的最外层电子排布式为3d10,而Cu2的最外层电子排布式为3d9,最外层电子排布
Cu O
达到全满时稳定,所以固态 2 稳定性强于CuO N>O>C
【分析】由题可知,元素a、b、c、d、e、f分别为H、C、N、O、Na、Cu。
【详解】(1)C位于周期表中p区,其基态原子核外各电子的运动状态都不相同,故有6种,故答
案为:p;6;
(2)基态N原子中有3个未成对电子,其中能量最高的电子所在原子轨道为2p轨道,电子云轮廓
图为哑铃(纺锤)形,故答案为:3;哑铃(纺锤)形;
H
H:N:H :H
(3)根据铵根离子与氢负离子推测,离子化合物 为 ,其电子式为 ,故
NH NH H H
5 4
H
H:N:H :H
答案为: ;
H
(4)基态
Cu2
外围电子的电子排布图为 ;
Cu+
的最外层电子排布式为
3d10
,
Cu2 3d9 Cu O
而 的最外层电子排布式为 ,最外层电子排布达到全满时稳定,所以高温下 2 稳定性
强于CuO,故答案为: ;
Cu+
的最外层电子排布式为
3d10
,而
Cu2
的最外3d9 Cu O
层电子排布式为 ,最外层电子排布达到全满时稳定,所以固态 2 稳定性强于CuO;
(5)同周期 从左到右元素的第一电离能呈增大趋势,N的2p半充满,较稳定,第一电离能大于
O,C、N、O三种元素的第一电离能由大到小的顺序为N>O>C,故答案为:N>O>C。
16. 共价 4 分子 4 分子间作用力 金刚石晶
>MgO>
体 金刚石 碘单质>冰 小于 MgO晶体中离子所带的电荷数
1016
大于NaCl晶体中离子所带的电荷数,且r(Mg2+)