文档内容
素养说明:能依据事实,分析研究对象的构成要素和各要素的关系,建立认识模
型,反映研究对象的本质特征,揭示规律;高考大纲也要求能够通过对实际事物、
实验现象、实物、模型、图形的观察,获取有关的感性知识和印象,并进行初步加
工、吸收、有序存储的能力,数形结合的解题思想符合核心素养与考试大纲要求,
是提高学生解题能力的有效途径。
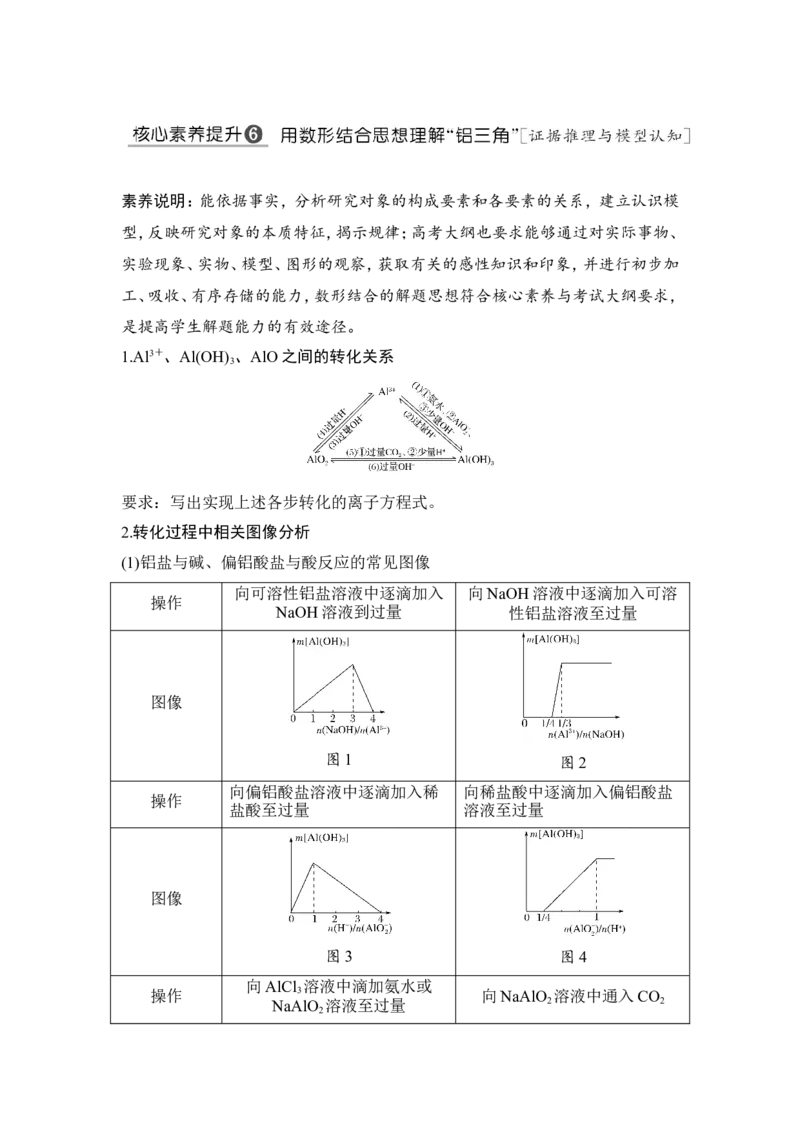
1.Al3+、Al(OH) 、AlO之间的转化关系
3
要求:写出实现上述各步转化的离子方程式。
2.转化过程中相关图像分析
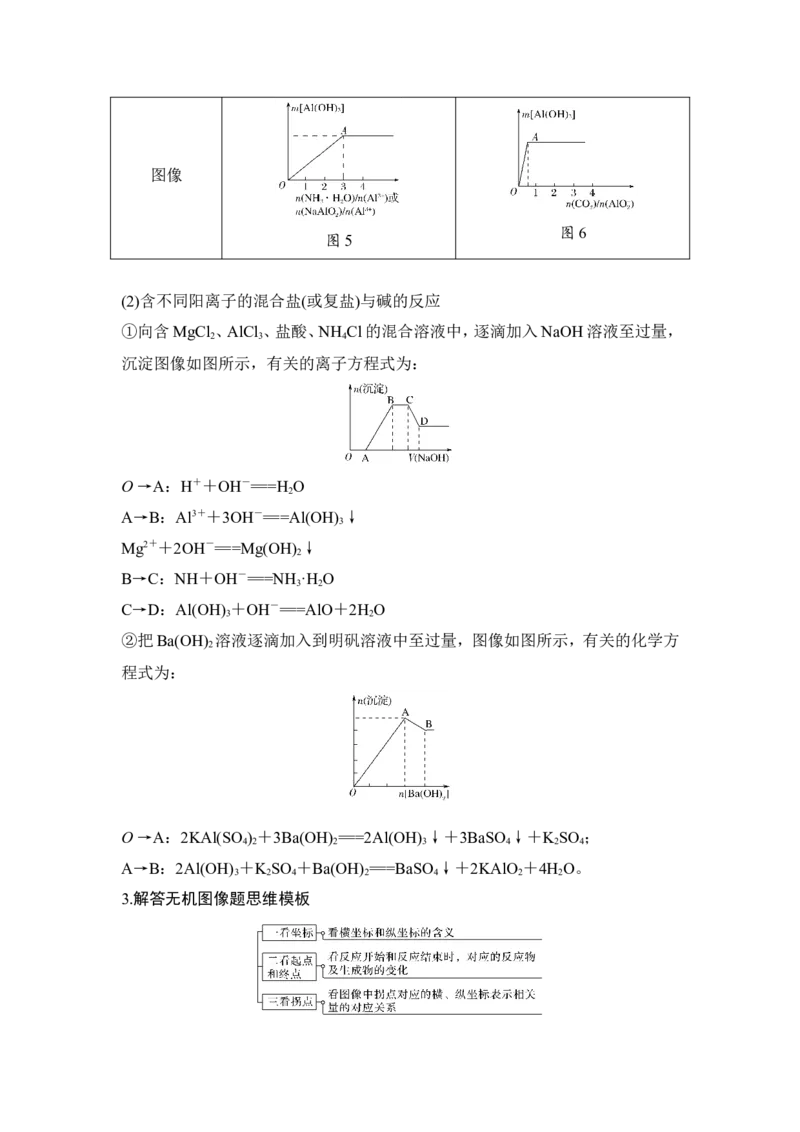
(1)铝盐与碱、偏铝酸盐与酸反应的常见图像
向可溶性铝盐溶液中逐滴加入 向NaOH溶液中逐滴加入可溶
操作
NaOH溶液到过量 性铝盐溶液至过量
图像
图1 图2
向偏铝酸盐溶液中逐滴加入稀 向稀盐酸中逐滴加入偏铝酸盐
操作
盐酸至过量 溶液至过量
图像
图3 图4
向AlCl 溶液中滴加氨水或
操作 3 向NaAlO 溶液中通入CO
NaAlO 溶液至过量 2 2
2图像
图6
图5
(2)含不同阳离子的混合盐(或复盐)与碱的反应
①向含MgCl 、AlCl 、盐酸、NH Cl的混合溶液中,逐滴加入NaOH溶液至过量,
2 3 4
沉淀图像如图所示,有关的离子方程式为:
O →A:H++OH-===H O
2
A→B:Al3++3OH-===Al(OH) ↓
3
Mg2++2OH-===Mg(OH) ↓
2
B→C:NH+OH-===NH ·H O
3 2
C→D:Al(OH) +OH-===AlO+2H O
3 2
②把Ba(OH) 溶液逐滴加入到明矾溶液中至过量,图像如图所示,有关的化学方
2
程式为:
O →A:2KAl(SO ) +3Ba(OH) ===2Al(OH) ↓+3BaSO ↓+K SO ;
4 2 2 3 4 2 4
A→B:2Al(OH) +K SO +Ba(OH) ===BaSO ↓+2KAlO +4H O。
3 2 4 2 4 2 2
3.解答无机图像题思维模板[题型专练]
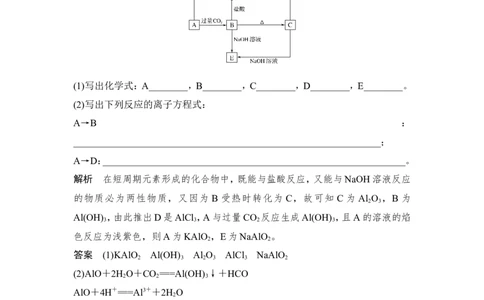
1.A、B、C、D、E五种化合物均含有某种短周期常见元素,它们的转化关系如图所
示,其中A的溶液为澄清溶液,C为难溶的白色固体,E则易溶于水,取A的溶液
灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
(1)写出化学式:A________,B________,C________,D________,E________。
(2)写出下列反应的离子方程式:
A→B :
_______________________________________________________________;
A→D:______________________________________________________________。
解析 在短周期元素形成的化合物中,既能与盐酸反应,又能与NaOH溶液反应
的物质必为两性物质,又因为 B 受热时转化为 C,故可知 C 为 Al O ,B 为
2 3
Al(OH) ,由此推出D是AlCl ,A与过量CO 反应生成Al(OH) ,且A的溶液的焰
3 3 2 3
色反应为浅紫色,则A为KAlO ,E为NaAlO 。
2 2
答案 (1)KAlO Al(OH) Al O AlCl NaAlO
2 3 2 3 3 2
(2)AlO+2H O+CO ===Al(OH) ↓+HCO
2 2 3
AlO+4H+===Al3++2H O
2
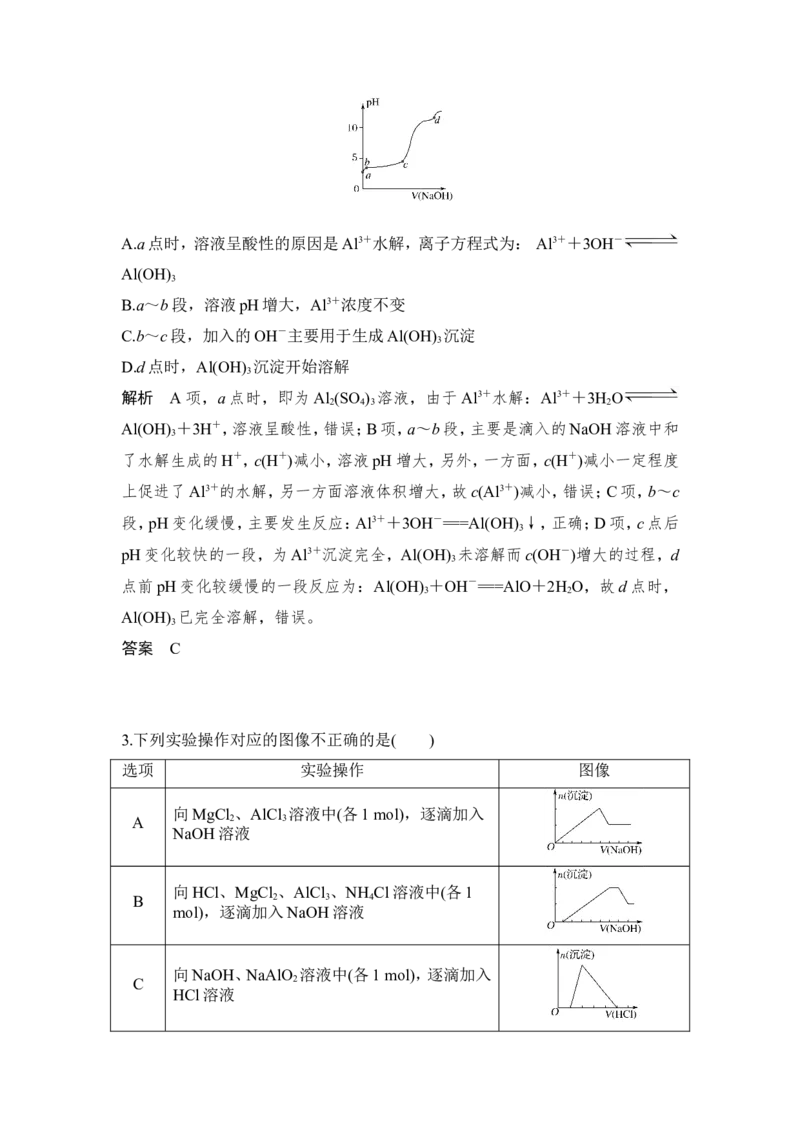
2.(安徽高考)室温下,在 0.2 mol·L-1 Al (SO ) 溶液中,逐滴加入 1.0 mol·L-1
2 4 3
NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列有关说法正
确的是( )A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为: Al3++3OH-
Al(OH)
3
B.a~b段,溶液pH增大,Al3+浓度不变
C.b~c段,加入的OH-主要用于生成Al(OH) 沉淀
3
D.d点时,Al(OH) 沉淀开始溶解
3
解析 A项,a点时,即为Al (SO ) 溶液,由于Al3+水解:Al3++3H O
2 4 3 2
Al(OH) +3H+,溶液呈酸性,错误;B项,a~b段,主要是滴入的NaOH溶液中和
3
了水解生成的H+,c(H+)减小,溶液pH增大,另外,一方面,c(H+)减小一定程度
上促进了Al3+的水解,另一方面溶液体积增大,故c(Al3+)减小,错误;C项,b~c
段,pH变化缓慢,主要发生反应:Al3++3OH-===Al(OH) ↓,正确;D项,c点后
3
pH变化较快的一段,为Al3+沉淀完全,Al(OH) 未溶解而c(OH-)增大的过程,d
3
点前pH变化较缓慢的一段反应为:Al(OH) +OH-===AlO+2H O,故d点时,
3 2
Al(OH) 已完全溶解,错误。
3
答案 C
3.下列实验操作对应的图像不正确的是( )
选项 实验操作 图像
向MgCl 、AlCl 溶液中(各1 mol),逐滴加入
A 2 3
NaOH溶液
向HCl、MgCl 、AlCl 、NH Cl溶液中(各1
B 2 3 4
mol),逐滴加入NaOH溶液
向NaOH、NaAlO 溶液中(各1 mol),逐滴加入
C 2
HCl溶液向NaOH、Na CO 混合溶液中(各1 mol)滴加
D 2 3
稀盐酸
解析 A项,向MgCl 、AlCl 溶液中加入NaOH溶液,会产生Al(OH) 、Mg(OH)
2 3 3 2
沉淀,当NaOH溶液过量时,Al(OH) 沉淀又逐渐溶解,最后只剩余Mg(OH) 沉淀
3 2
图像与反应事实符合,正确;B项,向HCl、MgCl 、AlCl 、NH Cl溶液中加入
2 3 4
NaOH溶液,首先与HCl反应,无沉淀产生,然后产生Al(OH) 、Mg(OH) 沉淀,再
3 2
生成NH ·H O,最后Al(OH) 沉淀溶解,只有Mg(OH) 沉淀,图像与反应事实符合,
3 2 3 2
正确;C项,向NaOH、NaAlO 溶液中加入HCl溶液,首先与NaOH反应,没有沉
2
淀生成,然后与AlO反应生成Al(OH) 沉淀,HCl溶液过量后,Al(OH) 沉淀完全
3 3
溶解,图像与反应事实符合,正确;D项,向NaOH、Na CO 混合溶液中滴加稀盐
2 3
酸,首先与NaOH反应,没有气体生成,后与Na CO 反应生成NaHCO ,没有气体
2 3 3
生成,再与NaHCO 生成气体,图像与反应事实不符合,符合题意。
3
答案 D
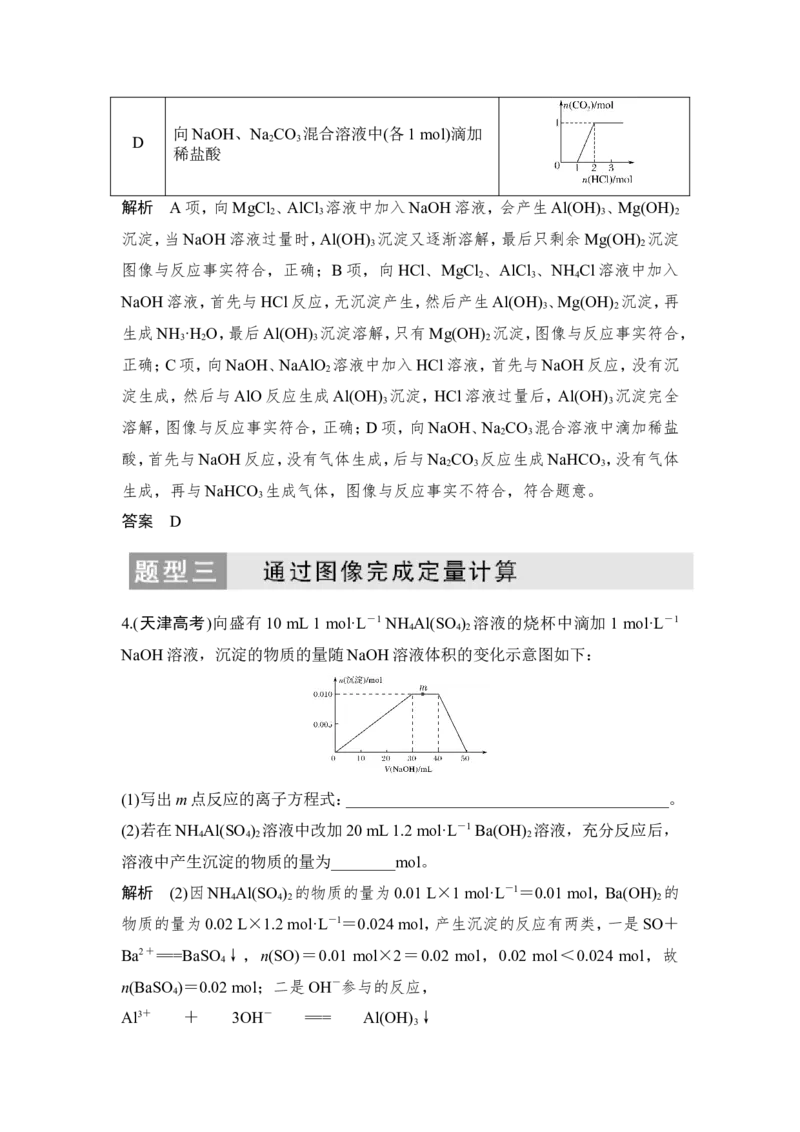
4.(天津高考)向盛有10 mL 1 mol·L-1 NH Al(SO ) 溶液的烧杯中滴加 1 mol·L-1
4 4 2
NaOH溶液,沉淀的物质的量随NaOH溶液体积的变化示意图如下:
(1)写出m点反应的离子方程式:________________________________________。
(2)若在NH Al(SO ) 溶液中改加20 mL 1.2 mol·L-1 Ba(OH) 溶液,充分反应后,
4 4 2 2
溶液中产生沉淀的物质的量为________mol。
解析 (2)因NH Al(SO ) 的物质的量为0.01 L×1 mol·L-1=0.01 mol,Ba(OH) 的
4 4 2 2
物质的量为0.02 L×1.2 mol·L-1=0.024 mol,产生沉淀的反应有两类,一是SO+
Ba2+===BaSO ↓,n(SO)=0.01 mol×2=0.02 mol,0.02 mol<0.024 mol,故
4
n(BaSO )=0.02 mol;二是OH-参与的反应,
4
Al3+ + 3OH- === Al(OH) ↓
30.01 mol 0.03 mol 0.01 mol
OH-余 0.024 mol×2-0.03 mol=0.018 mol,之后发生反应:NH+OH-
===NH ·H O,n(NH)=0.01 mol,再消耗OH- 0.01 mol,则剩余OH-为0.018 mol
3 2
-0.01 mol=0.008 mol,最后发生沉淀的溶解:Al(OH) +OH-===AlO+2H O,
3 2
OH-为0.008 mol,溶解Al(OH) 0.008 mol,则剩余Al(OH) 为0.01 mol-0.008
3 3
mol=0.002 mol。溶液中产生沉淀的物质的量为 0.02 mol+0.002 mol=0.022
mol。
答案 (1)NH+OH-===NH ·H O
3 2
(2)0.022