文档内容
素养说明:对于常见金属钠、镁、铝、铁、铜金属之外的陌生金属镍、钴、锰、钒、钛
等金属及其化合物的实验探究和工艺流程图是近几年高考重要题源,通过对这些
陌生金属及其化合物探究,充分体现考生的归纳、分析及信息运用能力。
1.钒及化合物
(1)钒单质的性质:银白色金属,熔点高,有延展性,质坚硬,无磁性。具有耐酸性,
在空气中不被氧化,可溶于氢氟酸、硝酸和王水。
(2)钒的氧化物
钒能分别以+2、+3、+4、+5价与氧结合,形成四种氧化物,一氧化钒,三氧化
二钒,二氧化钒,五氧化二钒。
(3)钒盐
钒盐包括V4+、 VO(偏钒酸盐)、VO(正钒酸盐),包括:偏钒酸铵、偏钒酸钠、偏钒
酸钾、正钒酸钠、焦钒酸钠;四价盐:硫酸氧钒、草酸氧钒。不同价态的钒离子有不
同的颜色:(VO )+颜色为浅黄色或深绿色,(VO)2+颜色为蓝色,V3+为绿色,V2+为
2
紫色。
2.铬(Cr)及化合物
(1)铬单质的性质:铬是银白色的金属,难熔(熔点1 800℃),铬是最硬的金属,铬的
化学性质很稳定,在常温下,放在空气中或浸在水里,不会生锈。
(2)重要化合物
①Cr O :
2 3
性质:绿色颜料,俗称“铬绿”,它是一种两性氧化物,能与酸或浓碱溶液反应。
②K Cr O (重铬酸钾)
2 2 7
性质:橙红色晶体,具有强氧化性,与盐酸反应(加热)制备氯气,K Cr O 还可以用
2 2 7
来检测司机酒驾。在分析化学中,可以用K Cr O 来测定铁的含量。
2 2 7
3.锰及其化合物
(1)锰单质的性质:银白色金属,硬而脆,熔沸点高;在空气中易氧化生成褐色氧化
物覆盖层,燃烧时生成四氧化三锰;溶于稀盐酸、稀硫酸生成二价锰盐。
(2)锰的化合物①二氧化锰
黑色结晶体或无定形粉末。熔点390 ℃,不溶于水和硝酸,与苛性碱和氧化剂共
熔,放出二氧化碳而生成高锰酸盐,在535 ℃分解成三氧化二锰和氧气,是强氧
化剂。
②高锰酸钾:又名灰锰氧
性质:紫色的结晶固体,溶于水、碱液,微溶于甲醇、丙酮、硫酸。具有强氧化性,
在生活、医疗上广泛用作杀菌消毒剂,在实验室中和工业上常用作氧化剂,作氧
化剂时其还原产物因介质的酸碱性而不同。
[题型专练]
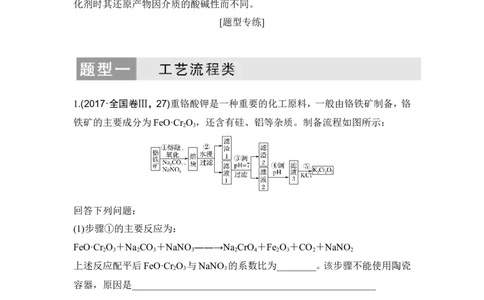
1.(2017·全国卷Ⅲ,27)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬
铁矿的主要成分为FeO·Cr O ,还含有硅、铝等杂质。制备流程如图所示:
2 3
回答下列问题:
(1)步骤①的主要反应为:
FeO·Cr O +Na CO +NaNO ――→Na CrO +Fe O +CO +NaNO
2 3 2 3 3 2 4 2 3 2 2
上述反应配平后FeO·Cr O 与NaNO 的系数比为________。该步骤不能使用陶瓷
2 3 3
容器,原因是__________________________________________________
______________________________________________________________。
(2)滤渣1中含量最多的金属元素是________,滤渣2的主要成分是________及含
硅杂质。
(3)步骤④调滤液 2 的 pH 使之变________(填“大”或“小”),原因是
_____________________________________________________________________
(用离子方程式表示)。
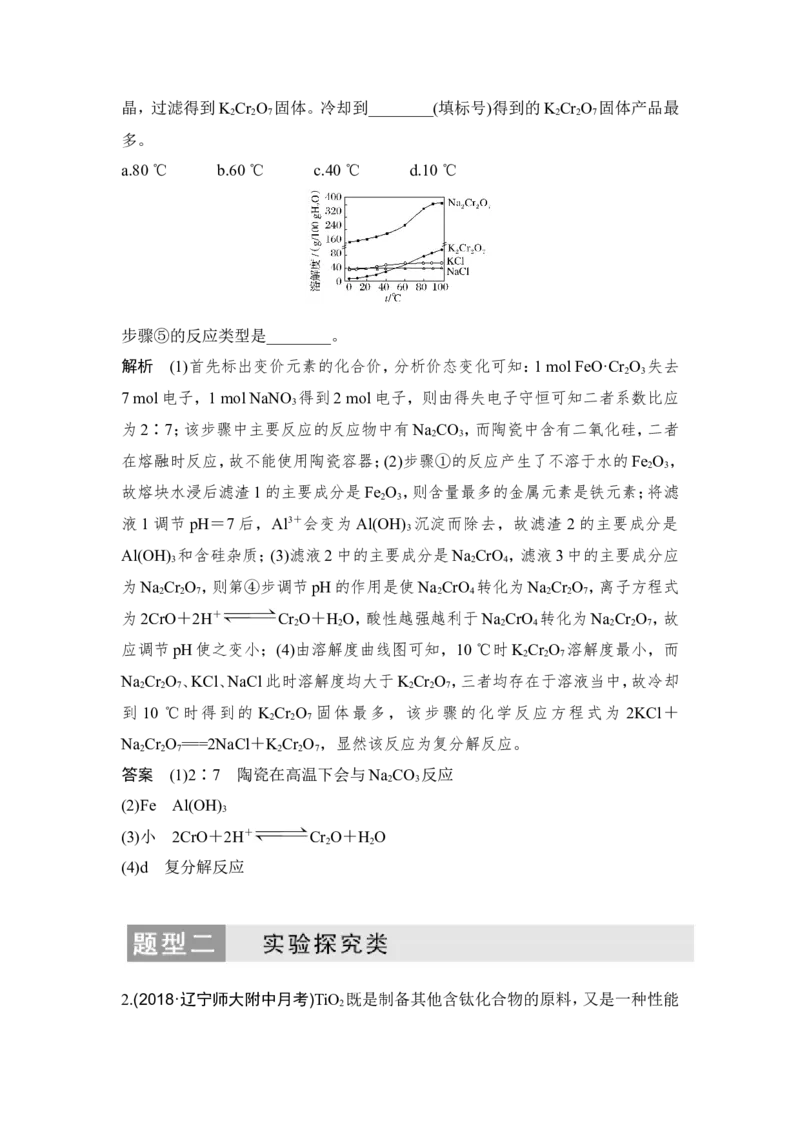
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K Cr O 固体。冷却到________(填标号)得到的K Cr O 固体产品最
2 2 7 2 2 7
多。
a.80 ℃ b.60 ℃ c.40 ℃ d.10 ℃
步骤⑤的反应类型是________。
解析 (1)首先标出变价元素的化合价,分析价态变化可知:1 mol FeO·Cr O 失去
2 3
7 mol电子,1 mol NaNO 得到2 mol电子,则由得失电子守恒可知二者系数比应
3
为2∶7;该步骤中主要反应的反应物中有Na CO ,而陶瓷中含有二氧化硅,二者
2 3
在熔融时反应,故不能使用陶瓷容器;(2)步骤①的反应产生了不溶于水的Fe O ,
2 3
故熔块水浸后滤渣1的主要成分是Fe O ,则含量最多的金属元素是铁元素;将滤
2 3
液1调节pH=7后,Al3+会变为Al(OH) 沉淀而除去,故滤渣 2的主要成分是
3
Al(OH) 和含硅杂质;(3)滤液2中的主要成分是Na CrO ,滤液3中的主要成分应
3 2 4
为Na Cr O ,则第④步调节pH的作用是使Na CrO 转化为Na Cr O ,离子方程式
2 2 7 2 4 2 2 7
为2CrO+2H+ Cr O+H O,酸性越强越利于Na CrO 转化为Na Cr O ,故
2 2 2 4 2 2 7
应调节pH使之变小;(4)由溶解度曲线图可知,10 ℃时K Cr O 溶解度最小,而
2 2 7
Na Cr O 、KCl、NaCl此时溶解度均大于K Cr O ,三者均存在于溶液当中,故冷却
2 2 7 2 2 7
到 10 ℃时得到的 K Cr O 固体最多,该步骤的化学反应方程式为 2KCl+
2 2 7
Na Cr O ===2NaCl+K Cr O ,显然该反应为复分解反应。
2 2 7 2 2 7
答案 (1)2∶7 陶瓷在高温下会与Na CO 反应
2 3
(2)Fe Al(OH)
3
(3)小 2CrO+2H+ Cr O+H O
2 2
(4)d 复分解反应
2.(2018·辽宁师大附中月考)TiO 既是制备其他含钛化合物的原料,又是一种性能
2优异的白色颜料。
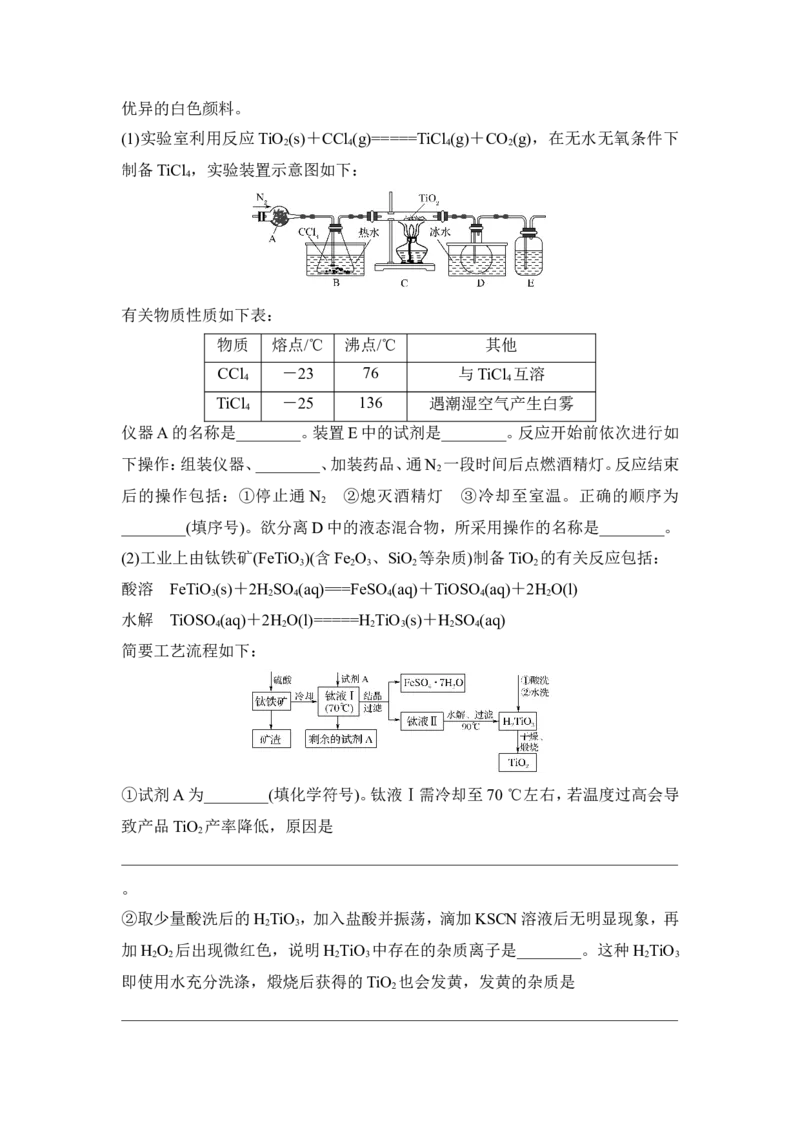
(1)实验室利用反应TiO (s)+CCl (g)=====TiCl (g)+CO (g),在无水无氧条件下
2 4 4 2
制备TiCl ,实验装置示意图如下:
4
有关物质性质如下表:
物质 熔点/℃ 沸点/℃ 其他
CCl -23 76 与TiCl 互溶
4 4
TiCl -25 136 遇潮湿空气产生白雾
4
仪器A的名称是________。装置E中的试剂是________。反应开始前依次进行如
下操作:组装仪器、________、加装药品、通N 一段时间后点燃酒精灯。反应结束
2
后的操作包括:①停止通N ②熄灭酒精灯 ③冷却至室温。正确的顺序为
2
________(填序号)。欲分离D中的液态混合物,所采用操作的名称是________。
(2)工业上由钛铁矿(FeTiO )(含Fe O 、SiO 等杂质)制备TiO 的有关反应包括:
3 2 3 2 2
酸溶 FeTiO (s)+2H SO (aq)===FeSO (aq)+TiOSO (aq)+2H O(l)
3 2 4 4 4 2
水解 TiOSO (aq)+2H O(l)=====H TiO (s)+H SO (aq)
4 2 2 3 2 4
简要工艺流程如下:
①试剂A为________(填化学符号)。钛液Ⅰ需冷却至70 ℃左右,若温度过高会导
致产品TiO 产率降低,原因是
2
_____________________________________________________________________
。
②取少量酸洗后的H TiO ,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再
2 3
加H O 后出现微红色,说明H TiO 中存在的杂质离子是________。这种H TiO
2 2 2 3 2 3
即使用水充分洗涤,煅烧后获得的TiO 也会发黄,发黄的杂质是
2
_____________________________________________________________________(填化学式)。
解析 (1)制取TiCl 需要在无水无氧的环境中进行,实验中用N 排出装置内的空
4 2
气,干燥管A中盛有的试剂是为了除去空气中的O 和水蒸气。E中应盛有浓硫酸,
2
防止空气中的水蒸气进入装置,使TiCl 发生水解,反应前,先组装仪器、检查装
4
置的气密性,再装入药品。反应后,应先熄灭酒精灯,待装置冷却至室温,再停止
通入N 。D中的液态混合物为生成的TiCl 和挥发出的CCl ,由表中信息可知,二
2 4 4
者互溶但沸点相差较大,可采取分馏(或蒸馏)的方法予以分离。
(2)①钛铁矿中含有Fe O 、SiO 等杂质,用硫酸溶解时,溶液中生成Fe (SO ) ,则
2 3 2 2 4 3
钛液Ⅰ中含有TiOSO 、FeSO 和Fe (SO ) ,加入试剂A后,结晶、过滤得到的是
4 4 2 4 3
FeSO ·7H O,所以试剂A是铁粉,把Fe3+还原为Fe2+;由于TiOSO 容易水解,若
4 2 4
温度过高,则会有较多的TiOSO 水解为H TiO 沉淀,过滤后混入FeSO ·7H O中,
4 2 3 4 2
导致TiO 产率降低。②先加KSCN溶液无现象,加H O 后出现红色,说明存在
2 2 2
Fe2+;经加热后Fe2+被氧化为Fe O 而使产品发黄。
2 3
答案 (1)干燥管 浓硫酸 检验装置气密性 ②③①
分馏(或蒸馏) (2)①Fe 温度过高会导致TiOSO 提前水解,产生H TiO 沉淀
4 2 3
②Fe2+ Fe O
2 3