文档内容
素养说明:氯的氧化物、含氧酸及含氧酸盐是近几年高考实验探究新宠,通过对
含氯化合物的性质探究,能培养学生变化观念的核心素养。
1. 氯的常见氧化物的性质
(1)一氧化二氯
性质:是次氯酸的酸酐,溶于水产生不稳定的次氯酸并最终变为盐酸
外观与性状: 黄棕色气体,有刺激性气味。
制法:用新制备的黄色氧化汞与氯气反应可制得一氧化二氯:
2HgO+2Cl ===Cl O+HgCl ·HgO
2 2 2
同样也可以用氯气与潮湿的碳酸钠反应来制取:
2Na CO +H O+2Cl ===2NaCl+2NaHCO +Cl O
2 3 2 2 3 2
(2)二氧化氯
物理性质:是一种黄绿色到橙黄色的气体,极易溶于水。
制取:
Cl +2NaClO ===2ClO ↑+2NaCl
2 2 2
或:5NaClO +4HCl===4ClO ↑+5NaCl+2H O
2 2 2
用途:是一种广谱、高效的灭菌剂。
(3)Cl O 、Cl O 、Cl O 分别为HClO 、HClO 、HClO 的酸酐。
2 3 2 5 2 7 2 3 4
2.氯的含氧酸
(1)氯的含氧酸的种类
氯的含氧酸有:HClO(次氯酸)、HClO (亚氯酸)、HClO (氯酸)、HClO (高氯酸)。
2 3 4
(2)氯的含氧酸的性质
酸性:HClO >HClO >HClO >HClO
4 3 2
氧化性:HClO>HClO >HClO >HClO
2 3 4
3.氯的含氧酸盐
(1)NaClO (亚氯酸钠)
2
性质:黄绿色液体,呈碱性,是一种强氧化剂,遇酸放出ClO 气体。
2
用途:是一种高效氧化剂漂白剂。主要用于棉纺、亚麻、纸浆漂白、食品消毒、水处理、杀菌灭藻和鱼药制造。
(2)氯酸钾(KClO )
3
性质:是一种白色晶体,有毒,在冷水中溶解度较小,易溶于热水。是强氧化剂。
用途:可用作制造炸药,也可用来制造火柴、烟火。
[题型专练]
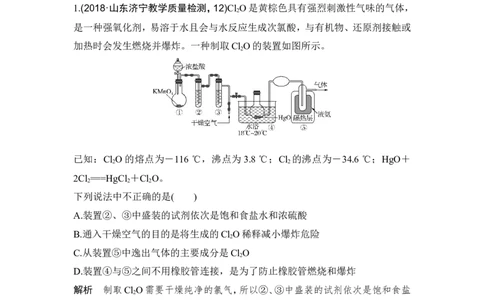
1.(2018·山东济宁教学质量检测,12)Cl O是黄棕色具有强烈刺激性气味的气体,
2
是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或
加热时会发生燃烧并爆炸。一种制取Cl O的装置如图所示。
2
已知:Cl O的熔点为-116 ℃,沸点为3.8 ℃;Cl 的沸点为-34.6 ℃;HgO+
2 2
2Cl ===HgCl +Cl O。
2 2 2
下列说法中不正确的是( )
A.装置②、③中盛装的试剂依次是饱和食盐水和浓硫酸
B.通入干燥空气的目的是将生成的Cl O稀释减小爆炸危险
2
C.从装置⑤中逸出气体的主要成分是Cl O
2
D.装置④与⑤之间不用橡胶管连接,是为了防止橡胶管燃烧和爆炸
解析 制取Cl O需要干燥纯净的氯气,所以②、③中盛装的试剂依次是饱和食盐
2
水和浓硫酸,A项正确;高浓度的Cl O易爆炸,所以通入干燥空气的目的是将生
2
成的Cl O稀释减小爆炸危险,B项正确;装置⑤是收集Cl O,所以温度低于3.8
2 2
℃,此时氯气是气体,逸出的气体主要是空气和剩余的Cl ,C项错误;Cl O与有
2 2
机物接触会发生燃烧并爆炸,装置④与⑤之间不用橡胶管连接,是为了防止橡胶
管燃烧和爆炸,D项正确。
答案 C
2.(重庆高考)ClO 与Cl 的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛
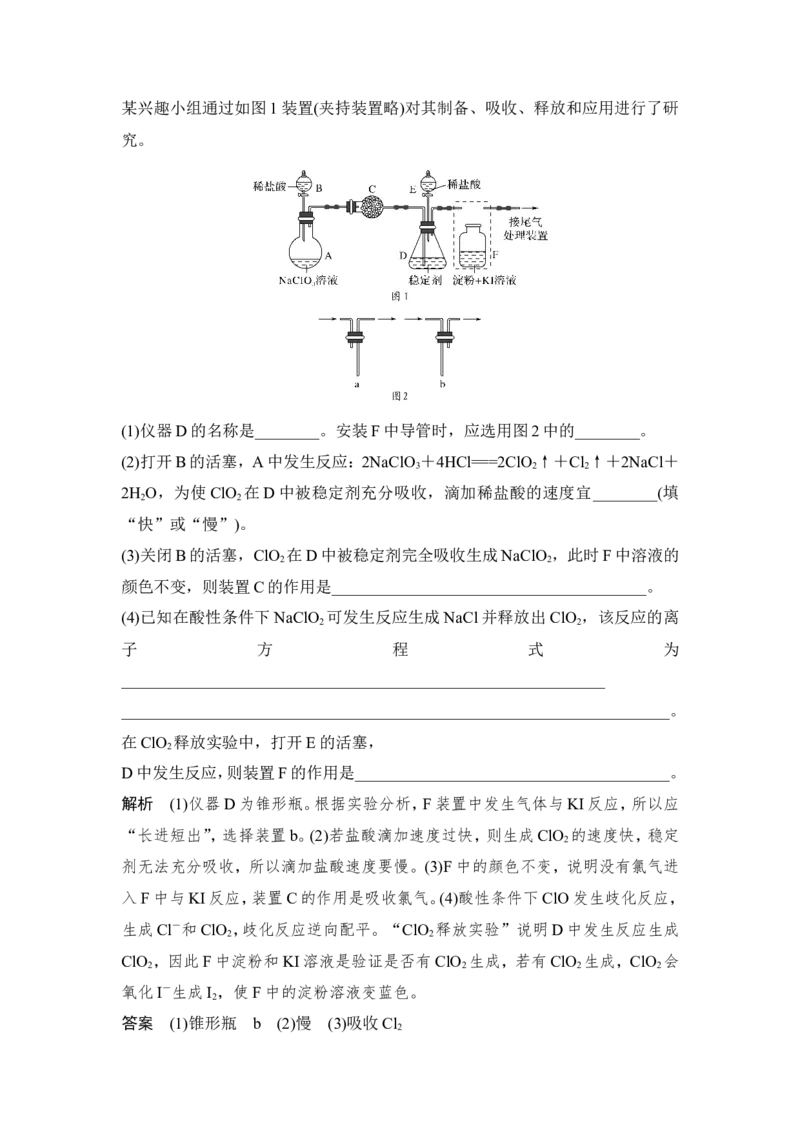
2 2某兴趣小组通过如图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研
究。
(1)仪器D的名称是________。安装F中导管时,应选用图2中的________。
(2)打开B的活塞,A中发生反应:2NaClO +4HCl===2ClO ↑+Cl ↑+2NaCl+
3 2 2
2H O,为使ClO 在D中被稳定剂充分吸收,滴加稀盐酸的速度宜________(填
2 2
“快”或“慢”)。
(3)关闭B的活塞,ClO 在D中被稳定剂完全吸收生成NaClO ,此时F中溶液的
2 2
颜色不变,则装置C的作用是_______________________________________。
(4)已知在酸性条件下NaClO 可发生反应生成NaCl并释放出ClO ,该反应的离
2 2
子 方 程 式 为
____________________________________________________________
____________________________________________________________________。
在ClO 释放实验中,打开E的活塞,
2
D中发生反应,则装置F的作用是_______________________________________。
解析 (1)仪器D为锥形瓶。根据实验分析,F装置中发生气体与KI反应,所以应
“长进短出”,选择装置b。(2)若盐酸滴加速度过快,则生成ClO 的速度快,稳定
2
剂无法充分吸收,所以滴加盐酸速度要慢。(3)F中的颜色不变,说明没有氯气进
入F中与KI反应,装置C的作用是吸收氯气。(4)酸性条件下ClO发生歧化反应,
生成Cl-和ClO ,歧化反应逆向配平。“ClO 释放实验”说明D中发生反应生成
2 2
ClO ,因此F中淀粉和KI溶液是验证是否有ClO 生成,若有ClO 生成,ClO 会
2 2 2 2
氧化I-生成I ,使F中的淀粉溶液变蓝色。
2
答案 (1)锥形瓶 b (2)慢 (3)吸收Cl
2(4)4H++5ClO===Cl-+4ClO ↑+2H O 验证是否有ClO 生成
2 2 2
3.(2016·新课标全国Ⅰ,28)NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物
2
等,其一种生产工艺如下:
回答下列问题:
(1)NaClO 中Cl的化合价为________。
2
(2) 写 出 “ 反 应 ” 步 骤 中 生 成 ClO 的 化 学 方 程 式
2
____________________________________________________________________
__________________________________________________________________。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入
的试剂分别为________、________。“电解”中阴极反应的主要产物是________。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO 。此吸收反应中,氧化剂与
2
还原剂的物质的量之比为________,该反应中氧化产物是________。
解析 本题工艺流程图典型、简明,解读流程图推知反应物和产物,根据氧化还
原化合价升降守恒进行配平:2NaClO +SO +H SO ===2ClO +2NaHSO 。该题
3 2 2 4 2 4
难点之一是判断出电解食盐水并加入ClO ,产物有NaClO 和Cl 生成,由于阴极
2 2 2
发生还原反应,所以应该是ClO 在阴极被还原生成NaClO ,难点之二是判断尾
2 2
气吸收过程中的氧化剂ClO 与还原剂H O ,无需配平氧化还原反应方程式,只
2 2 2
根据反应中得失电子守恒求得其比值为2∶1。
答案 (1)+3 (2)2NaClO +H SO +SO ===2NaHSO +2ClO (3)NaOH 溶液
3 2 4 2 4 2
Na CO 溶液 ClO(或NaClO ) (4)2∶1 O
2 3 2 2