文档内容
模板 04 电极反应式的书写及相关计算
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明·模板构建 答题模板 + 技巧点拨
技法01 电极反应式的书写方法 技法02 电化学的相关计算与分析
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
电化学知识是中学化学中的重要基本概念,也是近年来高考化学的持续热点,在复杂、陌生、新颖的
研究对象和真实问题情境下,体现了对电化学知识基础性、综合性、创新性和应用性的考查。近年高
考中对电化学的考查出现了新的变化,以装置图为载体来考查电化学的相关知识,成为近年高考的新
亮点,考查的关键能力侧重于两个方面:一是理解与辨析能力,要求学生能够从图示电化学装置中提
取有效信息,判断装置种类、辨别电极名称等;二是分析与推理能力,要求学生能够根据图示信息和
电解池的工作原理,分析电极反应的类型、电解质的作用、离子的移动方向以及定量分析转移电子的
物质的量等。
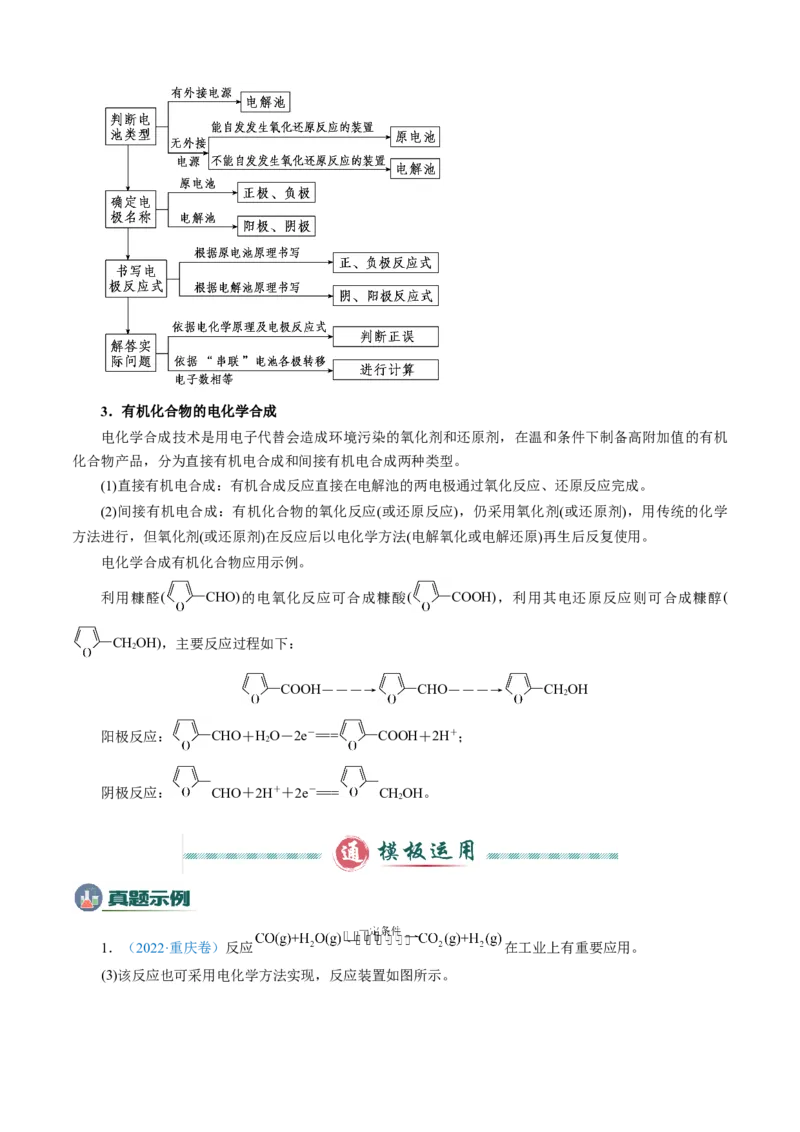
第一步 判断装置 阅读题目获取信息,抓住元素化合价的变化,分析电化学装置中的氧化还原
反应,准确判断装置是原电池还是电解池,结合发生的反应确定电极的名
称。
第二步 书写分析 根据电化学原理及装置所处的环境,书写电极反应式,分析电解液变化。
第三步 综合解答 题目要求,准确计算,规范解答。
技法01 电极反应式的书写方法1.二次电池的电极反应书写思维模型
以xMg+MoSMgMoS 为例说明
3 4 x 3 4
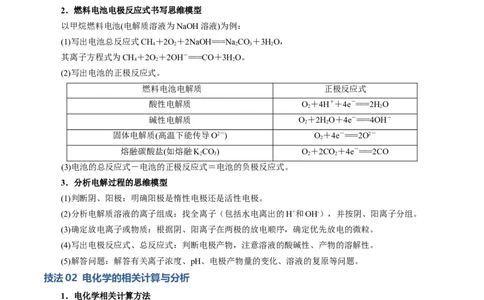
2.燃料电池电极反应式书写思维模型
以甲烷燃料电池(电解质溶液为NaOH溶液)为例:
(1)写出电池总反应式CH+2O+2NaOH===Na CO+3HO,
4 2 2 3 2
其离子方程式为CH+2O+2OH-===CO+3HO。
4 2 2
(2)写出电池的正极反应式。
燃料电池电解质 正极反应式
酸性电解质 O+4H++4e-===2H O
2 2
碱性电解质 O+2HO+4e-===4OH-
2 2
固体电解质(高温下能传导O2-) O+4e-===2O2-
2
熔融碳酸盐(如熔融KCO) O+2CO+4e-===2CO
2 3 2 2
(3)电池的总反应式-电池的正极反应式=电池的负极反应式。
3.分析电解过程的思维模型
(1)判断阴、阳极:明确阳极是惰性电极还是活性电极。
(2)分析电解质溶液的离子组成:找全离子(包括水电离出的H+和OH-),并按阴、阳离子分组。
(3)确定放电离子或物质:根据阴、阳离子在两极的放电顺序,确定优先放电的微粒。
(4)写出电极反应式、总反应式:判断电极产物,注意溶液的酸碱性、产物的溶解性。
(5)解答问题:解答有关离子浓度、pH、电极产物量的变化、溶液的复原等问题。
技法02 电化学的相关计算与分析
1.电化学相关计算方法
(1)用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电
子数相等。
(2)先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(3)根据得失电子守恒计算所需的关系式。
(M为金属,n为其阳离子所带电荷数)
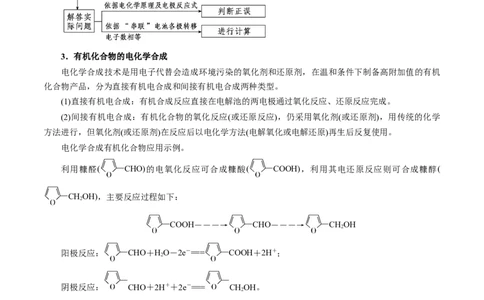
2.“串联”类装置的解题流程3.有机化合物的电化学合成
电化学合成技术是用电子代替会造成环境污染的氧化剂和还原剂,在温和条件下制备高附加值的有机
化合物产品,分为直接有机电合成和间接有机电合成两种类型。
(1)直接有机电合成:有机合成反应直接在电解池的两电极通过氧化反应、还原反应完成。
(2)间接有机电合成:有机化合物的氧化反应(或还原反应),仍采用氧化剂(或还原剂),用传统的化学
方法进行,但氧化剂(或还原剂)在反应后以电化学方法(电解氧化或电解还原)再生后反复使用。
电化学合成有机化合物应用示例。
利用糠醛( CHO)的电氧化反应可合成糠酸( COOH),利用其电还原反应则可合成糠醇(
CHOH),主要反应过程如下:
2
COOH―――→ CHO―――→ CHOH
2
阳极反应: CHO+HO-2e-=== COOH+2H+;
2
阴极反应: CHO+2H++2e-=== CHOH。
2
1.(2022·重庆卷)反应 在工业上有重要应用。
(3)该反应也可采用电化学方法实现,反应装置如图所示。①固体电解质采用 (填“氧离子导体”或“质子导体”)。
②阴极的电极反应式为 。
③同温同压下,相同时间内,若进口Ⅰ处n(CO):n(H O)=a:b,出口Ⅰ处气体体积为进口Ⅰ处的y倍,
2
则CO的转化率为 (用a,b,y表示)。
【答案】质子导体
【第一步 判断装置】该装置为电解池
【第二步 书写分析】
①电解时,CO和HO水从均从阳极口进入,阳极一氧化碳转化为二氧化碳,则氢气要在阴极产生,故阳
2
极产生二氧化碳的同时产生氢离子,氢离子通过固体电解质进入阴极附近得电子产生氢气,故固体电解质
应采用质子导体。
②电解时,阴极发生还原反应,电极反应式为: ;
【第三步 综合判断】
③根据三段式:
出口Ⅰ处气体为 体积为x,进口Ⅰ处的气体体积为 ,则 ,CO的转化率为:
。1. (2023·河北选考)氮是自然界重要元素之一,研究氮及其化合物的性质以及氮的循环利用对解决环
境和能源问题都具有重要意义。
(2)①以空气中的氮气为原料电解合成氨时,N 在 ________(填“阴”或“阳”)极上发生反应,产生
2
NH 。
3
②氨燃料电池和氢燃料电池产生相同电量时,理论上消耗 NH 和H 的质量比为17∶3,则在碱性介质
3 2
中氨燃料电池负极的电极反应式为 ________________________。
2.(2023·北京卷)(3)近年研究发现,电催化 和含氮物质( 等)在常温常压下合成尿素,有
助于实现碳中和及解决含氮废水污染问题。向一定浓度的 溶液通 至饱和,在电极上反应生成
,电解原理如图所示。
①电极 是电解池的__________极。
②电解过程中生成尿素的电极反应式是______________________。
1.一氯甲烷广泛用作溶剂、提取剂、推进剂、制冷剂、甲基化试剂,用于生产农药、医药等。
(2)甲醇也可通过电化学方法由甲烷直接制得,装置如右图所示:
已知,电解生成甲醇的过程分3步:
①通电时,氯离子先转化成高活性的原子氯(Cl·);②Cl·与吸附在电极上的 CH 反应生成 HCl和
4
CHCl;③在碱性电解液中,CHCl转化为目标产物CHOH。当步骤①有2 mol Cl·生成时,外电路中转移
3 3 3的电子数为 ________(用含N 的代数式表示)。阴极的电极反应为 _____________________________。
A
2.烯丙醇是生产甘油、医药、农药、香料和化妆品的中间体。(2)烯丙醇的电氧化过程有重要应用。
其在阳极放电时,同时存在三种电极反应(烯丙醇→丙烯酸、烯丙醇→丙烯醛、烯丙醇→丙二酸),各反应
决速步骤的活化能如下表所示。
反应 烯丙醇→丙烯酸 烯丙醇→丙烯醛 烯丙醇→丙二酸
活化能(单位:eV) 8.6a 2.5a 13.7a
①该条件下,相同时间内,阳极产物中含量最多的为 ________。
② 碱 性 条 件 下 , 烯 丙 醇 在 电 极 上 生 成 丙 烯 醛 (CH===CHCHO) 的 电 极 反 应 式 为
2
_____________________。
3.处理和利用CO是环境科学研究的热点课题。
(2)我国科学家成功实现了用电催化CO高选择性直接制备乙烯,该方法的工作原理如图所示。阴极材
料为优化的铜基催化剂。写出阴极的电极反应式: ________________________________________电解的总
反应化学方程式为 ________________________________________。
4.乙醇被广泛应用于能源、化工、食品等领域,工业上可用以下两种方法制备乙醇。
(3)研究发现,在酸性乙醇燃料电池中加入硝酸,可使电池持续大电流放电,工作原理如图。
①负极的电极反应式为 __________________________。
②当向正极通入1 mol O 且全部被消耗时,理论上正负极溶液质量变化的绝对值之差为 ________g(保
2
留两位小数)。
5.新能源的利用对实现“碳中和”也有重要意义。搭载钠离子电池的新能源汽车,动力充足、冬天
也无需频繁充电。第二代钠离子电池是以硬碳(C)为基底材料的嵌钠硬碳(NaC)和锰基高锰普鲁士白
y x y
NaMn[Mn(CN)]为电极的一种新型二次电池,在充放电过程中,Na+在两个电极之间往返嵌入和脱嵌。其
2 6
工作原理如图所示。(5)若用该钠离子电池给铅酸蓄电池充电,普鲁士白电极连接 ________(填“Pb”或“PbO ”)极,钠离子
2
电池负极的电极反应式为 ________。
6.我国科学家最近发明了一种Zn-PbO 电池,电解质为KSO 、HSO 和KOH,由a和b两种离子
2 2 4 2 4
交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下,回答下列问题:
(1)电池中,Zn为________极,B区域的电解质为______(填“KSO ”“HSO ”或“KOH”)
2 4 2 4
(2)电池反应的离子方程式为____________________________________________________
(3)阳离子交换膜为图中的________(填“a”或“b”)膜。
(4)此电池中,消耗6.5 g Zn,理论上可产生的容量(电量)为________毫安时(mAh)(1 mol电子的电量为1
F,1 F=96 500 C·mol-1,结果保留整数)
(5)已知E为电池电动势[电池电动势即电池的理论电压,是两个电极电位之差,E=E -E ],ΔG为
(+) (-)
电池反应的自由能变,则该电池与传统铅酸蓄电池相比较, _______ ; ____
(填“>”或“<”)
7.KIO 也可采用“电解法”制备,装置如图所示
3
(1)写出电解时阴极的电极反应式:_________________________________________。
(2)电解过程中通过阳离子交换膜的离子主要为________,其迁移方向是_______________。
8.有人设想以N 和H 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固
2 2
氮的新型燃料电池,装置如图所示,电池正极的电极反应式是____________________,A是________。9.利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质
NASICON(固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或“从b到a”),负极发生
的电极反应式为________________________。
10.含乙酸钠和对氯酚(ClOH)的废水可以利用微生物电池除去,其原理如图所示
①B是电池的________(填“正”或“负”)极
②A极的电极反应式为_______________________________。
11.新型固体燃料电池的电解质是固体氧化锆和氧化钇,高温下允许氧离子(O2-)在其间通过。如图所
示,其中多孔电极不参与电极反应
(1)该电池的负极反应式为_____________________________。
(2)如果用该电池作为电解装置,当有16 g甲醇发生反应时,则理论上提供的电量表达式为_________
(1个电子的电量为1.6×10-19C)。
12.以CH(g)为燃料可以设计甲烷燃料电池,该电池以稀HSO 作电解质溶液,其负极电极反应式为
4 2 4
_________________________________________,已知该电池的能量转换效率为86.4%,甲烷的燃烧热为-
890.3 kJ·mol-1,则该电池的比能量为______kW·h·kg-1[结果保留1位小数,比能量=,1 kW·h=3. 6×106
J]。
13.SO 、CO、CO 、NO 是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存
2 2 x环境的有效途径
(1)利用电化学原理将CO、SO 转化为重要化工原料,装置如图所示
2
①若A为CO,B为H,C为CHOH,则通入CO的为________(填“正”或“负”)极。
2 3
②若A为SO ,B为O,C为HSO ,则负极的电极反应式为________________________。
2 2 2 4
(2)碳酸盐燃料电池,以一定比例LiCO 和NaCO 低熔混合物为电解质,操作温度为650 ℃,在此温
2 3 2 3
度下以镍为催化剂,以煤气(CO、H 的体积比为1∶1)直接做燃料,其工作原理如图所示
2
①电池总反应为_______________________________。
②以此电源电解足量的硝酸银溶液,若阴极产物的质量为 21.6 g,电解后溶液体积为2 L,溶液的pH
约为___________。
(3)某研究小组利用下列装置用NO 生产新型硝化剂NO
2 4 2 5
①现以H 、O 、熔融盐NaCO 组成燃料电池,采用电解法制备 NO ,装置如图所示,其中 Y为
2 2 2 3 2 5
CO。在石墨(Ⅱ)电极上同时还引入CO 的目的是______________________________________________。
2 2
②电解过程中,生成NO 的电极反应式为______________________________________。
2 5
14.利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCr O 的总反应方程式为:
2 4 2 2 7
4NaCrO +4HO=====2NaCr O +4NaOH+2H↑+O↑。则NaCr O 在______(填“阴”或“阳”)极
2 4 2 2 2 7 2 2 2 2 7
室制得,电解时通过膜的离子主要为___________________。
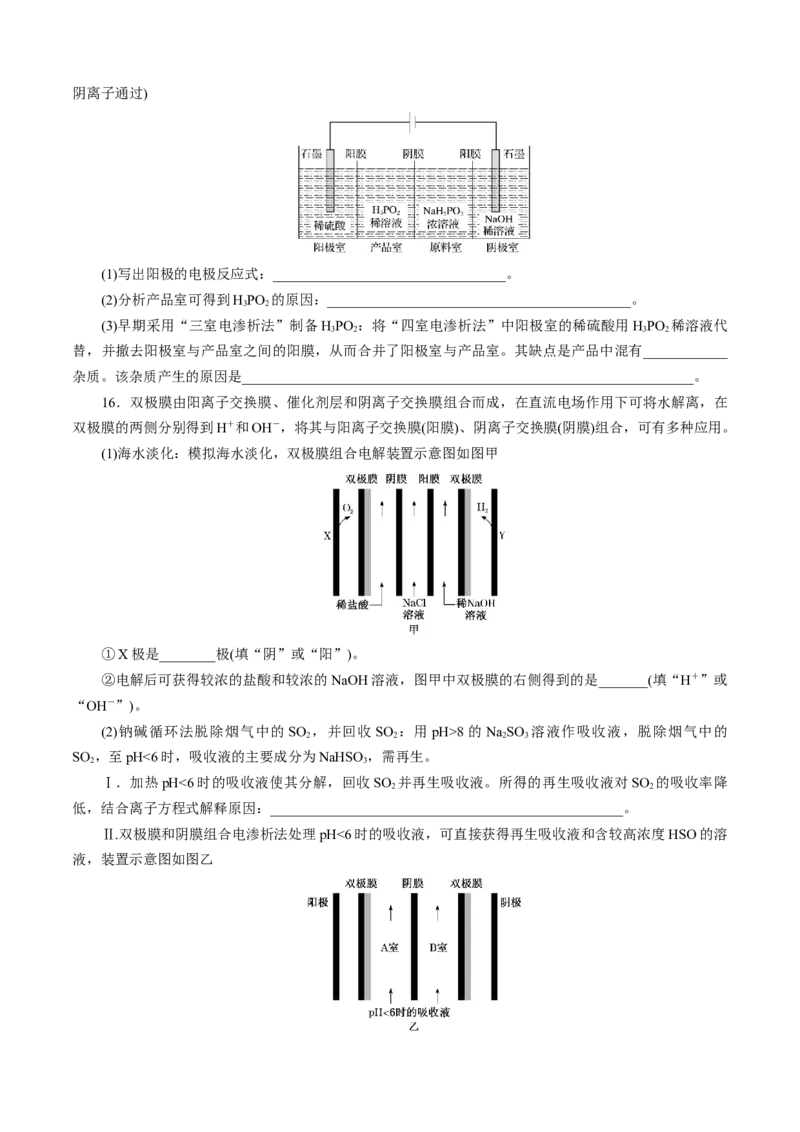
15.HPO 也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、
3 2阴离子通过)
(1)写出阳极的电极反应式:_________________________________。
(2)分析产品室可得到HPO 的原因:___________________________________________。
3 2
(3)早期采用“三室电渗析法”制备HPO :将“四室电渗析法”中阳极室的稀硫酸用HPO 稀溶液代
3 2 3 2
替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有____________
杂质。该杂质产生的原因是________________________________________________________________。
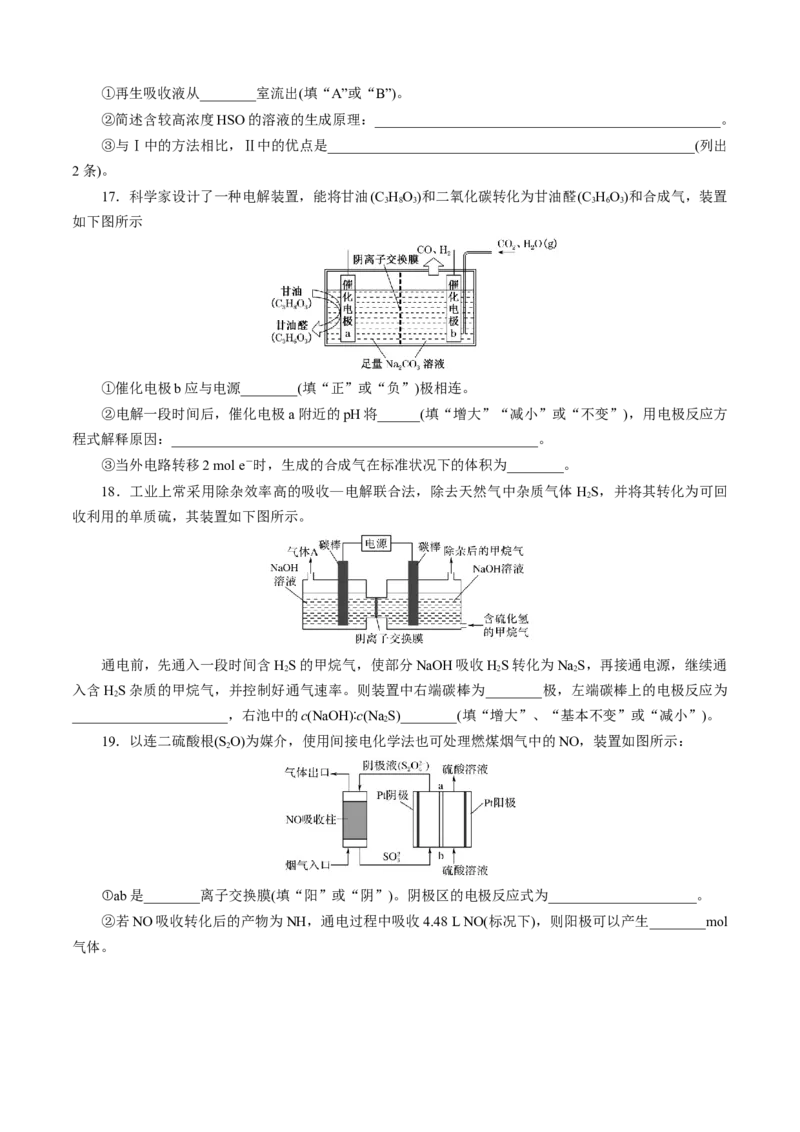
16.双极膜由阳离子交换膜、催化剂层和阴离子交换膜组合而成,在直流电场作用下可将水解离,在
双极膜的两侧分别得到H+和OH-,将其与阳离子交换膜(阳膜)、阴离子交换膜(阴膜)组合,可有多种应用。
(1)海水淡化:模拟海水淡化,双极膜组合电解装置示意图如图甲
①X极是________极(填“阴”或“阳”)。
②电解后可获得较浓的盐酸和较浓的NaOH溶液,图甲中双极膜的右侧得到的是_______(填“H+”或
“OH-”)。
(2)钠碱循环法脱除烟气中的 SO ,并回收SO :用pH>8的NaSO 溶液作吸收液,脱除烟气中的
2 2 2 3
SO ,至pH<6时,吸收液的主要成分为NaHSO,需再生。
2 3
Ⅰ.加热pH<6时的吸收液使其分解,回收SO 并再生吸收液。所得的再生吸收液对SO 的吸收率降
2 2
低,结合离子方程式解释原因:__________________________________________________。
Ⅱ.双极膜和阴膜组合电渗析法处理pH<6时的吸收液,可直接获得再生吸收液和含较高浓度HSO的溶
液,装置示意图如图乙①再生吸收液从________室流出(填“A”或“B”)。
②简述含较高浓度HSO的溶液的生成原理:_________________________________________________。
③与Ⅰ中的方法相比,Ⅱ中的优点是____________________________________________________(列出
2条)。
17.科学家设计了一种电解装置,能将甘油(C HO)和二氧化碳转化为甘油醛(C HO)和合成气,装置
3 8 3 3 6 3
如下图所示
①催化电极b应与电源________(填“正”或“负”)极相连。
②电解一段时间后,催化电极a附近的pH将______(填“增大”“减小”或“不变”),用电极反应方
程式解释原因:____________________________________________________。
③当外电路转移2 mol e-时,生成的合成气在标准状况下的体积为________。
18.工业上常采用除杂效率高的吸收—电解联合法,除去天然气中杂质气体HS,并将其转化为可回
2
收利用的单质硫,其装置如下图所示。
通电前,先通入一段时间含HS的甲烷气,使部分NaOH吸收HS转化为NaS,再接通电源,继续通
2 2 2
入含HS杂质的甲烷气,并控制好通气速率。则装置中右端碳棒为________极,左端碳棒上的电极反应为
2
______________________,右池中的c(NaOH)∶c(Na S)________(填“增大”、“基本不变”或“减小”)。
2
19.以连二硫酸根(S O)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
2
①ab是________离子交换膜(填“阳”或“阴”)。阴极区的电极反应式为_____________________。
②若NO吸收转化后的产物为NH,通电过程中吸收4.48 L NO(标况下),则阳极可以产生________mol
气体。