文档内容
2022-2023 学年第一学期期初六校联合调研考试
高二化学试卷
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Fe 56 S 32 Cl 35.5 Cu 64
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项符合题意。
1.生活中处处有化学,下列叙述正确的是
A.HB铅笔芯的成分为二氧化铅 B.碳酸氢钠可做食品膨松剂
C.青铜和黄铜是不同结构的单质铜 D.焰火中红色来源于钠盐灼烧
2.少量NaO 与HO反应生成HO 和NaOH。下列说法正确的是
2 2 2 2 2
A.NaO 的电子式为 B.HO分子中含非极性共价键
2 2 2
C.NaOH中只含离子键 D.HO 的结构式 H-O-O-H
2 2
3.下列有关物质的性质与用途具有对应关系的是
A.NH Cl溶液呈酸性,可用于除铁锈剂
4
B.SO 具有氧化性,可用作葡萄酒抗氧化剂
2
C.小苏打可以和碱反应,可用作抗酸药
D.FeCl 具有氧化性,可用作净水剂
3
4.四种短周期元素W、X、Y、Z的原子序数依次增大,W元素的最外层电子数是其电子
层数的二倍;X的原子半径是短周期主族元素原子中最大的;Y是地壳中含量最多的金属
元素;X与Z形成的离子化合物的水溶液呈中性。下列叙述中,不正确的是
A.W的非金属性小于Z的非金属性
B.将X单质投入到CuSO 溶液中,生成紫红色固体
4
C.工业上用电解熔融Y的氧化物的方法治炼金属Y
D.Z的最高价氧化物对应水化物为强酸
5.KMnO 溶液、NaClO溶液分别与浓盐酸混合反应都能生成Cl。下列制取、净化Cl、
4 2 2
验证其氧化性并进行尾气吸收的装置和原理能达到实验目的的是
A.制取Cl B.除去HCl C.验证Cl 氧化性 D.吸收尾气
2 2
阅读下列资料,完成6~8题: 硫酸是重要的化工原料。浓硫酸具有很强的氧化性,能
氧化大多数金属单质和部分非金属单质。金属冶炼时产生的含SO 废气经回收处理、催化
2
氧化、吸收后可制得硫酸。2SO (g)+O(g) 2SO (g) ΔH=-196.6kJ·mol-1。工业制硫酸尾
2 2 3
气中的SO 可用氨水吸收,吸收液经处理后释放出的SO 又可循环利用。
2 26.下列有关含硫物质的说法的说法正确的是
A.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
B.浓硫酸与铁在常温下不能反应,所以可用铁质容器贮运浓硫酸
C.芒硝、重晶石、黄铜矿都是硫酸盐
D.用石灰右-石膏法对燃煤烟气进行脱硫,同时可得到石膏
7.在指定条件下,下列选项所示的物质间转化能实现的是
Cu C
A.S CuS B.稀HSO (aq) SO (g)
△ 2 4 △ 2
Cu
C.浓HSO SO (g) D.SO (g) (NH )SO (aq)
2 4 2 2 4 2 3
8.对于反应2SO (g)+O(g) 2SO (g),下列说法正确的是
2 2 3
A.反应的ΔH < 0,ΔS >0
B.反应的平衡常数可表示为K=
C.使用催化剂能改变反应路径,降低反应的活化能
D.增大体系的压强能增大活化分子百分数,加快反应的速率
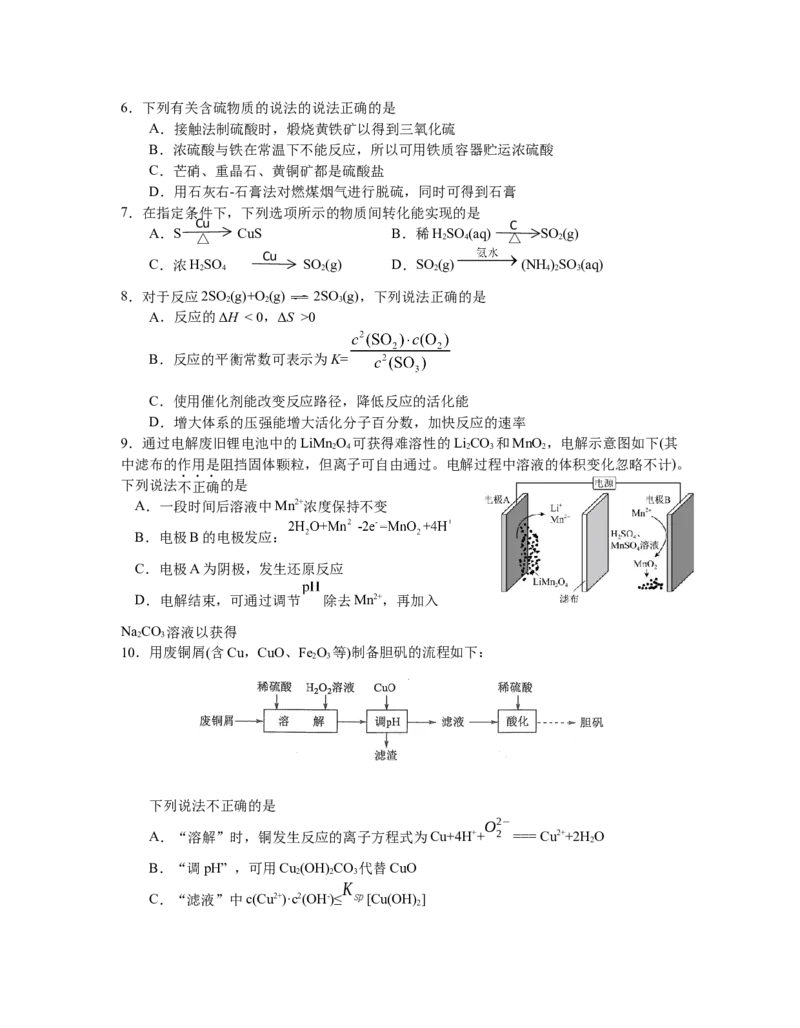
9.通过电解废旧锂电池中的LiMn O 可获得难溶性的LiCO 和MnO ,电解示意图如下(其
2 4 2 3 2
中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。
下列说法不正确的是
A.一段时间后溶液中Mn2+浓度保持不变
B.电极B的电极发应:
C.电极A为阴极,发生还原反应
D.电解结束,可通过调节 除去Mn2+,再加入
NaCO 溶液以获得
2 3
10.用废铜屑(含Cu,CuO、Fe O 等)制备胆矾的流程如下:
2 3
下列说法不正确的是
O2−
A.“溶解”时,铜发生反应的离子方程式为Cu+4H++ 2 === Cu2++2H O
2
B.“调pH” ,可用Cu (OH) CO 代替CuO
2 2 3
K
C.“滤液”中c(Cu2+)·c2(OH-)≤ sp[Cu(OH) ]
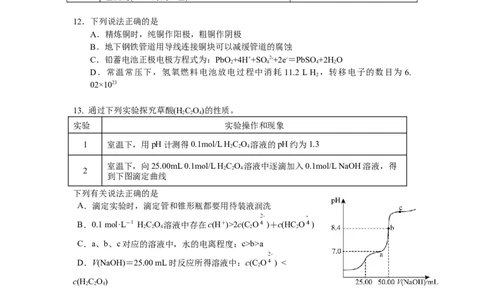
2D.“酸化”时,加入稀硫酸的目的是抑制Cu2+的水解11.根据下列实验操作和现象所得出的结论正确的是
选项 实验操作和现象 结论
相同条件下,分别测量0.1 mol/L和0.01 mol/L醋
A 醋酸浓度越大,电离程度越大
酸溶液的导电性,前者的导电性强
常温下,分别测定浓度均为0.1mol/L NaF和
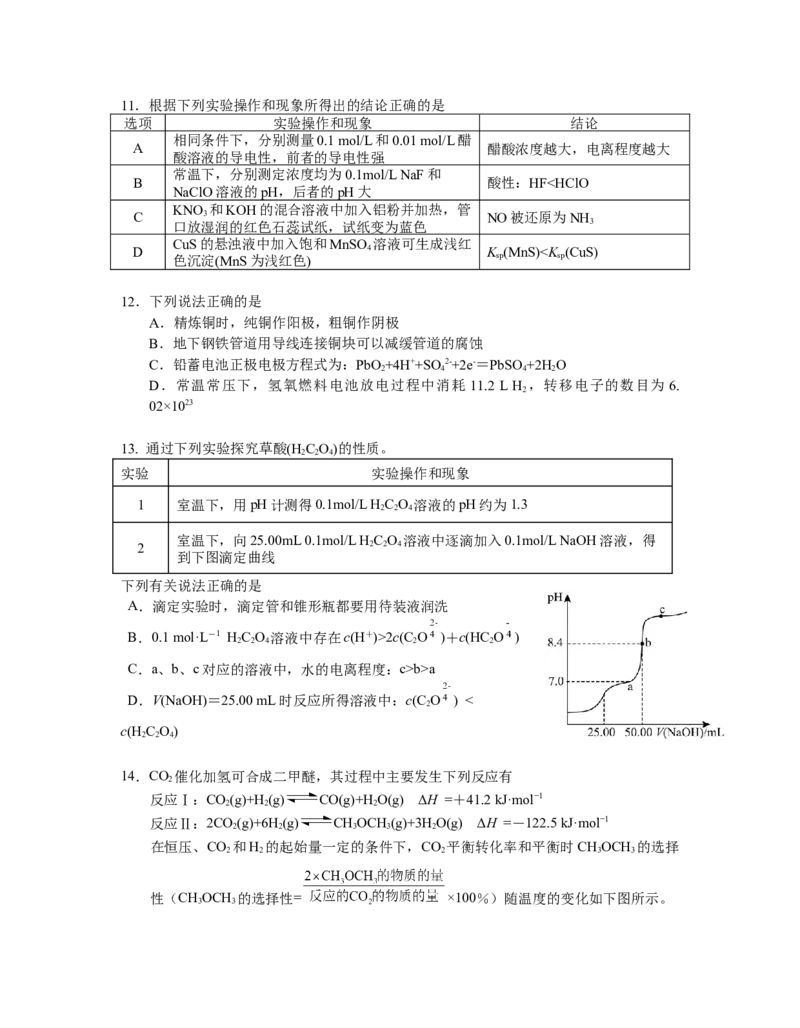
B 酸性:HF2c(C O )+c(HC O )
2 2 4 2 2
C.a、b、c对应的溶液中,水的电离程度:c>b>a
D.V(NaOH)=25.00 mL时反应所得溶液中:c(C O ) <
2
c(H C O)
2 2 4
14.CO 催化加氢可合成二甲醚,其过程中主要发生下列反应有
2
反应Ⅰ:CO(g)+H(g) CO(g)+HO(g) ΔH =+41.2 kJ·mol−1
2 2 2
反应Ⅱ:2CO(g)+6H(g) CHOCH (g)+3HO(g) ΔH =-122.5 kJ·mol−1
2 2 3 3 2
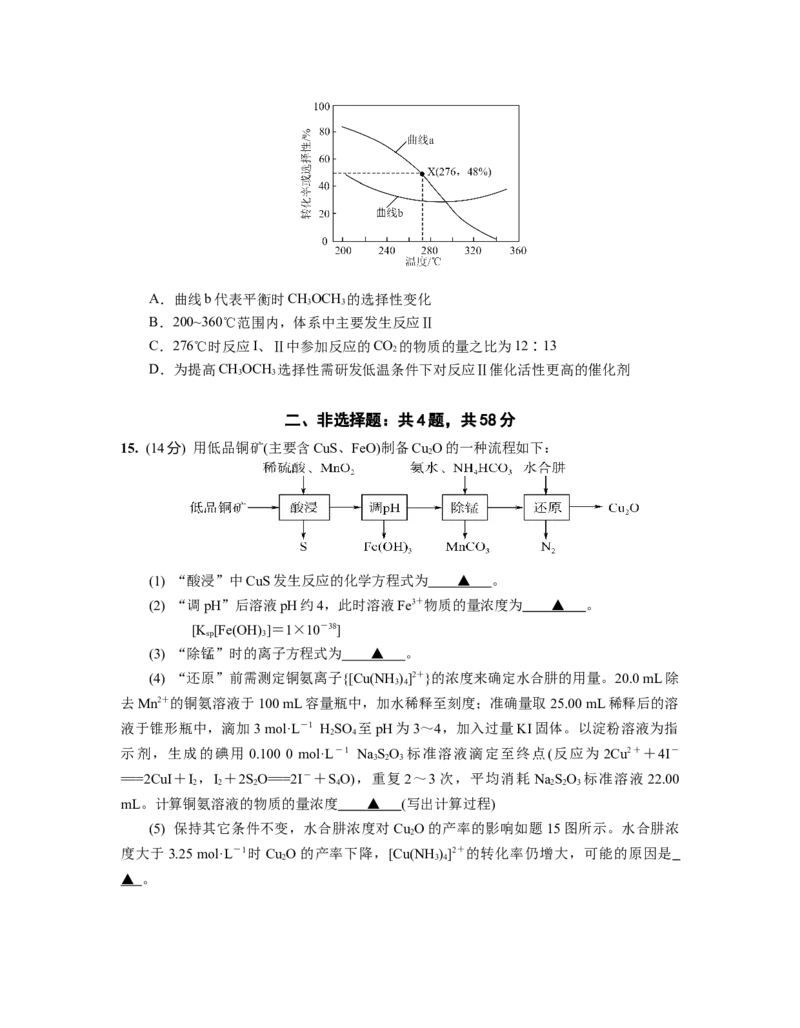
在恒压、CO 和H 的起始量一定的条件下,CO 平衡转化率和平衡时CHOCH 的选择
2 2 2 3 3
性(CHOCH 的选择性= ×100%)随温度的变化如下图所示。
3 3下列说法正确的是A.曲线b代表平衡时CHOCH 的选择性变化
3 3
B.200~360℃范围内,体系中主要发生反应Ⅱ
C.276℃时反应I、Ⅱ中参加反应的CO 的物质的量之比为12∶13
2
D.为提高CHOCH 选择性需研发低温条件下对反应Ⅱ催化活性更高的催化剂
3 3
二、非选择题:共4题,共58分
15. (14分) 用低品铜矿(主要含CuS、FeO)制备Cu O的一种流程如下:
2
(1) “酸浸”中CuS发生反应的化学方程式为 ▲ 。
(2) “调pH”后溶液pH约4,此时溶液Fe3+物质的量浓度为 ▲ 。
[K [Fe(OH) ]=1×10-38]
sp 3
(3) “除锰”时的离子方程式为 ▲ 。
(4) “还原”前需测定铜氨离子{[Cu(NH )]2+}的浓度来确定水合肼的用量。20.0 mL除
3 4
去Mn2+的铜氨溶液于100 mL容量瓶中,加水稀释至刻度;准确量取25.00 mL稀释后的溶
液于锥形瓶中,滴加3 mol·L-1 HSO 至pH为3~4,加入过量KI固体。以淀粉溶液为指
2 4
示剂,生成的碘用 0.100 0 mol·L-1 Na SO 标准溶液滴定至终点(反应为 2Cu2++4I-
3 2 3
===2CuI+I ,I +2SO===2I-+SO),重复2~3次,平均消耗 NaSO 标准溶液 22.00
2 2 2 4 2 2 3
mL。计算铜氨溶液的物质的量浓度 ▲ (写出计算过程)
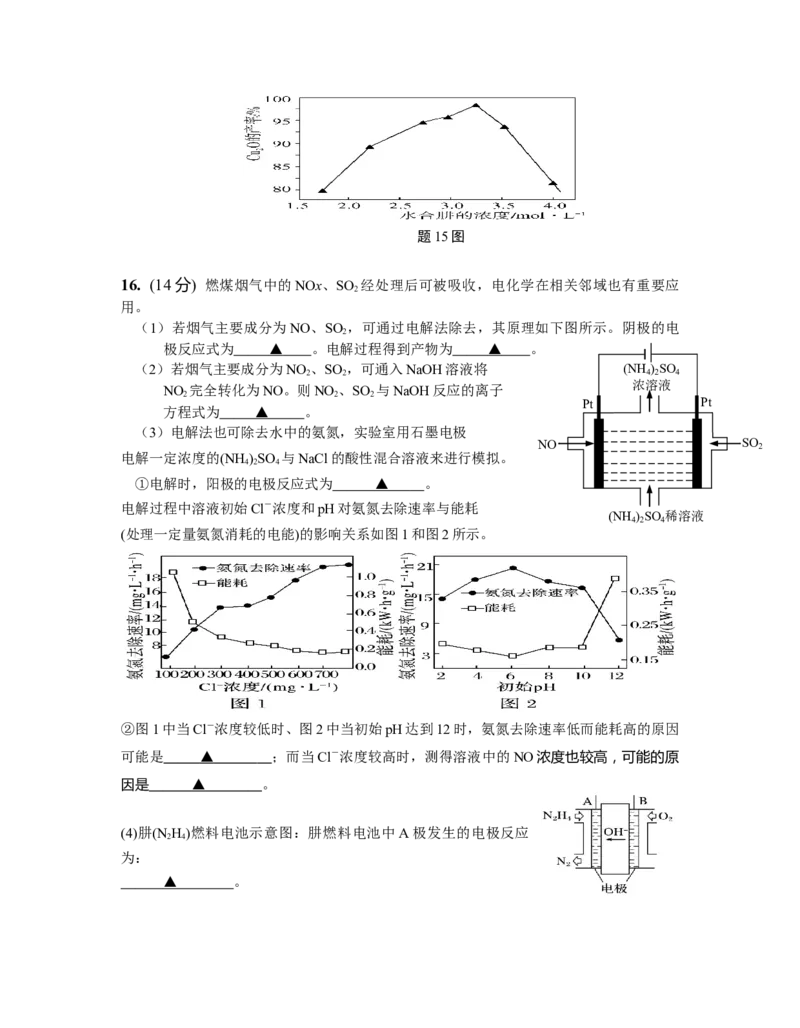
(5) 保持其它条件不变,水合肼浓度对Cu O的产率的影响如题15图所示。水合肼浓
2
度大于3.25 mol·L-1时Cu O的产率下降,[Cu(NH )]2+的转化率仍增大,可能的原因是
2 3 4
▲ 。题15图
16. (14分) 燃煤烟气中的NOx、SO 经处理后可被吸收,电化学在相关邻域也有重要应
2
用。
(1)若烟气主要成分为NO、SO ,可通过电解法除去,其原理如下图所示。阴极的电
2
极反应式为 ▲ 。电解过程得到产物为 ▲ 。
(2)若烟气主要成分为NO、SO,可通入NaOH溶液将 (NH ) SO
2 2 4 2 4
浓溶液
NO 完全转化为NO。则NO、SO 与NaOH反应的离子
2 2 2
Pt Pt
方程式为 ▲ 。
(3)电解法也可除去水中的氨氮,实验室用石墨电极
NO SO 2
电解一定浓度的(NH )SO 与NaCl的酸性混合溶液来进行模拟。
4 2 4
①电解时,阳极的电极反应式为 ▲ 。
电解过程中溶液初始Cl-浓度和pH对氨氮去除速率与能耗
(NH ) SO 稀溶液
4 2 4
(处理一定量氨氮消耗的电能)的影响关系如图1和图2所示。
②图1中当Cl-浓度较低时、图2中当初始pH达到12时,氨氮去除速率低而能耗高的原因
可能是 ▲ ;而当Cl-浓度较高时,测得溶液中的NO浓度也较高,可能的原
因是 ▲ 。
(4)肼(N H)燃料电池示意图:肼燃料电池中A极发生的电极反应
2 4
为:
▲ 。17. (16分) 以硫铁矿(主要成分是FeS ,含少量Al O 、SiO 和Fe O)为原料制备磷酸铁
2 2 3 2 3 4
(FePO )。
4
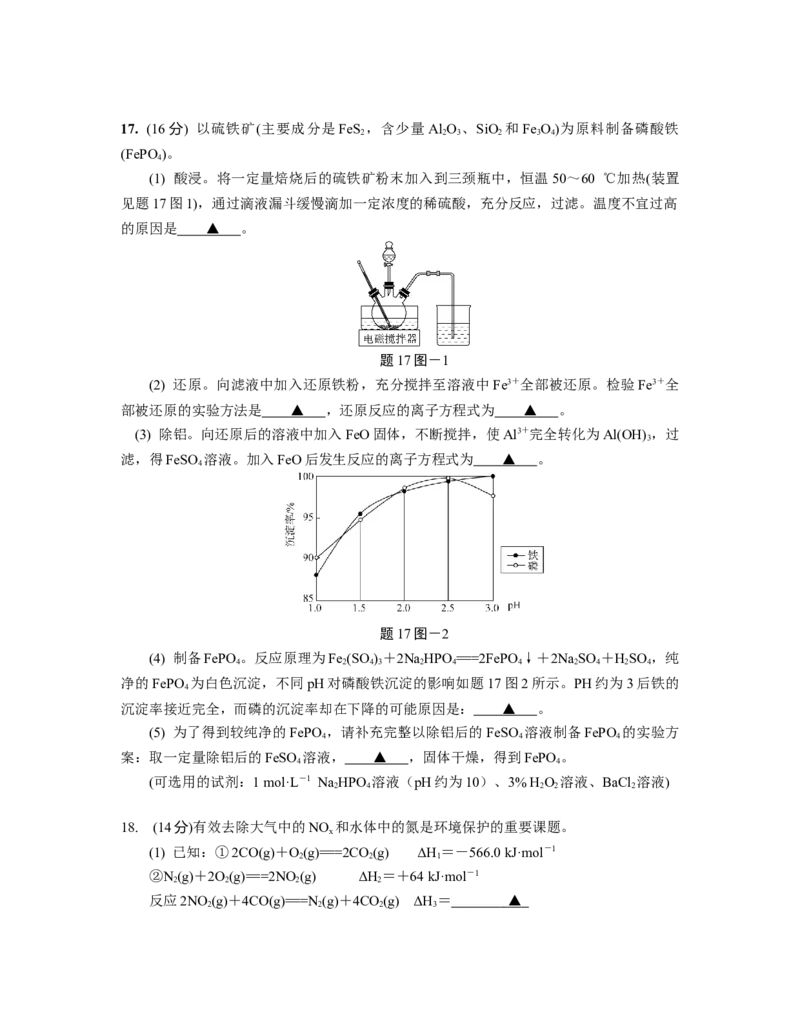
(1) 酸浸。将一定量焙烧后的硫铁矿粉末加入到三颈瓶中,恒温50~60 ℃加热(装置
见题17图1),通过滴液漏斗缓慢滴加一定浓度的稀硫酸,充分反应,过滤。温度不宜过高
的原因是 ▲ 。
题17图-1
(2) 还原。向滤液中加入还原铁粉,充分搅拌至溶液中Fe3+全部被还原。检验Fe3+全
部被还原的实验方法是 ▲ ,还原反应的离子方程式为 ▲ 。
(3) 除铝。向还原后的溶液中加入FeO固体,不断搅拌,使Al3+完全转化为Al(OH) ,过
3
滤,得FeSO 溶液。加入FeO后发生反应的离子方程式为 ▲ 。
4
题17图-2
(4) 制备FePO 。反应原理为Fe (SO ) +2NaHPO ===2FePO↓+2NaSO +HSO ,纯
4 2 4 3 2 4 4 2 4 2 4
净的FePO 为白色沉淀,不同pH对磷酸铁沉淀的影响如题17图2所示。PH约为3后铁的
4
沉淀率接近完全,而磷的沉淀率却在下降的可能原因是: ▲ 。
(5) 为了得到较纯净的FePO ,请补充完整以除铝后的FeSO 溶液制备FePO 的实验方
4 4 4
案:取一定量除铝后的FeSO 溶液, ▲ ,固体干燥,得到FePO 。
4 4
(可选用的试剂:1 mol·L-1 Na HPO 溶液(pH约为10)、3% H O 溶液、BaCl 溶液)
2 4 2 2 2
18. (14分)有效去除大气中的NO 和水体中的氮是环境保护的重要课题。
x
(1) 已知:①2CO(g)+O(g)===2CO (g) ΔH=-566.0 kJ·mol-1
2 2 1
②N(g)+2O(g)===2NO(g) ΔH=+64 kJ·mol-1
2 2 2 2
反应2NO (g)+4CO(g)===N (g)+4CO(g) ΔH = ▲
2 2 2 3(2) 磷酸铵镁(MgNHPO )沉淀法可去除水体中的氨氮(NH和NH )
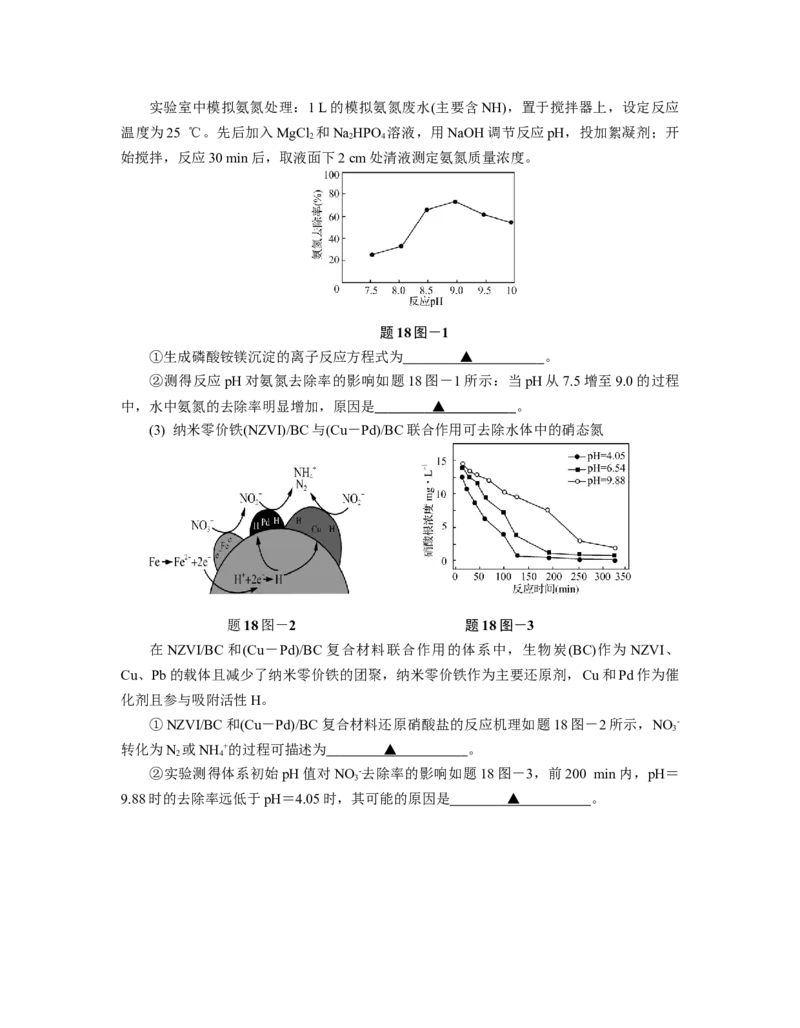
4 4 3实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含NH),置于搅拌器上,设定反应
温度为25 ℃。先后加入MgCl 和NaHPO 溶液,用NaOH调节反应pH,投加絮凝剂;开
2 2 4
始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。
题18图-1
①生成磷酸铵镁沉淀的离子反应方程式为 ▲ 。
②测得反应pH对氨氮去除率的影响如题18图-1所示:当pH从7.5增至9.0的过程
中,水中氨氮的去除率明显增加,原因是 ▲ 。
(3) 纳米零价铁(NZVI)/BC与(Cu-Pd)/BC联合作用可去除水体中的硝态氮
题18图-2 题18图-3
在NZVI/BC和(Cu-Pd)/BC复合材料联合作用的体系中,生物炭(BC)作为NZVI、
Cu、Pb的载体且减少了纳米零价铁的团聚,纳米零价铁作为主要还原剂,Cu和Pd作为催
化剂且参与吸附活性H。
①NZVI/BC和(Cu-Pd)/BC复合材料还原硝酸盐的反应机理如题18图-2所示,NO -
3
转化为N 或NH +的过程可描述为 ▲ 。
2 4
②实验测得体系初始pH值对NO -去除率的影响如题18图-3,前200 min内,pH=
3
9.88时的去除率远低于pH=4.05时,其可能的原因是 ▲ 。2022-2023 学年第一学期期初六校联合调研考试
高二化学参考答案
一、单项选择题:共14题,每题3分,共42分。
1、B 2、D 3、A 4、B 5、C 6、D 7、D 8、C 9、A 10、A 11、C 12、C
13、B 14、D
说明:方程式物质正确未配平扣1分。
二、非选择题:共4题,共58分
15. (14分)
(1) CuS+MnO +2HSO ===CuSO+MnSO +S+2HO (3分)
2 2 4 4 4 2
(2)1×10-8 mol·L-1 (2分)
(3) Mn2++NH ·H O+HCO===MnCO↓+NH+HO (3分)
3 2 3 2
(4) 根据反应关系式为2Cu2+~I~2SO
2 2
n(Cu2+)=n(Na SO)=0.100 0 mol·L-1×22.00 mL×10-3=2.200×10-3 mol(1分)
2 2 3
则铜氨离子的物质的量为2.200×10-3 mol(1分)
c(铜氨离子)=2.200×10-3 mo×4÷0.02L=0.440 0 mol·L-1(2分)
(5) Cu O被NH·H O进一步还原成铜单质(2分)
2 2 4 2
16.(14分,每空2分)
(1)NO+5e-+6H+=NH++HO (NH)SO HSO (对一个给1分,错不给分)
4 2 4 2 4 2 4
(2)2NO+SO+4OH-=2NO ﹣+SO2-+2H O
2 2 2 4 2
(3)①2Cl--2e-===Cl↑
2
②阳极可能OH-放电,产生大量氧气,消耗电能
Cl-浓度较高时,产生的Cl(或HClO)较多,会将NH氧化为NO
2
(4) NH-4e-+4OH-===N+4HO
2 4 2 2
17. (16分)
(1) 避免Fe3+水解生成Fe(OH) ,损失铁元素(2分)
3
(2) 取少许溶液于试管中,滴入少许KSCN溶液,若溶液不变红色,则Fe3+全部被还原。
(3分,取样1分,试剂1分,现象与结论1分) 2Fe3++Fe=3Fe2+ (2分)
(3) 2Al3++3FeO+3HO===2Al(OH) +3Fe2+(2分,分步写酌情给分)
2 3
(4) PH大于2.5后,FePO 沉淀会转化为Fe(OH) 沉淀, 释放PO 3- (2分)(“FePO 沉淀会
4 3 4 4
转化为Fe(OH) 沉淀”1分,“释放PO 3-”1分)
3 4
(5) (5分)加入足量的3%双氧水溶液,充分反应,使FeSO 溶液全部被氧化为Fe (SO )
4 2 4 3溶液,(1分)边搅拌边将1 mol·L-1NaHPO 溶液缓慢加入到Fe (SO ) 溶液中,(1分)至溶
2 4 2 4 3
液的pH约为2.5,(1分)过滤,(1分)洗涤至最后一次洗涤液加入BaCl 溶液无沉淀出
2
现(1分)
18. (14分)
(1) -1196 kJ·mol-1(2分)
(2) ①Mg2++OH-+NH+HPO===MgNH PO ↓+HO(3分)
4 4 2
(反应物、产物正确2分,配平、符号共1分)
②随着pH的增大,HPO转化为PO,c(PO)浓度增大,使得生成沉淀的反应速率加快,
氨氮去除率增加(3分) (答“HPO转化为PO,c(PO)浓度增大”得2分,“使得
生成沉淀的反应速率加快”1分)
(3) ①NO在铁表面得到电子被还原为 NO,NO被吸附在Cu和Pd表面的活性H继续
还原为N 或NH(3分)(答到1点得1分,答全2点得3分)
2
②酸性越强,Fe越易失去电子,NO越易得到电子被还原;酸性越强,H+浓度大,可
以减少表面氢氧化物的形成,从而可以暴露更多的反应活性位点,促进反应的进行。
(3分)(“酸性越强,Fe越易失去电子,NO越易得到电子被还原”1分;“减少表面
氢氧化物的形成,从而可以暴露更多的反应活性位点,促进反应的进行”2分)