文档内容
六校联合体 2023 届高三 8 月联合调研
化学试题
考试时间:75分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 O-16 Co-59
一.选择题:共13题,每题3 分,共计39分。每题只有一个选项最符合题意。
1.中国人民在悠久的历史中创造了绚丽多彩的中华文化,下列说法不正确的是
A.宋▪王希孟《千里江山图》卷中的绿色颜料铜绿的主要成分是碱式碳酸铜
B. “冰糖葫芦”是一种传统美食,山楂外面包裹的“糖衣”的主要成分是麦芽糖
C. “澄泥砚”是一种传统工艺品,是用胶泥烧制而成,其主要成分为硅酸盐
D.“蜀绣”是用蚕丝线在丝绸或其他织物上绣出图案的工艺,蚕丝的主要成分蛋白质
2.双氧水和“84”消毒液两者混合时可发生反应:NaClO+H O =NaCl+H O+O ↑。下列有关
2 2 2 2
说法不正确的是
A. Na O 中含有非极性共价键 B. NaClO 的电子式为
2 2
C. H O 中O元素的化合价为-1 D. H O的空间构型为直线形
2 2 2
3.短周期元素X、Y、Z、M的原子序数依次增大,他们组成一种团簇分子,结构如图所示。X、M
的族序数等于周期数,Y是地壳中最丰富、分布最广的元素,Z原子最外层电子数为2。下列说
法不正确的是
A.该团簇分子的分子式为 X Z M Y B.简单离子半径:Y>M
2 2 2 6
C.工业上常电解熔融的ZY制取Z单质 D.第一电离能: M<Z
4. 若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列
分析正确的是
A. Cu与浓硫酸反应,只体现H SO 的酸性
2 4
B. a处变红,说明SO 是酸性氧化物
2
C. b或c处褪色,均说明SO 具有漂白性
2
D. 试管底部出现白色固体,说明反应中无H O生成
2
阅读下列材料,完成5~7题:
周期表中ⅦA族中氯元素及其化合物在生产、生活中有着广泛的应用。盐酸工业用途广泛,
稀盐酸和稀氢氧化钠溶液反应的中和热为57.3kJ/mol;氯化镁,通常含有六个分子的结晶水,
即MgCl ·6H O,易潮解,置于干燥空气中会风化而失去结晶水,若在空气中加热MgCl ·6H O,
2 2 2 2
生成的是Mg(OH)Cl或MgO。次氯酸钠与二氧化碳反应产生的次氯酸是漂白剂的有效成分。氯仿(CHCl )常因保存不慎而被氧化,产生剧毒物光气(COCl )
3 2
5. 下列说法正确的是
A. CHCl 、COCl 分子中所有原子的最外层电子都满足8电子稳定结构
3 2
B. COCl 、CO 都是由极性键构成的非极性分子
2 2
C. 氯原子基态核外电子排布式为3s23p5
D. ⅦA族元素单质的晶体类型相同,沸点:HF>HCl
6. 下列化学反应表示正确的是
A. 在空气中加热MgCl ·6H O:MgCl ·6H O=Mg(OH)Cl+HCl↑+5H O↑
2 2 2 2 2
B. 过量SO 通入NaClO溶液中:SO +H O +ClO-=HClO + HSO -
2 2 2 3
C. 用惰性电极电解饱和MgCl 溶液:2C1-+2H O Cl ↑+H ↑+2OH-
2 2 2 2
D. 稀硫酸与稀氢氧化钾溶液发生反应:
H SO (l) + 2KOH(l) = K SO (l) + 2H O(l) △H=﹣57.3kJ/mol
2 4 2 4 2
7. 下列有关物质的性质与用途具有对应关系的是
A. NaCl易溶于水,可用于工业电解制备钠
B. FeCl 溶液具有酸性,可用于腐蚀印刷电路板上的Cu
3
C.次氯酸(盐)具有不稳定性,可作杀菌消毒剂,还可作漂白剂
D.氨气具有还原性,用浓氨水检验氯气管道是否泄漏
8. 工业上以 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法不正确的是
3
已知:NaHSO 溶液呈弱酸性
3
A.工业上用黄铁矿(FeS ,其中硫元素为-1价)在高温下和氧气反应制备SO
2 2
B.结晶后母液中含有NaHCO
3
C.中和后溶液中含Na SO 和NaHCO
2 3 3
D.侯氏制碱法以H O、NH 、CO 、NaCl为原料制备NaHCO 和NH Cl
2 3 2 3 4
9.莽草酸(a)是抗病毒和抗癌药物中间体,其官能团修饰过程如图所示,下列说法不正确 的
是A.“M”为甲醇
B.有机物b存在顺反异构
C.等物质的量的a和b分别与足量的NaOH溶液反应,消耗NaOH的量不同
D.有机物a、b、c分子中均含有3个手性碳原子
10.随着人们环保意识的增强,燃油汽车都已经装上了尾气处理装置。汽车尾气在催化剂作用
下可发生如下反应:,下列说法不正确的是
A. 该反应能自发进行,△H﹤0
B. 反应的平衡常数表达式为
C. 反应中每消耗1mol NO转移电子的数目约等于
D. 实际应用中,加入高效催化剂的量越多,燃油汽车排放的尾气对空气污染程度越小
11.室温下进行下列实验,根据实验操作和现象所得到的结论不正确的是
选项 实验操作和现象 实验目的或结论
A 向PbO 中滴加浓盐酸,出现黄绿色气体 PbO 具有氧化性
2 2
向溶有SO 的BaCl 溶液中通入气体X,出现白色
B 2 2 气体X一定具有强氧化性
沉淀
向FeSO 溶液中先加入KSCN溶液,无现象,再加
C 4 Fe2+具有还原性
入HO 溶液,溶液变成血红色
2 2
向KI溶液中滴加几滴NaNO 溶液,再滴加淀粉溶
D 2 NO的氧化性比I 的强
液后变蓝色 2
12. 室温下,通过下列实验探究0.010 0 mol·L-1 Na C O 溶液的性质。
2 2 4
实验1:实验测得0.010 0 mol·L-1 Na C O 溶液pH为8.6。
2 2 4
实验2:向溶液中滴加等体积0.010 0 mol·L-1 HCl溶液,pH由8.6降为4.8。
实验3:向溶液中加入等体积0.020 0 mol·L-1 CaCl 溶液,出现白色沉淀。
2
实验4:向稀硫酸酸化的KMnO 溶液中滴加NaC O 溶液至溶液褪色。
4 2 2 4
已知室温时K (CaC O)=2.5×10-9,下列说法正确的是
sp 2 4
A. 0.010 0 mol·L-1 Na C O 溶液中满足:.>2
2 2 4
B. 实验2滴加盐酸过程中某一点不能满足:c(Na+)=c(HC O)+2c(C O)+c(Cl-)
2 2
C. 实验3所得上层清液中c(C O)=2.5×10-7 mol·L-1
2
D. 实验4发生反应的离子方程式为C O+4MnO+12H+===2CO ↑+4Mn2++6HO
2 2 2
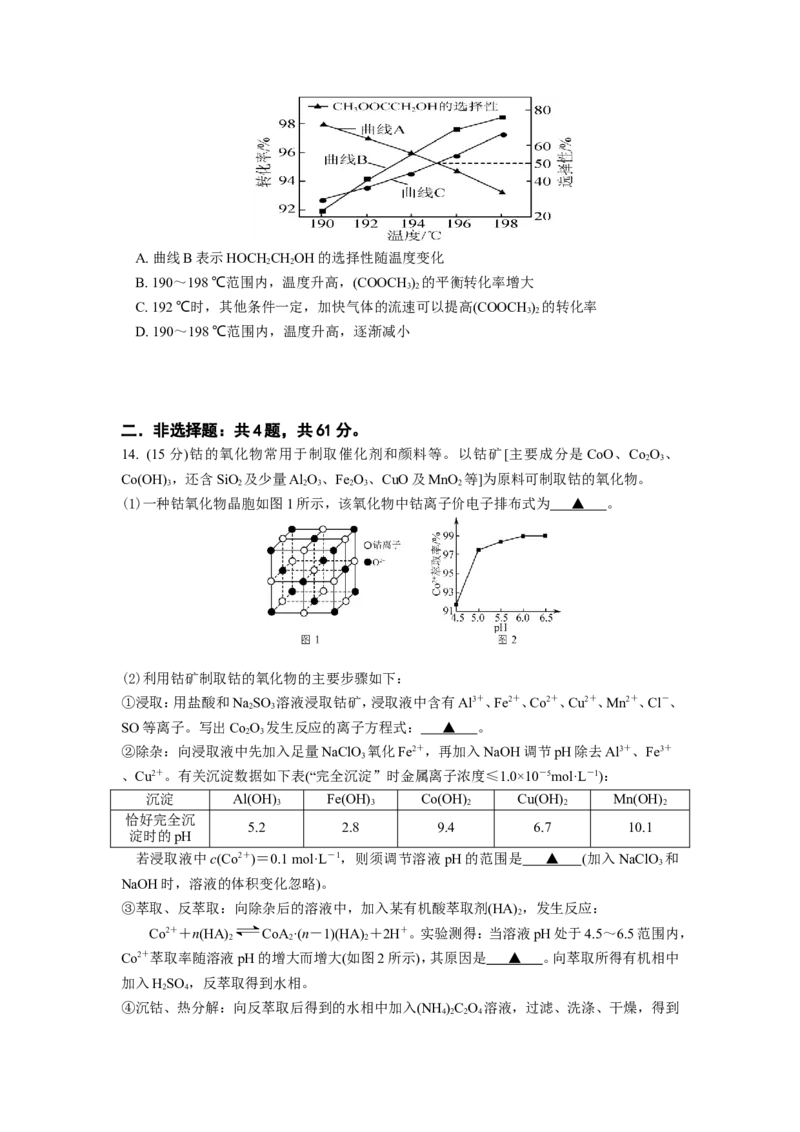
13. 草酸二甲酯[(COOCH)]催化加氢制乙二醇的反应体系中,发生的主要反应如下:
3 2
反应Ⅰ: (COOCH )(g)+2H(g) CHOOCCH OH(g)+CHOH(g);ΔH<0
3 2 2 3 2 3 1
反应Ⅱ: (COOCH )(g)+4H(g) HOCH CHOH(g)+2CHOH(g);ΔH<0
3 2 2 2 2 3 2
压强一定的条件下,将(COOCH )、H 按一定比例、流速通过装有催化剂的反应管,测得
3 2 2
(COOCH ) 的转化率及CHOOCCH OH、HOCH CHOH的选择性
3 2 3 2 2 2
{×100%}与温度的关系如图所示。下列说法正确的是A. 曲线B表示HOCH CHOH的选择性随温度变化
2 2
B. 190~198 ℃范围内,温度升高,(COOCH ) 的平衡转化率增大
3 2
C. 192 ℃时,其他条件一定,加快气体的流速可以提高(COOCH ) 的转化率
3 2
D. 190~198 ℃范围内,温度升高,逐渐减小
二.非选择题:共4题,共61分。
14. (15分)钴的氧化物常用于制取催化剂和颜料等。以钴矿[主要成分是CoO、Co O 、
2 3
Co(OH) ,还含SiO 及少量Al O、Fe O、CuO及MnO 等]为原料可制取钴的氧化物。
3 2 2 3 2 3 2
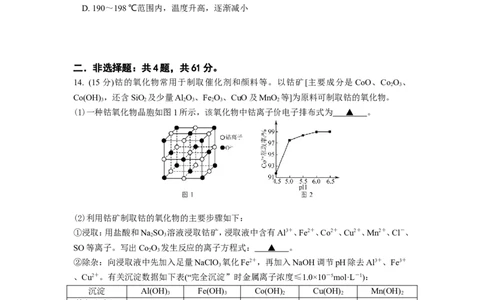
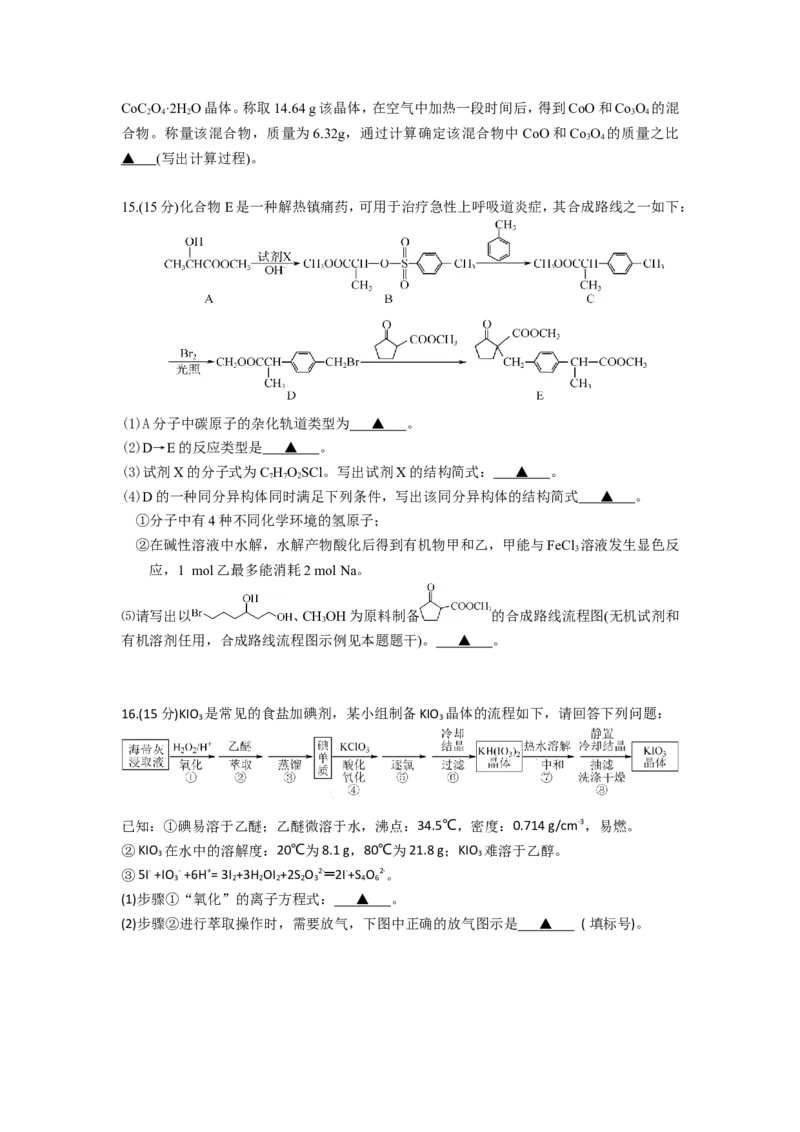
(1)一种钴氧化物晶胞如图1所示,该氧化物中钴离子价电子排布式为 ▲ 。
(2)利用钴矿制取钴的氧化物的主要步骤如下:
①浸取:用盐酸和NaSO 溶液浸取钴矿,浸取液中含有Al3+、Fe2+、Co2+、Cu2+、Mn2+、Cl-、
2 3
SO等离子。写出Co O 发生反应的离子方程式: ▲ 。
2 3
②除杂:向浸取液中先加入足量NaClO 氧化Fe2+,再加入NaOH调节pH除去Al3+、Fe3+
3
、Cu2+。有关沉淀数据如下表(“完全沉淀”时金属离子浓度≤1.0×10-5mol·L-1):
沉淀 Al(OH) Fe(OH) Co(OH) Cu(OH) Mn(OH)
3 3 2 2 2
恰好完全沉
5.2 2.8 9.4 6.7 10.1
淀时的pH
若浸取液中c(Co2+)=0.1 mol·L-1,则须调节溶液pH的范围是 ▲ (加入NaClO 和
3
NaOH时,溶液的体积变化忽略)。
③萃取、反萃取:向除杂后的溶液中,加入某有机酸萃取剂(HA) ,发生反应:
2
Co2++n(HA) CoA·(n-1)(HA) +2H+。实验测得:当溶液pH处于4.5~6.5范围内,
2 2 2
Co2+萃取率随溶液pH的增大而增大(如图2所示),其原因是 ▲ 。向萃取所得有机相中
加入HSO ,反萃取得到水相。
2 4
④沉钴、热分解:向反萃取后得到的水相中加入(NH )C O 溶液,过滤、洗涤、干燥,得到
4 2 2 4CoC O·2H O晶体。称取14.64 g该晶体,在空气中加热一段时间后,得到CoO和Co O 的混
2 4 2 3 4
合物。称量该混合物,质量为6.32g,通过计算确定该混合物中CoO和Co O 的质量之比
3 4
▲ (写出计算过程)。
15.(15分)化合物E是一种解热镇痛药,可用于治疗急性上呼吸道炎症,其合成路线之一如下:
(1)A分子中碳原子的杂化轨道类型为 ▲ 。
(2)D→E的反应类型是 ▲ 。
(3)试剂X的分子式为C HOSCl。写出试剂X的结构简式: ▲ 。
7 7 2
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式 ▲ 。
①分子中有4种不同化学环境的氢原子;
②在碱性溶液中水解,水解产物酸化后得到有机物甲和乙,甲能与FeCl 溶液发生显色反
3
应,1 mol乙最多能消耗2 mol Na。
⑸请写出以 、CHOH为原料制备 的合成路线流程图(无机试剂和
3
有机溶剂任用,合成路线流程图示例见本题题干)。 ▲ 。
16.(15分)KIO 是常见的食盐加碘剂,某小组制备KIO 晶体的流程如下,请回答下列问题:
3 3
已知:①碘易溶于乙醚;乙醚微溶于水,沸点:34.5℃,密度:0.714 g/cm-3,易燃。
②KIO 在水中的溶解度:20℃为8.1 g,80℃为21.8 g;KIO 难溶于乙醇。
3 3
③5I- +IO - +6H+= 3I +3H OI +2S O 2-═2I-+S O 2-。
3 2 2 2 2 3 4 6
(1)步骤①“氧化”的离子方程式: ▲ 。
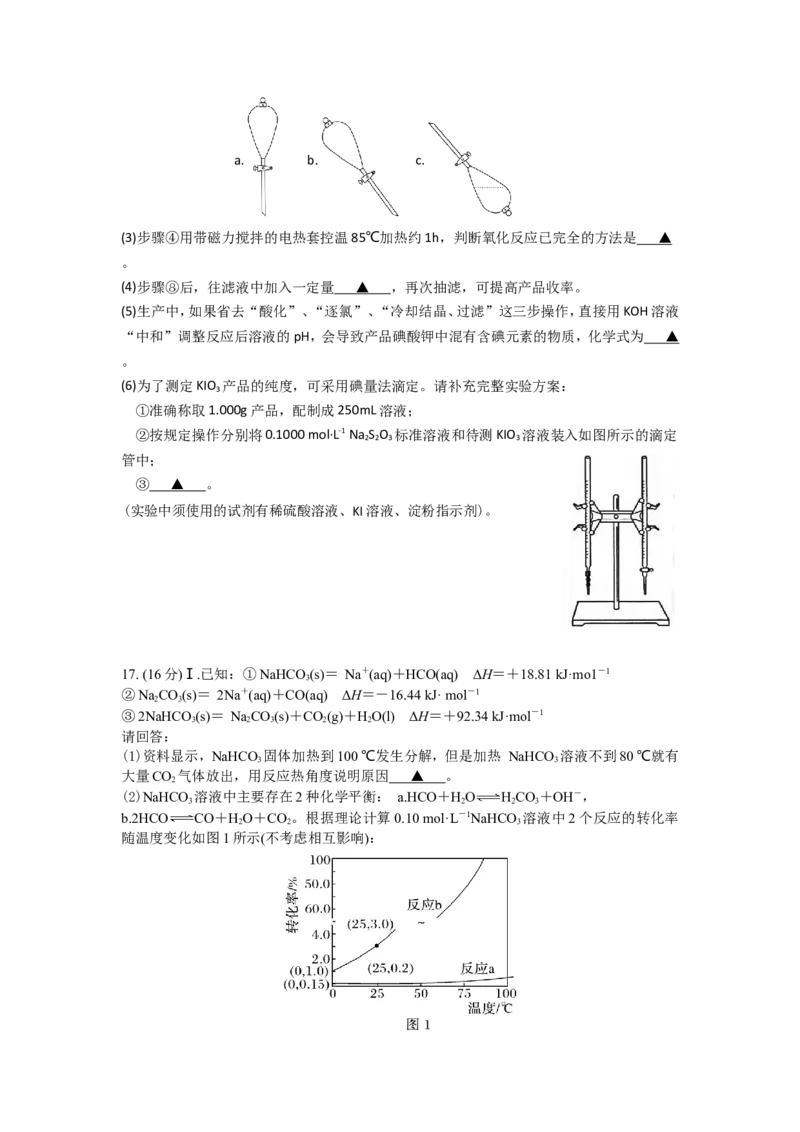
(2)步骤②进行萃取操作时,需要放气,下图中正确的放气图示是 ▲ ( 填标号)。a. b. c.
(3)步骤④用带磁力搅拌的电热套控温85℃加热约1h,判断氧化反应已完全的方法是 ▲
。
(4)步骤⑧后,往滤液中加入一定量 ▲ ,再次抽滤,可提高产品收率。
(5)生产中,如果省去“酸化”、“逐氯”、“冷却结晶、过滤”这三步操作,直接用KOH溶液
“中和”调整反应后溶液的pH,会导致产品碘酸钾中混有含碘元素的物质,化学式为 ▲
。
(6)为了测定KIO 产品的纯度,可采用碘量法滴定。请补充完整实验方案:
3
①准确称取1.000g产品,配制成250mL溶液;
②按规定操作分别将0.1000 mol·L-1 Na S O 标准溶液和待测KIO 溶液装入如图所示的滴定
2 2 3 3
管中;
③ ▲ 。
(实验中须使用的试剂有稀硫酸溶液、KI溶液、淀粉指示剂)。
17. (16分)Ⅰ.已知:①NaHCO (s)= Na+(aq)+HCO(aq) ΔH=+18.81 kJ·mo1-1
3
②NaCO(s)= 2Na+(aq)+CO(aq) ΔH=-16.44 kJ· mol-1
2 3
③2NaHCO (s)= NaCO(s)+CO(g)+HO(l) ΔH=+92.34 kJ·mol-1
3 2 3 2 2
请回答:
(1)资料显示,NaHCO 固体加热到100 ℃发生分解,但是加热 NaHCO 溶液不到80 ℃就有
3 3
大量CO 气体放出,用反应热角度说明原因 ▲ 。
2
(2)NaHCO 溶液中主要存在2种化学平衡: a.HCO+HO HCO+OH-,
3 2 2 3
b.2HCO CO+HO+CO 。根据理论计算0.10 mol·L-1NaHCO 溶液中2个反应的转化率
2 2 3
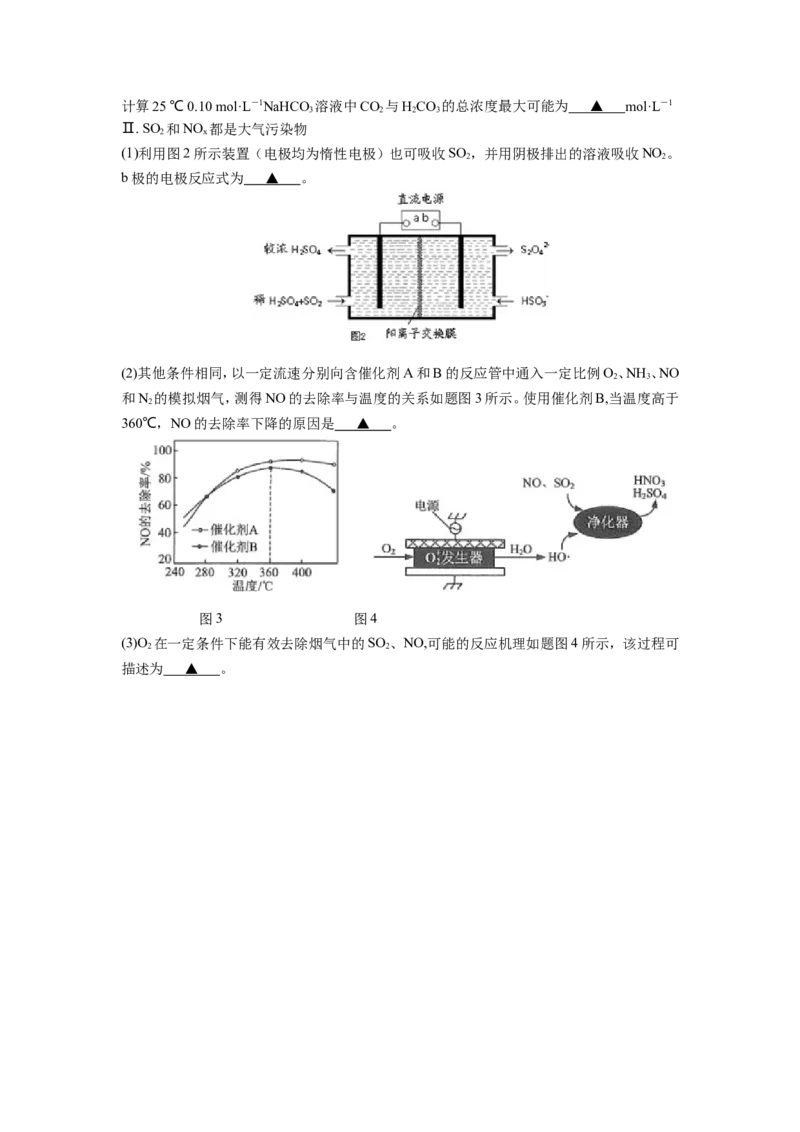
随温度变化如图1所示(不考虑相互影响):计算25 ℃ 0.10 mol·L-1NaHCO 溶液中CO 与HCO 的总浓度最大可能为 ▲ mol·L-1
3 2 2 3
Ⅱ. SO 和NO 都是大气污染物
2 x
(1)利用图2所示装置(电极均为惰性电极)也可吸收SO ,并用阴极排出的溶液吸收NO 。
2 2
b极的电极反应式为 ▲ 。
(2)其他条件相同,以一定流速分别向含催化剂A和B的反应管中通入一定比例O、NH 、NO
2 3
和N 的模拟烟气,测得NO的去除率与温度的关系如题图3所示。使用催化剂B,当温度高于
2
360℃,NO的去除率下降的原因是 ▲ 。
图3 图4
(3)O 在一定条件下能有效去除烟气中的SO 、NO,可能的反应机理如题图4所示,该过程可
2 2
描述为 ▲ 。六校联合体 2023 届高三 8 月联合调研
化学参考答案
1-13
BDCBD ADBCCBAD
14. (15分)
(1) 3d7(2分)
(2) ① Co O+SO+4H+===2Co2++SO+2HO(3分) ② 6.7~7.4(3分)
2 3 2
③ pH越大,溶液中c(H+)越小,有利于Co2++n(HA) CoA·(n-1)(HA) +2H+反
2 2 2
应正向进行,Co2+萃取率越高(3分)
④n(CoC O·2H O)==0.08 mol(1分)
2 4 2
n(CoO)+3n(Co O)=0.08 mol(1分)
3 4
n(CoO)×75 g·mol-1+n(Co O)×241 g·mol-1=6.32 g
3 4
则n(CoO)=0.02 mol n(Co O)=0.02 mol(1分)
3 4
==(1分)
15. (15分)
(1) sp2 sp3(2分)
(2) 取代反应(2分)
(5)
(5分)
16(15分)⑴2 I- + 2H+ + HO=I +2HO (3分) ⑵c (2分) ⑶反应液褪色(2分)
2 2 2 2⑷乙醇 (2分)
⑸KIO (3分)
4
⑹从右侧酸式滴定管中放出一定体积的待测KIO 溶液于锥形瓶中,加稀硫酸酸化,再加入足
3
量KI溶液充分反应,加淀粉指示剂,用装有0.1000 mol·L-1 Na S O 标准溶液左侧碱式滴定管
2 2 3
滴定,当滴入最后半滴标准液时,溶液由蓝色变为无色,且半分钟内不变色,即达到滴定终点,
记录标准液的体积(3分)
17(16分)
Ⅰ.(1)2HCO(aq)===CO(aq)+CO(g)+HO(l) ΔH=+38.28 kJ·mol-1,反应需要的能量比固
2 2
体小(3分)
(2)1.7×10-3 (3分)
Ⅱ. ⑴2HSO -+2H++2e-=S O2-+2H O (3分)
3 2 4 2
⑵温度高于360 ℃时,催化剂B活性降低,反应速率减慢(3分)
⑶O 在O发生器中失去电子转化为O;O与水作用生成HO·; HO·在净化器中将NO和SO
2 2
氧化为HNO 和HSO (4分)
3 2 4