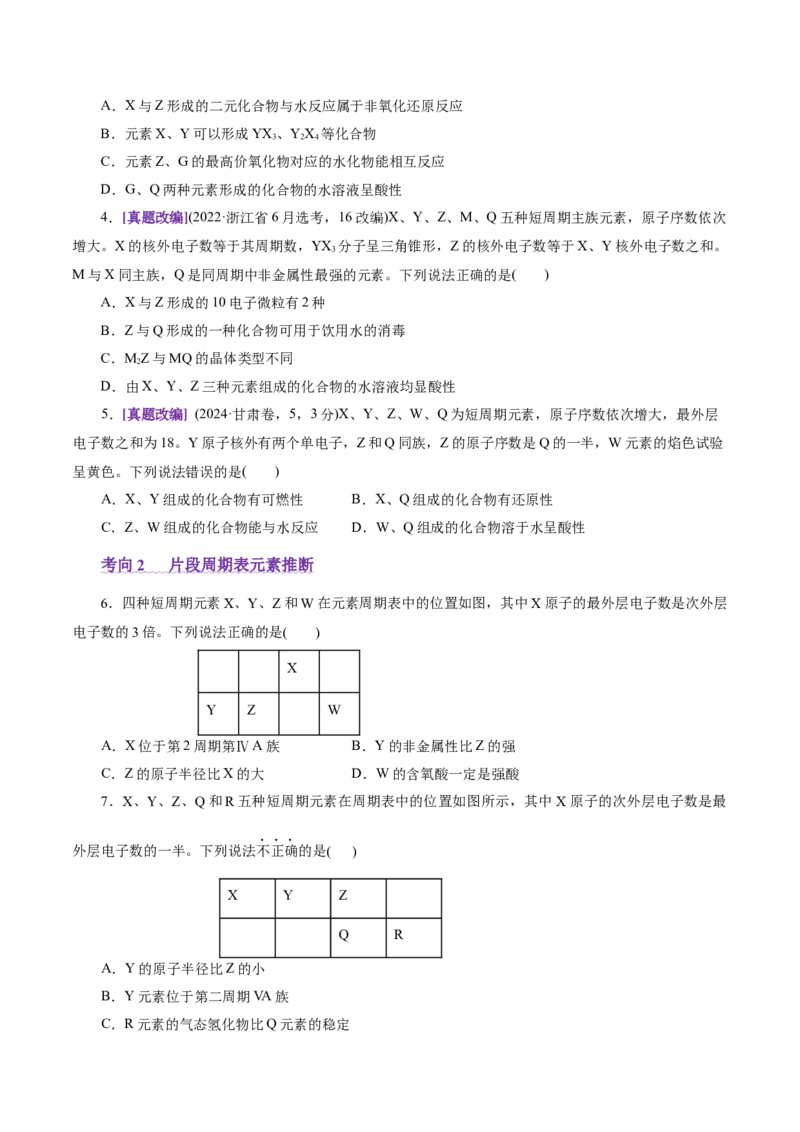文档内容
热点专项 元素"位一构一性”关系的分析
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.元素推断题解题的一般步骤.............................................................................................................................
2.元素推断题的思维模型.....................................................................................................................................
3.元素推断题的解题思路.....................................................................................................................................
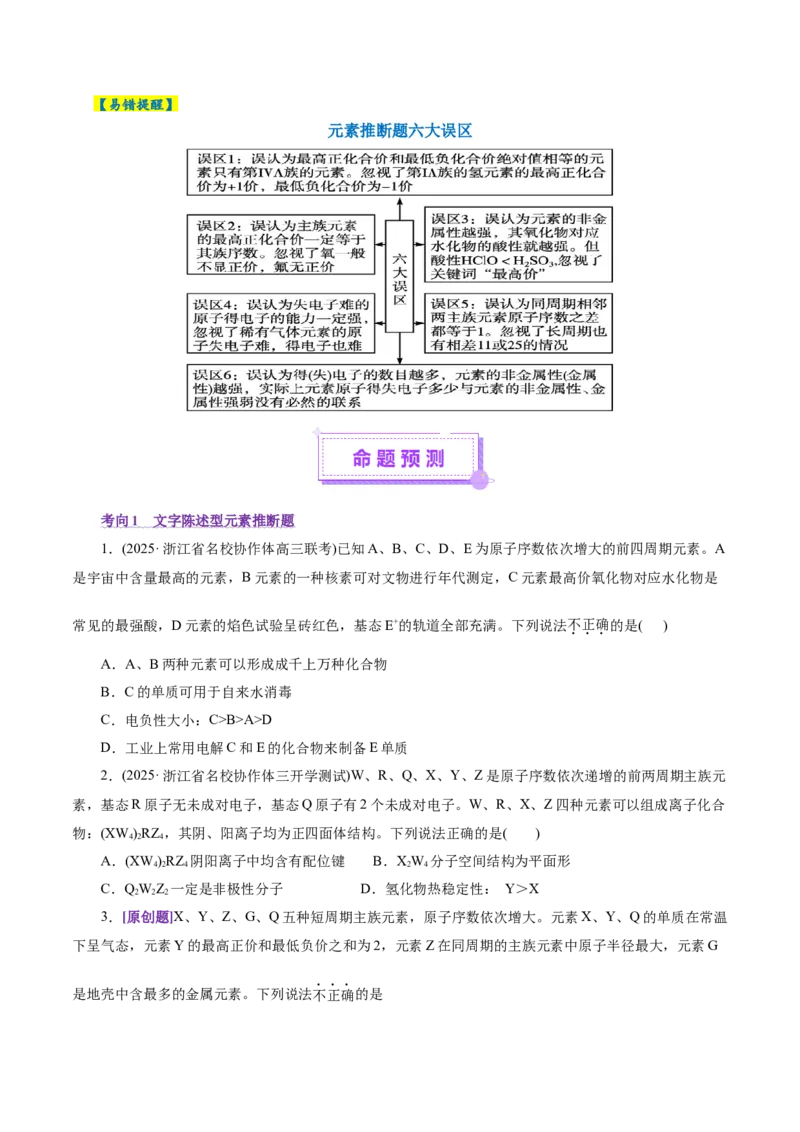
4.元素金属性、非金属性强弱判断方法......................................................
5.原子或离子半径比较....................................................................
【命题预测】...........................................................................................................................................................
考向1文字陈述型元素推断题...............................................................................................................................
考向2片段周期表元素推断...................................................................................................................................
考向3物质结构式元素推断...................................................................................................................................
考向4根据化合物转化关系推断...........................................................................................................................
考点要求 考题统计 考情分析
2024·全国甲卷,5,6分;2024·浙江 1月 元素推断题主要考查元素周
期表中“位、构、性”的关
卷,12,3分;2024·浙江6月卷,10,3分;
系及学生利用物质结构和性
2024·河北卷,7,3分;2024·全国新课标卷, 质进行综合推断的能力,是
高考命题中的常客。解题
文字陈述
5,6分;2024·辽吉黑卷,11,3分;2024·江西
时,首先确定其为何种元
型元素推
素,然后以此为突破口,推
断 卷,5,3分;2023•全国乙卷,10,6分;2023•
知其他未知元素。预计2025
浙江省 1 月,10,3 分;2023•湖北卷,6,3 年高考仍会以考查递变规律
和性质为主,题目一般通过
分;2023•湖南卷,6,3分;2023•全国甲卷,
图表、文字等手段推断元素
11,6分;2023•浙江省6月,11,3分;2023•广 种类,尤其是通过未知物的东卷,14,3 分;2022•重庆卷,10,3 分;
2022•福建卷,4,3分;2022•全国甲卷,12,6
分;2022•全国乙卷,11,6分;2022•海南卷,
结构式,在确定元素的基础
10,2分;2022•辽宁卷,5,3分;2022•浙江省
上,能将元素周期表、原子
结构、元素单质及其化合物
1月,11,3分;2022•浙江省6月,11,3分;
的性质等内容结合起来进行
2024·湖北卷,9,3分;2024·福建卷,3,4分; 综合运用。
物质结构 2024·广西卷,1,3分;2024· 重庆卷,12,3
式型元素 分;2024· 贵州卷,9,3 分;2024·广东卷,
推断 12,3分;2024·甘肃卷,5,3分;2023•辽宁
卷,9,3分;2022•湖南卷,3,3分;
的
1.(2024·全国甲卷,5,3分)W、X、Y、Z为原子序数依次增大 短周期元素。W和X原子序数之和
等于 的核外电子数,化合物W+[ZY]-可用作化学电源的电解质。下列叙述正确的是( )
6
A.X和Z属于同一主族 B.非属性:
C.气态氢化物的稳定性: D.原子半径:2.(2024·浙江1月卷,12,3分)X、Y、Z、M和Q五种主族元素,原子序数依次增大,X原子半径最
小,短周期中M电负性最小,Z与Y、Q相邻,基态Z原子的s能级与p能级的电子数相等,下列说法不
正确的是( )
A.沸点:XZ>XQ
2 2
B.M与Q可形成化合物MQ、MQ
2 2 2
C.化学键中离子键成分的百分数: MZ>MQ
2 2
D.YZ-与QZ2-离子空间结构均为三角锥形
3 3
3.(2024·浙江6月卷,10,3分)X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同
短周期,Y与M同主族,Y与Z核电荷数相差2,Z的原子最外层电子数是内层电子数的3倍。下列说法
不正确的是( )
A.键角:YX +>YX - B.分子的极性:YX>XZ
3 3 2 2 2 2
C.共价晶体熔点:Y>M D.热稳定性:YX >MX
4 4
4.(2024·河北卷,7,3分)侯氏制碱法工艺流程中的主反应为QR+YW +XZ +WZ=QWXZ +YW R,其
3 2 2 3 4
中W、X、Y、Z、Q、R分别代表相关化学元素。下列说法正确的是( )
A.原子半径:W<X<Y B.第一电离能:X<Y<Z
C.单质沸点:Z<R<Q D.电负性:W<Q<R
5.(2024·全国新课标卷,5,3分)我国科学家最近研究的一种无机盐Y[Z(WX)] 纳米药物具有高效的
3 6 2
细胞内亚铁离子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周
期元素。W的外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层
未成对电子数为4。下列叙述错误的是( )
A.W、X、Y、Z四种元素的单质中Z的熔点最高
的
B.在X 简单氢化物中X原子轨道杂化类型为sp3
C.Y的氢氧化物难溶于NaCl溶液,可以溶于NH Cl溶液
4
D.Y[Z(WX)] 中WX-提供电子对与Z3+形成配位键
3 6 2
6.(2024·辽吉黑卷,11,3分)如下反应相关元素中,W、X、Y、Z为原子序数依次增大的短周期元素,
基态X原子的核外电子有5种空间运动状态,基态Y、Z原子有两个未成对电子,Q是ds区元素,焰色试
验呈绿色。下列说法错误的是( )
QZY 溶液 QZX YW 溶液
4 4 4 12
A.单质沸点:Z>Y>W B.简单氢化物键角:X>YC.反应过程中有蓝色沉淀产生 D.QZX YW 是配合物,配位原子是Y
4 4 12
7.(2024·江西卷,5,3分)某新材料阳离子为W X YZM+。W、X、Y、Z和M是原子序数依次增大
36 18 2 6
的前20号主族元素,前四周期中M原子半径最大,X、Y、Z同周期。XW 分子含有大π键( ),XZ 分
6 6 2
子呈直线形。下列说法正确的是( )
A.WYZ 是强酸 B.MZW是强碱 C.MZ 是共价化合物 D.XW 是离子化合物
2 2 2 2 2
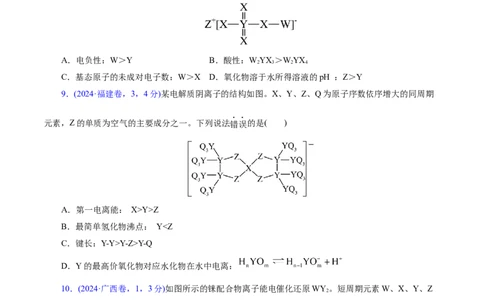
8.(2024·湖北卷,9,3分)主族元素W、X、Y、Z原子序数依次增大,X、Y的价电子数相等,Z的
价电子所在能层有16个轨道,4种元素形成的化合物如图。下列说法正确的是( )
A.电负性:W>Y B.酸性:WYX >WYX
2 3 2 4
C.基态原子的未成对电子数:W>X D.氧化物溶于水所得溶液的pH :Z>Y
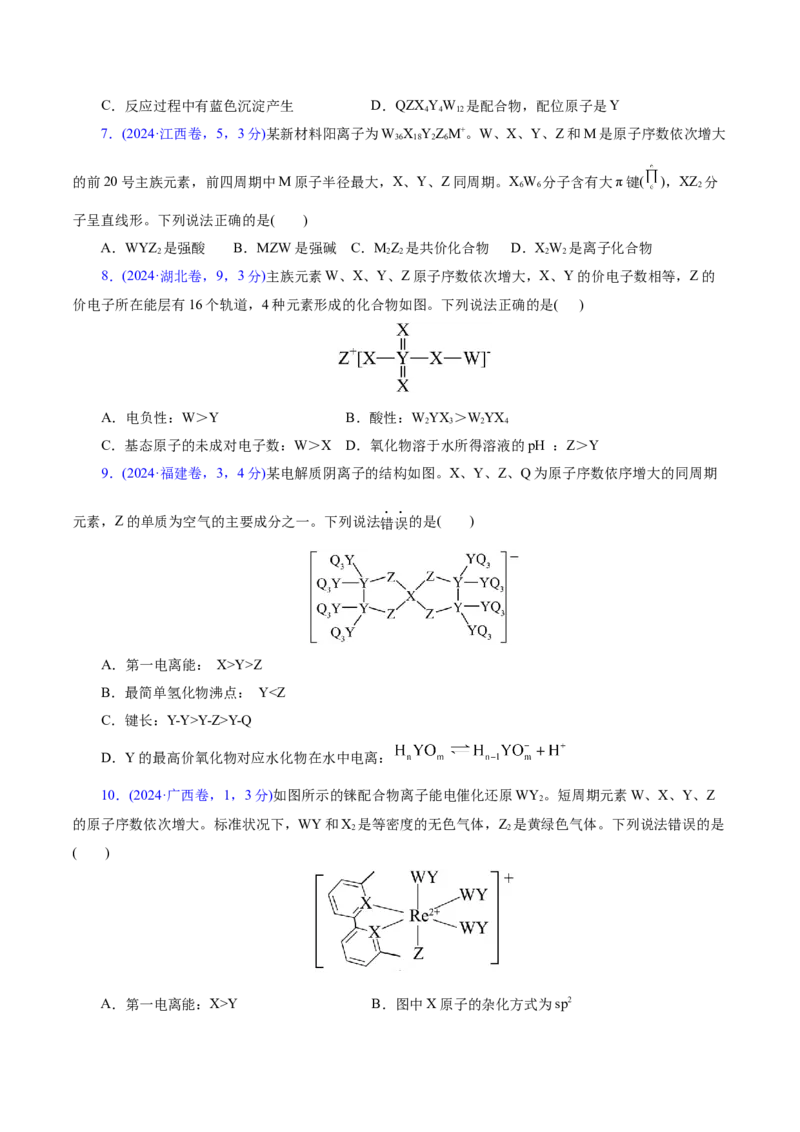
9.(2024·福建卷,3,4分)某电解质阴离子的结构如图。X、Y、Z、Q为原子序数依序增大的同周期
元素,Z的单质为空气的主要成分之一。下列说法错误的是( )
A.第一电离能: X>Y>Z
B.最简单氢化物沸点: YY-Z>Y-Q
D.Y的最高价氧化物对应水化物在水中电离:
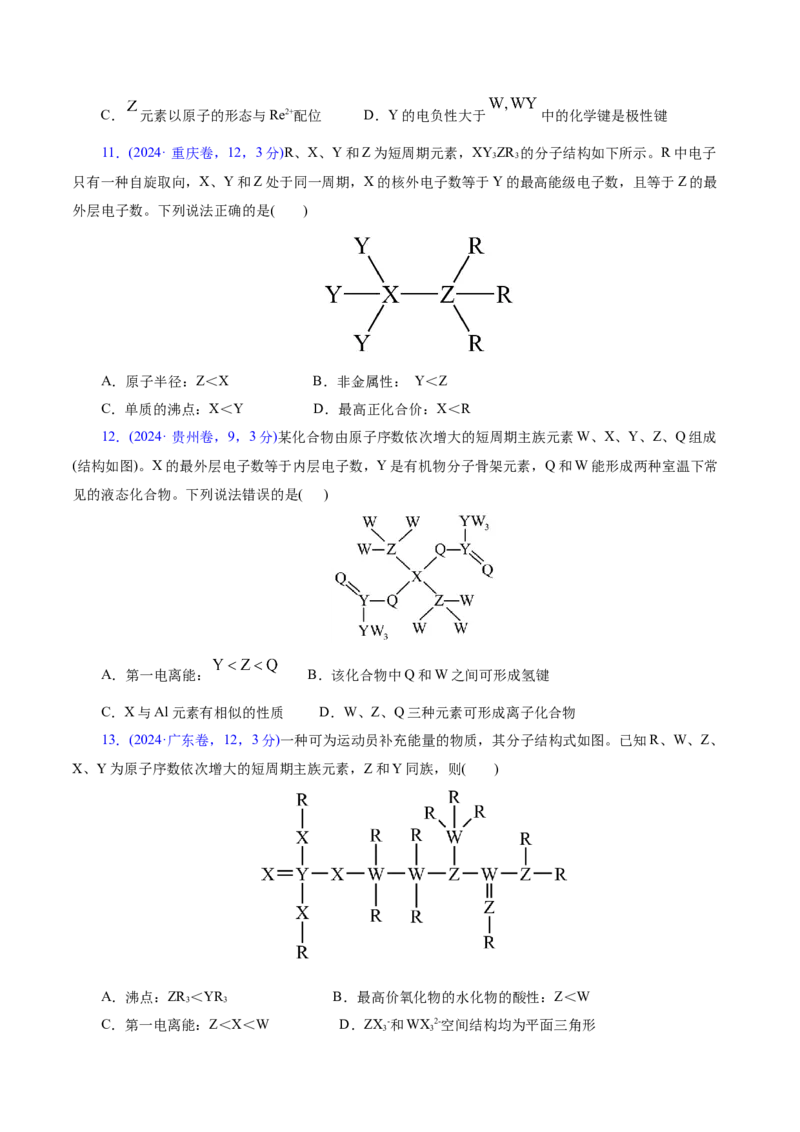
10.(2024·广西卷,1,3分)如图所示的铼配合物离子能电催化还原WY。短周期元素W、X、Y、Z
2
的原子序数依次增大。标准状况下,WY和X 是等密度的无色气体,Z 是黄绿色气体。下列说法错误的是
2 2
( )
A.第一电离能:X>Y B.图中X原子的杂化方式为sp2C. 元素以原子的形态与Re2+配位 D.Y的电负性大于 中的化学键是极性键
11.(2024· 重庆卷,12,3分)R、X、Y和Z为短周期元素,XY ZR 的分子结构如下所示。R中电子
3 3
只有一种自旋取向,X、Y和Z处于同一周期,X的核外电子数等于Y的最高能级电子数,且等于Z的最
外层电子数。下列说法正确的是( )
A.原子半径:Z<X B.非金属性: Y<Z
C.单质的沸点:X<Y D.最高正化合价:X<R
12.(2024· 贵州卷,9,3分)某化合物由原子序数依次增大的短周期主族元素W、X、Y、Z、Q组成
(结构如图)。X的最外层电子数等于内层电子数,Y是有机物分子骨架元素,Q和W能形成两种室温下常
见的液态化合物。下列说法错误的是( )
A.第一电离能: B.该化合物中Q和W之间可形成氢键
C.X与Al元素有相似的性质 D.W、Z、Q三种元素可形成离子化合物
13.(2024·广东卷,12,3分)一种可为运动员补充能量的物质,其分子结构式如图。已知R、W、Z、
X、Y为原子序数依次增大的短周期主族元素,Z和Y同族,则( )
A.沸点:ZR <YR B.最高价氧化物的水化物的酸性:Z<W
3 3
C.第一电离能:Z<X<W D.ZX-和WX2-空间结构均为平面三角形
3 3复杂元素“位—构—性”推断模型
1 .元素推断题解题的一般步骤
(1)寻找突破口——元素推断的关键。综合把握题中关键信息,确定突破口。
①图表信息——题中直接给出的元素周期表片段。
②文字信息——把题中给出的文字信息进行提炼。
③结构信息——题中给出的原子结构信息如微粒的质子数或电子数等。
(2)推断元素——正确解题的基础。根据关键信息,结合突破口找出关键元素,然后根据题中描述或结
构片段推出所有元素,充分利用元素周期律结合选项作答。
(3)解题——明确要求,规范作答。
(4)验证——确保答题正确无误。
2 .元素推断题的思维模型
3 .元素推断题的解题思路4 . 元素金属性、非金属性强弱判断方法
①在金属活动性顺序表中越靠前,金属性越强
②单质与水或非氧化性酸反应越剧烈,金属性越强
③单质还原性越强或阳离子氧化性越弱,金属性越强
金属性判
断方法 ④最高价氧化物对应水化物的碱性越强,金属性越强
金属性 ⑤若Xn++Y→X+Ym+,则Y比X的金属性强
或非金
属性 ⑥元素在周期表中的位置:左边或下方元素的金属性强
①与H 化合越容易,气态氢化物越稳定,非金属性越强
2
非金属判 ②单质氧化性越强或阴离子还原性越弱,非金属性越强
断方法
③最高价氧化物对应水化物的酸性越强,非金属性越强
④元素在周期表中的位置:右边或上方元素的非金属性强
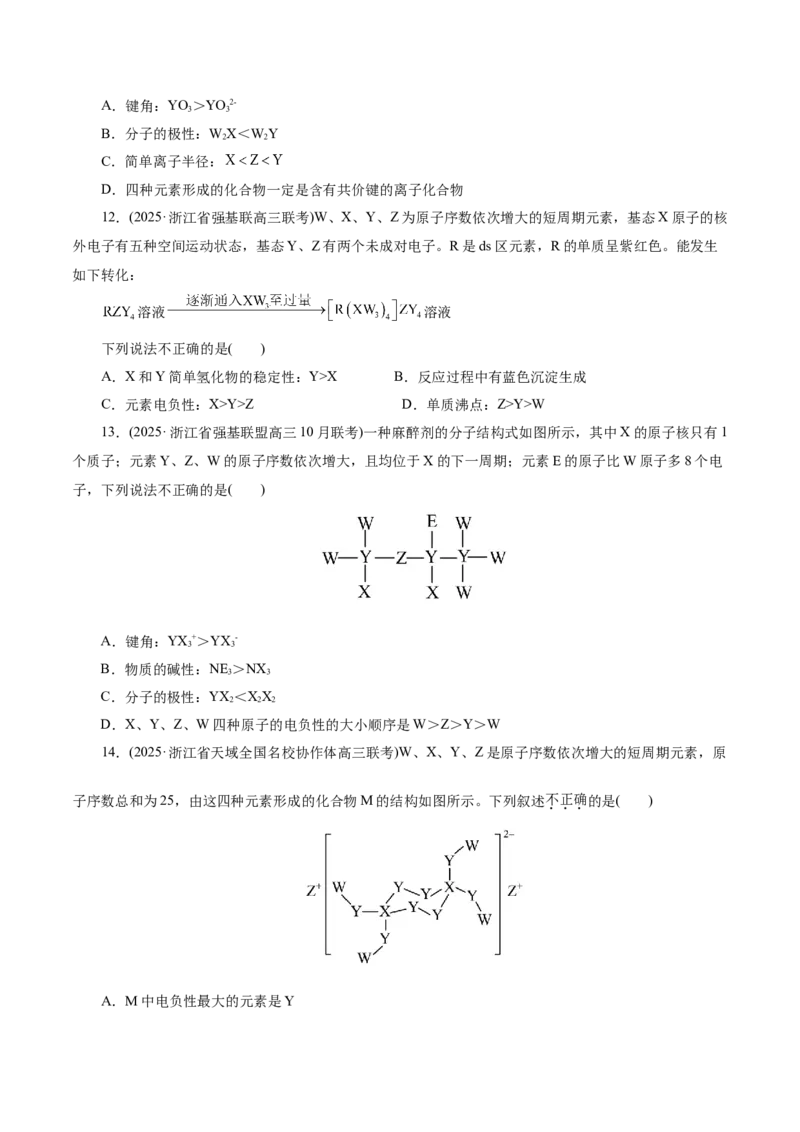
5 . 原子或离子半径比较【易错提醒】
元素推断题六大误区
考向 1 文字陈述型元素推断题
1.(2025·浙江省名校协作体高三联考)已知A、B、C、D、E为原子序数依次增大的前四周期元素。A
是宇宙中含量最高的元素,B元素的一种核素可对文物进行年代测定,C元素最高价氧化物对应水化物是
常见的最强酸,D元素的焰色试验呈砖红色,基态E+的轨道全部充满。下列说法不正确的是( )
A.A、B两种元素可以形成成千上万种化合物
B.C的单质可用于自来水消毒
C.电负性大小:C>B>A>D
D.工业上常用电解C和E的化合物来制备E单质
2.(2025·浙江省名校协作体三开学测试)W、R、Q、X、Y、Z是原子序数依次递增的前两周期主族元
素,基态R原子无未成对电子,基态Q原子有2个未成对电子。W、R、X、Z四种元素可以组成离子化合
物:(XW )RZ ,其阴、阳离子均为正四面体结构。下列说法正确的是( )
4 2 4
A.(XW )RZ 阴阳离子中均含有配位键 B.XW 分子空间结构为平面形
4 2 4 2 4
C.QWZ 一定是非极性分子 D.氢化物热稳定性: Y>X
2 2 2
3.[原创题]X、Y、Z、G、Q五种短周期主族元素,原子序数依次增大。元素X、Y、Q的单质在常温
下呈气态,元素Y的最高正价和最低负价之和为2,元素Z在同周期的主族元素中原子半径最大,元素G
是地壳中含最多的金属元素。下列说法不正确的是A.X与Z形成的二元化合物与水反应属于非氧化还原反应
B.元素X、Y可以形成YX 、YX 等化合物
3 2 4
C.元素Z、G的最高价氧化物对应的水化物能相互反应
D.G、Q两种元素形成的化合物的水溶液呈酸性
4.[真题改编](2022·浙江省6月选考,16改编)X、Y、Z、M、Q五种短周期主族元素,原子序数依次
增大。X的核外电子数等于其周期数,YX 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。
3
M与X同主族,Q是同周期中非金属性最强的元素。下列说法正确的是( )
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C.MZ与MQ的晶体类型不同
2
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
5.[真题改编] (2024·甘肃卷,5,3分)X、Y、Z、W、Q为短周期元素,原子序数依次增大,最外层
电子数之和为18。Y原子核外有两个单电子,Z和Q同族,Z的原子序数是Q的一半,W元素的焰色试验
呈黄色。下列说法错误的是( )
A.X、Y组成的化合物有可燃性 B.X、Q组成的化合物有还原性
C.Z、W组成的化合物能与水反应 D.W、Q组成的化合物溶于水呈酸性
考向 2 片段周期表元素推断
6.四种短周期元素X、Y、Z和W在元素周期表中的位置如图,其中X原子的最外层电子数是次外层
电子数的3倍。下列说法正确的是( )
X
Y Z W
A.X位于第2周期第ⅣA族 B.Y的非金属性比Z的强
C.Z的原子半径比X的大 D.W的含氧酸一定是强酸
7.X、Y、Z、Q和R五种短周期元素在周期表中的位置如图所示,其中 X原子的次外层电子数是最
外层电子数的一半。下列说法不正确的是( )
X Y Z
Q R
A.Y的原子半径比Z的小
B.Y元素位于第二周期VA族
C.R元素的气态氢化物比Q元素的稳定D.与X元素同主族的下一周期元素的单质可作为半导体材料
8.[真题改编](2022•广东选择性考试,7)甲~戊均为短周期元素,在元素周期表中的相对位置如图所
示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是( )
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
9.如表为元素周期表的一部分,其中 、 、 、 为短周期元素, 元素的原子质子数为 元素
的原子的 倍,下列说法不正确的是( )
A.R、W、Z元素的原子半径依次递增,而 、 、 的氢化物的空间结构都呈 形, 的氢化物
的沸点高于 的氢化物
B.Y、Z、W的最高价氧化物的水化物的酸性依次递增
C.I:Z>W,是因为 的3p轨道电子填充处于半充满状态
1
D.YR 晶体熔化、液态WR 气化克服的作用力不同
2 3
10. X、Y、Z、W为短周期元素,它们在周期表的位置如图所示,Y原子的最外层电子数是次外层
电子数的3倍。下列说法中正确的是( )
X Y
Z W
A.X的单质中 键和 键个数之比为1∶1 B.Y和Z只能组成一种化合物
C.Z的氧化物的晶体属于分子晶体 D.最高价氧化物对应水化物的酸性:Z>W
考向 3 物质结构式元素推断
11.(2025·浙江省Z20名校联盟高三联考)主族元素 、 、 、 原子序数依次增大, 、 的价
电子数相等, 的基态原子核外电子的空间运动状态共10种,四种元素形成的化合物如图。
下列说法不正确的是( )A.键角:YO >YO 2-
3 3
B.分子的极性:WX<WY
2 2
C.简单离子半径:
D.四种元素形成的化合物一定是含有共价键的离子化合物
12.(2025·浙江省强基联高三联考)W、X、Y、Z为原子序数依次增大的短周期元素,基态X原子的核
外电子有五种空间运动状态,基态Y、Z有两个未成对电子。R是ds区元素,R的单质呈紫红色。能发生
如下转化:
溶液 溶液
下列说法不正确的是( )
A.X和Y简单氢化物的稳定性:Y>X B.反应过程中有蓝色沉淀生成
C.元素电负性:X>Y>Z D.单质沸点:Z>Y>W
13.(2025·浙江省强基联盟高三10月联考)一种麻醉剂的分子结构式如图所示,其中X的原子核只有1
个质子;元素Y、Z、W的原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电
子,下列说法不正确的是( )
A.键角:YX +>YX -
3 3
B.物质的碱性:NE>NX
3 3
C.分子的极性:YX <XX
2 2 2
D.X、Y、Z、W四种原子的电负性的大小顺序是W>Z>Y>W
14.(2025·浙江省天域全国名校协作体高三联考)W、X、Y、Z是原子序数依次增大的短周期元素,原
子序数总和为25,由这四种元素形成的化合物M的结构如图所示。下列叙述不正确的是( )
A.M中电负性最大的元素是YB.M中不存在配位键
C.M具有强氧化性,可用于消毒杀菌
D.X元素的最高价含氧酸可以形成分子间氢键
15.(2025·浙江省新阵地教育联盟高三第一次联考)有一种净水剂,结构如图所示,短周期元素X、
Y、W原子序数依次增大,X、Y、W分布在不同周期,X、Y原子的最外层电子数之和等于W原子的最外
层电子数,Z的原子最外层电子数与次外层电子数相差12且基态原子含4个未成对电子,下列叙述正确的
是( )
A.Y、W的简单离子的半径:Y>W B.ZW 在一定条件下可形成ZW
3 4
C.化学键中离子键成分的百分数:ZW>ZY D.分子极性:WY>XY
3 2 3 2 2
16.如图所示的化合物是一种重要的化工原料,X、Y、Z、W、E是原子序数依次增大的短周期主族
元素,其中Z、E同族,基态Y原子的核外有3个未成对电子。下列说法正确的是( )
A.原子半径:W>Y>Z>E B.WZ 中只含有离子键
2 2
C.Z、W、E组成化合物的水溶液一定显中性 D.电负性:Z>Y>X
17.某化合物结构如图所示。其中 为原子序数依次增大的短周期非金属元素,X是有机
分子的骨架元素,W基态原子的M层为全充满、N层只有一个电子。下列说法正确的是( )
A.原子半径:X>Y>Z B.第一电离能:X>Y>M>W
C.该配合物中X均满足8电子稳定结构 D.该配合物中X的杂化类型有sp2、sp3
18.M、X、Y、Z、Q为相邻两个短周期的主族元素,且原子序数依次增大。这五种元素可形成化合
物甲,其结构式如图所示,1mol甲含58mol电子。下列说法正确的是( )A.Q是五种元素中原子半径最大的 B.水中溶解性:MQ<YZ
2
C.XQ 中所有原子均达到8e-稳定结构 D.甲中X、Y、Z均为sp3杂化
3
考向 4 根据化合物转化关系推断
19.(2024·浙江省绍兴鲁迅中学高三选考模拟)短周期主族元素W、X、Y、Z的原子序数依次增大,Y
和Z同主族,且Z的原子序数是Y的2倍。n、q、s是上述元素的单质。m、p、r是由这些元素组成的二元
化合物,其中m的水溶液显碱性。上述物质的转化关系如图所示。下列说法正确的是( )
A.Z的常见氧化物均为酸性氧化物
B.W和X形成的化合物一定是共价化合物
C.原子半径:Z>Y>X
D.四种元素组成的化合物一定能促进水的电离
20.(2024·内蒙古赤峰三模)X、Y、Z、W、Q为短周期主族元素,原子序数依次增大且原子序数总和
为49。它们的化合物在常温下有如图所示的转化关系:
已知:乙、戊分子都含有 10个电子。甲为三元化合物,其他化合物均为二元化合物。下列说法错误
的是( )
A.原子半径:
B.简单氢化物的沸点:C.化合物WQ 中含有非极性键和离子键
2 2
D.最高价氧化物对应水化物的酸性:
21.(2024·陕西铜川高三模拟预测)X、Y、Z、W为原子序数依次增大的四种短周期主族元素,其中Z
为金属元素,X、W为同一主族元素。X、Z、W的最高价氧化物分别为甲、乙、丙,x、y、z、w分别为
X、Y、Z、W的单质,单质w为常见半导体材料,丁是剧毒化合物,其转化关系如图所示。下列说法正确
的是( )
A.原子半径:Z>W>X>Y B.甲分子中含有非极性共价键
C.熔融条件下乙不可以导电 D.最简单氢化物热稳定性:W>X
22.已知X、Y、Z是三种原子序数依次增大的短周期元素。甲、乙、丙分别是三种元素形成的单质,
A、B、C、D分别是由三种元素中的两种形成的化合物,且A与C中均含有10个电子。它们之间的转化
关系如图所示。下列说法正确的是( )
A.原子半径:Z>Y>X
B.X与Z形成的化合物为共价晶体
C.Y有多种同素异形体,且均具有高熔点、高沸点、硬度大的性质
D.Y的最简单氢化物的空间结构为正四面体形
23.短周期主族元素W、X、Y、Z的原子序数依次增大,Y和Z位于同一主族。m、n、p均为由这些
元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为淡黄色固体,易溶于 XZ ,n是一
2
种二元弱酸。上述物质的转化关系如图所示(反应条件省略)。下列说法正确的是( )
A.原子半径:W>Y>X B.W与X组成的化合物中只含有极性键
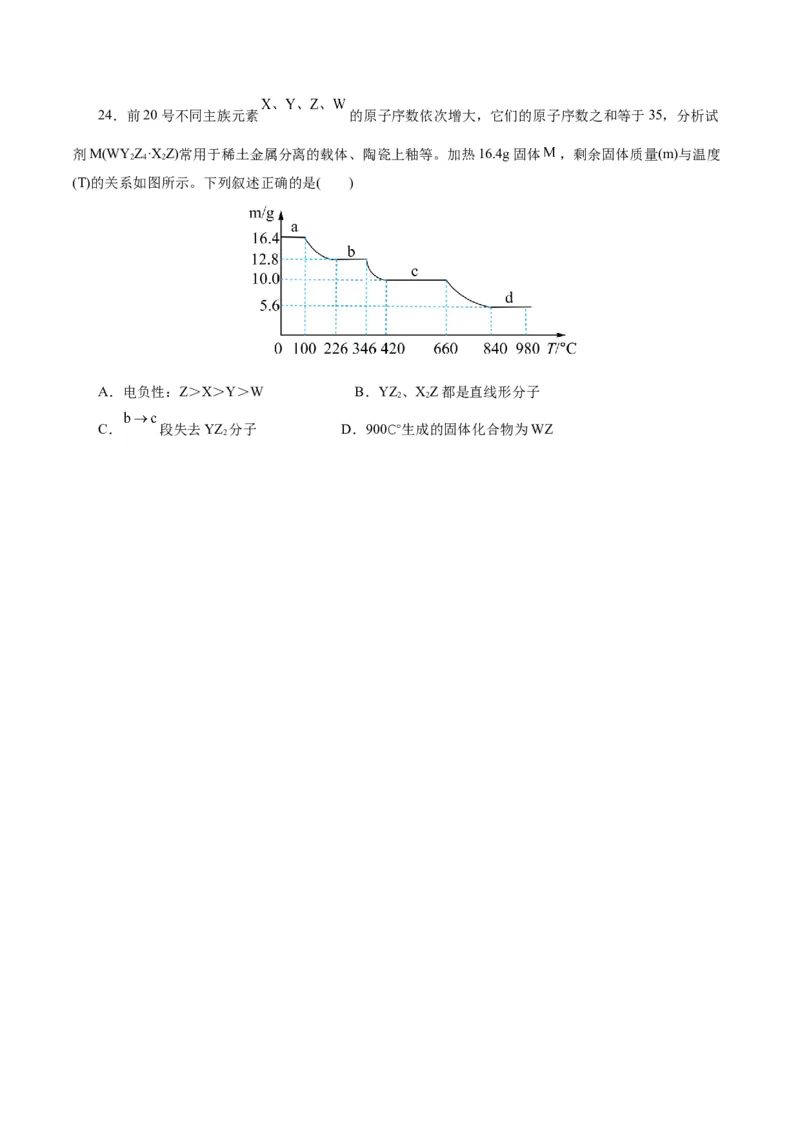
C.简单氢化物的沸点:YX>W24.前20号不同主族元素 的原子序数依次增大,它们的原子序数之和等于35,分析试
剂M(WY Z·X Z)常用于稀土金属分离的载体、陶瓷上釉等。加热16.4g固体 ,剩余固体质量(m)与温度
2 4 2
(T)的关系如图所示。下列叙述正确的是( )
A.电负性:Z>X>Y>W B.YZ、XZ都是直线形分子
2 2
C. 段失去YZ 分子 D.900℃生成的固体化合物为WZ
2