文档内容
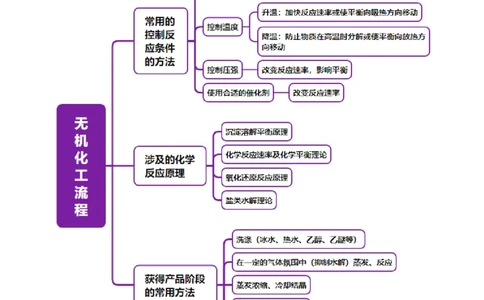
热点专项 无机化工微流程分析
目录
01考情透视·目标导航............................................................................................................................
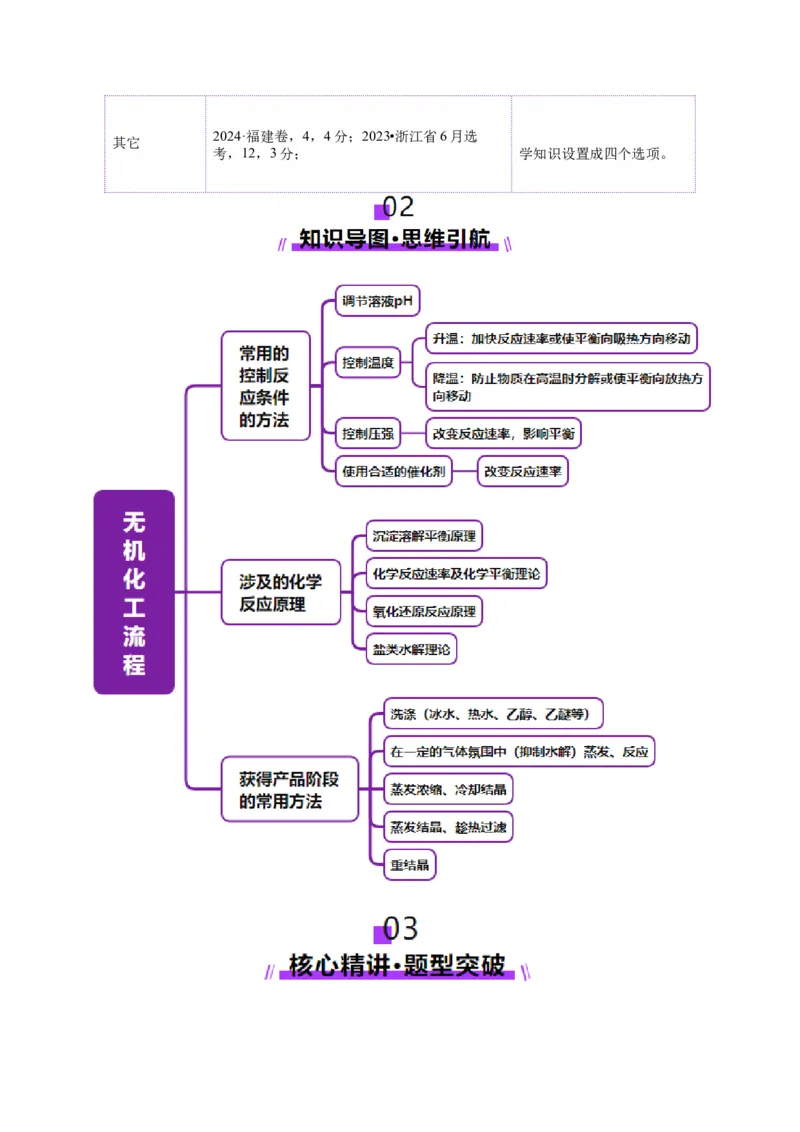
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】...................................................................................................................................................................
【核心精讲】...................................................................................................................................................................
1.微型工艺流程中题的呈现方式............................................................
2.工艺流程题过程解读....................................................................
3.流程图中主要环节的分析................................................................
4.制备工艺中提纯实例....................................................................
【命题预测】...................................................................................................................................................................
考向1以物质的制备为背景...............................................................................................................................
考向2以废旧资源利用为背景...........................................................................................................................
考向3以物质分离提纯为背景...........................................................................................................................
考点要求 考题统计 考情分析
2024·广西卷,1,3分;2024·北京卷,7,3
微型工艺流程题一般分题
分;2024·湖南卷,11,3分;2023•湖北省选择 干、流程图和问题三部
以物质的制备
性考试,3,3分;2023•辽宁省选择性考试, 分。题干一般是简单介绍
为背景
10,3分;2023•山东卷,13,3分;2022•福 该工艺生产的原材料和生
建,6,3分;2022•河北省选择性,4,3分; 成目的,流程图主要用框
图形式将原料到产品的主
要生产工艺流程表示出
2024·福建卷,5,4分;2024· 贵州卷,13,3
来,在流程中一般分为3个
以废旧资源利 分;2024·辽吉黑卷,13,3分;2024·辽吉黑
过程:原料处理→分离提
用为背景 卷,13,3分;2023•湖南卷,9;2023•江苏
纯→获得产品,问题部分
卷,12,3分;
主要根据生产中涉及的化2024·福建卷,4,4分;2023•浙江省6月选
其它
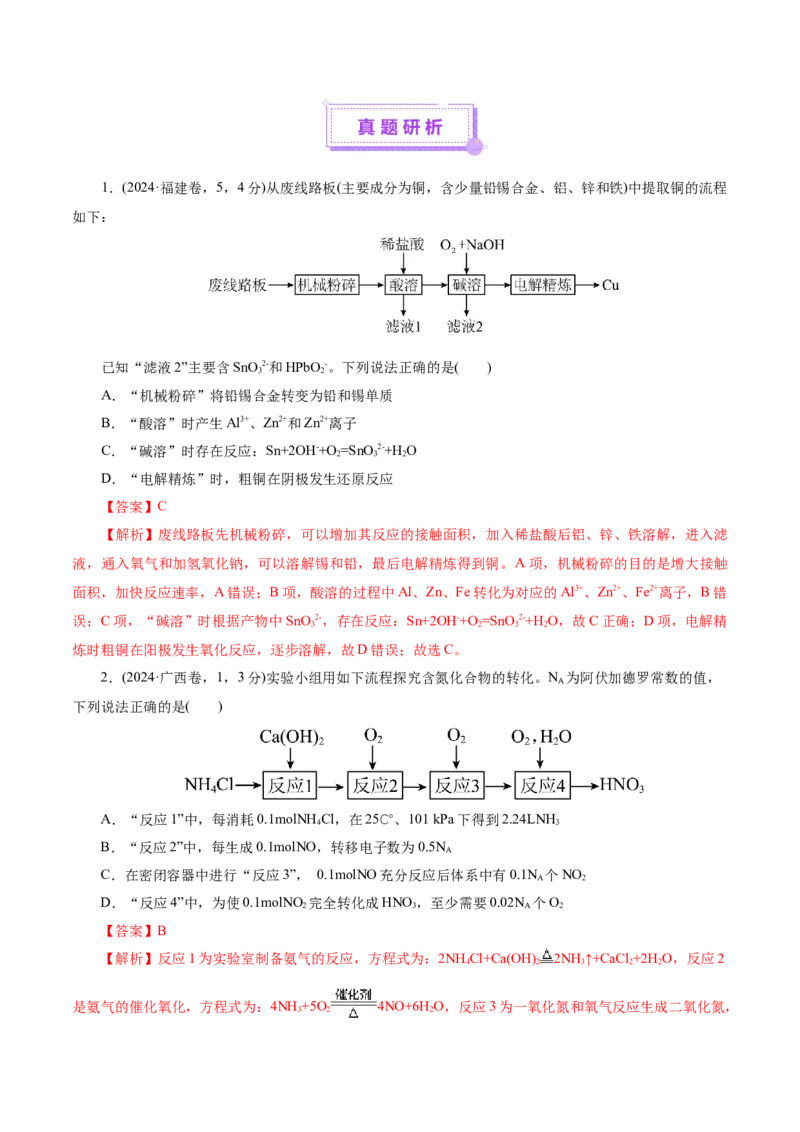
考,12,3分; 学知识设置成四个选项。1.(2024·福建卷,5,4分)从废线路板(主要成分为铜,含少量铅锡合金、铝、锌和铁)中提取铜的流程
如下:
已知“滤液2”主要含SnO2-和HPbO-。下列说法正确的是( )
3 2
A.“机械粉碎”将铅锡合金转变为铅和锡单质
B.“酸溶”时产生Al3+、Zn2+和Zn2+离子
C.“碱溶”时存在反应:Sn+2OH-+O =SnO2-+H O
2 3 2
D.“电解精炼”时,粗铜在阴极发生还原反应
【答案】C
【解析】废线路板先机械粉碎,可以增加其反应的接触面积,加入稀盐酸后铝、锌、铁溶解,进入滤
液,通入氧气和加氢氧化钠,可以溶解锡和铅,最后电解精炼得到铜。A项,机械粉碎的目的是增大接触
面积,加快反应速率,A错误;B项,酸溶的过程中Al、Zn、Fe转化为对应的Al3+、Zn2+、Fe2+离子,B错
误;C项,“碱溶”时根据产物中SnO2-,存在反应:Sn+2OH-+O =SnO2-+H O,故C正确;D项,电解精
3 2 3 2
炼时粗铜在阳极发生氧化反应,逐步溶解,故D错误;故选C。
2.(2024·广西卷,1,3分)实验小组用如下流程探究含氮化合物的转化。N 为阿伏加德罗常数的值,
A
下列说法正确的是( )
A.“反应1”中,每消耗0.1molNH Cl,在25℃、101 kPa下得到2.24LNH
4 3
B.“反应2”中,每生成0.1molNO,转移电子数为0.5N
A
C.在密闭容器中进行“反应3”, 0.1molNO充分反应后体系中有0.1N 个NO
A 2
D.“反应4”中,为使0.1molNO 完全转化成HNO,至少需要0.02N 个O
2 3 A 2
【答案】B
【解析】反应1为实验室制备氨气的反应,方程式为:2NH Cl+Ca(OH) 2NH ↑+CaCl +2H O,反应2
4 2 3 2 2
是氨气的催化氧化,方程式为:4NH +5O 4NO+6H O,反应3为一氧化氮和氧气反应生成二氧化氮,
3 2 2方程式为:2NO+O =2NO ,反应4为二氧化氮,氧气和水反应生成硝酸,4NO +2H O+O=4HNO 。A项,
2 2 2 3
根据分析可知,每消₂ 耗0.1₂molNH
4
Cl,生成0.1mol氨气,但是由于不是标准状况,则气体不是2.24L,A错
误;B项,反应2方程式为:4NH +5O 4NO+6H O,该反应转移20e-,则每生成0.1molNO,转移电
3 2 2
子数为0.5N ,B正确;C项,根据反应3,0.1molNO充分反应后生成0.1N 个NO ,但是体系中存在
A A 2
2NO ⇌NO,则最终二氧化氮数目小于0.1N ,C错误;D项,根据反应4可知,为使0.1molNO 完全转化
2 2 4 A 2
成HNO,至少需要0.025N 个O,D错误;故选B。
3 A 2
3.(2024·福建卷,4,4分)用CuCl探究Cu(I)、Cu(II)性质,实验步骤及观察到的现象如下:
的
该过程中可能涉及 反应有:
①CuCl+2NH ·H O=[Cu(NH )]++Cl-+2H O
3 2 3 2 2
②2[Cu(NH )]+=[Cu(NH )]2++Cu↓
3 2 3 4
③[Cu(NH )]2++Cu=2[Cu(NH )]+
3 4 3 2
④4[Cu(NH )]++O +8NH ·H O=4[Cu(NH )]2++4OH-+6H O
3 2 2 3 2 3 4 2
下列说法错误的是( )
A.与Cu2+的配位能力:NH <OH- B.[Cu(NH )]+(aq)无色
3 3 2
C.氧化性:[Cu(NH )]+<[Cu(NH )]2+ D.探究过程未发生反应②
3 2 3 4
【答案】A
【解析】CuCl加入过量氨水生成无色溶液,过程中发生反应CuCl+2NH ·H O=[Cu(NH )]++Cl-+2H O,
3 2 3 2 2
其中[Cu(NH )]+(aq)为无色,无色溶液在空气中被氧气氧化为蓝色溶液,发生反应 4[Cu(NH )]+
3 2 3 2
+O +8NH ·H O=4[Cu(NH )]2++4OH-+6H O,其中[Cu(NH )]2+(aq)为蓝色,加入铜粉发生反应[Cu(NH )]2+
2 3 2 3 4 2 3 4 3 4
+Cu=2[Cu(NH )]+,放置在空气中又发生反应4[Cu(NH )]++O +8NH ·H O=4[Cu(NH )]2++4OH-+6H O,溶液
3 2 3 2 2 3 2 3 4 2
又变为蓝色。A项,NH 中由N原子提供孤对电子用于形成配位键,OH-中由O原子提供孤对电子用于形
3
成配位键,电负性O>N,则O给电子能力弱,则与Cu2+的配位能力:NH >OH-,故A错误;B项,
3
[Cu(NH )]+(aq)无色,故 B 正确;C 项,氧化剂的氧化性大于氧化产物,由方程式[Cu(NH )]2+
3 2 3 4
+Cu=2[Cu(NH )]+可知,氧化性:[Cu(NH )]+<[Cu(NH )]2+,故C正确;D项,探究整个过程未发生反应
3 2 3 2 3 4
②,故D正确;故选A。
4.(2024· 贵州卷,13,3分)贵州重晶石矿(主要成分BaSO)储量占全国1/3以上。某研究小组对重晶
4
石矿进行“富矿精开”研究,开发了制备高纯纳米钛酸钡(BaTiO )工艺。部分流程如下:
3下列说法正确的是( )
A.“气体”主要成分是HS,“溶液1”的主要溶质是NaS
2 2
B.“系列操作”可为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
C.“合成反应”中生成BaTiO 的反应是氧化还原反应
3
D.“洗涤”时可用稀HSO 去除残留的碱,以提高纯度
2 4
【答案】B
【解析】重晶石矿(主要成分为BaSO)通过一系列反应,转化为BaS溶液;加盐酸酸化,生成BaCl 和
4 2
HS气体;在 BaCl 溶液中加入过量的 NaOH,通过蒸发浓缩,冷却结晶、过滤、洗涤、干燥,得到
2 2
Ba(OH) ·8H O;过滤得到的溶液1的溶质主要含NaCl及过量的NaOH;Ba(OH) ·8H O加水溶解后,加入
2 2 2 2
Ti(OC H) ,进行合成反应,得到BaTiO 粗品,最后洗涤得到最终产品。A项,“气体”主要成分为HS
4 9 4 3 2
气体,“溶液 1”的溶质主要含 NaCl 及过量的 NaOH,A 项错误;B 项,,“系列操作”得到的是
Ba(OH) ·8H O晶体,故“系列操作”可以是蒸发浓缩,冷却结晶、过滤、洗涤、干燥,B项正确;C项,
2 2
“合成反应”是Ba(OH) ·8H O和Ti(OC H) 反应生成BaTiO ,该反应中元素化合价未发生变化,不是氧化
2 2 4 9 4 3
还原反应,C项错误;D项,“洗涤”时,若使用稀HSO ,BaTiO 会部分转化为难溶的BaSO ,故不能
2 4 3 4
使用稀HSO ,D项错误;故选B。
2 4
5.(2024·北京卷,7,3分)硫酸是重要化工原料,工业生产制取硫酸的原理示意图如下。
下列说法不正确的是( )
A.I的化学方程式:3FeS+8O Fe O+6SO
2 2 3 4 2
B.Ⅱ中的反应条件都是为了提高SO 平衡转化率
2
C.将黄铁和换成硫黄可以减少废渣的产生
D.生产过程中产生的尾气可用碱液吸收
【答案】B
【解析】黄铁矿和空气中的O 在加热条件下发生反应,生成SO 和Fe O,SO 和空气中的O 在
2 2 3 4 2 2
400~500℃、常压、催化剂的作用下发生反应得到SO ,用98.3%的浓硫酸吸收SO ,得到HSO 。A项,
3 3 2 4反应I是黄铁矿和空气中的O 在加热条件下发生反应,生成SO 和Fe O,化学方程式:3FeS+8O
2 2 3 4 2 2
Fe O+6SO,故A正确;B项,反应Ⅱ条件要兼顾平衡转化率和反应速率,还要考虑生产成本,如Ⅱ中
3 4 2
“常压、催化剂”不是为了提高SO 平衡转化率,故B错误;C项,将黄铁矿换成硫黄,则不再产生
2
Fe O,即可以减少废渣产生,故C正确;D项,硫酸工业产生的尾气为SO 、SO ,可以用碱液吸收,故
3 4 2 3
D正确;故选B。
6.(2024·湖南卷,11,3分)中和法生产NaHPO ·12H O的工艺流程如下:
2 4 2
已知:①HPO 的电离常数:K =6.9×10-3,K =6.2×10-8,K =4.8×10-13
3 4 a1 a2 a3
②NaHPO ·12H O易风化。
2 4 2
下列说法错误的是( )
A.“中和”工序若在铁质容器中进行,应先加入NaCO 溶液
2 3
B.“调pH”工序中X为NaOH或HPO
3 4
C.“结晶”工序中溶液显酸性
D.“干燥”工序需在低温下进行
【答案】C
【解析】HPO 和NaCO 先发生反应,通过加入X调节pH,使产物完全转化为NaHPO ,通过结晶、
3 4 2 3 2 4
过滤、干燥,最终得到NaHPO ·12H O成品。A项,铁是较活泼金属,可与HPO 反应生成氢气,故“中
2 4 2 3 4
和”工序若在铁质容器中进行,应先加入NaCO 溶液,A项正确;B项,若“中和”工序加入NaCO 过
2 3 2 3
量,则需要加入酸性物质来调节pH,为了不引入新杂质,可加入HPO ;若“中和”工序加入HPO 过量,
3 4 3 4
则需要加入碱性物质来调节pH,为了不引入新杂质,可加入NaOH,所以“调pH”工序中X为NaOH或
HPO ,B项正确;C项,“结晶”工序中的溶液为饱和NaHPO 溶液,由已知可知HPO 的K =6.2×10-
3 4 2 4 3 4 a2
8,K =4.8×10-13,则HPO 2-的水解常数 ,由于 ,则NaHPO 的
a3 4 2 4
水解程度大于电离程度,溶液显碱性,C项错误;D项,由于NaHPO ·12H O易风化失去结晶水,故“干
2 4 2
燥”工序需要在低温下进行,D项正确;故选C。
7.(2024·辽吉黑卷,13,3分)某工厂利用铜屑脱除锌浸出液中的Cl-并制备Zn,流程如下“脱氯”步
骤仅Cu元素化合价发生改变。下列说法正确的是( )锌浸出液中相关成分(其他成分无干扰)
离子 Zn2+ Cu2+ Cl-
浓度(g·Lˉ1) 145 0.03 1
A.“浸铜”时应加入足量HO,确保铜屑溶解完全
2 2
B.“浸铜”反应:2Cu+4H++H O=2Cu2++ H ↑+2H O
2 2 2 2
C.“脱氯”反应:Cu+Cu2++2Cl-=2CuCl↓
D.脱氯液净化后电解,可在阳极得到Zn
【答案】C
【解析】铜屑中加入HSO 和HO 得到Cu2+,反应的离子方程式为:Cu+2H++H O=Cu2++2H O,再加
2 4 2 2 2 2 2
入锌浸出液进行“脱氯”,“脱氯”步骤中仅Cu元素的化合价发生改变,得到CuCl固体,可知“脱氯”
步骤发生反应的化学方程式为:Cu+Cu2++2Cl-=2CuCl↓,过滤得到脱氯液,脱氯液净化后电解,Zn2+可在阴
极得到电子生成Zn。A项,“浸铜”时,铜屑不能溶解完全,Cu在“脱氯”步骤还需要充当还原剂,A
错误;B项,“浸铜”时,铜屑中加入HSO 和HO 得到Cu2+,反应的离子方程式为:Cu+2H++H O=Cu2+
2 4 2 2 2 2
+2H O,B错误;C项,“脱氯”步骤中仅Cu元素的化合价发生改变,得到CuCl固体,即Cu的化合价升
2
高,Cu2+的化合价降低,发生归中反应,化学方程式为:Cu+Cu2++2Cl-=2CuCl↓,C正确;D项,脱氯液净
化后电解,Zn2+应在阴极得到电子变为Zn,D错误;故选C。
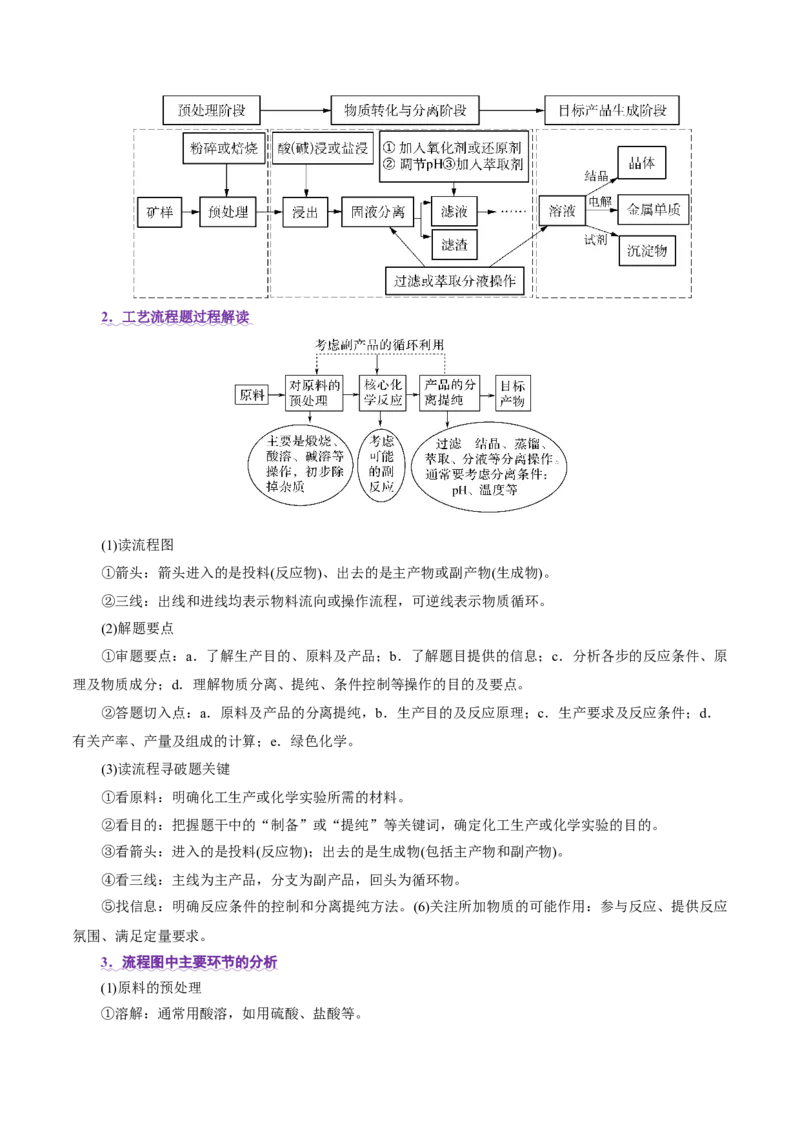
1 . 微型工艺流程中题的呈现方式2 .工艺流程题过程解读
(1)读流程图
①箭头:箭头进入的是投料(反应物)、出去的是主产物或副产物(生成物)。
②三线:出线和进线均表示物料流向或操作流程,可逆线表示物质循环。
(2)解题要点
①审题要点:a.了解生产目的、原料及产品;b.了解题目提供的信息;c.分析各步的反应条件、原
理及物质成分;d.理解物质分离、提纯、条件控制等操作的目的及要点。
②答题切入点:a.原料及产品的分离提纯,b.生产目的及反应原理;c.生产要求及反应条件;d.
有关产率、产量及组成的计算;e.绿色化学。
(3)读流程寻破题关键
①看原料:明确化工生产或化学实验所需的材料。
②看目的:把握题干中的“制备”或“提纯”等关键词,确定化工生产或化学实验的目的。
③看箭头:进入的是投料(反应物);出去的是生成物(包括主产物和副产物)。
④看三线:主线为主产品,分支为副产品,回头为循环物。
⑤找信息:明确反应条件的控制和分离提纯方法。(6)关注所加物质的可能作用:参与反应、提供反应
氛围、满足定量要求。
3 . 流程图中主要环节的分析
(1)原料的预处理
①溶解:通常用酸溶,如用硫酸、盐酸等。水浸 与水接触发生反应或溶解
浸出 固体加水(酸)溶解得到离子
酸浸 在酸溶液中反应,使可溶性金属离子进入溶液,不溶物通过过滤除去
浸出率 固体溶解后,离子在溶液中的含量的多少
②灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解。
③审题时要“瞻前顾后”,注意物质性质及反应原理的前后联系。
(3)常用的分离方法
①过滤:分离难溶物和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法。
②萃取和分液:利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用CCl 或苯萃取溴水中
4
的溴。
③蒸发结晶:提取溶解度随温度变化不大的溶质,如从溶液中提取NaCl。
④冷却结晶:提取溶解度随温度变化较大的溶质、易水解的溶质或结晶水合物,如 KNO 、FeCl 、
3 3
CuCl 、CuSO ·5H O、FeSO ·7H O等。
2 4 2 4 2
⑤蒸馏或分馏:分离沸点不同且互溶的液体混合物,如分离乙醇和甘油。
⑥冷却法:利用气体液化的特点分离气体,如合成氨工业采用冷却法分离平衡混合气体中的NH 。
3
4 . 制备工艺中提纯实例
制备过程及工艺 提纯方案
气体产物先通过盛有焦性没食子酸溶液的洗气瓶除去少量氧
气同时除去挥发出的氯化氢气体,再通过盛有酸性高锰酸钾
含硫锌粒与稀盐酸反应制备
溶液的洗气瓶除去硫化氢气体,最后通过盛有浓硫酸的洗气
纯净氢气(用作还原剂)
瓶除去水蒸气。“含硫锌粒”是指锌粒中含有杂质硫化锌,
硫化锌与稀硫酸反应会产生硫化氢气体。
潮湿的二氧化碳与过氧化钠 气体产物通过盛有碱石灰(或新制生石灰)的干燥管或U形管除
反应制备纯净氧气 去未反应完的二氧化碳和水蒸气。
气体产物通过盛有碱石灰(或新制生石灰)的干燥管或U形管除
加热分解碳酸氢铵制备纯净 去碳酸氢铵分解产生的二氧化碳和水蒸气。注意:用于干燥
氨气 氨气的干燥剂可以选择碱石灰或新制生石灰,不能用无水氯
化钙,因为CaCl +8NH ===CaCl ·8NH 。
2 3 2 3
气体产物先通过盛有饱和硫氢化钠溶液的洗气瓶除去氯化
用硫化亚铁与稀盐酸反应制
氢,后通过盛有五氧化二磷的球形干燥管或U形管除去水蒸
备纯净的硫化氢
气。
加入稀硫酸或稀盐酸溶液,充分反应后,再过滤、洗涤、干
除去铜粉中混有的氧化铜 燥。不能加入稀硝酸,因为稀硝酸具有强氧化性,既能溶解
氧化铜,又能溶解铜粉。
工业上以粉碎、筛选后的铝
先加入过量氢氧化钠溶液溶解、过滤,再向滤液中通入过量
土矿为原料制备较高纯度
CO,过滤出沉淀,进行煅烧。
Al O 的主要工艺流程 2
2 3
除去MgCl (或CuCl 、 先向混合溶液中加入HO(把亚铁离子氧化为铁离子),再加入
2 2 2 2
ZnCl 等)溶液中的FeCl 、 过量MgO或Mg(OH) (或过量CuO、ZnO)、使铁离子完全沉
2 3 2
FeCl 淀。
2考向 2 以物质的制备为背景
1.[新题型] (2025·浙江省七彩阳光新高考研究联盟高三联考)海水淡化有许多新工艺,某工艺的流程
示意图如图所示。以下说法不正确的是( )
A.由于连续的热交换,a处海水的温度更高
B.减压蒸馏时的压强二级闪蒸室内更低
C.广泛使用太阳能、风能和发电厂的余热以及热交换可降低海水淡化成本
D.淡化后的盐水常用于生产食盐、钾、铝、碘等化工产品
【答案】D
【解析】A项,a处的海水被2次加热,所以海水的温度:a>b,A正确;B项,盐水能够从一级闪蒸
室流入二级闪蒸室,说明一级闪蒸室中的压强大于二级闪蒸室的压强,B正确;C项,广泛使用太阳能、
风能和发电厂的余热以及热交换可降低海水淡化成本,C正确;D项,铝、碘并非从海水提取,D错误;
故选D。
2.(2022·江苏省南京、镇江市部分名校学情调研考试)由绿矾(FeSO ·7H O)制备三草酸合铁酸钾晶体
4 2
{ K[Fe(C O) ]·3H O}的流程如图
3 2 4 3 2
下列说法正确的是( )
A.“溶解”时加硫酸的目的是抑制 水解
B.将“沉淀”所得的FeC O 加入酸性高锰酸钾溶液,观察到溶液褪色,说明产物中含C O2-
2 4 2 4
C.“氧化”过程中HO 被还原为O
2 2 2
D.隔绝空气加热K[Fe(C O) ]·3H O,分解产物为KCO、Fe O、CO、HO
3 2 4 3 2 2 3 2 3 2 2【答案】A
【解析】由题给流程可知,绿矾溶于稀硫酸得到酸性硫酸亚铁溶液,向溶液中加入草酸溶液得到草酸
亚铁沉淀,向沉淀中加入草酸钾、草酸和过氧化氢混合溶液将草酸亚铁氧化得到三草酸合铁酸钾晶体。A
项,亚铁离子在溶液中易发生水解,溶解时加入稀硫酸的目的是抑制亚铁离子的水解,故A正确;B项,
向草酸亚铁沉淀中加入酸性高锰酸钾溶液时,亚铁离子和草酸根离子都能与酸性高锰酸钾溶液反应,使溶
液褪色,则观察到溶液褪色不能说明产物中含草酸根离子,故B错误;C项,氧化过程中过氧化氢为反应
的氧化剂,被草酸亚铁还原为水,故C错误;D项,由氧化还原反应规律可知,隔绝空气加热三草酸合铁
酸钾晶体时,三草酸合铁酸钾晶体受热分解生成碳酸钾、氧化铁、一氧化碳和水,故D错误;故选A。
3.(2025·浙江省第二届辛愉杯高三线上模拟考试)某兴趣小组用铬铁矿(FeCr O)制备CrCl ·6H O,流程
2 4 3 2
如下:
已知:①4FeCr O+10Na CO+7O 8NaCr O+4NaFeO+10CO ;
2 4 2 3 2 2 2 7 2 2
②Cr(OH) 不溶于乙醚。
3
下列说法不正确的是( )
A.步骤I应该将铬铁矿粉碎,以加快反应速率
B.步骤III从反应后溶液分离甲醇可用蒸馏法
C.步骤III应该滴加盐酸至恰好完全反应,方便后续调节pH
D.步骤V可用乙醚洗涤
【答案】C
【解析】由流程可知,铬铁矿加入碳酸钠,通入氧气发生高温氧化反应:4FeCr O+10Na CO+7O
2 4 2 3 2
8NaCr O+4NaFeO+10CO ,加入盐酸酸化将NaCrO 转化为NaCr O ,加入甲醇还原NaCr O 为+3
2 2 7 2 2 2 4 2 2 7 2 2 7
价Cr,调节pH沉淀Cr3+得到Cr(OH) ,加入浓盐酸溶解Cr(OH) ,得到CrCl 溶液,再结晶、过滤、洗涤得
3 3 3
到CrCl ·6H O。A项,步骤I应该将铬铁矿粉碎,可增大固体的接触面积,以加快反应速率,A正确;B项,
3 2
根据物质的沸点不同,步骤III从反应后溶液分离甲醇可用蒸馏法,B正确;C项,步骤III滴加盐酸应过
量,形成酸性条件,促进甲醇还原NaCr O 为+3价Cr,C错误;D项,已知Cr(OH) 不溶于乙醚,步骤V
2 2 7 3
可用乙醚洗涤Cr(OH) ,D正确;故选C。
3
4.(2025·浙江省名校协作体高三联考)某兴趣小组用铬铁矿(FeCr O)制备CrCl ·6H O,流程如下:
2 4 3 2已知:①4FeCr O+10Na CO+7O 8NaCr O+4NaFeO+10CO ;
2 4 2 3 2 2 2 7 2 2
②Cr(OH) 不溶于乙醚。
3
下列说法不正确的是( )
A.步骤I应该将铬铁矿粉碎,以加快反应速率
B.步骤III从反应后溶液分离甲醇可用蒸馏法
C.步骤III应该滴加盐酸至恰好完全反应,方便后续调节
D.步骤V可用乙醚洗涤
【答案】C
【解析】由流程可知,铬铁矿加入碳酸钠,通入氧气发生高温氧化反应:4FeCr O+10Na CO+7O
2 4 2 3 2
8NaCr O+4NaFeO+10CO ,加入盐酸酸化将NaCrO 转化为NaCr O,加入甲醇还原NaCr O 为+3
2 2 7 2 2 2 4 2 2 7 2 2 7
价Cr,调节pH沉淀Cr3+得到Cr(OH) ,加入浓盐酸溶解Cr(OH) ,得到CrCl 溶液,再结晶、过滤、洗涤得
3 3 3
到CrCl ·6H O。A项,步骤I应该将铬铁矿粉碎,可增大固体的接触面积,以加快反应速率,A正确;B项,
3 2
根据物质的沸点不同,步骤III从反应后溶液分离甲醇可用蒸馏法,B正确;C项,步骤III滴加盐酸应过
量,形成酸性条件,促进甲醇还原NaCr O 为+3价Cr,C错误;D项,已知Cr(OH) 不溶于乙醚,步骤V
2 2 7 3
可用乙醚洗涤Cr(OH) ,D正确;故选C。
3
考向 2 以废旧资源利用为背景
5.以废铁屑为原料制备硫酸亚铁晶体的实验过程如图,下列说法正确的是( )
A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明废铁屑中不含+3价铁元素
B.人体血红素是亚铁离子配合物,硫酸亚铁可用于治疗缺铁性贫血
C.过滤步骤说明硫酸亚铁晶体难溶于水
D.实验过程不直接蒸发结晶的原因是防止FeSO 水解生成Fe(OH)
4 2
【答案】B
【解析】废铁屑用稀硫酸酸浸后得到FeSO 溶液,FeSO 溶液经结晶、过滤得到硫酸亚铁晶体。A项,
4 4取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明酸浸后的溶液中不存在Fe3+,但不能说明废铁
屑中不含+3价铁元素,因为废铁屑中若含+3价铁元素,在酸浸时会被Fe还原成Fe2+,A项错误;B项,
人体血红素是亚铁离子配合物,硫酸亚铁可提供亚铁离子,从而可用于治疗缺铁性贫血,B项正确;C项,
硫酸亚铁晶体溶于水,题给实验过程中是经结晶析出晶体后过滤的,C项错误;D项,实验过程不直接蒸
发结晶的原因是:防止硫酸亚铁被氧化、防止硫酸亚铁晶体失去结晶水,D项错误;故选B。
6.无水FeCl 常用作芳烃氯代反应的催化剂。以废铁屑(主要成分Fe,还有少量Fe O、C和SiO)制取
3 2 3 2
无水FeCl 的流程如下,下列说法正确的是( )
3
A.“过滤”所得滤液中大量存在的离子有:Fe3+、Fe2+、H+、Cl-
B.“氧化”时可使用新制氯水作氧化剂
C.将“氧化”后的溶液蒸干可获得FeCl ·6H O
3 2
D.“脱水”时加入SOCl 能抑制FeCl 的水解,原因是SOCl 与水反应生成HSO 和HCl
2 3 2 2 4
【答案】B
【解析】废铁屑加入盐酸酸溶,碳、二氧化硅不反应,铁转化为盐溶液,过滤滤液加入新制氯水将亚
铁离子氧化为铁离子,处理得到FeCl ·6H O,加入SOCl 脱水得到FeCl 。A项,铁屑中主要成分Fe ,铁
3 2 2 3
和铁离子生成亚铁离子,故“过滤”所得滤液中大量存在的离子有:Fe2+、H+、Cl-,A错误;B项,氯气
具有氧化性,且不引入新杂质,故“氧化”时可使用新制氯水作氧化剂,B正确;C项,铁离子水解生成
氢氧化铁,故不能将“氧化”后的溶液蒸干来获得FeCl ·6H O,C错误;D项,是SOCl 与水反应生成SO
3 2 2 2
和HCl,D错误;故选B。
7.(2025·浙江省金华第一中学高三选考模拟)乙酸铜常用作有机合成的催化剂或氧化剂。实验室中制
备乙酸铜的流程如图所示。下列说法正确的是( )
A.反应①中双氧水起催化作用
B.为提高化学反应速率,反应①反应温度越高越好
C.步骤Ⅱ和步骤Ⅲ存在相同的操作
D.反应③碱式碳酸铜固体中加入的试剂X为冰醋酸
【答案】C【解析】先用热碱液除去铜屑表面油污,过氧化氢在酸性条件下氧化铜屑得到CuSO ,CuSO 再与纯
4 4
碱反应得到碱式碳酸铜,再与乙酸反应得到乙酸铜溶液,经过结晶得到乙酸铜晶体。A项,HO 起到氧化
2 2
作用,将Cu氧化为Cu(Ⅱ),A错误;B项,反应①反应温度过高,HO 分解程度变大,应选适宜的温度,
2 2
B错误;C项,步骤Ⅱ和步骤Ⅲ都有固体生成,因此需要进行固液分离,因此,存在相同的操作为过滤,C
正确;D项,碱式碳酸铜固体中加入的试剂X为醋酸溶液,在水溶液中便于反应发生,D错误; 故选C。
8.(2025·浙江省新阵地教育联盟高三第一次联考)以下流程可从含Cu²+的废液中回收高品质Cu O。已
2
知:CuCl是白色固体,难溶于水,可溶于Cl-浓度较大的体系,CuCl+2Cl- CuCl 2-(棕色),在碱性条
3
件下易水解转化为Cu O。
2
下列说法不正确的是( )
A.SO 在反应中表现还原性 B.试剂①可用饱和NaCl溶液
2
C.操作②是加水稀释,过滤 D.步骤③发生氧化还原反应
【答案】D
【解析】由流程图可知,先将含铜废液通SO 和饱和NaCl溶液反应生成CuCl 2-,加水稀释,氯离子
2 3
浓度降低,生成CuCl沉淀,过滤,控制温度和pH使其水解转化为Cu O。A项,SO 将Cu2+还原为Cu+,
2 2
为还原剂,在反应中表现还原性,故A项正确;B项,试剂①可用饱和NaCl溶液,故B项正确;C项,操
作②为加水稀释,氯离子浓度降低,生成CuCl沉淀,过滤,故C项正确;D项,步骤③中各元素化合价
均为改变,则未发生氧化还原反应,故D项错误;故选D。
9.用硫酸渣(主要成分为Fe O、SiO)制备铁基颜料铁黄(FeOOH)的一种工艺流程如图。
2 3 2
已知:“还原”时,发生反应FeS+14Fe3++8H O=2SO 2-+15Fe2++16H+;FeS 与HSO 不反应。下列有
2 2 4 2 2 4
关说法不正确的是( )
A.“酸溶”时适当提高硫酸浓度可加快反应速率
B.“还原”时氧化产物与还原产物质的物质的量之比为1∶7
C.“过滤I”所得滤液中存在的阳离子主要有Fe2+、Fe3+和H+
D.“沉降、氧化”时发生反应的离子方程式:4Fe2++8NH•H O+O=8NH++4FeOOH↓+2H O
3 2 2 4 2
【答案】C【解析】硫酸渣(主要成分为Fe O、SiO)加硫酸溶解,金属氧化物转化为金属阳离子,二氧化硅不溶,
2 3 2
再加FeS 把铁离子还原为亚铁离子,同时生成SO 2-,过滤,滤渣含有SiO 和FeS,滤液中含有Fe2+和
2 4 2 2
H+,滤液中通入空气氧化,同时加入氨水调节pH生成FeOOH沉淀,过滤、洗涤、烘干,得到纯净的
FeOOH。A项,适当提高硫酸浓度,增大氢离子浓度,可增大反应速率,A正确;B项,有关的离子方程
式为FeS+14Fe3++8H O=2 SO 2-+15Fe2++16H+,反应中FeS 的Fe元素化合价不变,S元素化合价升高,则
2 2 4 2
SO 2-为氧化产物,Fe3+转化为Fe2+,化合价降低,Fe2+为还原产物,则“还原”时氧化产物与还原产物质的
4
物质的量之比为2∶14=1∶7,B正确;C项,滤液中含有硫酸亚铁和过量的硫酸,且生成氢离子,则“过滤I”
所得滤液中存在的阳离子主要有Fe2+和H+,C错误;D项,滤液中通入空气氧化,同时加入氨水调节pH
生成FeOOH沉淀,发生的离子方程式为4Fe2++8NH•H O+O=8NH++4FeOOH↓+2H O,D正确;故选C。
3 2 2 4 2
10.某新型纳米材料氧缺位铁酸盐ZnFe O(3