文档内容
热点强化练 13 多平衡体系的综合分析
1.(2020·江苏盐城高三三模)CO 催化重整CH 的反应如下:
2 4
(Ⅰ)CH (g)+CO (g)2CO(g)+2H (g) ΔH ,
4 2 2 1
主要副反应:(Ⅱ)H (g)+CO (g)CO(g)+H O(g) ΔH >0,
2 2 2 2
(Ⅲ)4H (g)+CO (g)CH (g)+2H O(g) ΔH <0。
2 2 4 2 3
在恒容反应器中按体积分数V(CH )∶V(CO )=50%∶50%充入气体,加入催
4 2
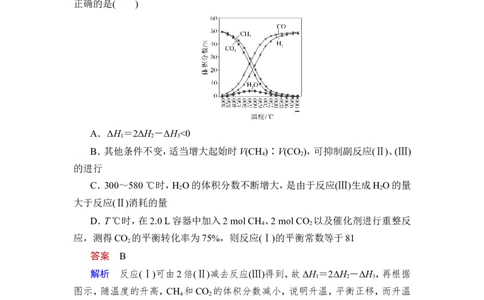
化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法
正确的是( )
A.ΔH =2ΔH -ΔH <0
1 2 3
B.其他条件不变,适当增大起始时V(CH )∶V(CO ),可抑制副反应(Ⅱ)、(Ⅲ)
4 2
的进行
C.300~580 ℃时,H O的体积分数不断增大,是由于反应(Ⅲ)生成H O的量
2 2
大于反应(Ⅱ)消耗的量
D.T ℃时,在2.0 L容器中加入2 mol CH 、2 mol CO 以及催化剂进行重整反
4 2
应,测得CO 的平衡转化率为75%,则反应(Ⅰ)的平衡常数等于81
2
答案 B
解析 反应(Ⅰ)可由2倍(Ⅱ)减去反应(Ⅲ)得到,故ΔH =2ΔH -ΔH ,再根据
1 2 3
图示,随温度的升高,CH 和CO 的体积分数减小,说明升温,平衡正移,而升温
4 2
平衡向吸热方向移动,正反应吸热,ΔH >0,A不正确;其他条件不变,适当增大起
1
始时V(CH )∶V(CO ),即增大CH 浓度或减小CO 浓度,根据平衡移动原理,减
4 2 4 2
小反应物浓度或增加生成物浓度,平衡都逆向移动,B正确;300~580 ℃时,H O
2
的体积分数不断增大,反应(Ⅲ)是放热反应,升温时,平衡逆移消耗H O,反应(Ⅱ)
2
是吸热反应,升温时正移,生成H O,而由于反应(Ⅲ)消耗H O的量小于反应(Ⅱ)
2 2
生成水的量,C错误;T ℃时,在2.0 L容器中加入2 mol CH 、2 mol CO 以及催化
4 2
剂进行重整反应,测得CO 的平衡转化率为75%,则CO 转化的浓度=×75%=
2 20.75 mol/L根据三段式:
若不考虑副反应,则反应(Ⅰ)的平衡常数==81,但由于副反应(Ⅲ)中,消耗
的氢气的量比二氧化碳多的多,故计算式中,分子减小的更多,值小于81,D错误。
2.(2020·安徽省江南十校4月综合素质测试)CH 用水蒸气重整制氢包含的反
4
应为:
Ⅰ.水蒸气重整:CH (g)+H O(g)CO(g)+3H (g) ΔH=+206 kJ·mol-1
4 2 2
Ⅱ.水煤气变换:CO(g)+H O(g)CO (g)+H (g) ΔH=-41.2 kJ·mol-1
2 2 2
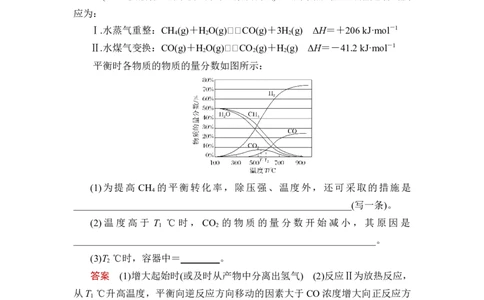
平衡时各物质的物质的量分数如图所示:
(1)为提高 CH 的平衡转化率,除压强、温度外,还可采取的措施是
4
_________________________________________________________(写一条)。
(2)温度高于 T ℃时,CO 的物质的量分数开始减小,其原因是
1 2
______________________________________________________________。
(3)T ℃时,容器中=________。
2
答案 (1)增大起始时(或及时从产物中分离出氢气) (2)反应Ⅱ为放热反应,
从T ℃升高温度,平衡向逆反应方向移动的因素大于CO浓度增大向正反应方
1
向移动的因素,净结果是平衡逆向移动 (3)7(或7∶1)
解析 (1)为提高CH 的平衡转化率,即要让反应向正向进行,除压强、温度
4
外,还可将生成的氢气从产物中分离出去,或增大起始时的;(2)反应Ⅰ是吸热反
应,升高温度,平衡正向移动,CO的浓度增大,反应Ⅱ为放热反应,升高温度,反
应逆向进行,CO 的量减少,出现如图所示CO 的物质的量分数开始减小,说明T
2 2 1
℃升高温度,平衡向逆向移动的因素大于CO浓度增大向正向移动的因素,结果
是平衡逆向移动;(3)根据图像,T ℃时,容器中一氧化碳和二氧化碳的物质的量
2分数相等,设T ℃时,二氧化碳的物质的量为x,列三段式:
2
根据上述分析,T ℃时,n(H )=6x+x=7x,n(CO )=x,则==7。
2 2 2
3.氨催化氧化时会发生如下两个竞争反应Ⅰ、Ⅱ。
4NH (g)+5O (g)4NO(g)+6H O(g) Ⅰ
3 2 2
4NH (g)+3O (g)2N (g)+6H O(g) ΔH<0 Ⅱ
3 2 2 2
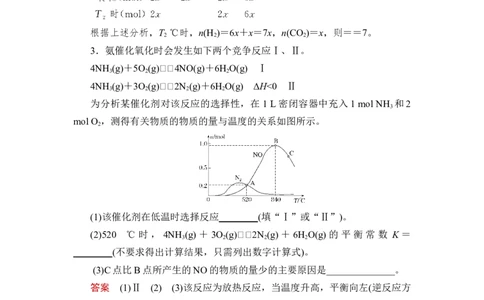
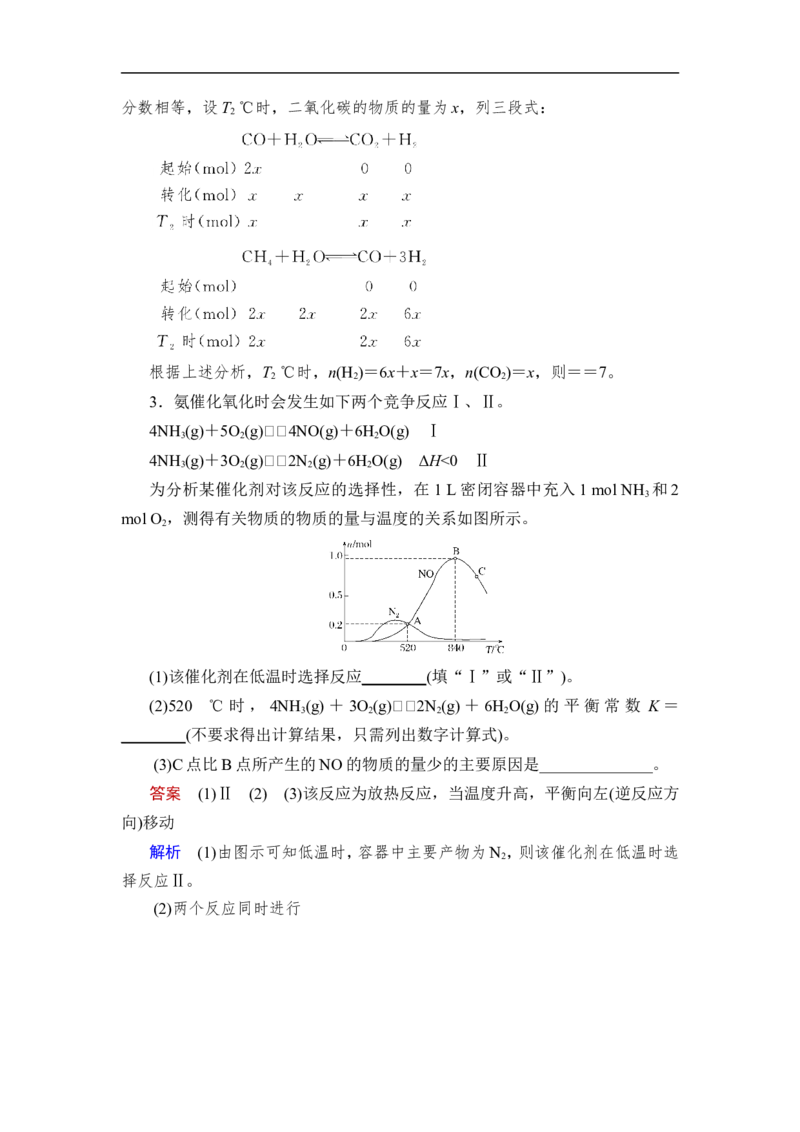
为分析某催化剂对该反应的选择性,在 1 L密闭容器中充入1 mol NH 和2
3
mol O ,测得有关物质的物质的量与温度的关系如图所示。
2
(1)该催化剂在低温时选择反应________(填“Ⅰ”或“Ⅱ”)。
(2)520 ℃ 时 , 4NH (g) + 3O (g)2N (g) + 6H O(g) 的 平 衡 常 数 K =
3 2 2 2
________(不要求得出计算结果,只需列出数字计算式)。
(3)C点比B点所产生的NO的物质的量少的主要原因是______________。
答案 (1)Ⅱ (2) (3)该反应为放热反应,当温度升高,平衡向左(逆反应方
向)移动
解析 (1)由图示可知低温时,容器中主要产物为N ,则该催化剂在低温时选
2
择反应Ⅱ。
(2)两个反应同时进行故520 ℃时4NH (g)+3O (g)2N (g)+6H O(g)的平衡常数K=。
3 2 2 2
(3)已知4NH (g)+5O (g)4NO(g)+6H O(g) ΔH<0,正反应是放热反应,
3 2 2
当反应达到平衡后,温度升高,平衡向左(逆反应方向)移动,导致NO的物质的量
逐渐减小,即C点比B点所产生的NO的物质的量少。
4.(2020·河南许昌、济源、平顶山三市二次联考)二甲醚(CH OCH )是无色气
3 3
体,是柴油的理想替代燃料。清华大学王志良等研究了由合成气(组成为H 、CO
2
和少量的CO )一步法制备二甲醚的问题,其中的主要过程包括以下三个反应:
2
(ⅰ)CO(g)+2H (g)CH OH(g)
2 3
ΔH =-90.1 kJ/mol
1
(ⅱ)CO(g)+H O(g)CO (g)+H (g)
2 2 2
ΔH =-41.1 kJ/mol
2
(ⅲ)2CH OH(g)CH OCH (g)+H O(g)
3 3 3 2
ΔH =-24.5 kJ/mol
3
(1) 由 H 和 CO 制备二甲醚 (另一产物为 CO )的热化学方程式为
2 2
___________________________________________________________________。
(2)合成气初始组成为n(H )∶n(CO)∶n(CO )=0.67∶0.32∶0.01的反应体系。
2 2
在250 ℃和5.0 MPa条件下,在1 L密闭容器中经10 min达到化学平衡时,各
组分的物质的量如下表:
成分 H CO H O CH OH CH OCH
2 2 3 3 3
物质的量(mol) 0.26 0.01 0.04 0.02 0.11
则反应(iii)在该条件下的平衡常数是________;在反应进行的10 min内,用
CH OH表示的反应(i)的平均速率是________。
3
(3)课题组探究了外界条件,对合成气单独合成甲醇反应体系和直接合成二
甲醚反应体系的影响。
①图1和图2显示了温度250 ℃和5.0 MPa条件下,合成气组成不同时,反
应达到平衡时的情况。(图中M代表甲醇、D代表二甲醚、D+M代表甲醇和二甲
醚。下同)由图可知,随着合成气中H 所占比例的提高,合成甲醇的反应体系中,CO转
2
化率的变化趋势是________。对于由合成气直接合成二甲醚的反应体系,为了提
高原料转化率和产品产率,的值应控制在________附近。
②在压强为5.0 MPa、=2.0及=的条件下,反应温度对平衡转化率和产率的
影响如图3和图4所示。
课题组认为图3所示的各反应物的转化率变化趋势符合反应特点,其理由是
____________________________________________________________________。
图中显示合成气直接合成二甲醚体系中,CO的转化率明显高于H 的转化率
2
原因是________________________________________________。图4显示随着温度增大,合成气单独合成甲醇时的产率,要比合成气直接合
成二甲醚时的产率减小的快,原因是________________________________。
答案 (1)3CO(g)+3H (g)===CO (g)+CH OCH (g) ΔH=-245.8 kJ/mol
2 2 3 3
(2)11 0.024 mol/(L·min) (3)①由小逐渐变大 1 ②反应体系中的所有反应均
为放热反应 反应(ⅱ)有H 生成 反应(ⅰ)的焓变大于反应(ⅲ)的焓变
2
解析 (1)已知:(ⅰ)CO(g)+2H (g)CH OH(g) ΔH =-90.1 kJ/mol
2 3 1
(ⅱ)CO(g)+H O(g)CO (g)+H (g)
2 2 2
ΔH =-41.1 kJ/mol
2
(ⅲ)2CH OH(g)CH OCH (g)+H O(g)
3 3 3 2
ΔH =-24.5 kJ/mol
3
根据盖斯定律,将(ⅰ)×2+(ⅱ)+(ⅲ),整理可得:3CO(g)+3H (g)===CO (g)
2 2
+CH OCH (g) ΔH=-245.8 kJ/mol;
3 3
(2)对于2CH OH(g)CH OCH (g)+H O(g),由于容器的容积是1 L,所以平
3 3 3 2
衡时各种物质的浓度与其物质的量在数值上相等,平衡时 c(CH OH)=0.02
3
mol/L,c(CH OCH )=0.11 mol/L,c(H O)=0.04 mol/L,故其平衡常数K==11;
3 3 2
对于反应(ⅰ),开始时从正反应方向开始,c(CH OH)=0 mol/L,10 min时
3
c(CH OCH )=0.11 mol/L,则发生反应(ⅲ)消耗甲醇的浓度是 c(CH OH)=0.11
3 3 3
mol/L×2=0.22 mol/L,此时还有c(CH OH)=0.02 mol/L,则反应(ⅰ)产生甲醇的
3
浓度是c(CH OH) =0.22 mol/L+0.02 mol/L=0.24 mol/L,故用甲醇表示的反应
3 总
速率v(CH OH)==0.024 mol/(L·min);
3
(3)①根据图1可知:在合成甲醇的反应体系中,随着合成气中H 所占比例的
2
提高,CO转化率的变化趋势是由小逐渐变大;
根据图1可知:在合成二甲醚的反应体系中,随着合成气中H 所占比例的提
2
高,CO转化率的变化趋势是由小逐渐变大,当=1时达到最大值,此后几乎不再
发生变化;根据图2可知:在=1时二甲醚的产率达到最大值,此后随着的增大,
产品产率又逐渐变小,故为了提高原料转化率和产品产率,的值应控制在1附近
②根据图示可知:在不变时,随着温度的升高,各个反应平衡转化率降低,这
是由于反应体系中的所有反应均为放热反应,升高温度,平衡向吸热的逆反应方
向移动,导致平衡时产生的物质相应的量减小;图中显示合成气直接合成二甲醚
体系中,CO 的转化率明显高于 H 的转化率,原因是反应(ⅱ) CO(g)+
2
H O(g)CO (g)+H (g)中有H 生成,增大了反应物H 的浓度,平衡正向移动,
2 2 2 2 2
因而可提高另一种反应物CO的转化率;根据图4显示:随着温度增大,合成气单独合成甲醇时的产率,要比合成气直接合成二甲醚时的产率减小的快,原因是反
应(ⅰ)的焓变大于反应(ⅲ)的焓变,平衡逆向移动消耗的多,故物质二甲醚转化率
降低的多。