文档内容
热点强化练 7 非金属及其化合物对环境的影响
1.(2020·辽宁丹东高三月考)化学与生产、生活息息相关,下列因果关系不正
确的是( )
选项 原因 结果
A 汽车尾气的排放 光化学烟雾
B 某酸雨样品吸收了空气中的CO pH由5.6变为4.3
2
用聚乳酸塑料代替聚乙烯
C 聚乳酸塑料可降解
塑料可减少白色污染
D 含氮、磷等生活废水的大量排放 赤潮
答案 B
解析 汽车尾气的大量排放,会产生氮氧化物,从而造成光化学烟雾,A正确;
某酸雨样品pH由5.6变为4.3是因为样品中的亚硫酸被氧化为硫酸,与二氧化碳
无关,B错误;聚乳酸塑料可降解,用聚乳酸塑料代替聚乙烯塑料可减少白色污
染,C正确;氮、磷是植物生长需要的营养元素,含氮、磷等生活废水的大量排放,
会导致水体富营养化,引发水华、赤潮,D正确。
2.(2020·大庆市高三开学考试)汽车尾气(含烃类、CO、NO和SO 等)是空气的
2
主要污染源。治理方法之一是在汽车排气管上加装“催化转化器”,使CO和NO
反应产生可参与大气循环的无毒气体,促使烃类充分燃烧及SO 的转化。下列说
2
法中错误的是( )
A.CO和NO反应生成CO 和N :2CO+2NO=====2CO +N
2 2 2 2
B.汽车改用天然气为燃料或开发氢能源,都可减少对空气的污染
C.此方法的缺点是由于CO 的增多,会大大提高空气的酸度
2
D.增大绿化面积,多植树造林,可有效控制城市空气污染
答案 C
解析 由信息可知,NO和CO反应生成无毒的氮气和二氧化碳,化学方程式
为:2CO+2NO=====2CO +N ,故A正确;天然气的燃烧产物为二氧化碳和水,
2 2
氢气的燃烧产物为水,不会产生NO和SO 等,所以改用天然气或开发氢能源可
2
减少对空气的污染,故B正确;二氧化碳是空气的成分,溶于水生成碳酸不稳定
分解,二氧化碳量增多不会增加空气的酸度,故C错误;增大绿化面积,多植树造
林,可有效控制城市空气污染,故D正确。
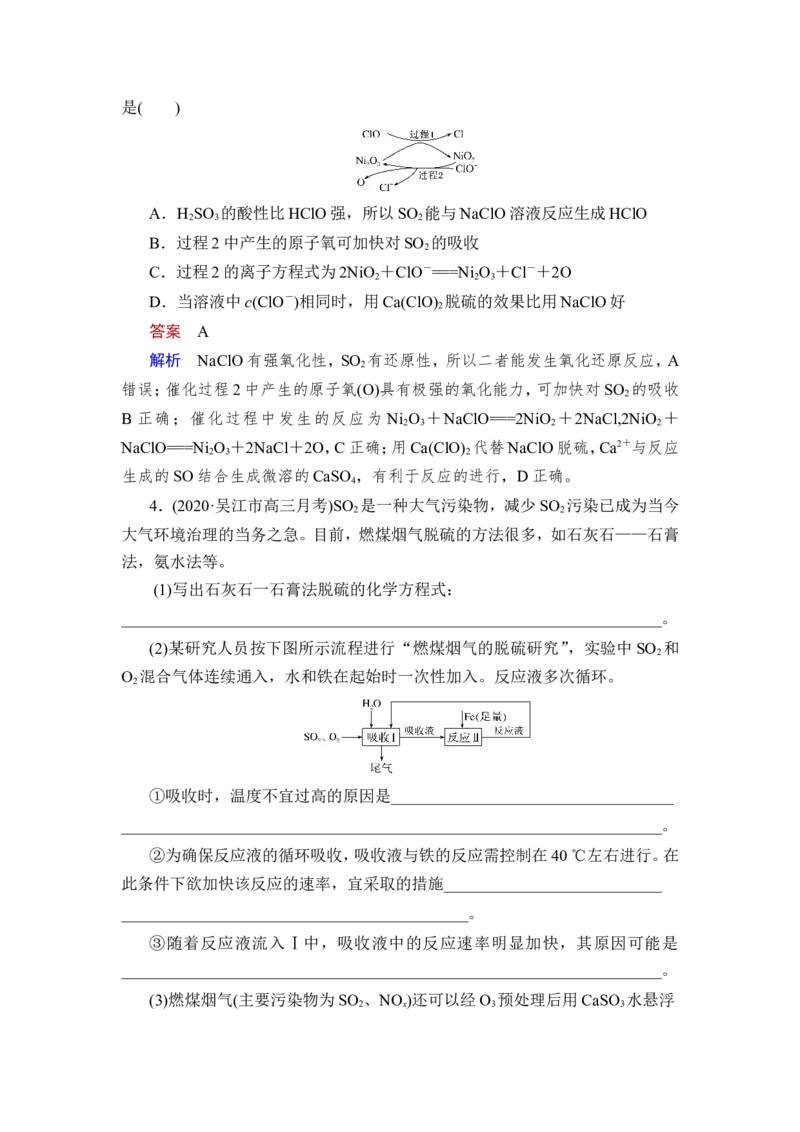
3.SO 是一种大气污染物,工业上可用NaClO碱性溶液吸收SO 。为了提高
2 2
吸收效率,常用Ni O 作为催化剂。该催化过程如图所示,下列有关说法不正确的
2 3是( )
A.H SO 的酸性比HClO强,所以SO 能与NaClO溶液反应生成HClO
2 3 2
B.过程2中产生的原子氧可加快对SO 的吸收
2
C.过程2的离子方程式为2NiO +ClO-===Ni O +Cl-+2O
2 2 3
D.当溶液中c(ClO-)相同时,用Ca(ClO) 脱硫的效果比用NaClO好
2
答案 A
解析 NaClO有强氧化性,SO 有还原性,所以二者能发生氧化还原反应,A
2
错误;催化过程2中产生的原子氧(O)具有极强的氧化能力,可加快对SO 的吸收
2
B 正确;催化过程中发生的反应为 Ni O +NaClO===2NiO +2NaCl,2NiO +
2 3 2 2
NaClO===Ni O +2NaCl+2O,C正确;用Ca(ClO) 代替NaClO脱硫,Ca2+与反应
2 3 2
生成的SO结合生成微溶的CaSO ,有利于反应的进行,D正确。
4
4.(2020·吴江市高三月考)SO 是一种大气污染物,减少SO 污染已成为当今
2 2
大气环境治理的当务之急。目前,燃煤烟气脱硫的方法很多,如石灰石——石膏
法,氨水法等。
(1)写出石灰石一石膏法脱硫的化学方程式:
___________________________________________________________________。
(2)某研究人员按下图所示流程进行“燃煤烟气的脱硫研究”,实验中SO 和
2
O 混合气体连续通入,水和铁在起始时一次性加入。反应液多次循环。
2
①吸收时,温度不宜过高的原因是___________________________________
___________________________________________________________________。
②为确保反应液的循环吸收,吸收液与铁的反应需控制在40 ℃左右进行。在
此条件下欲加快该反应的速率,宜采取的措施___________________________
___________________________________________。
③随着反应液流入Ⅰ中,吸收液中的反应速率明显加快,其原因可能是
___________________________________________________________________。
(3)燃煤烟气(主要污染物为SO 、NO )还可以经O 预处理后用CaSO 水悬浮
2 x 3 3液吸收。当用CaSO 水悬浮液吸收时,清液(pH约为8)中SO将NO 转化为NO,
3 2
其离子方程式为_______________________________________________。
答案 (1)SO +CaCO =====CaSO ↓+CO ;2CaSO +O ===2CaSO
2 3 3 2 3 2 4
(2)①温度过高SO 溶解度降低 ②搅拌 ③生成的Fe2+对亚硫酸氧化生成
2
硫酸的反应起催化作用
(3)SO+2NO +2OH-===SO+2NO+H O
2 2
解析 (1)石灰石-石膏法脱硫的原理第一步是 SO +CaCO =====CaSO ↓
2 3 3
+CO ,然后再将产物氧化制成石膏,2CaSO +O ===2CaSO ;(2)①温度高,气体
2 3 2 4
的溶解度较少,则吸收时,温度不宜过高的原因是温度过高SO 溶解度降低;②
2
为确保反应液的循环吸收效果,反应池中的反应需控制在40 ℃左右进行,在此
条件下欲加快该反应速率宜采取的措施有(用搅拌器进行)搅拌;③吸收液中的反
应速率明显加快,其原因可能是生成的 Fe2+对亚硫酸氧化生成硫酸的反应起催
化作用,(3)溶液pH约为8,说明溶液呈碱性,SO 将NO 转化为NO,同时SO被
2
氧化生成SO,根据反应物和生成物书写离子方程式为SO+2NO +2OH-===SO
2
+2NO+H O 。
2
5.(2020·湖北武汉高三零模)我国是以煤炭为主要能源的发展中国家,煤炭燃
烧产生的烟气中含有大量的NO 和SO ,带来了严重的大气污染。某化工小组进
x 2
行了ClO 协同氨水法脱除模拟烟气中NO 和SO 的实验研究,其流程如图:
2 x 2
回答下列问题:
(1)制备“模拟烟气”时应首先向装置管道内通入________,目的是
___________________________________________________________________。
(2)“喷淋液”中所含ClO 可通过向酸性氯酸钠溶液中加入葡萄糖的方法制
2
备,同时产生CO 等物质,则该反应的离子方程式为
2
___________________________________________________________________,
还可将葡萄糖替换为________(填字母标号)。
A.FeCl 溶液 B.SO
3 3
C.甲醇 D.酸性KMnO 溶液
4
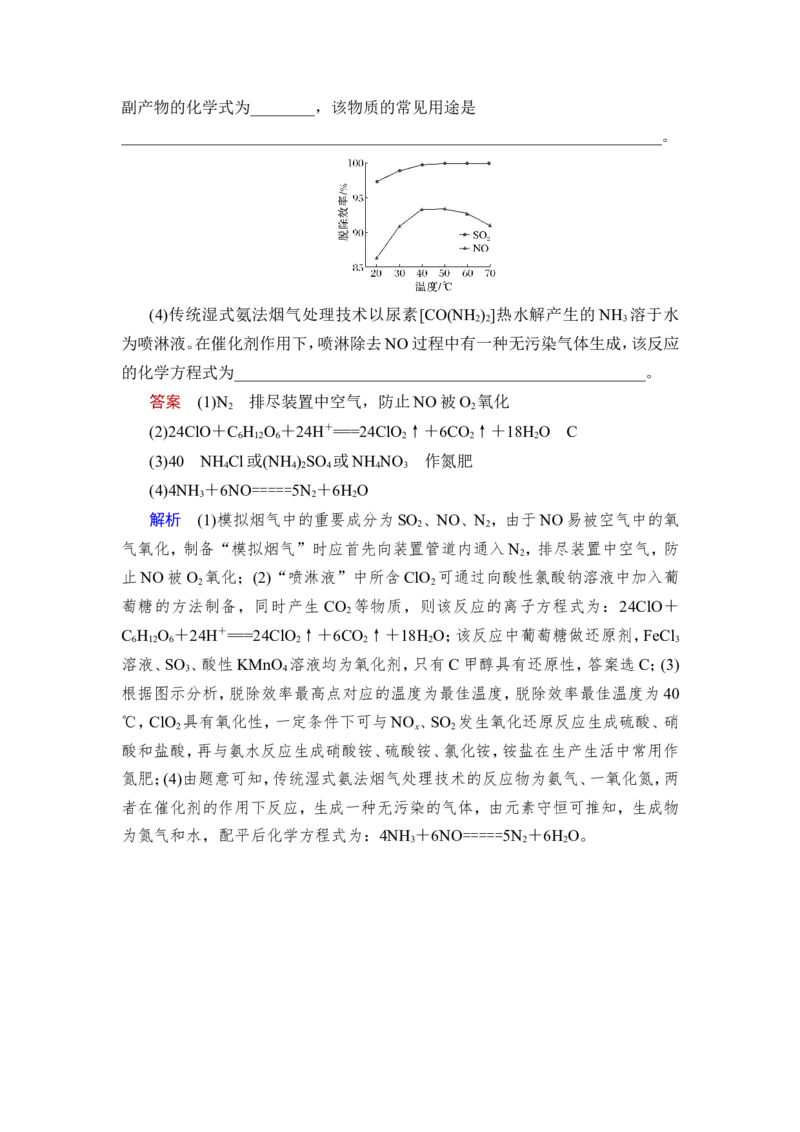
(3)利用ClO 协同氨水进行脱硫脱硝净化时,污染性气体脱除效率变化情况
2
如图所示,则该脱除技术的最佳温度应为________ ℃,喷淋塔中可能产生的一种副产物的化学式为________,该物质的常见用途是
___________________________________________________________________。
(4)传统湿式氨法烟气处理技术以尿素[CO(NH ) ]热水解产生的 NH 溶于水
2 2 3
为喷淋液。在催化剂作用下,喷淋除去NO过程中有一种无污染气体生成,该反应
的化学方程式为___________________________________________________。
答案 (1)N 排尽装置中空气,防止NO被O 氧化
2 2
(2)24ClO+C H O +24H+===24ClO ↑+6CO ↑+18H O C
6 12 6 2 2 2
(3)40 NH Cl或(NH ) SO 或NH NO 作氮肥
4 4 2 4 4 3
(4)4NH +6NO=====5N +6H O
3 2 2
解析 (1)模拟烟气中的重要成分为SO 、NO、N ,由于NO易被空气中的氧
2 2
气氧化,制备“模拟烟气”时应首先向装置管道内通入N ,排尽装置中空气,防
2
止NO被O 氧化;(2)“喷淋液”中所含ClO 可通过向酸性氯酸钠溶液中加入葡
2 2
萄糖的方法制备,同时产生 CO 等物质,则该反应的离子方程式为:24ClO+
2
C H O +24H+===24ClO ↑+6CO ↑+18H O;该反应中葡萄糖做还原剂,FeCl
6 12 6 2 2 2 3
溶液、SO 、酸性KMnO 溶液均为氧化剂,只有C甲醇具有还原性,答案选C;(3)
3 4
根据图示分析,脱除效率最高点对应的温度为最佳温度,脱除效率最佳温度为40
℃,ClO 具有氧化性,一定条件下可与NO 、SO 发生氧化还原反应生成硫酸、硝
2 x 2
酸和盐酸,再与氨水反应生成硝酸铵、硫酸铵、氯化铵,铵盐在生产生活中常用作
氮肥;(4)由题意可知,传统湿式氨法烟气处理技术的反应物为氨气、一氧化氮,两
者在催化剂的作用下反应,生成一种无污染的气体,由元素守恒可推知,生成物
为氮气和水,配平后化学方程式为:4NH +6NO=====5N +6H O。
3 2 2